1例信迪利單抗治療晚期胃癌致重癥藥疹的中西醫結合治療報告
錢琳,曾進浩,吳茂林,李志華,唐欣,黃裴,王曉艷,胡月,徐英君
(成都中醫藥大學附屬醫院腫瘤科,四川 成都 610000)
1 病例資料
患者,女,74歲,主訴“確診胃竇腺癌3個月余,首次化療及免疫治療后3周”,于2022年5月5日收入成都中醫藥大學附屬醫院住院治療。2022年1月患者無明顯誘因出現上腹部脹滿不適,無腹痛腹瀉,無惡心嘔吐等不適。2022年2月23日患者于四川大學華西醫院就診,完善胃鏡及病理檢查見:胃竇腺癌。術前分期為cT4acNtcM0cTNMIII。后于2022年2月28日在全麻下行腹腔鏡探查+腹腔惡性腫瘤特殊治療。術中分期為sT4bN+M0H0P0CYx。腹腔內無明顯腹水,腹腔無粘連,腹膜無種植結節,腹膜轉移分期為P0,PCI評分為0分,明顯轉移灶。探查膈頂、盆底、膽囊、胰腺、脾臟、小腸、大腸、系膜無異常。腫瘤位于胃竇,不屬于食管胃結合部腺癌。腫瘤大小為長徑×短徑為5 cm×4 cm,非多發癌,活動度差。腫瘤累及胰腺,橫穿橫結腸系膜,腫瘤致胃竇狹窄、變形,幽門梗阻。因腫瘤分期晚,無法行根治手術,遂行胃空腸吻合術以緩解梗阻情況。2022年4月26日,患者華西醫院免疫組化結果回示:CK7(+),CDX-2(+),SATB2(-)。MLH1(+,100%)、MSH2(+,100%),MSH6(+,100%),PMS2(+,100%),Her2(0-1+),Ki67陽性率約70%。出院后患者為求進一步中西醫結合治療,到我院住院治療。
既往史:診斷“高血壓病”6年余,最高血壓不詳,既往規律口服厄貝沙坦片75 mg,qd,控制血壓,自訴血壓控制情況可,確診胃惡性腫瘤后自行停藥。否認其他慢性病;無傳染性疾病;否認除本次胃空腸吻合術之外的其他手術、無外傷史,有輸血史,無藥物食物過敏史。根據2022年中國臨床腫瘤學會(chinese society of clinical oncology,CSCO)胃癌診療指南[1]推薦:針對晚期轉移性胃癌,在PD-L1 CPS<5或檢測不可及,可考慮使用XELOX聯合信迪利單抗(1B類),因患者美國東部腫瘤協作組(eastern cooperative oncology group,ECOG)評分[2]3分,化療和免疫治療風險高,鉑類化療的骨髓抑制較重,無法耐受,故僅用含氟尿嘧啶類藥物(替吉奧)聯合信迪利單抗進行治療。方案:替吉奧膠囊50 mg po bid d1-d14化療+信迪利單抗 200 mg ivgtt d1 q3w免疫治療,2022年5月5日開始首程治療,口服替吉奧7天后復查血常規,提示血紅蛋白從100 g/L持續下降至70 g/L,并且無消化道出血證據,考慮為替吉奧導致的骨髓抑制,故停用。
2022年5月27日復查血常規提示血紅蛋白80 g/L,故將替吉奧減量為20 mg po bid d1-d14+信迪利單抗200 mg ivgtt d1 q3w進行治療,輸注2 h后,患者出現發熱,體溫波動于38.4~39.0 ℃,雙下肢、胸腹部及后背部泛發皮疹,色紅,瘙癢,部分紅斑。請皮膚科會診后考慮藥物過敏,予以抗過敏治療并予以退熱補液等對癥治療;5月28日至5月29日皮疹進行性加重,并伴有表皮松解;5月30日予以左氧氟沙星聯合頭孢哌酮他唑巴坦鈉抗感染,并再請皮膚科會診,皮膚科會診考慮:重癥藥疹,steven-johnson綜合征給予甲潑尼龍琥珀酸鈉(2 mg·kg-1·d-1)治療,西咪替丁預防胃腸道反應,續用葡萄糖酸鈣及維生素C注射液補充鈣劑及維生素,經治療后,患者病情未見好轉,斑疹面積繼續增多,手足新發紅色斑疹。再請皮膚科及ICU會診后,建議轉入ICU繼續治療,家屬同意后于2022年5月31日轉入ICU繼續治療。
輸注信迪利單抗后,患者皮膚泛發皮疹并不斷加重,抗過敏、抗感染等治療均不顯效,可見表皮松解,多見紅斑與水皰,水皰迅速糜爛并露出鮮紅色糜爛面。見圖1。
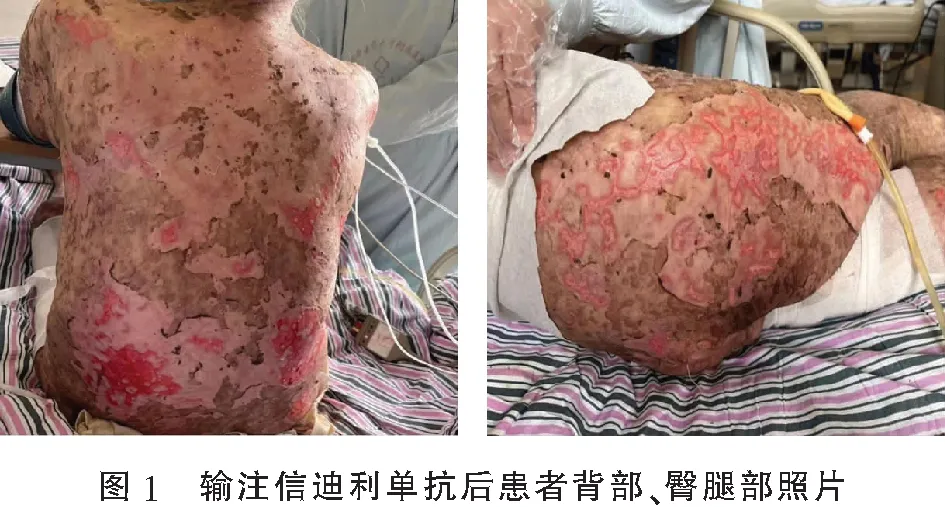
轉入后根據患者視診情況給與中藥辯證治療,犀角地黃湯與青蒿鱉甲湯涼血養陰,加味多皮飲利水消腫,方藥:水牛角20 g(先煎),生地黃15 g,赤芍10 g,牡丹皮10 g,青蒿10 g(后下),龜甲15 g,知母10 g,地骨皮10 g,五加皮10 g,桑白皮10 g,干姜皮10 g,大腹皮10 g,白鮮皮10 g,1日1劑,3次/d。5月31日至6月5日共行血漿置換5次,同時給予激素(起始劑量甲潑尼龍80 mg ivgtt q12 h),血漿置換停止后給予免疫球蛋白輸注,患者皮疹情況好轉,滲出減少,四肢及頭面部皮損基本已無滲出,于6月15日轉入腫瘤科繼續治療。后予以竹葉石膏湯辯證治療及逐漸減量激素治療,方藥:竹葉10 g,石膏30 g(先煎),黨參15 g,麥冬10 g,半夏10 g,甘草10 g,粳米10 g,1日1劑,3次/d。因患者胸腹部皮損面積大,滲出明顯,皮損區疼痛粘連明顯,為預防感染每日更換一次鈦銀金屬防護隔離布,修剪結痂脫落死皮,兩次/d予利多卡因配制生理鹽水沖洗皮膚后再用碘伏全身皮損處消毒,消毒后為防止粘連用我院皮膚科自制紫草油(主要中藥成分有紫草、地榆等)涂擦,并予重組牛堿性成纖維細胞生長因子促進皮損愈合,至皮疹發生3周后患者情況逐漸好轉,皮膚基本痊愈。
經中西醫結合治療、血漿置換等等治療后,患者情況好轉,紅斑、水皰等基本消失,皮損處收口良好,療效顯著。見圖2。

2 討論
免疫治療為人類的健康及腫瘤的治療開辟了一個全新領域[3],通過調整免疫機制,重啟免疫監視,殺滅腫瘤細胞。尤其是程序性死亡受體1(programmed death receptor1,PD-1)和程序性死亡配體1(programmed death ligand 1,PD-L1)免疫檢查點抑制劑在腫瘤治療中取得了突破性進展[4]。
信迪利單抗Sintilimab是一種完全人Ig G4單克隆抗體,作用于PD-1及其配體。信迪利單抗是我國自主研發的免疫藥物,與其他PD-1抑制劑相比,Sintilimab具有相似的抗腫瘤作用,更好的安全性和經濟優勢[5]。同時,中國臨床腫瘤學會(chinese society of clinical oncology,CSCO)2022年推薦:針對于晚期轉移性胃癌,在PD-L1 CPS<5或檢測不可及時,可考慮使用XELOX聯合信迪利單抗(1B類)[6]。
PD-1/L1抑制劑單藥或聯合其他治療方案能夠提高胃癌患者總生存率。但PD-1/L1抑制劑的臨床應用仍面臨諸多問題,例如PD-1/L1抑制劑聯合策略的選擇、尋找有效生物標志物、不良反應的管理等[7]。因此,在臨床上我們需要更多的關注此類藥物的不良反應和相應處置,盡可能減輕患者面臨的風險。
本文報告了1例信迪利單抗臨床應用階段發生的重癥藥疹(steven-johnson綜合征)的病例,通過中西醫結合綜合治療后得到緩解的案例。雖然藥品說明書中有關于出現steven-johnson綜合征的描述,但在臨床上2 h內出現如此嚴重反應的情況少有報道。
在免疫治療出現之前,晚期胃癌內科治療缺乏有效治療手段,且三線治療患者耐受性較差,Li等[8]報道晚期胃癌患者服用阿帕替尼19 d出現胃腸道出血穿孔。近年來,PD-1在晚期胃癌臨床實驗中表現突出,在東亞地區開展的多中心隨機對照3期臨床試驗ATTRACTION-2研究主要評估納武利尤單克隆抗體的療效,結果顯示,納武利尤單克隆抗體可延長總生存期,提示納武利尤單克隆抗體能對患者的遠期生存有益,該藥物于2020年獲得中國藥品監督管理局(NMPA)批準,成為國內晚期胃癌首個免疫治療藥物[9]。但免疫治療作為一種全新療法,在臨床上也面臨著一些新的問題,例如嚴重的不良反應。如何提高PD-1/L1抑制劑的有效率以及降低不良反應事件的產生也是目前胃癌免疫治療急需解決的問題。
本例患者第二程免疫治療后2 h即出現發熱及皮疹,給予指南[10]推薦糖皮質激素劑量治療,但病情無法控制,迅速加重,危及生命,如此嚴重的皮膚反應在首次使用信迪利單抗時并未出現,在內科治療效果不佳的情況下,及時使用血漿置換及皮膚科專科治療等,能救治該患者離不開多學科及時、準確的合作,中醫藥在本次診治過程中起到重要作用。重癥藥疹急性發作期中醫多辯證為毒入營血,氣血兩燔,為濕熱毒邪發于肌膚所致。在診治過程中使用青蒿鱉甲湯、犀角地黃湯與多皮飲加減合方。犀角地黃湯與青蒿鱉甲湯功在清熱養陰、涼血散瘀,方內青蒿擅清陰分之熱,水牛角涼血消斑,芍藥、丹皮清熱涼血、活血散瘀,生地、知母清熱養陰;另加多皮飲疏風和血、健脾除濕,方內大腹皮健脾利濕,干姜皮和胃固表,地骨皮、桑白皮瀉肺清熱,牡丹皮清熱散瘀,白鮮皮祛風除濕,五加皮利水消腫,“皆用皮者,因病在皮,以皮行皮”。三方合用,清熱、養陰、利水功效顯著,兩周后患者皮疹明顯好轉。重癥藥疹后期,熱毒傷陰,氣陰虧損,辯證后使用竹葉石膏湯以養陰清熱、益氣生津,方中竹葉、生石膏清熱瀉火,麥冬、黨參益氣養陰,半夏祛痰和胃,粳米、甘草健脾益氣,并配合院內制劑紫草油解毒消腫、化腐生肌,療效顯著。
免疫治療在腫瘤治療里如火如荼,隨著臨床試驗數據的進一步完善,免疫治療獲批更多的適應癥,臨床醫生在使用之前一定要做好處理免疫治療相關不良反應的準備,慎之敏之。

