腰動脈介入栓塞治療經皮內窺鏡下腰椎椎間盤切除術后腹膜后大出血1 例報告并文獻復習
王 波,吳曉明,舒錦爾,陳明高
金華市人民醫院放射科,金華 321000
近年來,經皮內窺鏡下腰椎椎間盤切除術(PELD)已成為一種治療腰椎椎間盤疾病的主要微創方法,因其創傷小、出血少、恢復快且對脊柱穩定性影響小,具有較高的患者接受度[1]。隨著PELD的適應證和臨床應用范圍的擴大,其圍手術期并發癥也成為亟需重視的問題。腹膜后大出血是PELD術后罕見但又極其兇險的并發癥,該并發癥的處理對于微創外科來說是一個非常棘手的問題[2]。本研究回顧性分析本院1 例PELD 術后腹膜后大出血并行腰動脈介入栓塞治療患者的臨床資料,同時檢索有關PELD 術后并發腹膜后大出血的相關文獻進行系統性復習,旨在提高臨床對該并發癥的重視,并對其處理提供參考。
1 病例資料
患者,男,82 歲,因反復左腰臀部及左下肢麻木疼痛3 個月余,加重伴不能站立1 周于2022 年8 月9 日入住本院脊柱外科。入院體格檢查:血壓130/76 mmHg(1 mmHg=0.133 kPa),生命體征穩定,腹軟,無壓痛、反跳痛,肝脾肋下未及,雙腎區無叩擊痛,雙下肢無水腫;腰椎活動受限,左腰臀部及左下肢麻木疼痛,不能站立,右下肢肌力5 級,左下肢肌力4 級,左側小腿及左足感覺差,雙側足背動脈搏動正常。影像學檢查:腰椎CT 及MRI 示L3/L4/L5椎間盤向左后方突出,相應水平左側神經根受壓。實驗室檢查:血紅蛋白120 g/L、白細胞計數8.5×109/L、中性粒細胞百分比60%、血小板計數154×109/L、凝血酶原時間11.40 s、纖維蛋白原2.5 g/L。完善相關檢查并排除手術禁忌證后于2022 年8 月10 日行PELD,手術過程順利。術后3 h 患者訴左下腹部及左腹股溝區脹痛,左下肢放射性疼痛,左下肢肌力下降至3 級。查體發現患者左下腹部明顯膨隆,血壓降至101/59 mmHg,立刻予以急診血常規檢查,示血紅蛋白降至62 g/L,緊急予以輸注紅細胞懸液、血漿及補液等對癥支持治療;同時急診行全腹部CT 及腹主動脈CTA 檢查,示左側腰大肌周圍及腹膜后巨大血腫(圖1a、b),考慮為左側L3動脈損傷(圖1c)。輸注紅細胞懸液800 mL 后復查血紅蛋白為56 g/L,判斷非手術治療無效,立即與患者家屬溝通,告知腰動脈栓塞術的相關手術風險,患者及家屬理解并同意進行腰動脈介入栓塞術并簽署知情同意書,遂轉入介入科行急診局部麻醉下腰動脈介入栓塞術。
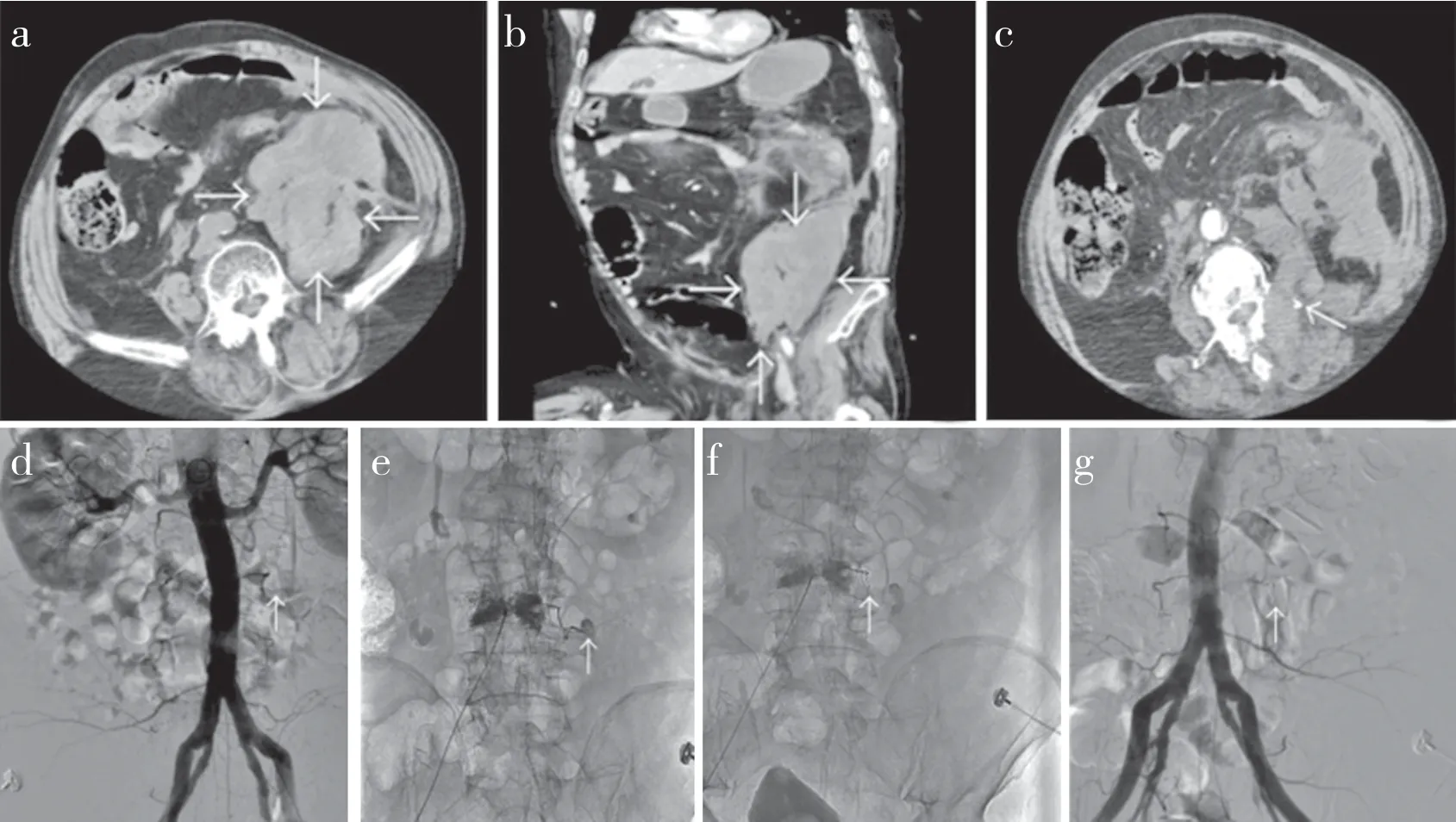
圖1 病例影像學資料
手術設備:數字減影血管造影機(DSA,飛利浦UNIQ FD2O,荷蘭);Mark V ProVis 高壓造影注射器(容量150 mL);穿刺套件(Terumo 公司,日本);5F pigtail導管(Cordis公司,美國)、5F RH導管(Cordis公司,美國);微導管、微導絲(ASAHI公司,日本);碘佛醇造影劑(江蘇恒瑞醫藥公司,中國)。栓塞材料:明膠海綿顆粒栓塞劑(粒徑150 ~ 350 μm,杭州艾力康公司,中國);栓塞彈簧圈(3 mm×12 cm,Boston Scientific 公司,美國)。
患者取平臥位,常規消毒、鋪巾,采用改良Seldinger法穿刺右側股動脈并置入5F血管鞘,送入5F pigtail導管至腹主動脈中段行腹主動脈造影,發現左側L3節段動脈遠端顯示欠佳,周圍少許造影劑外溢(圖1d),交換5F RH導管并導入Progret微導管超選擇性插入左側L3節段動脈再次造影,可見造影劑明顯外溢(圖1e),此時在出血點前方經微導管導入栓塞彈簧圈2枚并打入少量明膠海綿顆粒進行填充,再次行左側L3節段動脈造影未見造影劑外溢,異常染色消失(圖1f、g)。拔除鞘管,股動脈穿刺點局部加壓包扎,術后返回病房。手術時間30 min,術中出血量約10 mL。患者術后心電監護示心率、血壓逐步恢復正常,血壓回升至122/68 mmHg,治療后12 h患者訴左下腹脹痛情況較前明顯好轉,壓痛明顯減輕。術前及術中共輸注紅細胞懸液約1 200 mL,術后第2天復查血紅蛋白為85 g/L,術后第3天復查血紅蛋白升至100 g/L,術后1周復查血紅蛋白為120 g/L,狀況明顯好轉。患者術后出現發熱,體溫最高達37.8℃,考慮為血腫吸收引起,予以物理降溫并口服布洛芬口服液10 mL,持續低熱3 d 后體溫降至正常。患者左下腹為彌漫型血腫(血腫量≥500 mL),考慮患者年齡偏大,術后生命體征穩定,未行剖腹血腫清除術,后期以非手術對癥支持治療為主。術后第14天患者左側小腿及左足感覺較前改善,左下肢肌力恢復至4 級,考慮為血腫吸收后對股神經的壓迫緩解。復查影像學資料示腹部血腫較前明顯吸收,未再發生出血。
2 討 論
自Yeung 等[3]首次將PELD 引入腰椎椎間盤突出癥的治療,PELD憑借其微創、安全及療效顯著的優勢,已成為治療腰椎椎間盤突出癥的重要術式,隨著手術適應證的擴大,臨床推廣應用的增多,其手術并發癥也亟需引起重視。PELD 術后并發癥以神經功能障礙、術中出血及術后血腫、硬膜撕裂最為常見[4-5]。其中以術中出血較為常見,反復穿刺使手術通道肌肉內出血、髓核鉗操作過程中損傷椎管內靜脈引起出血、關節突打磨成形過程中引起松質骨滲血是術中三大出血原因,一旦出現上述情況,射頻電極止血是最常用的有效止血措施[6-7]。
相比術中出血,術后腹膜后大出血罕見報道。2009 年,Ahn 等[8]報道了412 例PELD 術后有4 例(0.97%)患者并發腹膜后大出血,根據血腫量的大小將其分為彌漫型血腫(血腫量≥500 mL)和局限型血腫(血腫量< 500 mL),其中,局限性血腫多采取非手術治療,彌漫性血腫多采取開放手術治療,但未提及阻斷出血責任血管的有效治療措施。Kim等[9]報道了1 例PELD 術后巨大腰大肌血腫,術前CT 提示突出椎間盤與局部走行的腰動脈解剖關系密切,故術者認為可能是內窺鏡手術時損傷了腰動脈。分析本例患者腹膜后大出血原因,本研究組回顧了患者術后的增強CT 掃描,發現患者L3左側橫突有骨折征象,而腰動脈緊貼腰椎椎體橫行,考慮到術中操作較暴力,加上患者高齡,血管脆性增加,損傷左側橫突的同時很容易造成其旁邊的腰橫動脈損傷,與Kim 等[9]的分析一致。
PELD 術后大出血可采用非手術治療,但因為患者凝血功能的差異,以及在對大血腫手術清除的過程中很難確保非手術治療能防止再出血的發生,可能導致患者因失血性休克而危及生命。為防止繼續出血及血腫進一步增大,穩定患者血容量,應科學選擇積極有效的干預手段。王華峰等[10]對血流動力學穩定且血腫較小、未進行性增大的腹膜后血腫患者采用非手術治療,血腫可自行吸收;對于血腫導致神經功能進行性受損者,依據具體情況選擇手術方式行血腫清除并進行神經根探查術;對于血流動力學不穩或存在凝血功能障礙且血腫進行性增大的患者,在DSA下發現明確出血點并進行栓塞治療則更為合理。一般不考慮單純外科開放血腫清除術,因為外科手術治療腰動脈大出血比較困難且創傷較大。單純開放性外科手術探查常常因為出血部位不容易分離暴露或動脈攣縮而難以找到出血點,且腹膜后探查會減弱周圍組織對血腫的包裹作用,也會進一步加重出血。鐘軍等[11]的研究表明,PELD手術過程中應注重細節,術前通過MRI和CT等影像學檢查評估患者椎間孔周圍情況,制訂合理的手術計劃,提高穿刺準確度,減少不必要的操作,可以明顯降低血管損傷的風險;椎間孔周圍血管豐富,盡量減少不必要的組織剝離也可明顯降低出血風險。
綜上所述,PELD 術后腹膜后大出血是一種罕見又兇險的并發癥,多因手術過程中損傷椎間孔區域的腰動脈,術前應通過影像學檢查仔細評估術區血管情況,盡可能減少其發生。對于活動性出血的患者,血腫持續增大,DSA 下進行動脈造影以明確出血點并進行栓塞是最為直接、安全、有效的止血手段。對于凝血功能差、內外科治療存在局限性且無明顯介入手術禁忌證的患者,介入栓塞應該作為首選治療方法。

