不同濃度硫酸新霉素對生物絮團氨氮轉化速率及抗生素抗性基因的影響
楊逸尊,羅國芝,2,3,譚洪新,2,3
(1.上海海洋大學,上海水產養殖工程技術研究中心,上海 201306;2.上海市水產動物良種創制與綠色養殖協同創新中心,上海 201306;3.上海海洋大學水產科學國家級實驗教學示范中心,上海 201306)
近幾年來,抗生素抗性基因引起了越來越多的關注[1,2],而水產養殖行業被越來越多地認為是抗生素抗性細菌的重要來源和抗生素抗性基因的貯存庫[3]。宏基因組學分析表明,抗生素選擇壓力顯著影響了抗生素抗性基因譜的組成,顯著促進了抗生素抗性基因的富集,包括相應的和非相應的抗生素抗性基因類型[4]。形成各種抗生素抗性基因的共存組合,共同選擇多種抗生素耐藥性。ZHAO等[5]發現在同一種抗生素選擇壓力下,非對應抗生素抗性基因的豐度也升高,表明抗生素具有顯著的共選擇效應,表現出抗生素的特異型。
生物絮凝技術(biofloc technology,BFT)作為一種新興的養殖技術,其主體生物絮團主要是水體中的大量微生物、飼料糞便殘渣、有機碎屑和一些聚合物通過復雜作用相互絮凝而成的細菌團[6]。目前,國內外對于抗生素在生物絮凝養殖技術中的使用研究較少,而硫酸新霉素在各種養殖及水處理系統中的使用也鮮有關注,故本實驗選取了硫酸新霉素這種常用漁藥,來探究不同濃度硫酸新霉素對生物絮團水質處理能力及抗生素抗性基因的影響。水體中細菌對硫酸新霉素產生耐藥性共有三種途徑[7],其中最具普適性的就是由細菌自身產生修飾氨基糖苷類抗生素的酶,而這種修飾氨基糖苷類的酶又可以細分為三種,一種是以aph基因為代表的對氨基糖苷磷酸轉移酶進行編碼的抗生素抗性基因,一種是以aac基因為代表的對氨基糖苷乙酰轉移酶進行編碼的抗生素抗性基因,最后一種就是以ant基因為代表的對氨基糖苷核苷轉移酶進行編碼的抗生素抗性基因。本實驗選取了5種硫酸新霉素抗性基因,包含了三種類別的氨基糖苷修飾基因,為用藥后抗性基因的積累給出數據支持,也為抗生素在生物絮凝養殖技術中的使用提供參考。
1 材料與方法
1.1 實驗裝置與材料
實驗在上海海洋大學循環水養殖與工程實驗室內進行,實驗室為封閉空間,溫度設定為25 ℃。反應容器為10 L透明圓柱形塑料桶,使用功率為370 W的氣泵(森森集團股份有限公司,型號:HG-370)進行曝氣,氣石為球形石英曝氣石,置于反應容器中心使水體和空氣充分且均勻接觸。實驗用水經過提前24 h充分曝氣以去除水中殘留氯。絮團取自上海海洋大學循環水養殖與工程實驗基地未添加過抗生素的羅非魚養殖池,養殖密度約為20 kg/m3。添加的碳源為一水合葡萄糖(C6H12O6·H2O,分析純,含碳量為36.4%);使用的飼料為通威魚用膨化配合飼料(江蘇省宿遷市沭陽縣扎下鎮,粗蛋白為31.0%,碳含量為37.3%),實驗所用氯化銨(分析純,純度≥99.5%)及所有水質檢測使用試劑均采購自國藥集團化學試劑有限公司,所用抗生素均采購自合肥中龍神力動物藥業有限公司。
1.2 實驗設計與管理
實驗分為4組,每組三個平行,A組作為對照組不添加硫酸新霉素,B組添加0.02 g硫酸新霉素(休藥期500 ℃·d),C組添加0.04 g硫酸新霉素,D組添加0.12 g硫酸新霉素。添加的藥量根據硫酸新霉素的推薦使用量計算,其中B組為推薦使用量的一半,初始濃度為0.50 mg/L,C組為推薦使用量,初始濃度為1.00 mg/L,D組為推薦使用量的3倍,初始濃度為3.00 mg/L。4組接種絮團后調節TSS至315~330 mg/L,水體體積為8 L。
第一次加藥連續檢測每組投加10 mg/L氨氮(氯化銨溶液),實驗期間反應器加蓋并及時補充因蒸發流失的少量水分。實驗開始時水體堿度為355~375 mg CaCO3/L,當低于150 mg CaCO3/L時添加適量小蘇打以維持堿度。當所有組氨態氮以及亞硝態氮濃度降低并維持在0.5 mg/L以內時視為第一次連續監測實驗結束。維持系統培養直到休藥期結束,加藥進行第二次連續監測。
第二次加藥連續檢測每組投加10 mg/L氨氮(氯化銨溶液),實驗期間反應器加蓋并及時補充因蒸發流失的少量水分。實驗開始時水體堿度為265~285 mg CaCO3/L,當低于150 mg CaCO3/L時添加適量小蘇打以維持堿度。當所有組氨態氮以及亞硝態氮濃度降低并維持在0.5 mg/L以內時視為實驗結束。
1.3 水質及絮團指標的檢測方法
水質指標檢測先用注射器取10 mL絮團水樣,再通過0.22 μm針頭濾器(上海航歐機電設備有限公司,型號:Collins MCE 0.22 μm)過濾后進行檢測。檢測方法見表1,檢測儀器為分光光度計(上海優尼科儀器有限公司,型號:UV2000),總有機碳分析儀(島津制作所,型號:TOC-4200),多參數手提測試儀(德國WTW,型號:Multi 3430),105 ℃電熱鼓風干燥箱(上海一恒科學儀器有限公司),碳氮元素分析儀(德國Elementar vario max CNS),馬弗爐(協郝上海儀器科技有限公司,型號:SX2-4-10Y)。

表1 水質指標檢測方法Tab.1 Water quality index detection method
1.4 硫酸新霉素的檢測
水體中硫酸新霉素在第一次休藥期結束和第二次加藥3 d后從各組實驗水體中均勻抽取50 mL水樣,通過0.22 μm針頭濾器過濾后通過冰袋運送至上海微譜化工技術有限公司進行檢測。硫酸新霉素含量檢測方法由LC-MS/MS外標法測定。液相型號為:Waters 1-Class;質譜型號為:Waters TQS;色譜柱為:ACQUITY UPLcr HSS T3 1.8 μm;柱溫:35 ℃;進樣量:5 μL;流動相為:0.1%甲酸水溶液和乙腈;流速:0.4 mL/min。
1.5 生物絮團中抗生素抗性基因的采集與測定
在第二次連續監測實驗結束后從各組實驗水體中均勻抽取150 mL水樣,通過0.22 μm濾膜抽濾后,將抽濾在濾紙上的絮團放進10 mL透明無菌離心管中,用干冰保存第一時間送至上海生工生物工程股份有限公司進行抗生素抗性基因的檢測。
實驗所用引物通過Primer Premier 5.0軟件設計,表2為所用目的基因引物。

表2 本實驗所研究基因參考引物Tab.2 Reference primers for genes studied in this lab
1.6 生物絮團中異養細菌的生物群落估算
用稀釋平板計數法來測定生物絮團中的異養細菌的群落數量。在對接種絮團擴培之前及擴培實驗結束之后采集絮團水樣。在無菌操作臺中,取1 mL均勻水樣,根據菌群的大致數量用合適倍數的無菌生理鹽水進行稀釋。將各組稀釋后的菌液用殺菌消毒后的干凈三角玻棒均勻涂布在大豆酪蛋白瓊脂培養基上(杭州百思生物技術有限公司)。將均勻涂布后的平板放入恒溫生化培養箱中(上海精宏實驗設備有限公司,型號:SHP-250),設定溫度為35 ℃,培養時間為24 h。最后對培養之后的菌落進行計數,菌落數(CFU/mL)為平板上所有菌落數量再乘以稀釋倍數進行計算。
1.7 氨氮去除效率和氨氮去除速率及抗生素使用量計算公式
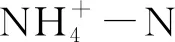
R=100%×(Ci-Ce)/Ci
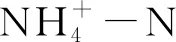
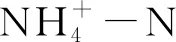
S=(Ci-Ce)/(T×t)
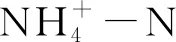
抗生素使用量計算公式:
M=ρ×V×Mi/k
式中,M為使用藥物的質量(g);ρ為養殖水體密度(kg/m3);V為實驗水體體積(L);Mi為抗生素藥物使用劑量(g);k為藥物有效成分含量(%)。
1.8 數據統計分析
實驗數據通過Excel2017軟件進行記錄和統計,由Origin Pro 2021和Graphpad Prism 9.0軟件繪制相關圖表。實驗數值用平均值(Mean±SD)形式表示,采用SPSS 22統計軟件對數據進行ANOVA單因素方差分析,P<0.05為差異性顯著。
2 結果與分析
2.1 實驗期間水質及絮團變化
在探究不同濃度硫酸新霉素對生物絮團氨氮轉化速率和抗生素抗性基因累積的效果前,對各個實驗組的水質指標進行檢測并無顯著差異,如表3所示。

表3 加藥之前4個組水質指標平均值、最小值和最大值Tab.3 Average,minimum and maximum values of water quality indicators in 4 groups before dosing
第一次加藥連續檢測水質變化如圖1所示,其中各組氨態氮變化如圖1(a)所示。4個組的氨態氮去除效率分別為99.80 %、99.70%、99.53%和99.29%;氨態氮去除速率分別為(3.88±0.02)mg TAN/(g TSS·h)、(2.22±0.03)mg TAN/(g TSS·h)、(2.17±0.04)mg TAN/(g TSS·h)和(1.72±0.02)mg TAN/(g TSS·h),氨態氮去除速率A組>B組>C組>D組。A組與其他三組去除速率有顯著差異,B組和C組的去除速率無顯著差異,D組與其他三組去除速率有顯著差異。

圖1 第一次加藥時4個組中三態氮(a,b,c)及溶解性有機碳(d)的變化圖Fig.1 Changes of tristate nitrogen(a,b,c)and dissolved organic carbon(d)in the four groups during the first dosing.
實驗期間4個組亞硝氮的濃度變化如圖1(b)所示,4個組的亞硝氮濃度變化趨勢總體一致,在實驗前4 h處于上升階段且在第4 h達到峰值,第4 h后A組和B組亞硝氮在第12 h下降到0.1 mg/L的低濃度水平,C組和D組亞硝氮分別在第16和18 h下降到0.1 mg/L的低濃度水平。
實驗期間4個組硝態氮的濃度變化如圖1(c)所示,4個組的硝態氮濃度在實驗結束后的濃度較實驗開始時均有下降,除C組外其余3組下降幅度不大,均在3.00 mg/L以內。
實驗期間4個組DOC濃度變化如圖1(d)所示,4個組的DOC均呈現下降趨勢,且總消耗量均在96.00至99.00 mg/L之間,各組無顯著差異。
在第一次連續監測前對4個組的TSS濃度進行了檢測,4組濃度分別為(315.00±3.00)mg/L、(315.00±2.00)mg/L、(325.00±2.00)mg/L和(315.00±1.00)mg/L。各組無顯著差異,連續監測結束后4組TSS濃度如圖2所示,各組TSS濃度較實驗開始前均有所下降,A組降至(210.00±14.51)mg/L;B組降至(243.33±18.93)mg/L;C組降至(252.00±26.73)mg/L;D組降至(238.67±14.64)mg/L。下降量A組>D組>B組>C組,A組與其余3組有顯著性差異。

圖2 第一次加藥結束4個組TSS濃度變化圖Fig.2 Changes of TSS concentration in 4 groups at the end of the first dosing
第二次加藥連續檢測水質變化如圖3所示,其中各組氨態氮變化如圖3(a)所示。4個組的氨態氮去除效率分別為99.70%、99.68%、99.73%和99.79%。4個組的氨態氮去除速率分別為(2.99±0.08) mg TAN/(g TSS·h)、(2.98±0.03) mg TAN/

圖3 第二次加藥時4個組中三態氮(a,b,c)及溶解性有機碳(d)的變化圖Fig.3 Changes of tristate nitrogen(a,b,c)and dissolved organic carbon(d)in the four groups during the second dosing
(g TSS·h)、(2.97±0.08)mg TAN/(g TSS·h)和(5.10±0.03)mg TAN/(g TSS·h),氨態氮去除速率D組>A組>B組>C組。D組與其他三組去除速率有顯著差異,A組、B組和C組的去除速率無顯著差異。
實驗期間4個組亞硝氮的濃度變化如圖3(b)所示,4個組的亞硝氮濃度變化趨勢總體一致,在實驗前4 h處于上升階段且在第4 h達到峰值,在第10 h下降到0.02 mg/L以下的低濃度水平。4個組硝態氮的濃度變化如圖3(c)所示,4個組的硝態氮濃度在實驗結束后的濃度較實驗開始時均有下降,但下降幅度均在2.00 mg/L以內。
實驗期間4個組DOC濃度變化如圖3(d)所示,4個組的DOC均呈現下降趨勢,且總消耗量均在90.00~94.00 mg/L之間,各組無顯著差異。
在第二次連續監測前對4個組的TSS濃度進行了檢測,4組濃度分別為(331.30±7.59)mg/L、(329.00±3.27)mg/L、(327.00±3.56)mg/L和(323.30±3.30)mg/L。各組無顯著差異,連續監測結束后4組TSS濃度如圖4所示,各組TSS濃度較實驗開始前均有所下降,A組降至(264.67±19.62)mg/L;B組降至(301.33±4.99)mg/L;C組降至(267.33±5.25)mg/L;D組降至(262.67±4.99)mg/L。下降量D組>A組>C組>B組,B組與其余3組有顯著性差異。

圖4 第二次加藥結束4個組TSS濃度變化圖Fig.4 Changes of TSS concentration in 4 groups at the end of the second dosing
各組連續檢測后絮團組分如表4所示,絮團VSS/TSS為B組>C組>A組>D組,B組與C組與A、D組呈顯著差異。粗灰分則為D組>A組>C組>B組,A組與D組無顯著差異,其余各組間均有顯著差異。粗蛋白各組無顯著差異。粗脂肪B組>C組>A組>D組,B組與其他各組呈顯著差異。
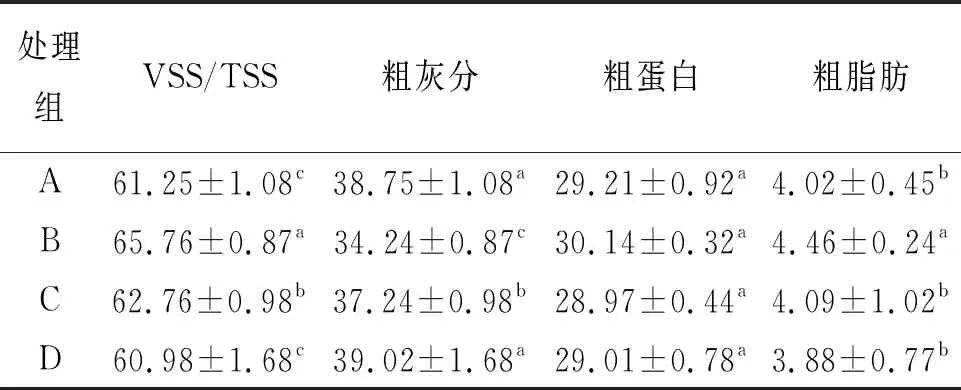
表4 實驗結束時絮團VSS/TSS、粗灰分、粗蛋白、粗脂肪的含量Tab.4 Contents of floc VSS/TSS,crude ash,crude protein and crude fat at the end of the experiment %
2.2 水體抗生素含量
在休藥期結束也就是第二次連續監測前和第二次連續監測結束后3 d對水體中的硫酸新霉素進行檢測,檢測結果如表5所示。4個組前后兩次均未在水體中檢測到硫酸新霉素的存在,或低于檢出閾值。

表5 休藥期結束時4組水體硫酸新霉素含量Tab.5 The contents of neomycin sulfate in the four groups of water at the end of the withdrawal period (mg/L)
2.3 生物絮團中抗生素抗性基因含量
在第二次連續監測結束后,對水體送樣檢測抗生素抗性基因,其中包含5種氨基糖苷類抗生素抗性基因和1種整合子基因。檢測結果如圖5所示,實驗結束后4個組的intl1的拷貝數分別為1.17×106copies/mL、6.51×105copies/mL、2.17×106copies/mL和2.13×106copies/mL,拷貝數C組>D組>A組>B組;4個組aadB的拷貝數分別為2.86×105copies/mL、2.13×105copies/mL、4.03×105copies/mL和6.17×105copies/mL,拷貝數D組>C組>A組>B組;4個組aph(3′)-Ia的拷貝數分別為7.10×103copies/mL、3.63×103copies/mL、3.01×104copies/mL和1.03×106copies/mL,拷貝數D組>>C組>>A組>B組;4個組aph(3′)-Ⅱa的拷貝數分別為3.43×103copies/mL、1.86×103copies/mL、2.17×104copies/mL和6.64×105copies/mL,拷貝數D組>>C組>A組>B組;4個組aac(6′)-Ⅰb的拷貝數分別為5.50×105copies/mL、3.25×105copies/mL、2.34×106copies/mL和4.00×106copies/mL,拷貝數D組>C組>A組>B組;4個組aac(3)-Ⅱ的拷貝數分別為7.04×103copies/mL、6.00×103copies/mL、1.53×104copies/mL和1.43×105copies/mL,拷貝數D組>>C組>A組>B組。

圖5 第二次加藥后4組6種抗生素抗性基因拷貝數Fig.5 Copy numbers of 6 antibiotic resistance genes in 4 groups after the second dosing
2.4 生物絮團中異養細菌生物群落數量
如圖6所示,在連續監測實驗結束后4個實驗組與初始水樣的異養菌生物群落數量相差較大,各組培養后菌群擴增量較大與初始組有顯著差異。連續監測實驗結束后,4個實驗組的異養菌群落數量為B組>C組>D組>A組。其中B組與A組、C組、D組有顯著差異,A組、C組和D組無顯著差異。

圖6 第二次加藥后初始和4個實驗組的異養菌數量Fig.6 The number of heterotrophic bacteria in the initial and 4 experimental groups after the second dosing
3 討論
3.1 不同濃度硫酸新霉素對生物絮團氨氮轉化的影響
通過第一次連續監測,直觀地看出硫酸新霉素的添加會對水體氨氮處理速率產生影響,硫酸新霉素的濃度越高影響越大,第一次加藥后的氨氮處理速率也就越低。但是通過一個休藥期的培養后,水體中的菌群對硫酸新霉素有了明顯的抗性,同樣的濃度再次添加已經無法對氨氮處理速率產生負面的影響,反而在添加了較高濃度硫酸新霉素的D組中,較高濃度的硫酸新霉素在不影響亞硝氮和硝氮轉化的情況下,促進了氨氮轉化的速率。這和LI等[15]使用四環素對生物膜系統對脫氮性能探究的結果相反。據推測,高濃度硫酸新霉素的選擇使菌群多樣性降低同時也對具有抗生素抗性的細菌大量富集,使之成為新的優勢種。在適應高濃度抗生素環境后,相關菌群恢復了其生態功能,且菌群數量較加藥前有所提升,最終使生物絮團對氨態氮的轉化速率提高。
3.2 不同濃度硫酸新霉素在生物絮團中累積情況
在對第二次連續監測前和第二次連續監測結束后3 d的水體進行采集送樣檢測發現,水體中的抗生素含量低于檢測閾值未能檢出或者已經被分解甚至轉移至絮團內部。這與LIANG等[16]在研究通過生物膜法去除抗生素抗性基因的時候對于水體中硫酸新霉素去除率的結果相似。這說明了生物絮團在適應抗生素環境后,能夠快速轉移和代謝水體中的硫酸新霉素。不過這也反映出,水體中硫酸新霉素并不能維持在所使用濃度條件下。那么在生物絮團中使用抗生素時,濃度的選擇要與常規養殖模式有所區別。
3.3 不同濃度硫酸新霉素對生物絮團抗生素抗性基因的影響
在對第二次加藥后的生物絮團進行抗生素抗性基因檢測后,發現了硫酸新霉素的添加對于aph(3′)-Ia、aph(3′)-Ⅱa、aac(6′)-Ⅰb、aac(3)-Ⅱ這四種硫酸新霉素抗性基因具有較大的選擇和富集的能力,尤其是aph(3′)-Ia、aph(3′)-Ⅱa和aac(3)-Ⅱ這三種基因隨著硫酸新霉素濃度的增加,基因拷貝數成倍上漲,呈現顯著的正相關。這與ZHAO等[17]在活性污泥反應器中使用不同種類抗生素得出的結果相似。但是本實驗中添加了0.5 mg/L硫酸新霉素的B組,在實驗結束后的所有抗生素抗性基因均低于未添加抗生素的A組,這與ZHAO等[17]和WAN等[18]的結論有所差異,推測原因可能是低濃度的硫酸新霉素對于絮團的選擇壓力較小,而B組的細菌群落數量有大幅增加,使對應的幾種抗生素抗性基因相對豐度降低。

