長吻苗種適宜圈養密度研究
張新福,楊 軍,何盛亮,黃路全,賈智明,徐聚臣,宗巍巍,呂亞兵,侯 杰,3,何緒剛,3
(1.華中農業大學水產學院,武漢 430070;2.湖北省宜昌市水產技術推廣站,湖北宜昌 443000;3.長江經濟帶大宗水生生物產業綠色發展教育部工程研究中心,武漢 430070)
綠色高效圈養模式(簡稱“圈養模式”)是由華中農業大學基于“時時打掃衛生”的理念提出,采用圈養裝備實現高效養殖并及時收集和處理養殖廢棄物的一種新型養殖模式[1],因其養殖效率高、“零排放”、產品優質、捕撈方便等突出優勢,倍受產業關注,推廣應用勢頭迅猛。長吻(Leiocassislongirostris),俗稱江團、肥魚、肥沱等,具有個體大、生長快、肉質細嫩、營養價值高、味道豐富鮮美、無肌間刺等諸多優點,是一種高價值的淡水名優品種[2]。當前長吻苗種培育以池塘培育為主,但池塘培育存在病害多發、餌料利用率低、存活率低等生產問題[3]。本研究在圈養模式下,探究3種不同養殖密度對長吻苗種生長性能、血清生化指標及非特異性免疫指標的影響,為長吻苗種適宜的圈養密度提供參考依據,同時為后期長吻成魚的生態、高效、健康養殖提供借鑒。
1 材料與方法
1.1 實驗條件
本養殖實驗在湖北省枝江市漁丫頭水產養殖專業合作社進行,養殖池塘面積為16 675 m2,平均水深為2.5 m,池塘內共架設60個圈養桶,其中9個圈養桶用于本試驗。實驗所用長吻苗種均為同一批人工繁育所得,規格整齊,生長良好。
1.2 實驗設計與飼養管理
1.3 生長數據采集與計算
存活率(SR)=100%(N0-Nt)/N0
增重率(WGR)=100%(Wt-W0)/W0
特定生長率(SGR)=100%(lnWt-lnW0)/t
體質量變異系數(CVw)=100%Ws/Wt
餌料系數(FCR)=FI/(Wt-W0)
攝食率(FR)=100%FI/[0.5(Wt+W0)×t]
肥滿度(CF)=100%Wb/L3
其中:W0(g)為魚體初始均重;Wt(g)為魚體終末均重;t為飼喂天數;FI(g)為尾均攝食量(濕重);Nt為死亡尾數;N0(g)為放養尾數;Wb(g)、L(cm)分別代表體重和體長,Ws(g)為體質量標準差。
1.4 血清樣品采集與處理
在30、60、90 d于每個重復隨機取5尾魚,用MS-222溶液麻醉后,用2.5 mL注射器進行尾靜脈取血,4 ℃下靜置2 h后,在3 500 r/min,4 ℃條件下離心15 min,取血清放于-80 ℃保存,用于生化、抗氧化及免疫指標測定。
1.5 血清生化、抗氧化及免疫指標的測定
血糖、總蛋白、白蛋白、膽固醇、總甘油三酯、谷草轉氨酶、谷丙轉氨酶、堿性磷酸酶在Selectra-xl型全自動生化分析儀(荷蘭威圖公司)上測定,試劑盒購自中生北控生物技術股份有限公司。血清抗氧化指標超氧化物歧化酶、過氧化氫酶、丙二醛及血清免疫指標溶菌酶、補體3、補體4均采用南京建成生物科技研究生產的試劑盒測定,操作步驟嚴格按照說明書進行。
1.6 數據整理與分析
實驗結果均采用平均值±標準差(Mean±SD)表示,用Excel對數據進行常規計算與統計,運用SPSS25.0軟件對各組數據進行單因素方差分析處理,P<0.05為差異水平顯著,并使用Origin2019繪圖。
2 結果
2.1 養殖密度對長吻苗種生長性能的影響
表1 90 d后不同密度組長吻苗種生長情況Tab.1 Growth of the juveniles of L.longirostris in different density groups after 90 days
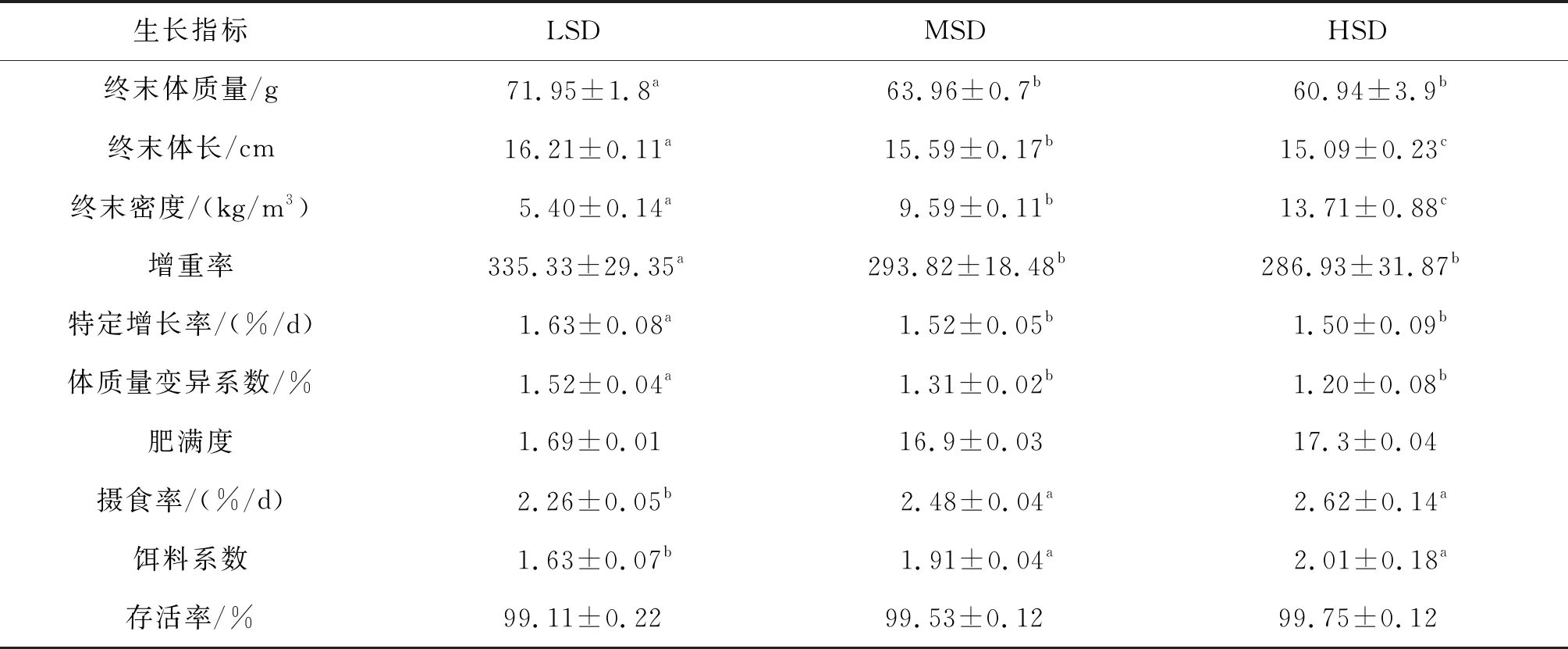
表1 90 d后不同密度組長吻苗種生長情況Tab.1 Growth of the juveniles of L.longirostris in different density groups after 90 days
生長指標LSDMSDHSD終末體質量/g71.95±1.8a 63.96±0.7b 60.94±3.9b終末體長/cm16.21±0.11a15.59±0.17b15.09±0.23c終末密度/(kg/m3)5.40±0.14a9.59±0.11b13.71±0.88c增重率335.33±29.35a293.82±18.48b286.93±31.87b特定增長率/(%/d)1.63±0.08a1.52±0.05b1.50±0.09b體質量變異系數/%1.52±0.04a1.31±0.02b1.20±0.08b肥滿度1.69±0.01 16.9±0.03 17.3±0.04 攝食率/(%/d)2.26±0.05b2.48±0.04a2.62±0.14a餌料系數1.63±0.07b1.91±0.04a2.01±0.18a存活率/%99.11±0.22 99.53±0.12 99.75±0.12
注:表中同行不同的上標字母表示組間差異性顯著(P<0.05)。下表同。

圖1 不同密度組下長吻苗種體質量和體長Fig.1 Body weight and length of the juveniles of L.longirostris under different densities不同字母表示組間差異顯著(P<0.05)。
2.2 養殖密度對長吻苗種血清生化指標的影響
血清總蛋白和白蛋白的含量均隨著養殖時間進行而逐漸升高,在90 d時,HSD組血清白蛋白和總蛋白含量顯著高于LSD、MSD組。血糖含量隨著養殖時間推移呈先升高后降低的趨勢,且各密度組間的差異不顯著;總甘油三脂和膽固醇水平隨著養殖時間而逐漸升高,且各密度組兩者均差異不顯著;血清中谷草轉氨酶含量變化較小,且差異不顯著;谷丙轉氨酶含量隨著養殖時間推進而升高,養殖后期其含量隨著養殖密度升高而降低,但不呈顯著性差異;LSD組堿性磷酸酶含量高于其余兩組,但差異不顯著,90 d各密度組堿性磷酸酶含量略有升高(表2)。
表2 各密度組長吻苗種血清生化指標Tab.2 Serum biochemical indexes of the juveniles of L.longirostris under different densities

表2 各密度組長吻苗種血清生化指標Tab.2 Serum biochemical indexes of the juveniles of L.longirostris under different densities
指標時間/d組別LSDMSDHSD血糖/(mmol/L)304.63±1.055.84±0.545.21±0.936011.20±1.239.44±0.269.53±1.84906.76±0.616.68±0.196.41±0.59膽固醇/(mmol/L)304.20±0.034.14±0.184.16±0.14604.76±0.264.52±0.314.64±0.12904.94±0.064.89±0.275.13±0.45總甘油三脂/(mmol/L)305.66±0.175.23±0.524.88±0.10607.44±1.166.44±1.6310.64±1.469010.68±0.858.91±1.1212.07±3.52總蛋白/(g/L)3024.39±2.9724.67±2.3525.49±0.396030.11±0.7329.74±2.3830.82±2.209037.37±1.40b38.32±1.31b43.44±3.58a白蛋白/(g/L)308.05±0.217.63±0.387.66±0.11608.29±0.247.91±0.308.61±0.51909.56±0.38b10.28±0.40b11.45±1.47a谷草轉氨酶/(U/L)30394.83±4.81383.60±10.57400.31±31.3160386.79±38.72360.83±26.30441.48±31.5790363.94±40.13384.40±16.16412.62±23.15谷丙轉氨酶/(U/L)3035.01±12.9524.90±6.5023.26±0.846055.40±18.7250.41±18.4792.22±13.6590129.58±12.47116.30±32.06113.08±14.09堿性磷酸酶/(U/L)30217.33±53.24161.00±20.22167.67±3.6860219.67±1.70184.33±48.61168.67±17.4490282.33±42.41197.67±20.43222.33±45.04
2.3 養殖密度對長吻苗種血清抗氧化及免疫指標的影響
血清超氧化物歧化酶、過氧化氫酶含量變化范圍較小,養殖密度對其影響也不顯著;丙二醛含量隨著養殖時間推進呈現先升高后降低的趨勢,90 d時,HSD組丙二醛含量顯著高于LSD、MSD組。溶菌酶含量隨著時間推進先升高后降低,60 d時溶菌酶含量約2倍于90 d,但各密度組間含量差異不顯著。補體3、補體4含量整體上隨時間呈升高趨勢,且隨著密度的增大而升高,但各密度組間差異不顯著(表3)。
表3 各密度組長吻苗種血清抗氧化及免疫指標Tab.3 Antioxidant and immune indexes in serum of the juveniles of L.longirostris under different densities
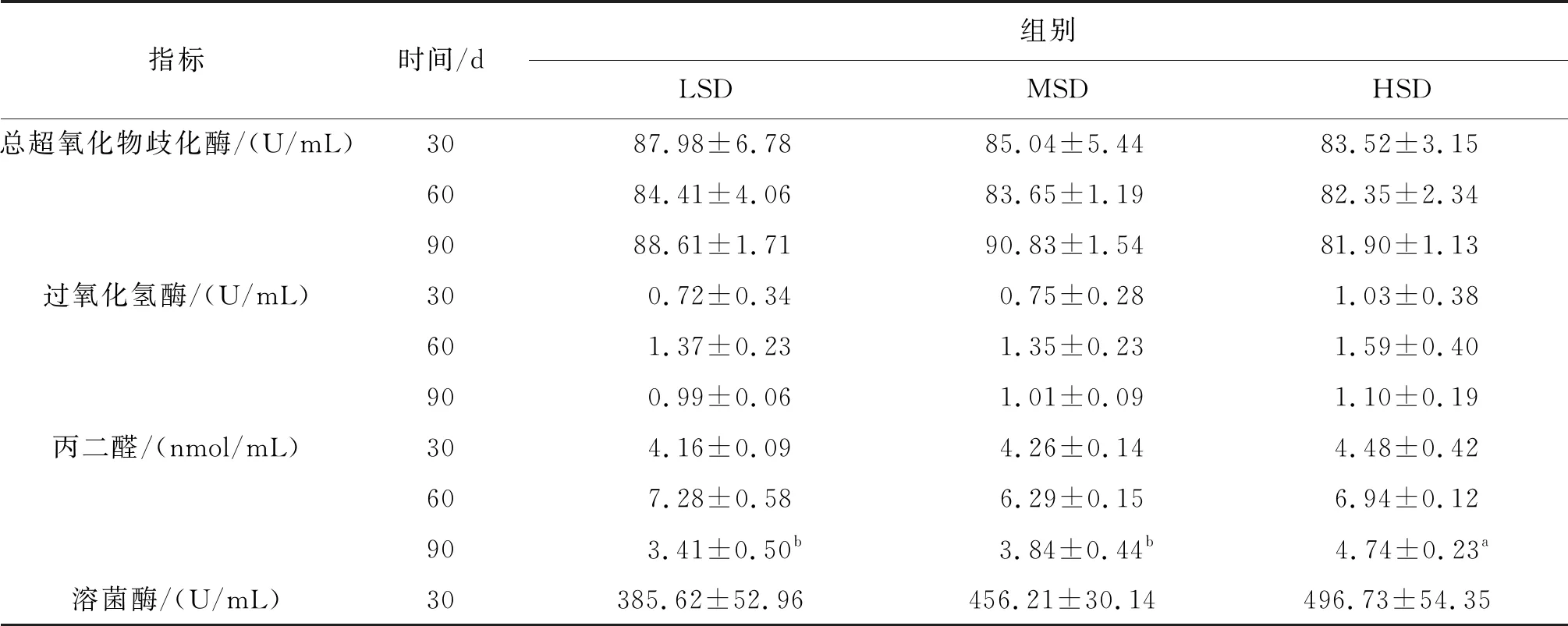
表3 各密度組長吻苗種血清抗氧化及免疫指標Tab.3 Antioxidant and immune indexes in serum of the juveniles of L.longirostris under different densities
指標時間/d組別LSDMSDHSD總超氧化物歧化酶/(U/mL)3087.98±6.7885.04±5.4483.52±3.156084.41±4.0683.65±1.1982.35±2.349088.61±1.7190.83±1.5481.90±1.13過氧化氫酶/(U/mL)300.72±0.340.75±0.281.03±0.38601.37±0.231.35±0.231.59±0.40900.99±0.061.01±0.091.10±0.19丙二醛/(nmol/mL)304.16±0.094.26±0.144.48±0.42607.28±0.586.29±0.156.94±0.12903.41±0.50b3.84±0.44b4.74±0.23a溶菌酶/(U/mL)30385.62±52.96456.21±30.14496.73±54.35
續表3
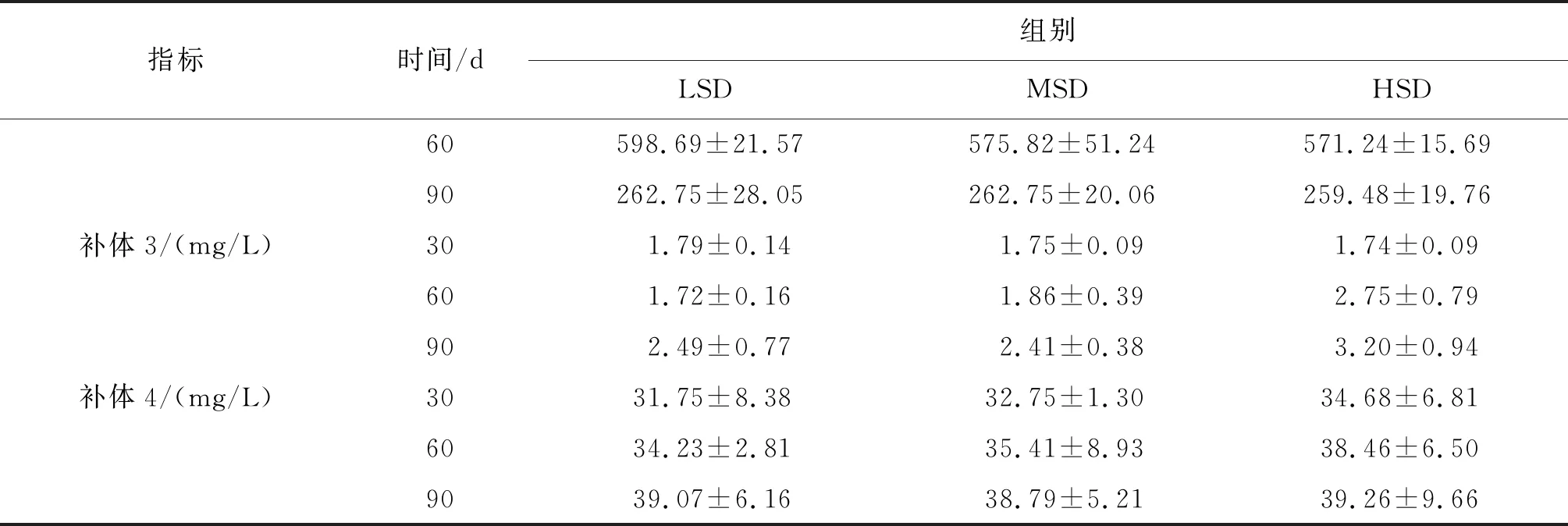
表3 各密度組長吻苗種血清抗氧化及免疫指標Tab.3 Antioxidant and immune indexes in serum of the juveniles of L.longirostris under different densities
指標時間/d組別LSDMSDHSD60598.69±21.57575.82±51.24571.24±15.6990262.75±28.05262.75±20.06259.48±19.76補體3/(mg/L)301.79±0.141.75±0.091.74±0.09601.72±0.161.86±0.392.75±0.79902.49±0.772.41±0.383.20±0.94補體4/(mg/L)3031.75±8.3832.75±1.3034.68±6.816034.23±2.8135.41±8.9338.46±6.509039.07±6.1638.79±5.2139.26±9.66
3 討論
3.1 養殖密度對長吻苗種生長性能的影響
養殖密度升高可導致魚類的生長性能降低,養殖密度越高對魚類生長的抑制作用越強[4]。有學者認為,養殖魚類為適應高密度的養殖環境,機體功能產生一系列的調節活動,一系列的調節活動需消耗大量能量,肝臟中的糖原等能源物質被大量分解,糖異生作用加強產生大量能量,導致用于生長的能量大幅減少抑制其生長[5]。在本試驗中,整體上長吻苗種體質量和體長隨著養殖時間進行而逐漸增大,且隨著密度的增大而逐漸降低,45 d之前(體質量<50 g),各密度間差異不顯著,45 d之后(體質量>50 g),LSD組顯著大于MSD、HSD組,MSD和HSD差異不顯著。增重率和特定生長率也與養殖密度呈負相關性,LSD組顯著大于MSD、HSD組。有學者認為多數魚類也存在社會行為,養殖密度是造成魚類表現社會行為的關鍵原因,過高或過低的養殖密度使魚類產生慢性脅迫,造成個體差異增加[6-8]。各密度組長吻苗種的體質量變異系數隨養殖密度升高表現為負相關性,說明低密度組長吻苗種個體差異更明顯。各密度組長吻苗種的攝食率和飼料系數均隨養殖密度的升高而升高,該結果表明養殖密度的增大降低了養殖魚類對餌料吸收和利用的效率;各密度組的苗種一直保持良好的食欲,且在短時間內吃完餌料,但高密度組的飼料系數大于低密度組,表明同樣進食了相等量的餌料,但LSD組可以更好吸收和利用飼料。肥滿度是一項常用的形體指標,反映的是魚類生長情況、能量儲存狀態和魚體肥瘦程度,肥滿度的下降通常被解釋為能量儲備的消耗,如儲存的肝糖原或體脂肪被消耗[9,10]。在本研究中,隨著養殖密度的升高肥滿度未表現出變化趨勢,說明本實驗設置的養殖密度未對長吻苗種的形體指標造成影響。各密度組死亡量相近,平均成活率均在99.11%以上,各密度組間差異不顯著,說明長吻苗種可以較好地適應本實驗的養殖密度范圍,高密度組的養殖密度也并未達到該規格下長吻臨界養殖密度。從生長性能方面看,為保證較高的生長速度,建議在養殖中后期(體質量約50 g)時降低養殖密度,控制在2 000~3 000 尾/圈為宜。
3.2 養殖密度對長吻苗種血清生化指標的影響
血液承擔著體內多種物質的運輸,同時也是機體代謝的主要調節途徑,健康的血液也是魚體行駛正常生理功能的前提條件,血液生化指標的變化一定程度上指示了機體組織器官的健康狀態[11-13]。血糖、血脂及血液蛋白質均可作為能源物質為機體提供能量,其三者在不同情況時可以相互轉化,被機體利用的順序也因種類不同而變化[14,15]。在本研究中,養殖密度對血糖、血脂影響不顯著,而血清總蛋白含量隨著養殖密度的增大而顯著升高,白蛋白含量變化趨勢也與總蛋白相同,血清中的白蛋白對維持血液的滲透壓平衡起著重要作用,是血液中含量最高的一種蛋白質,也是機體重要的免疫因子,抵御入侵機體的病原體和異物,也有修復受損組織的重要作用[16]。因此,持續作用的密度脅迫對長吻苗種產生了一定不利影響,高養殖密度脅迫作用對長吻苗種的組織器官造成了損傷,導致白蛋白得到相應的升高。血清酶的含量和活力變化趨勢反映了機體物質轉化和代謝情況,可以反映魚體生理狀態和健康狀況[17]。在正常條件下,轉氨酶主要存在于肝臟等的細胞內,一般血液中含量較低,當肝細胞損傷時,就被大量釋放到血液中,導致其含量顯著升高,因此兩種轉氨酶含量的高低指示了肝臟的健康狀態及蛋白質的合成和代謝正常與否[18]。在本研究中,谷丙轉氨酶含量隨著養殖密度的增大而呈升高趨勢,隨著養殖時間進行谷草轉氨酶含量變化不大勢,不同時期各密度組間差異不顯著,魚體應對養殖密度的不同發生相應的調整機制,高密度組肝臟細胞可能受到一定程度的損傷。堿性磷酸酶通常是一種肝臟功能和骨損傷的標志酶,在肝臟損傷或者功能障礙時可引起其含量升高。同時,堿性磷酸酶也直接參與機體新陳代謝中磷酸基團的代謝和轉移過程,在機體的物質代謝和免疫系統中發揮著關鍵功能[19]。在本研究中,堿性磷酸酶含量隨著養殖時間而略有升高趨勢,表明養殖后期高密度條件對機體肝臟功能產生了一定負面影響。從血清生化指標方面看,建議在養殖后期高密度組應降低養殖密度,控制在2 000~3 000 尾/圈為宜。
3.3 養殖密度對長吻苗種血清抗氧化及免疫指標的影響
高密度條件下魚體長期處于不利環境脅迫中,此時機體會產生大量的強氧化性的活性氧自由基,它是魚體內的重要的活性物質,完成體內各種生理生化的調節活動,但過量的氧自由基機體并不能及時清除,造成相應器官及機體的氧化損傷、機體對不良環境抵抗力降低,而活性氧自由基的消除則主要依賴于抗氧化系統發揮作用[20,21]。超氧化物歧化酶和過氧化氫酶是抗氧化物酶中兩種關鍵酶[22],超氧化物歧化酶是去除活性氧自由基的關鍵酶,主要將細胞內氧自由基轉化為過氧化氫和氧分子[23]。過氧化氫酶可將超氧化物歧化酶催化產生的過氧化氫催化分解為氧分子和水分子以降低過氧化氫的毒性[24]。在本試驗中,隨著養殖密度增加長吻苗種超氧化物歧化酶含量沒有顯著差異,高密度組過氧化氫酶含量在整個養殖周期均略高于中低密度組且差異不顯著,表明該條件下中低密度下長吻苗種的抗氧化系統處于正常狀態,機體沒有受到活性氧自由基的侵害,高密度組過氧化氫酶活性升高表明氧自由基濃度升高,相應細胞組織一定程度上被氧化毒害,脂質過氧化產物丙二醛含量也有所反映,丙二醛含量隨著養殖密度先升高后降低,30、60 d時各密度組間差異不顯著,90 d時高密度組丙二醛含量顯著大于低密度組,表明高密度脅迫使魚體內活性氧自由基含量增多,脂質過氧化反應增強,過量的自由基并沒有及時被清除,氧自由基就會直接攻擊細胞膜中的不飽和脂肪酸發生脂質過氧化反應,其分解反應產物則為丙二醛,因此丙二醛是用來評價細胞氧化損傷及肝臟和胰腺損傷程度的重要指標。
魚類非特異性免疫因子主要由溶菌酶、補體及干擾素等構成[25,26]。溶菌酶是存在于許多魚類的體表黏液、腸道黏液、巨噬細胞和血清中的水解酶,是一種堿性蛋白質[27],其通過破壞細菌內外滲透壓平衡導致細菌細胞膜破裂,從而達到免疫防御作用[28,29]。補體是魚類抵抗外界不良生存環境的重要成分,具有溶菌、殺菌及免疫吸附等的作用[26,30],補體3是補體激活旁路中的關鍵成分,補體4在經典途徑中發揮重要作用,兩者含量可以一定程度上顯示機體免疫病理性受損的情況[31,32]。本研究中,溶菌酶含量呈現先升高后降低趨勢,補體3、補體4含量均是呈升高趨勢,且各密度間差異不顯著,表明養殖密度對溶菌酶、補體3、補體4水平影響較小,對非特異性免疫系統影響不顯著,長吻苗種可以通過生理調節適應擁擠脅迫。從血清抗氧化指標方面看,建議在養殖后期高密度組應降低養殖密度,控制在2 000~3 000尾/圈為宜。

