肺炎支原體肺炎并發塑型性支氣管炎患兒的臨床特征及危險因素分析
高蘭芳 李蕾 管仁政 王芳 毛成剛 郭興青 曲政海
(1 青島大學附屬醫院兒科,山東 青島 266555; 2 中國人民解放軍聯勤保障部隊第九七〇醫院)
塑型性支氣管炎(plastic bronchitis,PB)是指由不同原因導致氣管或支氣管內形成長短不一、密度較高的樹枝樣膠凍狀塑型物的一種肺部疾病,屬于少見的急性危重疾病,發病機制迄今尚不明確[1]。由于阻塞范圍及程度不同,PB可引起患者肺通氣和(或)換氣功能障礙,臨床上可出現一系列不同的表現,如咳嗽、喘息、發熱、胸悶、胸痛等,嚴重者可發生急性呼吸功能衰竭進而危及生命[2]。肺炎支原體(MP)是引起PB的首位病原體,在患兒感染癥狀較輕時即可發生PB[3-4]。隨著支氣管鏡技術應用的日益普遍,有關MP感染并發PB患者的報道也越來越多。本研究通過分析肺炎支原體肺炎(Mycoplas-mapneumoniaepneumonia,MPP)并發PB患兒的臨床特征及危險因素,為其臨床診療提供參考。現將結果報告如下。
1 資料與方法
1.1 一般資料
選取2021年7月16日—11月6日于我院兒科行支氣管鏡檢查并確診為MPP的患兒作為研究的對象,根據支氣管鏡下是否取出塑型物,分為PB組和非PB組。患兒納入標準:①符合兒童MPP診治專家共識(2015年版)[5]中關于MPP診斷標準者;②支氣管鏡操作符合中國兒科可彎曲支氣管鏡術指南(2018年版)[6]中的規定;③6個月≤患兒年齡≤14歲,入院前病程5~30 d;④患兒家長簽署支氣管鏡檢查知情同意書。排除標準:①嚴重心律失常、出血性疾病、凝血功能障礙、心肺或肝腎功能不全、先天性免疫缺陷、先天性心臟病者;②合并細菌性肺炎、病毒性肺炎、肺結核、支氣管異物等其他呼吸道疾病者;③對治療藥物過敏或依從性差者;④有支氣管鏡檢查禁忌證者。最終納入研究的患兒共有75例,PB組21例,非PB組54例,兩組患兒的一般資料比較無明顯差異(表1)。

表1 兩組患兒一般資料比較
1.2 觀察指標
①發熱指標:熱程、熱峰、發熱頻次;②實驗室檢查指標:白細胞計數、中性粒細胞計數、血小板計數、肺泡灌洗液(BALF)細胞分類檢測、紅細胞沉降率(ESR)及C-反應蛋白(CRP)、乳酸脫氫酶(LDH)、堿性磷酸酶(ALP)、降鈣素原(PCT)、D-二聚體、谷丙轉氨酶(ALT)水平;③胸部CT檢查結果;④支氣管鏡下表現;⑤支氣管塑型物的蛋白質質譜分析(由深圳華大基因研究院進行)。
1.3 數據處理
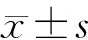
2 結 果
2.1 兩組患兒發熱表現及胸部CT檢查結果比較
兩組患兒熱程≥10 d的構成比、發熱頻次、肺實變構成比比較,差異具有顯著性(t=2.836,χ2=5.548、5.659,P<0.05),其他指標比較差異均無顯著性(P>0.05)。見表2。
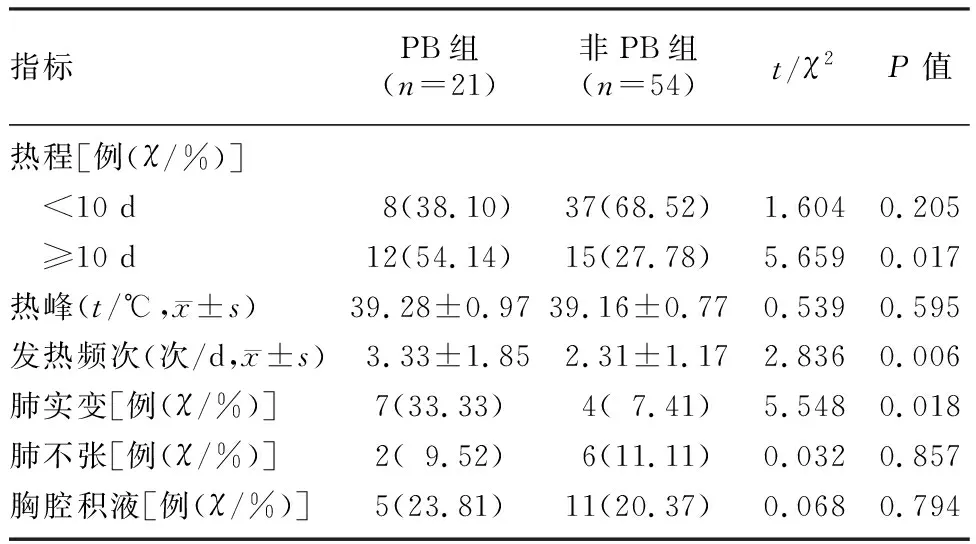
表2 兩組患兒發熱表現及胸部CT檢查結果比較
2.2 兩組患兒實驗室檢查結果比較
PB組患兒BALF中中性粒細胞比例、ESR及CRP、LDH、PCT、D-二聚體水平均顯著高于非PB組(t=2.290~3.793,Z=-2.085,P<0.05),其他指標比較差異均無統計學意義(P>0.05)。見表3。

表3 兩組患兒實驗室檢查結果比較
2.3 兩組患兒支氣管鏡檢查結果
PB組患兒堵塞部位以左下肺多見。在支氣管鏡下可見黏膜充血水腫以及糜爛,管壁皺縮、腫脹(圖1A);部分支氣管開口處有不同程度的炎性水腫、狹窄(圖1B);管腔內黏稠分泌物增多,阻塞部位可見灰白色分泌物(圖1C);可取出樹枝形膠凍狀支氣管塑型物,塑型物彈性較大不容易斷裂,長度約為2~5 cm(圖1D)。非PB組支氣管鏡下僅可見支氣管黏膜不同程度充血水腫。

A:左肺下葉支氣管黏膜充血、水腫、糜爛,B:右肺上葉支氣管開口處水腫、狹窄,C:左肺上葉支氣管管腔分泌物增多,D:樹枝形膠凍狀支氣管塑型物
2.4 導致MPP并發PB的多因素logistic回歸分析結果
將熱程(<10 d=0,≥10 d=1)、肺實變(否=0,是=1)、發熱頻次(否=0,是=1)、BALF中性粒細胞比例、ESR及CRP、LDH、PCT、D-二聚體水平作為自變量,以并發PB為應變量(否=0,是=1),行二元多因素logistic回歸分析,結果顯示PCT水平(OR=1.071,95%CI=1.015~1.130,P<0.05)和ESR(OR=1.088,95%CI=1.033~1.146,P<0.05)是MPP并發PB的獨立危險因素。見表4。

表4 MPP并發PB的多因素logistic回歸分析
繪制PCT水平及ESR的ROC曲線并計算曲線下面積(AUC),PCT水平的AUC為0.710,診斷靈敏度為0.524,診斷特異度為0.870;ESR的AUC為0.819,診斷靈敏度為0.952,診斷特異度為0.722。當患兒出現PCT水平≥0.19 μg/L或者ESR≥25.20 mm/1 h時,臨床上應警惕MPP并發PB的可能。見圖2、表5。
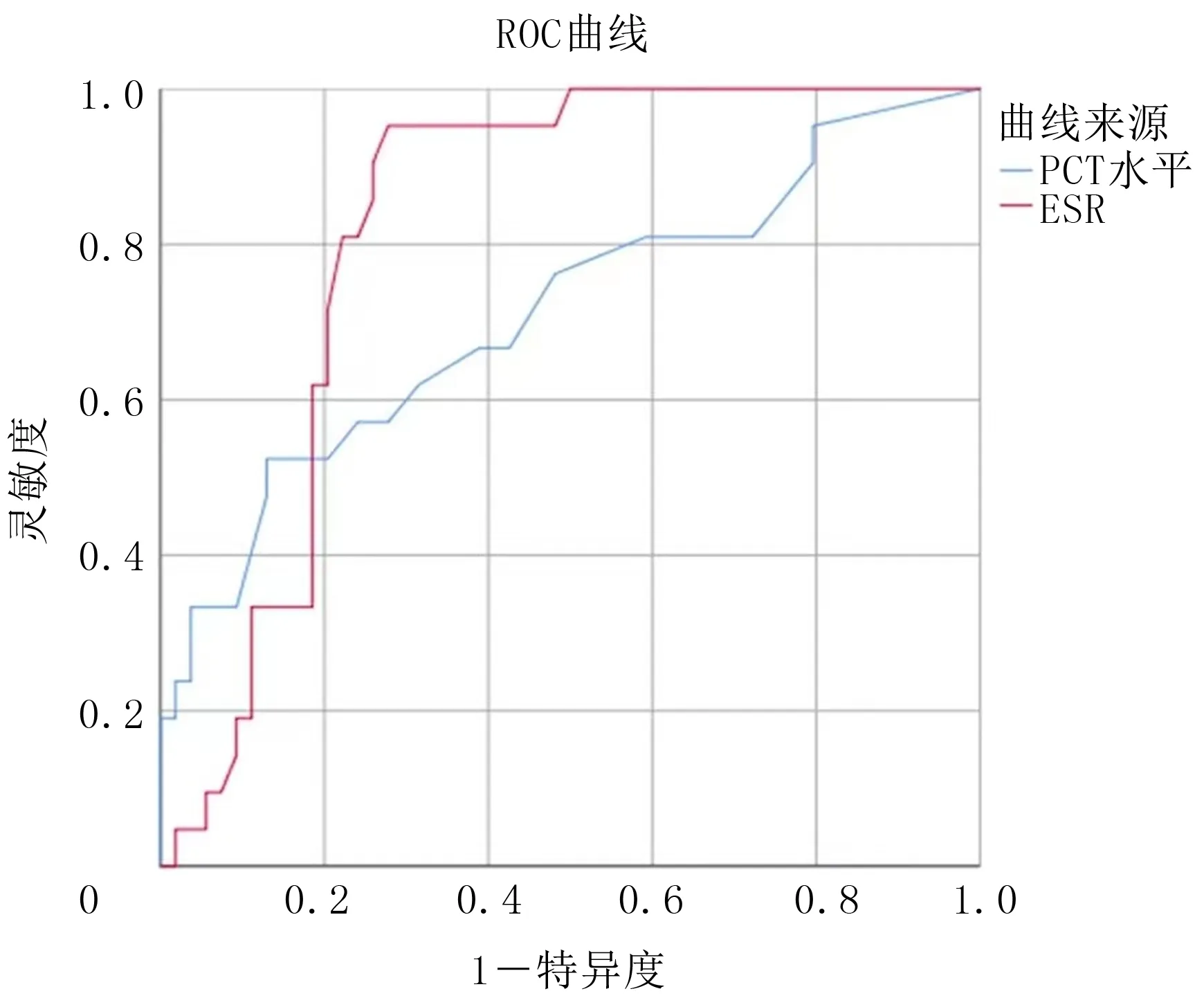
圖2 PCT、ESR的ROC曲線
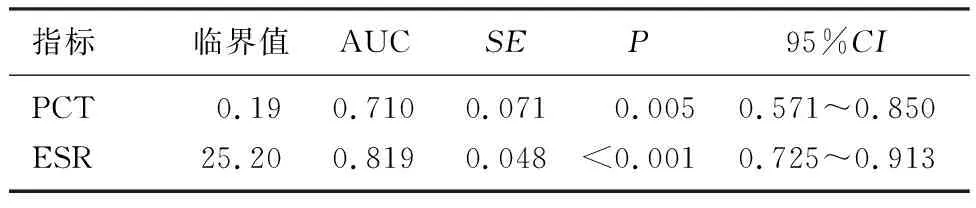
表5 PCT水平和ESR的ROC曲線結果分析
2.5 PB組患兒支氣管塑型物蛋白質質譜分析結果
PB組患兒支氣管塑型物蛋白質質譜分析結果顯示,患兒支氣管塑型物中含有豐富的纖維蛋白原(α、β、γ鏈)以及少量黏蛋白5B(MUC5B)、黏蛋白5AC(MUC5AC),此外還檢測到豐富的免疫細胞蛋白(免疫球蛋白γ、α、μ)及蛋白酶等。
3 討 論
目前我國MPP患兒的發病率逐年升高。部分MPP患兒病情進展快,早期表現為刺激性咳嗽,后期痰多不易咳出,經支氣管鏡檢查可見氣管內有局灶性或廣泛黏液增多,或分泌物阻塞形成管型,可取出樹枝樣支氣管塑型物[7-8]。本研究分析了MPP患兒并發PB的臨床特征及其危險因素,旨在為PB的早期診療提供依據。
既往文獻報道PB以4~12歲兒童高發[9],可能與兒童支氣管壁缺乏有力支撐、管腔中分泌物較難排出有關,年長患兒肺組織免疫反應更為強烈,故更易發生PB。本研究中PB組平均年齡為(6.33±1.82)歲,6歲及以上兒童占66.6%,以年長兒童為主,既往研究PB組平均年齡5.98~6.89歲,本研究與其相似[10-11]。PB組患兒以發熱、咳嗽起病為主,入院時多為高熱,發熱頻次和熱程≥10 d患兒構成比均大于非PB組,具有急性起病的特點。PB組患兒熱程長,MP感染后大量細胞因子和炎癥細胞浸潤肺上皮細胞,杯狀細胞增生,氣道水腫狹窄,持續免疫反應導致分泌物難以及時排除,從而增加了支氣管塑型物形成的風險。肺實變是支氣管塑型物形成過程中炎性滲出、壞死組織堆積的結果,本研究中PB組肺實變患兒構成比為33.33%,胸腔積液患兒構成比為23.81%(均為病變側少量積液),肺不張患兒構成比為9.52%。既往研究認為PB的影像學特征性改變是肺不張、胸腔積液[12-13],與本研究結果不符,推測可能MP感染后主要影響肺間質。MPP胸部影像學特征多變,不具有特征性,故而MPP影像學表現無特異性時亦不能忽視PB的發生。
CRP是在炎癥刺激后12~48 h內出現的一種急性時相非特異性反應蛋白,也是全身感染性炎癥反應的敏感指標,與MPP的嚴重程度呈正相關[14]。LDH也是一種非特異性炎癥標志物,與心肌細胞受損關系密切,在肺組織的表達水平低,但嚴重肺部感染時大量LDH可釋放入血。根據ZHANG等[15]的研究顯示,LDH與MPP的嚴重程度呈正相關。本研究中PB組患兒CRP、LDH水平均顯著高于非PB組,提示PB組患兒肺部炎性損傷更加嚴重。PB組患兒BALF中性粒細胞比例較非PB組更高,提示肺組織損傷時局部可存在活躍的炎癥反應。持續的炎癥反應可造成局部血管損傷,破壞血管內皮細胞的完整性,暴露細胞下膠原,激活凝血級聯信號通路,在凝血酶作用下纖維蛋白原形成纖維蛋白單體,繼而在Fa交聯下形成纖維蛋白凝塊,并堆積形成支氣管塑型物。纖維蛋白凝塊在纖溶酶的裂解下可產生D-二聚體,D-二聚體是纖維蛋白主要降解標志物,本研究中兩組患兒D-二聚體水平差異顯著,反映了PB時支氣管塑型物的形成,因此D-二聚體水平作為判斷MPP并發PB的指標也具有一定價值[16]。PCT水平能夠反應全身炎癥的活躍程度,與炎癥水平呈正相關,MP感染后誘導單核細胞、巨噬細胞增加PCT分泌,使其濃度上升造成細胞損傷,引起劇烈的免疫炎性反應[17]。ESR是一種非特異性炎癥指標,機體正常時維持較低水平,在炎癥反應刺激下表達水平顯著升高。PB患兒炎癥反應劇烈、支氣管塑型物形成等情況均可刺激ESR升高。本研究兩組患兒PCT水平和ESR均有顯著差異,且logistic回歸分析結果顯示,PCT水平≥0.19 μg/L和ESR≥25.20 mm/1 h為MPP合并PB的獨立危險因素,這與張嶸等[10]報道的MPP并發PB的危險因素為CRP、D-二聚體水平不同。
PB發生時,纖維蛋白原在凝血酶作用下轉化為纖維蛋白時形成不溶性凝塊或凝膠,形成支氣管塑型物[18]。目前國內大致公認支氣管塑型物從病理上分為兩型[19],其中Ⅰ型(炎癥型)塑型物主要由纖維組織及浸潤密布的嗜酸性粒細胞組成,Ⅱ型(無細胞型)塑型物則由黏蛋白及少量單核細胞組成。本研究中支氣管塑型物蛋白質質譜分析亦顯示其含有豐富的纖維蛋白原,考慮為Ⅰ型。HEATH等[20]和RACZ等[21]曾報道先心病患兒支氣管塑型物屬于Ⅰ型,SEEAR等[19]報道的病理特點則與之不符。本研究認為,肺部感染時形成的支氣管塑型物主要由纖維蛋白構成,考慮到MUC5B和MUC5AC是人氣道常見分泌物,故不排除本研究中檢測到的黏蛋白主要來源于非支氣管塑型物。既往研究認為,支氣管塑型物形成途徑可能為MPP異常激活凝血纖溶系統,導致多種細胞因子過度反應引起炎癥風暴,纖維蛋白原在凝血酶、Fa作用下使大量纖維蛋白交聯形成纖維蛋白凝塊,中性粒細胞和壞死細胞伴隨纖維蛋白凝塊聚集,最終則導致支氣管塑型物的產生[22-23]。
綜上所述,本研究表明ESR≥25.20 mm/1 h以及PCT≥0.19 μg/L均可作為MPP并發PB的預測指標,監測MPP患兒的上述指標有助于臨床醫師對PB的及早識別及診治。MPP并發PB患兒的支氣管塑型物含有大量纖維蛋白,其可能與炎癥反應引起的凝血-纖溶系統異常激活相關,但有待進一步研究驗證。
倫理批準和知情同意:本研究涉及的所有試驗均已通過青島大學附屬醫院醫學倫理委員會的審核批準(文件號QYFYWZLL26695)。所有試驗過程均遵照《臨床試驗質量管理規范》的條例進行。受試對象或其親屬已經簽署知情同意書。
作者聲明:高蘭芳、李蕾參與了研究設計;高蘭芳、李蕾、管仁政、王芳、毛成剛、郭興青、曲政海參與了論文的寫作和修改。所有作者均閱讀并同意發表該論文,且均聲明不存在利益沖突。

