艾塞那肽對2型糖尿病患者血脂譜及腎臟功能的影響
張倩,吳偉華
(信陽市中心醫院 全科醫學科,河南 信陽 464000;2.深圳市羅湖區人民醫院 全科醫學科,廣東 深圳 518000)
糖尿病(diabetes mellitus,DM)是最嚴重的全球健康問題之一。血脂紊亂和DM 相關的并發癥之間的關系一直是熱議的話題。70%的DM 患者至少有一種血脂異常[1]。血脂異常是DM 患者心血管疾病發病率和死亡率的一個重要的預測指標。糖尿病腎病是終末期腎衰竭的主要原因,超過三分之一的2 型糖尿病(type 2 diabetes mellitus,T2DM)患者有腎功能損害。GLP-1 受體激動劑是治療T2DM 的新型藥物;有研究發現GLP-1 受體激動劑不僅可以調節血糖,而且可以改善脂代謝、肥胖等多種代謝紊亂[2]。迄今為止,臨床研究中多見的是關于GLP-1 受體激動劑與糖尿病大血管病變的關系[3],而其對微血管病變的改善作用卻罕見報道。因此,本研究旨在探討GLP-1 受體激動劑艾塞那肽在治療T2DM 時對血脂代謝及腎功能的改善,為糖尿病大血管及微血管并發癥的防治提供新的思路。
1 資料與方法
1.1 一般資料
選取2020 年10 月至2022 年6 月于信陽市中心醫院內分泌科住院及門診就診的未使用降糖藥物治療的T2DM 患者96 例,根據隨機數字表將所有患者分成二甲雙胍組(n=48)和艾塞那肽組(n=48)。艾塞那肽組男27 例,女21 例,年齡(44.9±9.6)歲,病程(5.1±2.4)年,其中高血壓病12 例,吸煙8 例,脂肪肝32 例,動脈粥樣硬化28 例;糖尿病腎病(3 期以上)32 例。二甲雙胍組男29 例,女19 例,年齡(48.3±7.9)歲,病程(5.7±3.7)年,其中高血壓病14 例,吸煙10 例,脂肪肝28 例,動脈粥樣硬化26 例,糖尿病腎病(3 期以上)28 例。兩組性別、年齡、糖尿病病程、體重、腰圍、BMI、血糖、HbA1c、血脂、腎功能等一般資料比較,差異無統計學意義,(P>0.05),具有可比性。
納入標準:T2DM 的診斷均符合世界衛生組織(WHO)1999 年頒布的診斷標準,分型則采用美國糖尿病學會(ADA)2003 年標準。排除標準:①急性應激事件及慢性疾病史;②其他內分泌系統疾病史;③血肌酐清除率<60 mL/min;④腫瘤、妊娠或哺乳期婦女;⑤嚴重便秘;⑥胰腺炎病史;⑦各種遺傳疾病史。
1.2 觀察方法
1.2.1 資料采集 記錄臨床資料包括:年齡、性別、既往史、體重、身高、腰圍、體重指數(body mass index,BMI)、空腹血糖(fasting plasma glucose,FPG)、糖化血紅蛋白(hemoglobin A1c,HbA1c)、空腹血清C 肽和胰島素、總膽固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、高密度脂蛋白膽固醇(high-density lipoprotein cholesterol,HDL-C)、低密度脂蛋白膽固醇(low-density lipoprotein cholesterol,LDL-C)、載脂蛋白A-1(apolipoprotein A-1,ApoA-1)、載脂蛋白B(apolipoprotein-B,ApoB)、血尿酸、血肌酐、24 h 尿微量白蛋白(microalbunminuria,MAU)、腎小球濾過率(estimate glomerular filtration rate,eGFR)及尿β2 微球蛋白。腰圍測量取腰部肋下緣與髖骨上緣之中點的周徑,臀圍經恥骨聯合水平測量臀部最大周徑。受試者測定時只穿貼身衣褲。胰島素抵抗指數(HOMA-IR)計算公式:HOMA-IR=[空腹胰島素(FINS)(mU/L)×FPG(mmol/L)]/22.5。腎小球濾過率(eGFR)計算公式:eGFR=175×(Cr÷88.4)-1.234×年齡-0.179[mL/(min·1.73 m2)](女性×0.79)。
1.2.2 實驗材料及試劑 血清TC、TG、HDL-C、LDL-C、ApoA-1、ApoB、血肌酐、血尿酸檢測應用美國Beckman 有限公司提供的AU5800 全自動生化分析儀;HbA1C 檢測采用HPLC 法(試劑盒由美國Bio-Rad 公司提供);空腹血清C 肽及胰島素檢測采用熒光磁微粒酶免法測定(試劑盒由日本Tosoh 公司提供);24 h MAU 測定采用散射比濁法(試劑盒由西門子醫學診斷產品有限公司提供);尿β2 微球蛋白測定采用免疫比濁法(試劑盒由西門子醫學診斷產品有限公司提供)。
1.2.3 用藥及隨訪 艾塞那肽組連續使用艾塞那肽(商品名:百泌達;生產廠家:Baxter Pharmaceutical Solution LLC)12 周,起始劑量為皮下注射5 μg,每日2 次,治療1 月后如無不適增加至皮下注射10 μg,每日2 次,增量后不良反應嚴重者改回皮下注射5 μg,每日2 次,若仍無法耐受則停止用藥。二甲雙胍組使用二甲雙胍(商品名:格華止;生產廠家:中美上海施貴寶制藥有限公司)起始劑量為口服500 mg,每日2 次,根據患者血糖調整劑量,最大劑量為2 000 mg/d。
所有臨床觀察對象于治療前及12 周末均行資料采集。用藥4 周內每周電話隨訪1 次,用藥5~8周每4 周電話隨訪1 次。
1.2.4 不良事件記錄 記錄實驗對象出現的惡心、嘔吐、便秘、腹瀉、頭暈、皮疹以及其他各種不適感,將血糖低于3.9 mmol/L 確定為低血糖。
1.3 統計學方法
采用SPSS17.0 統計軟件進行數據分析處理。計量資料采用均數±標準差()表示,符合正態分布的計量資料組內比較用配對樣本t檢驗,組間比較用獨立樣本t檢驗;24 h 尿微量白蛋白、尿β2 微球蛋白及HOMA-IR 非正態分布經對數轉化符合正態分布的計量資料。P<0.05 為差異有統計學意義。
2 結果
2.1 不良反應事件
在觀察期間未發現低血糖事件。艾塞那肽組有4 例出現輕度惡心、腹脹等胃腸道不良反應,通過調整飲食后均能耐受;有1 例患者出現便秘,給予開塞露治療能耐受。有1 例患者由于注射部位出現過敏性皮疹,停用艾塞那肽,改用口服降糖藥物降糖。有1 例患者因頭暈不能耐受,停用艾塞那肽,改用其他降糖方案。有2 例因嚴重的惡心嘔吐,調整飲食及對癥治療后仍不能耐受,停用艾塞那肽,改為其他降糖方案。二甲雙胍組有2 例患者出現嚴重的惡心嘔吐,患者不能繼續服用,改用其他降糖口服藥,有2 例患者因為嚴重的腹瀉,改用其他口服降糖藥物。
2.2 艾塞那肽組治療前后對比觀察
體重、腰圍、FPG、BMI、HbA1c、TG、TC、LDL-C、ApoB、血尿酸、血肌酐較治療前明顯下降,差異有統計學意義(P<0.05);HDL-C、ApoA-1、空腹C 肽和空腹胰島素較治療前明顯升高,差異有統計學意義(P<0.05)。HOMA-IR 較治療前有明顯改善,差異有統計學意義(P<0.05)。eGFR 較治療前有明顯升高,差異有統計學意義(P<0.05)。24 h 尿微量白蛋白和尿β2 微球蛋白較治療前有明顯的降低,差異有統計學意義(P<0.05)。見表1。
表1 兩組治療前后臨床資料比較()
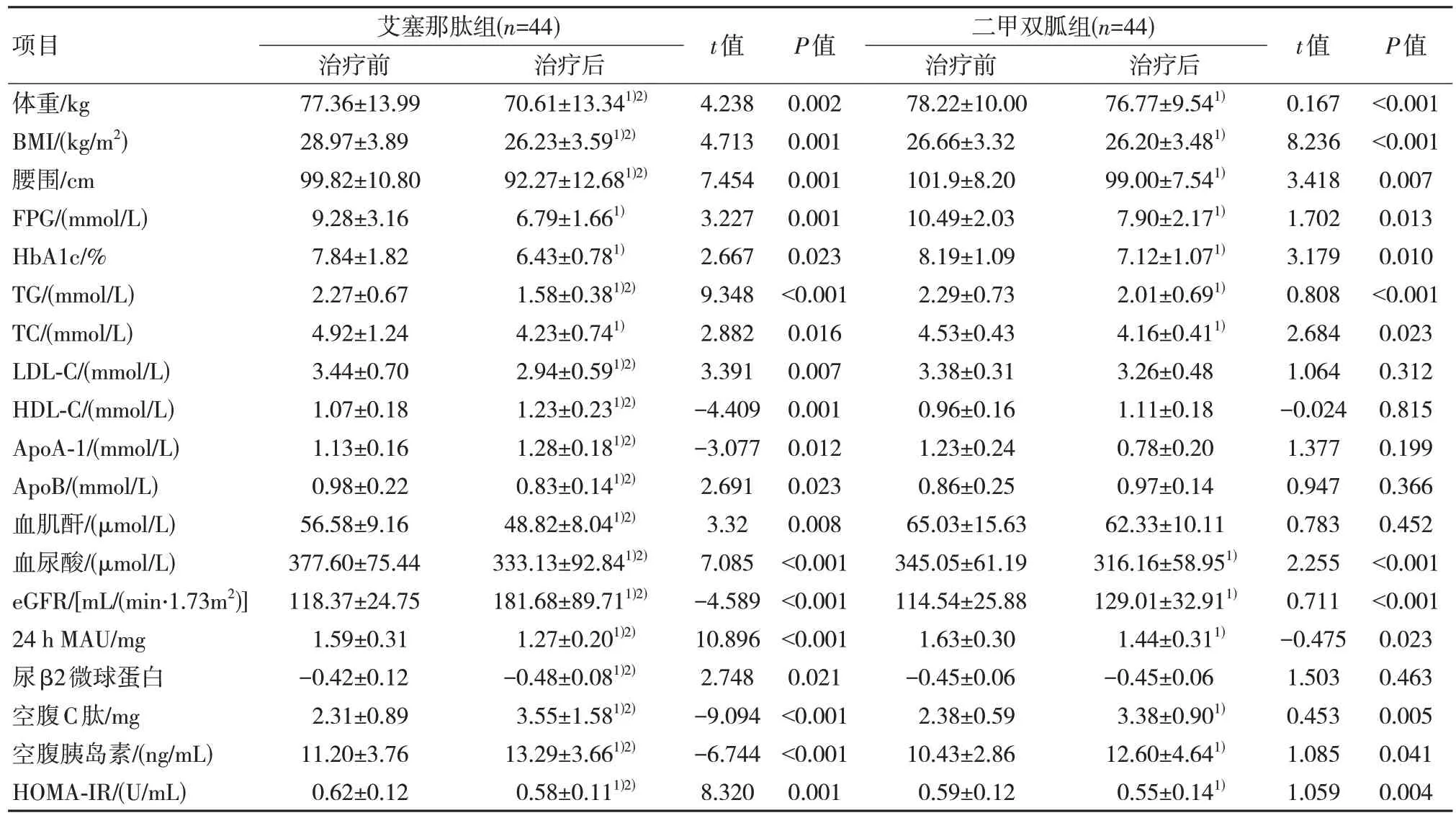
表1 兩組治療前后臨床資料比較()
注:1)與治療前比較,P<0.05;2)與二甲雙胍組比較,P<0.05。
2.3 二甲雙胍組治療前后對比觀察
體重、腰圍、FPG、BMI、HbA1c、TG、TC、血尿酸、HOMA-IR 均較治療前明顯下降,差異有統計學意義(P<0.05),空腹C 肽、空腹胰島素和eGFR 較治療前明顯升高,差異有統計學意義(P<0.05);24 h 尿微量白蛋白較治療前降低,差異有統計學意義(P<0.05),而HDL-C,LDL-C、ApoA-1、ApoB、血肌酐、尿β2 微球蛋白差異無統計學意義(P>0.05),見表1。
2.4 兩組單藥治療12 周后療效比較
與二甲雙胍組相比,治療后艾塞那肽組HDL-C、ApoA-1,空腹C-肽、空腹胰島素、eGFR 升高更明顯,差異有統計學意義(t=-3.892,-2.277,0.589,0.776,1.763,P均<0.05);體重、BMI、腰圍、TG、LDL-C、ApoB、HOMA-IR 降低更明顯,差異有統計學意義(t=6.272,0.019,6.625,1.512,1.383,0.711,0.904,P均<0.05);血尿酸、血肌酐、24 h尿微量白蛋白、尿β2 微球蛋白降低更明顯,差異有統計學意義(t=1.061,2.983,-2.941,-0.489,P均<0.05);兩組FPG、HbA1c、TC 的改善幅度,差異無統計學意義(P>0.05)。見表1。
3 討論
近年來,艾塞那肽降糖外的獲益受到越來越多的關注。本研究結果亦證明艾塞那肽在顯著的降糖作用外尚有降低體重、BMI、腰圍、改善血脂及胰島素抵抗、降低血肌酐和減少尿蛋白的作用。
迄今為止,艾塞納肽對血脂譜的影響研究大多局限于TC,TG,LDL-C 和HDL-C,未有對載脂蛋白的相關研究,糖尿病患者的血脂異常以TG 升高為主要特點,主要包括血清TC,TG,LDL-C 水平的升高和HDL-C 的降低。長期以來,TC、HDL-C及LDL-C 與動脈粥樣硬化的相關性一直備受關注,而TG 增高的致動脈粥樣硬化作用已經被逐漸淡化,甚至認為只有在TG 水平過高時,為防止發生胰腺炎才需要降低TG 治療[4]。然而,近年來,NORDESTGAARD 等[5]研究卻發現:長期中至重度的高TG 血癥大幅增加人群的總死亡率和發生心血管疾病的危險,認為對TG 的致心血管病風險的危害的忽視是不正確的。雖然艾塞那肽臨床應用初期很多學者曾擔心它會導致TG 水平增高從而增加胰腺炎的風險,但目前臨床研究均證明艾塞那肽的應用不僅不會升高,相反會顯著降低TG 水平[3]。本研究結果中,艾塞那肽治療后,不僅TC、LDL-C 水平有顯著下降,HDL-C 水平有顯著增高,TG 水平亦有顯著降低。這與既往研究結果一致[6]。與二甲雙胍組相比,發現TG 水平的降低可能不依賴于血糖的降低。艾塞那肽降低TG 的可能機制:GLP-1 受體表達于人肝細胞上,經艾塞那肽刺激后,能夠直接減少肝細胞內TG 含量;林倍思等[7]研究發現艾塞那肽可能通過sirtuin1 激活脂肪甘油三脂脂酶促進脂肪組織的脂解作用而降低TG;艾塞那肽可抑制肝臟脂肪生成,減輕肝細胞內脂質沉積及可能通過磷脂酰肌醇3 激酶/蛋白激酶B 信號通路抑制肥胖相關基因的表達,進而改善肝細胞內脂代謝紊亂而降低TG;QIN[8]等研究發現GLP-1 可以顯著減少腸道淋巴流動和減少TG的吸收而不抑制TC 的吸收,從而降低TG 的水平。另一方面,艾塞那肽可能通過降低體重改善胰島素抵抗及降低脂肪組織脂聯素的釋放從而改善TG 水平。
ApoA-1 是HDL-C 中的主要載脂蛋白,而ApoB 是其他致動脈粥樣硬化脂蛋白顆粒如VLDL,HDL-C 及LDL-C 的主要結構蛋白成分。S.R.SRINIVASAN 等[9]研究發現低水平的ApoA-1 濃度及ApoA-I/ApoB 與心肌梗死的發生率密切相關。AUSTIN 等[10]的研究發現,T2DM 患者中一個常見的血脂特點是含有ApoB 的載脂蛋白的數量增高而TC 及LDL-C 是正常的。LDL-C 在正常范圍內,而ApoB 水平的升高可能預示著小而致密的LDL-C 顆粒數量的增加,而這種顆粒是心肌梗死及動脈粥樣硬化的一個重要的危險因素,使冠心病發生的危險增加[10]。CARNEVALE 等[11]研究發現,ApoA-1/ApoB 的比率反映了血漿中抗動脈粥樣硬化和致動脈粥樣硬化脂蛋白的平衡,與血脂或脂蛋白及他們的的比值相比能夠更好的預測心血管疾病的發生。由本研究結果可見,艾塞那肽治療后ApoA-1 顯著升高,ApoB 顯著降低;與二甲雙胍組進行比較發現,艾塞那肽可以不依賴血糖的降低明顯的升高HDL-C 與ApoA-1 和降低LDL-C 與ApoB 的水平。而目前艾塞那肽降低載脂蛋白的機制是不明確的。CHEHADE 等[12]研究發現GLP-1通過促進肝臟ApoA-1mRNA 的表達和ApoA-1 啟動子的活性及肝臟ATP 結合盒式蛋白A1(ABCA1)的表達而升高ApoA-1 的水平。QIN等[8]研究發現GLP-1 可以顯著減少腸道淋巴流動和減少ApoB 的吸收從而降低ApoB 的水平。因此艾塞納肽可以不依賴血糖的降低改善載脂蛋白,可能在糖尿病大血管并發癥的發生和發展過程中起著積極干預作用。
T2DM 以胰島素分泌缺陷及胰島素抵抗為特點,胰島素抵抗又是血脂異常的發病機制之一;而血脂異常又可引起胰島素抵抗的發生,從而加重血脂紊亂,它們之間互為因果,相互促進。胰島素抵抗產生的機制可能是由于脂蛋白酯酶活性降低導致TG 水平顯著升高及HDL-C 的顯著降低和肝臟中ApoA-1 的合成及分泌減少。本研究結果可見,與二甲雙胍組相比,艾塞那肽可以不依賴其降糖作用顯著升高空腹C 肽及空腹胰島素,改善胰島素抵抗。艾塞那肽改善胰島素抵抗的分子機制目前還不明確,有研究證明艾塞那肽可通過上調脂肪組織中sirtuin1 的表達而改善胰島素抵抗;如上所述,艾塞那肽也可通過sirtuin1 降低TG,說明艾塞那肽可能通過共同的機制改善胰島素抵抗及血脂;而RYE 等[13]最新研究發現HDL-C 和ApoA-1 可以促進胰島β 細胞合成及分泌胰島素,可能與GLP-1 受體激動劑在高血糖條件下促進β細胞分泌胰島素的機制是類似的,進一步說明艾塞那肽改善血脂代謝與胰島素抵抗是相輔相成的。
腸促胰素保護腎功能的可能機制為:可上調調節GLP-1R 的表達;可抑制腎組織RAS 活性從而抑制腎組織AngⅡ的表達,減少尿蛋白,同時抑制腎組織炎癥[14];可抑制腎小管重吸收鈉并降低血壓[15];改善代謝異常等從而達到腎臟保護的作用。迄今為止,尚未有臨床研究艾塞那肽對糖尿病腎臟影響的相關報道。本研究結果發現,艾塞那肽治療后,血肌酐和血尿酸均有顯著的降低,說明艾塞那肽治療亦有一定腎保護作用。同時24 h 尿微量白蛋白的水平有明顯的降低,進一步說明了艾塞那肽對腎損害的改善作用。尿β2 微球蛋白較治療前均降低,說明艾塞那肽對腎小管也有一定的保護作用。艾塞那肽組的FBG,HbA1c 與二甲雙胍組差異不顯著,提示艾塞那肽降低血肌酐、尿蛋白、改善腎小球濾過率及尿β2 微球蛋白,可能不依賴于其降糖作用。趙偉等[14]臨床前期研究表明腸促胰素治療會降低血肌酐,減少尿蛋白,改善腎小球硬化及腎臟的氧化應激及纖維化;ZAVATTARO 等[16]研究發現利拉魯肽可以降低糖尿病患者的尿微量白蛋白,改善腎功能,這與本研究結果一致。證明艾塞那肽在防治糖尿病患者微血管并發癥方面亦具有潛在獲益。

