高考化學反應原理綜合試題分析與解題策略
于永卿
(安徽省利辛縣第十中學)
化學反應原理的知識點常在高考中多角度呈現,雖然單個知識點的難度不高,但綜合后難度會呈螺旋式上升。例如在2022年全國乙卷的28題中,就以H2S的回收處理與應用為背景考查了平衡移動的原理,但考查的方式是對平衡轉化率變化的原因分析,將難度提高了。本文是在對近五年全國卷的化學高考試題研究分析的前提下,同時又調研了2 000名不同學習程度學生的基礎上完成的,在幫助學生規避常規錯誤、優化解題策略方面提出了建設性意見,并構建出相關的解題模型。
一、近五年全國卷化學反應原理綜合試題考查統計
表1是近五年在全國卷中化學反應原理綜合試題的考查背景與知識點。
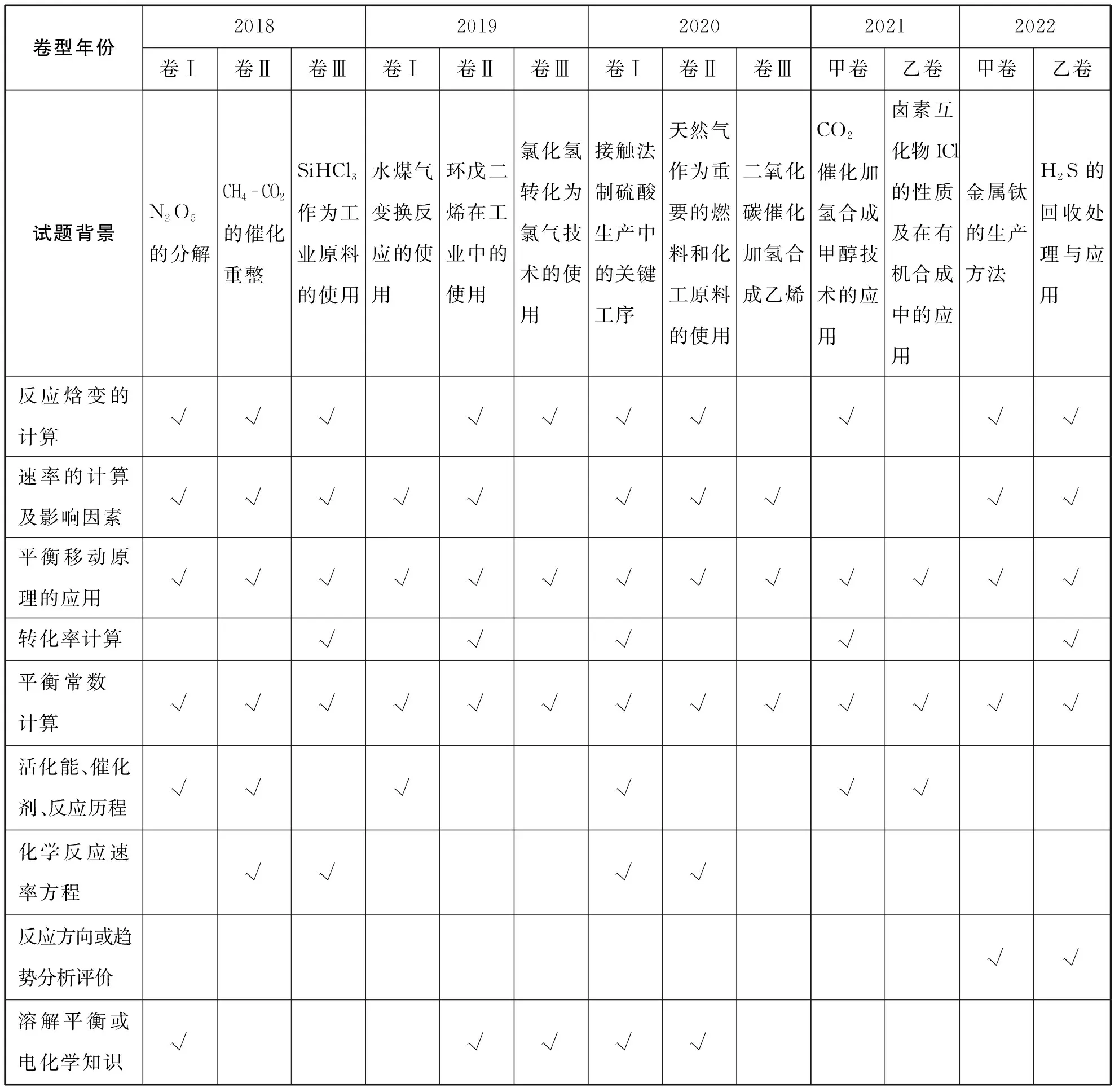
表1
二、試題特點及考查特點分析
(一)試題特點
從試題背景來看,近五年化學反應原理綜合題考查形式相近,雖然試題的背景素材不斷變化,考查形式不斷創新,但通常都是以化工生產中所涉及的化學反應為背景,也會涉及當前的熱點問題。如2021年全國甲卷28題中的CO2催化加氫合成甲醇,就對應了“碳中和”;也有經典化工生產流程的新考法,如2019年全國Ⅰ卷的水煤氣變換反應的使用;或者是常規情境下化學反應的改進使用,如2022年全國乙卷中的硫化氫的回收利用。
從考查范圍來看,化學反應原理綜合試題中的考查范圍非常廣,主要考查了反應焓變的計算、平衡移動原理綜合應用、平衡轉化率及化學反應速率的計算、分壓及分壓化學平衡常數的計算、圖像分析等。將化學熱力學與化學動力學進行了有機結合,既是對基礎知識的考查,也是對綜合應用能力的考查,還綜合考查了學生識圖、計算和文字表達等方面的能力。旨在區分考生能否把綜合題拆解成若干個較獨立的小問題,拆分以后明確了相應考點,難度就會隨之降低,充分體現了“證據推理與模型認知” “變化觀念與平衡思想” “科學探究與創新意識”等化學學科核心素養。
(二)考查特點
通過分析近五年全國卷化學反應原理綜合試題,發現有以下考查特點:
1.題型難度變化平穩
全國卷的化學反應原理綜合試題在分數、考查方式和具體知識點方面來看變化是比較平穩的。具體試題中涉及陌生信息的應用相對較少,題目中涉及的圖像分析問題一般都是一個,難度也不算大。比如2022全國乙卷28題中的第(4)問,只是考查了曲線的判斷。與之相關的原因分析的題目,注重文字的表達,要求學生能根據一定的試題背景,組織化學語言,科學、規范地回答相應問題。盡管不具備什么規律,但模式固定不變,無外乎是關于速率、轉化率的分析。有關計算的題目,雖然有復雜性難度卻不高,主要考驗的是學生的耐心與細心程度,設問數量基本在3個空,一般涉及ΔH、Kp、轉化率三個方面。總而言之,全國卷在該題的結構和難度方面沒有太大的“浮動”。
2.重視基礎知識及應用的考查
化學反應原理綜合題考查知識的基礎性比較強,包含焓變的計算,化學反應速率的計算、比較和影響因素的判斷,化學反應平衡狀態的判斷,化學平衡移動的影響因素,轉化率、壓強平衡常數計算等,所考知識的原型都可以在教材中尋得痕跡,屬于基礎知識范圍。例如2020年全國Ⅰ卷的28題中以接觸法制硫酸生產中的關鍵工序為背景,試題的(2)(3)兩問中就分別考查了轉化率、轉化率的影響因素、壓強及壓強平衡常數,同時給了信息說明。在第(4)問中圍繞著速率變化的實際情況展開原因分析,主要考查了學生對基礎知識的掌握和應用,旨在用化學知識處理工業所遇到的問題,體現學以致用、理論聯系實際的思路。在其他年份的不同考卷中通常還會涉及該如何提高反應物的轉化率、產品的產率及如何控制生產成本等問題。
3.重視對數據、圖像的分析和處理能力的考查
這類題目需要從圖像或者圖表中解讀出有效信息,對思維能力的要求相對比較高,要求學生能通過閱讀圖形和表格,提取相關的解題信息,再通過對圖像中的符號、數據、曲線變化特點等信息進行分析和整理,并結合已有的解題模型和化學理論知識,推理得出相應的結論,并能對具體的問題給出合理的解釋。近五年的試題中全國卷都有涉及,比如2021年全國甲卷的第28題中對“等壓過程曲線的判定和原因分析”的考查、2020年全國Ⅲ卷第28題中對“物質變化曲線判定”的考查、2019年全國Ⅰ卷第28題中對“物質壓強變化曲線判定”的考查等,借以實現對學生化學學科核心素養的全面考查,也是對學生思維能力的高階考查。在整體試題容量和難度的控制下,此類題目雖然有一定的難度,但不是沒有線索。“洞悉本質、逐個擊破”是解決問題的錦囊妙計。
4.重視對計算能力的考查
化學反應原理綜合試題中必然涉及化學計算過程,而計算則是對化學公式和邏輯思維的考查,是一個嚴密的數據推導過程,引導學生看待問題從定性的角度向定量的角度轉變。例如通過平衡常數的計算可以引導學生更好地理解化學反應的限度,以便更好地建立看待化學問題的“平衡觀”,比如2022年全國乙卷第28題第(3)問中壓強平衡常數的計算,第(4)問中分壓的平均變化率的計算。同時,在計算中還能實現對學生能力的全面考查,比如通過對焓變的計算考查了學生的數據處理能力;依托化學平衡常數的計算和轉化率的計算考查了學生的邏輯推理能力。不同的計算題型考查的角度是不同的,不太熟練的同學,在臨場時計算的速度和準確度可能會有所下降。
三、學生的錯因分析
為了更準確地掌握學生對化學反應原理基礎知識的掌握情況及應對高考化學反應原理綜合試題的能力,設計了本次的高考化學反應原題綜合試題解題情況調查。同時,為了更清晰地掌握學生丟分的原因,也對學生的解題思路進行了調查。調查的目的是通過調研,能對學情有更好的掌握,為針對性的解題策略的推行打下基礎。
本次調研選擇了三個不同層次高中的高三學生,共計2 000名,分發試題2 000份,回收試題 2 000份。分發的試題是2022年全國乙卷中的第28題,該化學反應原理綜合試題的分值是15分,共計4小題9個空,試題如下:
28.(15分)油氣開采、石油化工、煤化工等行業廢氣普遍含有的硫化氫,需要回收處理并加以利用。回答下列問題:
(1)已知下列反應的熱化學方程式:




(2)較普遍采用的H2S處理方法是克勞斯工藝。即利用反應①和②生成單質硫。另一種方法是利用反應④高溫熱分解H2S。相比克勞斯工藝,高溫熱分解方法的優點是________________,缺點是________________。
(3)在1 470 K、100 kPa反應條件下,將n(H2S)∶n(Ar)=1∶4的混合氣進行H2S熱分解反應。平衡時混合氣中H2S與H2的分壓相等,H2S平衡轉化率為________,平衡常數Kp=________kPa。
(4)在1 373 K、100 kPa反應條件下,對于n(H2S)∶n(Ar)分別為4∶1、1∶1、1∶4、1∶9、1∶19 的H2S-Ar混合氣,熱分解反應過程中H2S轉化率隨時間的變化如圖所示。
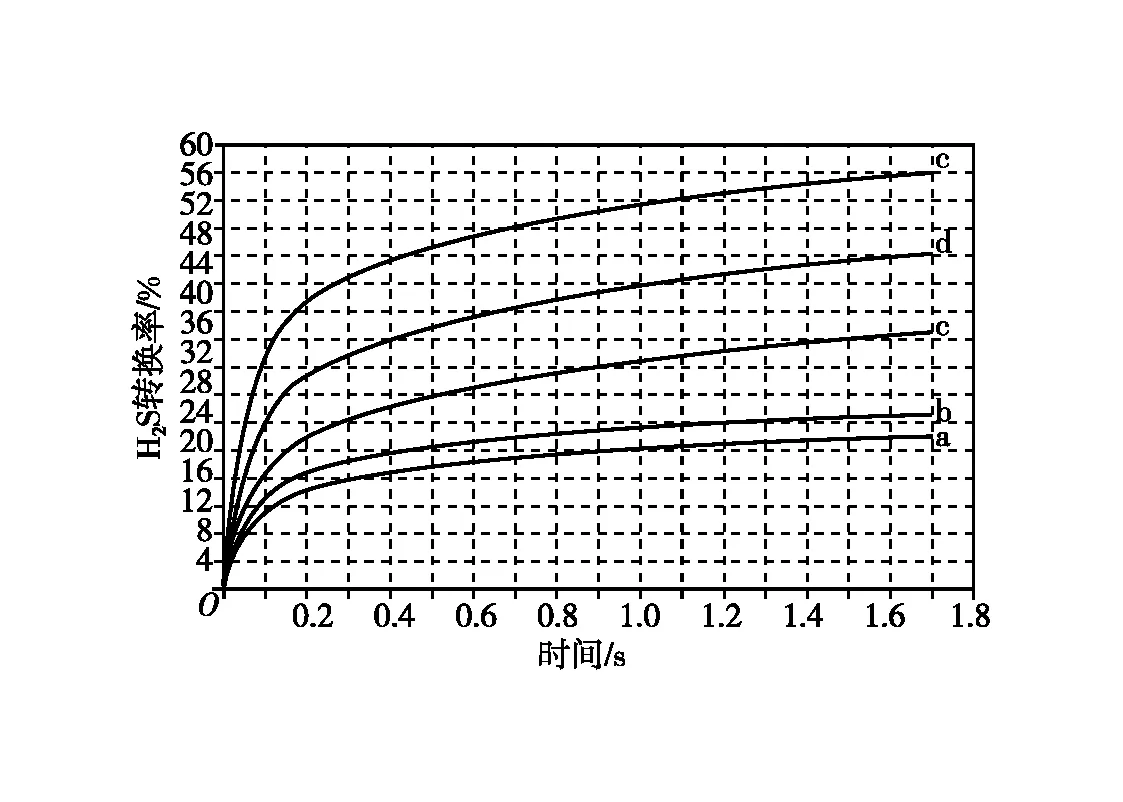
①n(H2S)∶n(Ar)越小,H2S平衡轉化率________,理由是____________________________________。
②n(H2S)∶n(Ar)=1∶9對應圖中曲線________,計算其在0~0.1 s之間,H2S分壓的平均變化率為________kPa·s-1。
得分統計如表2所示:
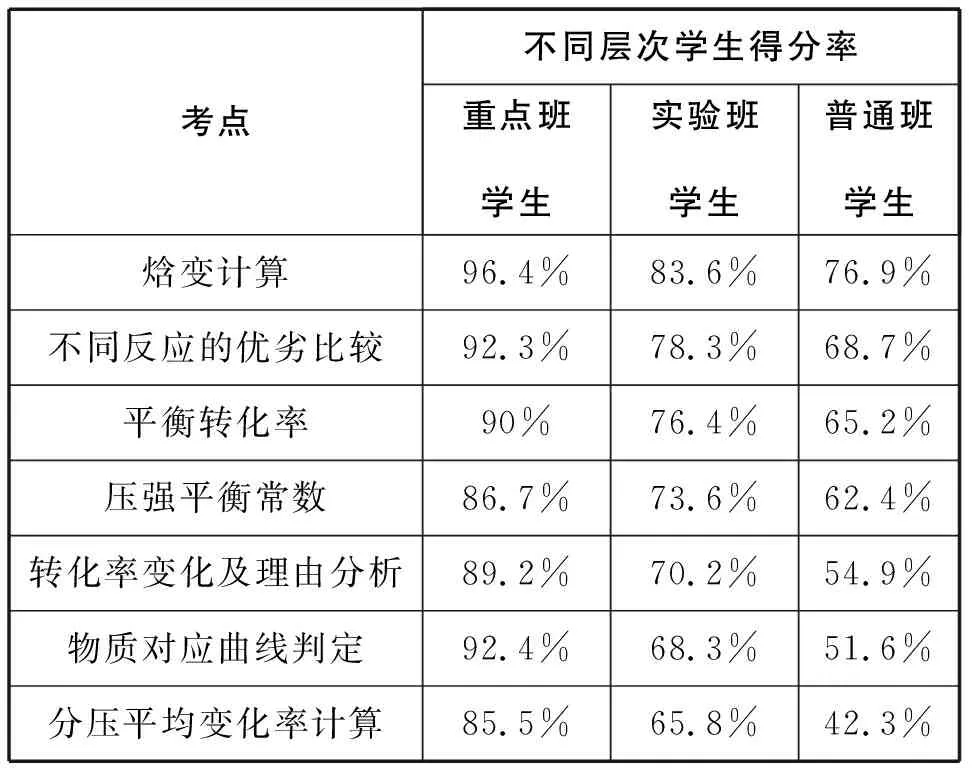
表2
通過對結果的分析發現,三個層次的學生得分率相差較大,無論是哪個題目都沒有百分之百的得分率,通過與學生的談話將具體的丟分原因歸類如下:
1.基礎知識方面存在馬虎和遺忘的現象。以本次調查的焓變計算為例,主要考查的是蓋斯定律的使用,普通班的學生存在概念不清的情況,對于由已知熱化學方程式求解未知焓變值的方法掌握的不牢固;實驗班和重點班的學生則存在符號錯誤的情況,除此之外,平常考試的熱化學方程式書寫也會有一些小錯誤。

3.計算能力方面邏輯思維有欠缺。首先是K值(K、Kp、Kx)的形式多變,單位的不一致性易造成錯誤,其次是多重平衡體系加大了試題的難度。比如在本題中的第(3)問中的計算。在恒溫、恒壓下,對于Δn≠0的反應,Kc、Kp計算有時很麻煩。因為要維持恒壓,加入某氣體物質時體系的體積就一定會變。而體積一變,所有物質的濃度及分壓就都會隨之改變。這里歸根到底還是三段式的使用,在計算了轉化率后,平衡常數也能迎刃而解。但是有相當一部分學生由于沒有解題思路,丟分也就自然而然了。
四、解題策略分析
俗話說:“知己知彼,百戰不殆”,縱觀近年來的高考化學試題,不難發現有些考點經久不衰,幾乎成為每年高考必考,有些考點則在不斷更新。在總結出學生錯因的前提下,對應的解題策略也就應運而生。
從學生學習方面來說,學生是學習的主體,要想有效地解決化學反應原理綜合試題,就必須做到有效的學習,針對基礎知識點不眼高手低,一輪復習中不留知識盲區。其次就是形成從“理清研究對象”到“關注反應體系”,進而“判定反應特點”,最后是“分析圖像變化”的解題思路,最終構建解題的模型,以K值的計算模型為例:
(一) 一般模型
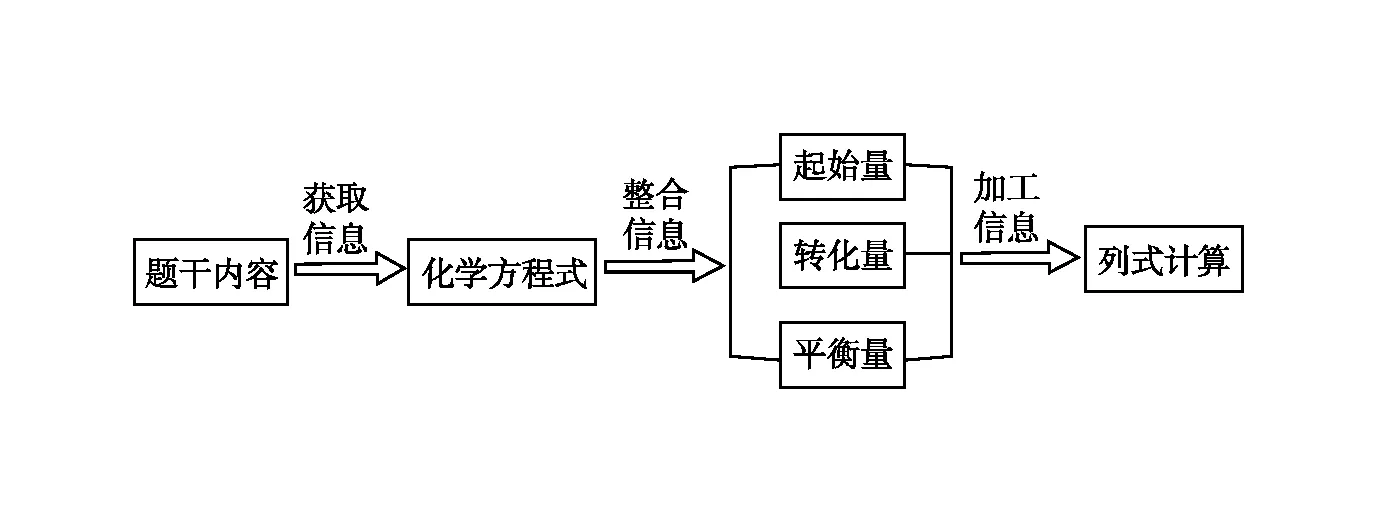
(二) Kp計算基本模型
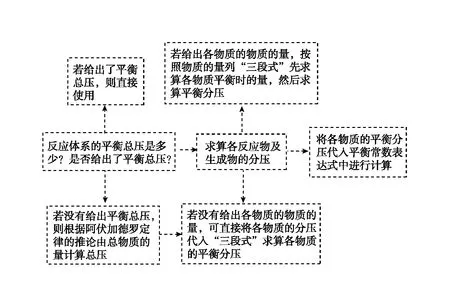
從教師教學方面來說,在進行化學反應原理備考復習過程中,應該引導學生做好以下幾個方面:
1.在基礎知識方面
①掌握利用蓋斯定律計算反應熱的方法,能利用化學鍵計算反應熱,會分析反應熱有關圖像;
②掌握外界條件對化學反應速率和化學平衡的影響,熟練掌握化學反應速率和化學平衡常數有關計算;
③對多步連鎖反應、速率方程、活化能等拓展知識,做適當訓練;
④加強解題能力訓練,具備識圖能力,分析圖形變化,正確理解題意,能利用規范語言正確回答問題。
2.在熱點信息方面準確把握高考熱點
高考熱點通常與新興科技有關,是在高考試題中經常出現的重要考點,在進行高考復習時,可以通過分析高考試題的變化,預測高考的趨勢及試題的載體,充分掌握高考熱點。高考重點考什么,我們就要重點復習什么,不能不分主次,搞平均分配。關注高考熱點,不是放棄冷點,而是將有限的時間,合理分配,適當安排,有的放矢,重點突破,這樣就可以做到把好鋼用在刀刃上,達到精準高效備考的目的。
五、結束語


