凝血功能障礙患兒臨床表現、實驗室檢查及預后分析
路幼佳, 劉洪軍, 陳天平, 屈麗君, 韋 楠, 呂文秀
安徽省兒童醫院 血液腫瘤科,安徽 合肥 230000
凝血功能障礙(coagulation disorders,CD)是指由于血管壁異常、凝血因子缺乏、血小板減少、藥物因素等導致血液凝固障礙,從而引起出血的一種異常表現[1]。該病患者多表現為鼻出血、牙齦出血、皮下瘀斑、月經量過多等,嚴重者會出現內臟出血、休克等,嚴重威脅患者的生命健康。根據病因,CD可分為遺傳性CD(血友病、遺傳性出血性毛細血管擴張癥、血管性假血友病等)和獲得性CD(由于凝血因子缺乏、血小板減少、藥物因素等導致的出血)[2]。糾正凝血功能異常是CD的治療目標。遺傳性CD一般不可根治,需要終生行凝血因子替代治療,進而控制病情[3]。獲得性CD經過對因治療后,一般可以根治凝血功能異常,不會影響壽命,若未積極治療原發疾病導致病情進展,可能并發彌散性血管內凝血、多臟器功能衰竭等,一般不可根治,預后較差[4]。目前,關于兒童CD的發病機制尚未明確。本研究分析總結CD患兒的臨床表現、實驗室檢查、預后等情況,旨在為臨床治療兒童CD提供更多決策依據。現報道如下。
1 對象與方法
1.1 研究對象 選取自2017年7月至2022年6月安徽省兒童醫院收治的209例CD患兒為研究對象。其中,男性138例,女性71例;年齡1個月至17歲,中位年齡4歲。納入標準:符合CD相關診斷標準[5];患兒家屬知曉本研究,并簽署知情同意書。排除標準:經醫師評估預計生存期<3個月;中途退出研究或失訪;存在心腦血管疾病;存在精神障礙疾病。本研究符合《赫爾辛基宣言》相關倫理準則。
1.2 治療方法 遺傳性CD患兒均行替代治療。血友病A患兒輸注人凝血因子Ⅷ(華蘭生物工程股份有限公司,國藥準字S20003004)替代治療,血友病B患兒輸注人凝血酶原復合物(華蘭生物工程股份有限公司,國藥準字S20083057)替代治療,因子Ⅶ缺乏癥患兒輸注注射用重組人凝血因子Ⅶa(丹麥諾和諾德公司,進口藥品注冊標準S2015006)替代治療,因子Ⅻ缺乏癥和因子Ⅴ缺乏癥患兒均輸注血漿替代治療,低纖維蛋白血癥患兒輸注人纖維蛋白原(fibrinogen,FIB,山東泰邦生物制品有限公司,國藥準字S20170007)替代治療。獲得性CD患兒均在治療原發病的同時,給予血漿、FIB、維生素K1等支持治療。維生素K依賴性凝血因子缺乏癥患兒給予維生素K1注射液(成都倍特藥業有限公司,國藥準字H32021752)進行治療;肝源性CD患兒在積極治療控制原發病的同時,輸注血漿支持,同時輸注冷沉淀或FIB治療;免疫性疾病導致的CD患兒在治療原發病的基礎上,輸注血漿支持治療;藥物導致的FIB合成減少需要輸注冷沉淀或人FIB治療;無明顯誘因的凝血功能異常,通過輸注血漿支持治療。
1.3 觀察指標 入院后詳細詢問病史、家族出血史及臨床表現,并進一步完成凝血功能指標[凝血酶原時間(prothrombin time,PT)、部分活化凝血酶原時間(activated partial thromboplastin time,APTT)、FIB]、凝血因子活性、肝功能[血清總膽紅素(total bilirubin,TBIL)、天門冬氨酸氨基轉移酶(aspartate transaminase,AST)、丙氨酸氨基轉移酶(alanine aminotransferase,ALT)]、腎功能(血肌酐、尿素氮、尿酸)、病原學檢測[EB病毒、巨細胞病毒、支原體等]、骨髓形態學、白血病免疫分型、染色體、融合基因等相關檢測。上述資料均由本院專職人員收集。患兒出院后,每3個月以電話或門診形式進行隨訪,以2022年12月為隨訪終點,記錄所有患兒的預后情況。
1.4 統計學方法 采用SPSS 22.0統計學軟件處理數據。非正態分布的計量資料以中位數(四分位數間距)[M(P25,P75)]表示,組間比較采用Mann-WhitneyU檢驗。計數資料以例(百分率)表示,組間比較采用χ2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 患兒病因及原發病 209例CD患兒中,遺傳性CD 38例(納入遺傳性CD組),其中,血友病A 24例,血友病B 8例,因子Ⅶ缺乏癥2例,因子Ⅺ缺乏癥2例,因子Ⅴ缺乏癥1例,低FIB血癥1例;獲得性CD 171例(納入獲得性CD組),其中,維生素K依賴性凝血因子缺乏癥11例(5例為溴鼠靈中毒,6例為晚發維生素K缺乏癥),25例源于感染或溶血性貧血[包括巨細胞病毒感染(血液巨細胞病毒DNA定量陽性)1例,EB病毒感染(EB病毒DNA定量陽性)2例,支原體感染(支原體IgM抗體陽性)5例,噬血細胞綜合征(hemophagocytic lymphohistiocytosis,HLH)15例(其中,EB相關HLH 10例),溶血性貧血2例],5例源于免疫性疾病(包括免疫性血小板減少癥1例,過敏性紫癜1例,系統性紅斑狼瘡3例),124例源于急性淋巴細胞白血病患兒應用培門冬酶化療時所致的凝血異常,6例無明顯誘因單純性凝血功能異常。
2.2 兩組患兒出血情況比較 遺傳性CD組出血率為86.84%(33/38),與獲得性CD組的78.95%(135/171)比較,差異無統計學意義(P>0.05)。見表1。
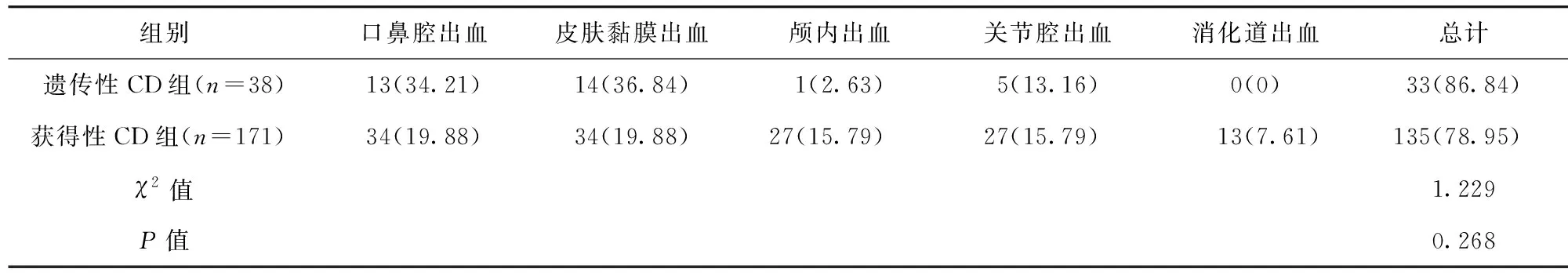
表1 兩組患兒出血情況比較/例(百分率/%)
2.3 兩組患兒凝血功能指標比較 兩組PT比較,差異無統計學意義(P>0.05)。獲得性CD組APTT、FIB低于遺傳性CD組,差異有統計學意義(P<0.05)。見表2。

表2 兩組患兒凝血功能指標比較[M(P25,P75)]
2.4 兩組患兒肝功能指標比較 兩組AST水平比較,差異無統計學意義(P>0.05)。獲得性CD組TBIL、ALT水平高于遺傳性CD組,差異有統計學意義(P<0.05)。見表3。

表3 兩組患兒肝功能指標比較[M(P25,P75)]
2.5 兩組患兒腎功能指標比較 兩組患兒血尿素氮、尿酸水平比較,差異無統計學意義(P>0.05)。獲得性CD組血肌酐水平高于遺傳性CD組,差異有統計學意義(P<0.05)。見表4。

表4 兩組患兒腎功能指標比較[M(P25,P75)]
2.6 兩組患兒預后情況比較 兩組患兒均未出現死亡,預后良好。
3 討論
CD是較常見的出血性疾病,主要表現為發生輕微外傷后,皮膚關節容易出現血流不止的癥狀。該病主要是由于患兒骨髓功能病變造成的嚴重血液系統疾病,主要表現為人體凝血因子、血小板等凝血功能物質降低,造成人體凝血功能異常[6]。臨床治療CD的首要步驟為查明引發出血的原因,根據患者實際病情正確補充凝血因子,提高凝血因子的數量與濃度,達到止血的效果[7]。本研究中,獲得性CD患兒與遺傳性CD患兒PT無明顯差異,而獲得性CD患兒APTT、FIB較低。獲得性CD患兒常見病因包括特殊藥物、各種原因引起的肝功能異常、晚發維生素K缺乏癥、風濕免疫疾病等。此外,急性白血病、淋巴瘤化療過程中應用的培門冬酶也易引起患兒CD[8],其主要原因是抑制蛋白合成,導致FIB、各類凝血因子水平降低。HLH患者發生CD最常見的原因是FIB水平下降[9-10],FIB<1.5 g/L是HLH的診斷指標之一[11]。這提示,FIB水平可能輔助區分獲得性CD與遺傳性CD。本研究發現,獲得性CD患兒與遺傳性CD患兒AST、血尿素氮、尿酸水平無明顯差異,而獲得性CD患兒TBIL、ALT、血肌酐水平高于遺傳性CD患兒,分析原因可能為獲得性CD多源于急性淋巴細胞白血病,應用培門冬酶進行化療可致重度脂肪肝伴膽汁淤積,出現凝血異常,肝損傷可能性較高[12]。
本研究中,209例CD患兒均未出現死亡,預后良好。遺傳性CD(如血友病)主要采取凝血因子替代治療,通過補充體內缺乏的凝血因子促進凝血,以達到止血的目的。20世紀50年代末和60年代初,新鮮冰凍血漿或凝血酶原復合物開始用于治療血友病[13]。同時,應該根據出血程度、所缺乏凝血因子成分及活性等情況進行替代治療。當血友病患兒發生出血事件時,特別是顱內出血、頸部/咽喉部出血、消化道出血等可能危及生命的嚴重出血事件,需要立即給予凝血因子替代治療[14]。本研究中,因子Ⅶ缺乏癥2例,因子Ⅺ缺乏癥2例,因子Ⅴ缺乏癥1例,低FIB血癥1例,均在正常生活中無出血傾向,擬進行手術等情況時,輸注相應凝血因子制品或血漿防止出血。對于獲得性CD,積極治療原發病是終止凝血異常的關鍵。維生素K缺乏為多因子聯合缺乏,常有自發性皮膚、黏膜和內臟出血傾向,去除病因和維生素K序貫應用可有效治療。HLH患者體內免疫調節異常,主要為淋巴細胞、單核細胞和巨噬細胞系統異常激活與增殖,分泌大量炎癥因子,異常活化的巨噬細胞在細胞因子作用下,刺激單核細胞上尿激酶纖溶酶原激活物受體表達,從而促進纖溶酶原細胞的激活,最終導致纖維蛋白降解[15]。
HLH合并CD的治療關鍵為及時給予免疫治療,清除炎癥因子,阻斷細胞因子風暴,進而降低死亡風險[16]。此外,輸注FIB、凝血酶原復合物、血漿等替代治療也是治療過程中不可缺少的一部分。白血病患兒治療過程中應用的培門冬酶是聚乙二醇與左旋門冬酰胺酶(L-asaraginase,L-ASP)共價連接而成的新型門冬酰胺酶制劑。L-ASP是蛋白質與核酸生物合成所必需的氨基酸,可催化血漿中門冬酰胺水解,耗竭門冬酰胺,抑制蛋白質合成,從而導致纖維蛋白溶酶、FIB、各類凝血因子等水平下降,出現凝血功能不全[17]。當患者FIB處于最低下限水平時,應及時輸注FIB或血漿替代治療,恢復凝血功能。膿毒癥、重癥肺炎、EB病毒感染等均可引起CD,主要由于感染后,血管內皮細胞損傷,釋放大量組織因子進入血液,導致凝血異常[18]。本研究中,6例原因不明的CD患兒以APTT延長為主,多因鼻出血就診,經過及早控制出血以減少顱內出血風險,補充維生素K和輸注血漿糾正CD等處理,后期隨訪中患兒凝血功能均恢復正常。
綜上所述,兒童獲得性CD多見,出血部位主要為口鼻腔和皮膚黏膜;遺傳性CD需要特異性凝血因子終生替代治療,預后取決于凝血因子缺乏的程度及干預的積極性;獲得性CD需要從根本上治療原發病,血液制品短期替代治療,預后主要取決于原發病的治療效果。

