pH 值對(duì)酪蛋白- 木糖醇復(fù)合物功能和結(jié)構(gòu)特性的影響
安悅嘉,曹雪妍,楊 梅,陶冬冰,張 旋,張 琦,潘 松,岳喜慶
(沈陽(yáng)農(nóng)業(yè)大學(xué)食品學(xué)院,遼寧 沈陽(yáng) 110866)
酪蛋白是十分重要的優(yōu)質(zhì)蛋白,其必需氨基酸含量較高,且比例適中,種類齊全,在人體發(fā)育成長(zhǎng)的過(guò)程中必不可少。木糖醇是糖尿病患者不可或缺的糖代品,其生物利用、醫(yī)學(xué)輔助治療預(yù)防方面都十分優(yōu)質(zhì),大眾需求不斷提高。
酪蛋白的功能性質(zhì)在食品加工中具有不可或缺的作用。酪蛋白較好的乳化性可提高脂肪乳化程度,常用于脂肪含量較高的蛋糕及咖啡伴侶中。較好的起泡性因可以形成穩(wěn)定膜使酪蛋白被用作泡沫穩(wěn)定劑,應(yīng)用于人造奶油中。但酪蛋白的溶解性較差,難以在室溫條件與其他緩沖液相融,導(dǎo)致其在食品加工行業(yè)的發(fā)展和利用中受到了阻礙[1]。pH 值是改變蛋白質(zhì)溶解性較為重要的因素,尤其當(dāng)pH 值接近酪蛋白等電點(diǎn)會(huì)對(duì)酪蛋白溶解性產(chǎn)生較大影響[2],且pH 值也會(huì)改變蛋白質(zhì)的分子構(gòu)象,結(jié)構(gòu)的改變往往會(huì)帶動(dòng)其功能性質(zhì)的變化。而木糖醇可以提高和改善酪蛋白的乳化穩(wěn)定性、起泡能力、起泡穩(wěn)定性及結(jié)構(gòu)特性,尤其是可以改善酪蛋白較差的溶解性[3]。
以解決酪蛋白自身較差的溶解性為基礎(chǔ)前提,利用圓二色光譜、熒光光譜、紫外分光光度等方法研究了不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物二級(jí)結(jié)構(gòu)、三級(jí)結(jié)構(gòu)及表面疏水性、乳化性、起泡性、溶解性的影響。以便選取最適宜的環(huán)境條件及加工技術(shù),更好地對(duì)復(fù)合物進(jìn)行加工及利用,對(duì)酪蛋白與木糖醇在乳制品、功能性食品的添加及研發(fā)提供理論指導(dǎo)。
1 材料與方法
1.1 材料與主要儀器
酪蛋白(蛋白質(zhì)含量≥95.0 %,相對(duì)分子質(zhì)量為50 000~375 000)、木糖醇(純度>99%,相對(duì)分子質(zhì)量為152.1),北京鼎國(guó)昌盛生物技術(shù)有限責(zé)任公司提供。
F-4600 型熒光光譜儀,日立公司產(chǎn)品;RH basic2 型磁力攪拌器,廣州科儀公司產(chǎn)品;Cary 50 型紫外- 可見分光光度計(jì),美國(guó)VARIAN 公司產(chǎn)品;DK-S26 型數(shù)顯電子恒溫水浴鍋,上海精宏公司產(chǎn)品;T18 basic 型高速分散器,德國(guó)IKA 公司產(chǎn)品;pHS-25 型數(shù)顯pH 計(jì),上海精密科儀公司產(chǎn)品;J-810 型圓二色譜儀,日本Jasco 公司產(chǎn)品。
1.2 試驗(yàn)方法
1.2.1 預(yù)處理方法
將酪蛋白粉末與木糖醇顆粒按照濃度比為1∶1,1∶2,1∶3,1∶4,1∶5 稱取并混合,再溶解于體積比為1∶1 的0.1 mol/L NaOH 溶液和0.05 mol/L 的Tris-HCl 溶液緩沖液中,置于50 ℃的水浴鍋中待沉淀完全溶解后,置于磁力攪拌器中攪拌[4]。測(cè)定在中性pH 值室溫25 ℃條件下,不同濃度配比對(duì)酪蛋白- 木糖醇復(fù)合物表面疏水性、起泡性、乳化性及溶解性的影響。選擇復(fù)合物溶解性最好的濃度配比1∶1,并將接下來(lái)的試驗(yàn)設(shè)定酪蛋白與木糖醇濃度為1∶1,pH 值的范圍設(shè)定為3,4,5,6,7,8,9,10,11。
1.2.2 表面疏水性的測(cè)定
將不同pH 值的酪蛋白- 木糖醇復(fù)合物溶液樣品用緩沖溶液稀釋適當(dāng)倍數(shù)后分別加入25 μL 的ANS探針溶液,振蕩均勻并放于室溫下避光靜置5 min。以樣品緩沖溶液為對(duì)照,采用日立F-4600 型熒光分光光度計(jì),激發(fā)波長(zhǎng)為390 nm,發(fā)射波長(zhǎng)為470 nm,激發(fā)和發(fā)射狹縫寬均為5 nm 條件下,測(cè)定樣品的熒光強(qiáng)度[5]。
1.2.3 起泡性的測(cè)定
分別取適量酪蛋白- 木糖醇復(fù)合物于高速分散器以轉(zhuǎn)速10 000 r/min 均質(zhì)60 s,迅速記錄泡沫體積即為初始泡沫體積。靜置30 min 后再次計(jì)算泡沫體積,基于以下公式計(jì)算起泡性(FAI,%) 以及起泡穩(wěn)定性(FSI,%)[6]:
式中:V——樣品溶液的體積,mL;
V0——均質(zhì)后即刻記錄的樣品初始泡沫體積,mL;
V30——靜置30min 后記錄的樣品泡沫體積,mL。
1.2.4 溶解性的測(cè)定
采用考馬斯亮藍(lán)法,分別將酪蛋白- 木糖醇復(fù)合物溶液以轉(zhuǎn)速8 000 r/min 離心20 min,取出1 mL的上清液稀釋10 倍或100 倍,滴加5 mL 考馬斯亮藍(lán)溶液,避光10 min,于波長(zhǎng)595 nm 處測(cè)定樣品的吸光度,根據(jù)牛血清白蛋白標(biāo)準(zhǔn)曲線計(jì)算上清液中蛋白質(zhì)含量,再根據(jù)以下公式計(jì)算溶解性(%):
1.2.5 乳化性的測(cè)定
將酪蛋白- 木糖醇復(fù)合物溶液與食用大豆油以3∶1 的比例混合,用高速分散器以轉(zhuǎn)速10 000 r/min均質(zhì)60 s,從乳化液即離心管底部吸取50 μL 的混濁液,立即用質(zhì)量分?jǐn)?shù)為0.1%的SDS 溶液稀釋適當(dāng)倍數(shù)后振蕩均勻,分別在0 min 和10 min 時(shí)用紫外分光光度計(jì)測(cè)定樣品在500 nm 波長(zhǎng)處的吸光度,以SDS 為空白對(duì)照。根據(jù)下式計(jì)算乳化活性(EAI,m2/g) 和乳化穩(wěn)定性(ESI,min)[7]:
式中:C——蛋白質(zhì)質(zhì)量,g;
φ——油相體積分?jǐn)?shù),%;
T=2.303;
DF——稀釋因子;
θ——油相體積分?jǐn)?shù)(0.25),%;
A0——0 min 時(shí)吸光度;
A10——10 min 時(shí)吸光度。
1.2.6 內(nèi)源熒光光譜的測(cè)定
將處于不同pH 值的酪蛋白- 木糖醇復(fù)合物溶液樣品稀釋10 倍后加入ANS 熒光探針溶液,搖晃均勻,在避光的條件下反應(yīng)5 min,以緩沖溶液(NaOH+Tris-HC)l 作為空白對(duì)照。激發(fā)波長(zhǎng)為280 nm,激發(fā)和發(fā)射狹縫均為5 nm,掃描發(fā)射波長(zhǎng)范圍為300~450 nm 的熒光光譜。
1.2.7 圓二色譜(CD) 分析
用圓二色譜儀在25 ℃條件下測(cè)定樣品在遠(yuǎn)紫外區(qū)域(190~250 nm) 的CD 光譜,以樣品的緩沖溶液(NaOH+Tris-HCl) 為空白對(duì)照,比色皿的光徑為0.1 cm,測(cè)定遠(yuǎn)紫外區(qū)的CD 光譜。掃描速率為100 nm/min,Data Fitch 為1.0 nm,Band Width 為2.0 nm,掃描3 次,取平均值得到最終的CD 光譜。使用帶有selcon3 算法的CDpro 軟件來(lái)計(jì)算蛋白質(zhì)二級(jí)結(jié)構(gòu)的組成和含量。
2 結(jié)果與分析
2.1 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物表面疏水性的影響
不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物表面疏水性的影響見圖1。
當(dāng)pH 值在酪蛋白等電點(diǎn)附近時(shí),其疏水性產(chǎn)生了明顯的下降。可能是由于復(fù)合物溶液在等電點(diǎn)附近形成明顯聚集沉降,疏水基團(tuán)被沉降大多包在沉淀內(nèi)部,使ANS 探針與位點(diǎn)的結(jié)合數(shù)量降低[8]。當(dāng)pH 值逐漸增大,復(fù)合物疏水性也隨之增大。由于木糖醇能夠增加酪蛋白于等電點(diǎn)附近所帶的電荷數(shù),有效防止酪蛋白分子的相互作用及出現(xiàn)明顯集聚,增強(qiáng)酪蛋白分子的結(jié)構(gòu)穩(wěn)定。
2.2 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物起泡活性的影響
不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物起泡活性的影響見圖2。
當(dāng)pH 值處于等電點(diǎn)左右時(shí),酪蛋白- 木糖醇復(fù)合物具有較差的起泡能力。由于此時(shí)酪蛋白的疏水性降低,影響了酪蛋白分子在水與空氣兩相的結(jié)合與吸收,溶液表面張力減小。當(dāng)pH 值增大,酪蛋白- 木糖醇的起泡能力提高。由于酪蛋白分子結(jié)構(gòu)變得松散,柔性增加,促進(jìn)了酪蛋白分子在水與空氣兩相的快速吸收和結(jié)構(gòu)展開[9]。
2.3 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物起泡穩(wěn)定性的影響
不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物起泡穩(wěn)定性的影響見圖3。
當(dāng)pH 值為4 左右時(shí),降低了復(fù)合物溶液的起泡穩(wěn)定性。由于酪蛋白的疏水性因pH 值的影響降低,其柔性也因溶液中產(chǎn)生了絮狀沉淀物而降低,使蛋白質(zhì)分子在水和空氣兩相之間形成膜狀結(jié)構(gòu)的能力降低。當(dāng)pH 值逐漸增大,復(fù)合物的起泡穩(wěn)定性增強(qiáng)。由于逐漸遞增的疏水性及疏松的分子內(nèi)部結(jié)構(gòu)使酪蛋白分子可以逐漸在水和空氣兩相形成綿密的泡沫,普拉長(zhǎng)邊界的數(shù)量增加[10]。
2.4 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物溶解性的影響
不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物溶解性的影響見圖4。
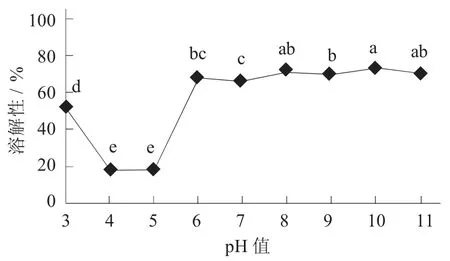
圖4 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物溶解性的影響
當(dāng)pH 值為4 左右時(shí),復(fù)合物的溶解性降低。由于酪蛋白分子所附的靜電荷數(shù)可忽略不計(jì),所以靜電斥力也基本消失[11]。但當(dāng)pH 值增加或降低時(shí),復(fù)合物溶液的溶解度顯著增加。酪蛋白分子之間的靜電斥力因其正負(fù)電荷而提高,防止蛋白質(zhì)發(fā)生沉降。
2.5 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物乳化活性的影響
不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物乳化活性的影響見圖5。
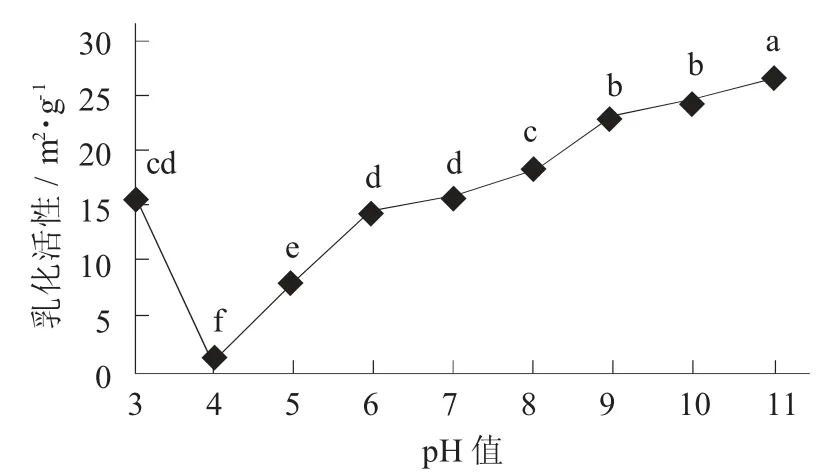
圖5 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物乳化活性的影響
當(dāng)pH 值靠近等電點(diǎn),復(fù)合物的乳化活性降低。由于酪蛋白自身的水合作用及靜電斥力均受到不良影響,使酪蛋白表現(xiàn)為微溶的狀態(tài)。同時(shí),酪蛋白分子向油- 水界面的擴(kuò)散,此時(shí)較低的溶解性受到影響,降低了其界面張力[12]。當(dāng)pH 值增加或降低時(shí),復(fù)合物的乳化活性增加。由于復(fù)合物的溶解性增加,酪蛋白分子與油和水兩相之間的相互作用隨之加大,使界面張力減小。
2.6 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物乳化穩(wěn)定性的影響
不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物乳化穩(wěn)定性的影響見圖6。
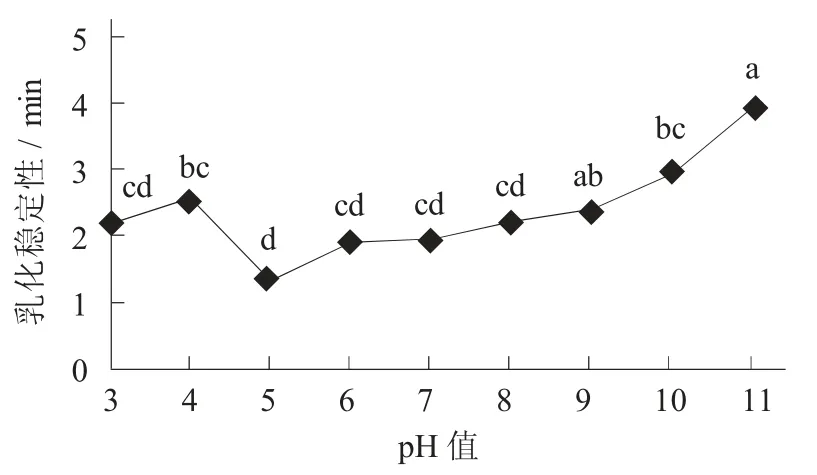
圖6 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物乳化穩(wěn)定性的影響
當(dāng)pH 值為5 時(shí),降低了復(fù)合物的乳化穩(wěn)定性。由于增加的復(fù)合物乳液分子相互作用表明其分子所帶電荷數(shù)量可能偏低,使復(fù)合物溶液產(chǎn)生沉降。但當(dāng)pH 值遠(yuǎn)離等電點(diǎn),復(fù)合物溶液的乳化穩(wěn)定性顯著增加。可以說(shuō)明酪蛋白的水合作用及靜電斥力是由于所帶電荷數(shù)量的變多而增加的。油—水界面的能量降低,避免溶液產(chǎn)生集聚[13]。
2.7 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物內(nèi)源熒光發(fā)射光譜的影響
不同pH 值條件下的酪蛋白- 木糖醇復(fù)合物內(nèi)源熒光發(fā)射光譜見圖7。
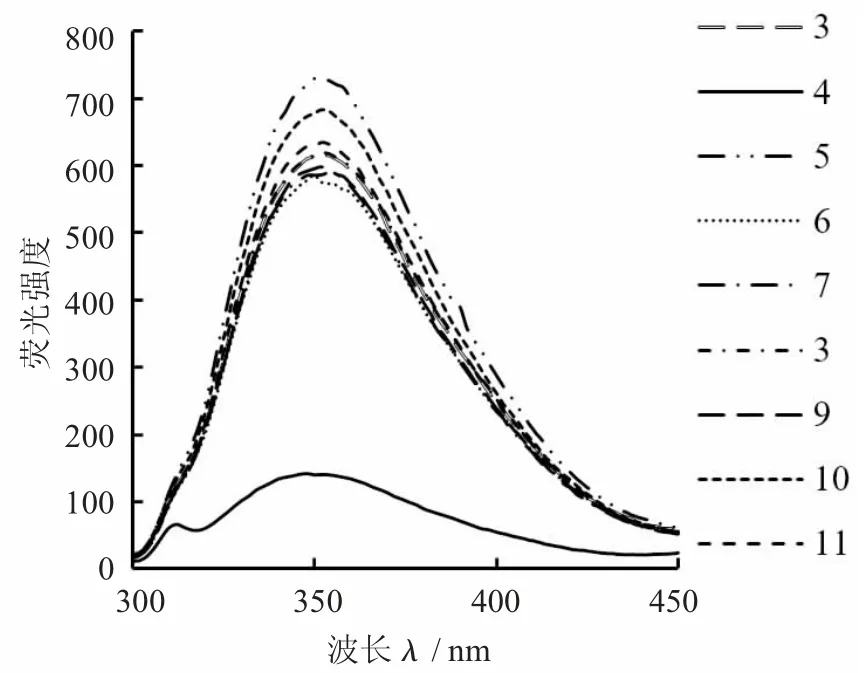
圖7 不同pH 值條件下的酪蛋白- 木糖醇復(fù)合物內(nèi)源熒光發(fā)射光譜
由圖7 可知,當(dāng)pH 值為4 時(shí),樣品的內(nèi)源熒光光譜λmax與pH 值為3 時(shí)的樣品相對(duì)比減小到348 nm,出現(xiàn)了少量的藍(lán)移,與此同時(shí),內(nèi)源熒光值大幅度降低。可能是因?yàn)閜H 值為4 左右時(shí),酪蛋白分子之間的靜電相互作用因其表面所帶電荷數(shù)的增加而增大。溶液中形成明顯的絮凝沉降,因其環(huán)境中的極性大幅度降低而減少了芳香族氨基酸殘基的暴露數(shù)量[14]。當(dāng)pH 值為7 時(shí),樣品的內(nèi)源熒光光譜λmax值增加為354 nm,產(chǎn)生了紅移,并且其內(nèi)源熒光值也照樣品pH 值為4 時(shí)大幅度增加。當(dāng)pH 值繼續(xù)逐漸增加至堿性條件下時(shí),內(nèi)源熒光值則沒有較明顯的變化。
2.8 不同pH 值對(duì)酪蛋白- 木糖醇復(fù)合物遠(yuǎn)紫外圓二色光譜的影響
不同pH 值條件下的酪蛋白- 木糖醇復(fù)合物遠(yuǎn)紫外圓二色光譜見圖8。
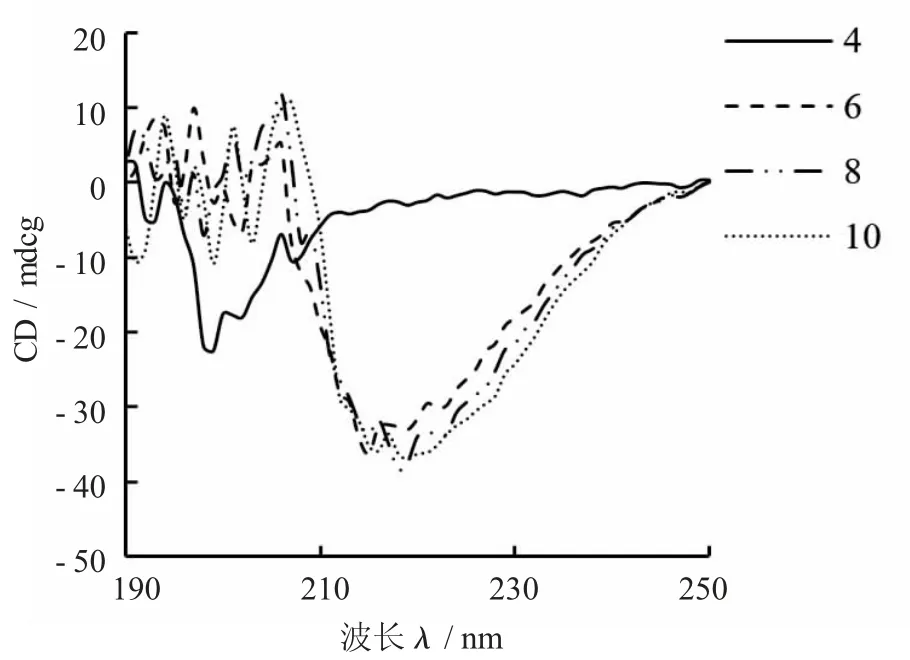
圖8 不同pH 值條件下的酪蛋白- 木糖醇復(fù)合物遠(yuǎn)紫外圓二色光譜
由圖8 可知,pH 值為6~10 時(shí)的樣品圓二色譜的負(fù)吸收峰出現(xiàn)在210~230 nm,而pH 值為4 時(shí),該樣品的圓二色譜負(fù)吸收峰出現(xiàn)在190~210 nm 內(nèi)。pH 值在6 附近時(shí),酪蛋白具有緊密的分子結(jié)構(gòu),與堿性條件下的分子結(jié)構(gòu)相差無(wú)異。當(dāng)pH 值降低到酪蛋白等電點(diǎn)附近時(shí),樣品的圓二色譜負(fù)吸收峰的位置產(chǎn)生明顯藍(lán)移,說(shuō)明此時(shí)酪蛋白分子中α- 螺旋結(jié)構(gòu)的數(shù)量明顯降低。當(dāng)pH 值為10 時(shí)酪蛋白結(jié)構(gòu)中α- 螺旋相對(duì)較多。
不同pH 值條件下的酪蛋白- 木糖醇復(fù)合物二級(jí)結(jié)構(gòu)含量分析見表1。
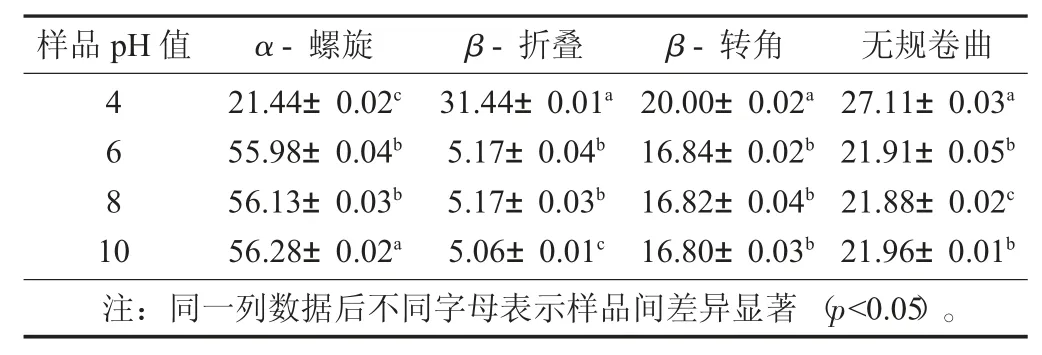
表1 不同pH 值條件下的酪蛋白- 木糖醇復(fù)合物二級(jí)結(jié)構(gòu)含量分析/%
由表1 可知,pH 值由10 降低到4,酪蛋白分子的α- 螺旋結(jié)構(gòu)從56.28%降低到21.44%,說(shuō)明酪蛋白分子表面的氨基酸等質(zhì)子化態(tài)會(huì)隨著環(huán)境中的pH值的變化而發(fā)生改變,致使其結(jié)構(gòu)中的α- 螺旋也隨之明顯改變[16]。與此同時(shí),當(dāng)pH 值為4 時(shí)的酪蛋白結(jié)構(gòu)中β- 折疊、β- 轉(zhuǎn)角及無(wú)規(guī)卷曲均出現(xiàn)相較于遠(yuǎn)離等電點(diǎn)條件而言明顯增大。蛋白質(zhì)分子的結(jié)構(gòu)會(huì)由于結(jié)構(gòu)中的無(wú)序轉(zhuǎn)角及無(wú)規(guī)則卷曲結(jié)構(gòu)數(shù)量的增多而變得松散,但因其表面所吸附的電荷量偏少,所以會(huì)在溶液中形成明顯的絮凝沉淀物。
3 結(jié)論
當(dāng)pH 值臨近酪蛋白等電點(diǎn)4.6 時(shí),酪蛋白與木糖醇復(fù)合物的功能特性(溶解性、乳化性、起泡性、疏水性) 均較差。復(fù)合物內(nèi)源熒光值大幅度降低。分子結(jié)構(gòu)穩(wěn)定性較差。當(dāng)pH 值遠(yuǎn)離等電點(diǎn)時(shí),酪蛋白與木糖醇復(fù)合物的功能特性(溶解性、乳化性、起泡性、疏水性) 均顯著提高。內(nèi)源熒光值明顯升高。分子結(jié)構(gòu)穩(wěn)定性較好。
在生產(chǎn)和加工含有酪蛋白- 木糖醇復(fù)合物的食品的過(guò)程中,應(yīng)避免環(huán)境pH 值臨近酪蛋白等電點(diǎn),趨于中性或弱堿性的pH 值環(huán)境較好。

