全方位透視氫鍵在2023年高考命題中的體現
邵 鴻 孫 晶
(1.山東省臨沂第十九中學 2.山東省日照市莒縣第四中學)
氫鍵在教材中著墨不多,卻是高考不可或缺的知識點.高考命題中常以選擇題中的某個選項或選考題中一個小問的形式出現,命題常涉及兩種或幾種化合物比較其熔沸點或溶解性等.若對氫鍵知識了解不深刻,很容易陷入解題誤區.本文對氫鍵的知識、高考命題呈現形式和答題模板進行闡釋,供大家參考.
1 全方位透視氫鍵知識
1.1 氫鍵的形成
氫鍵是指與分子中電負性較大的原子(一般是指O、N、F)相結合的氫原子和另一個分子中電負性極大的原子間產生的作用力.
1.2 氫鍵的相關概念
1)特點:具有飽和性和方向性.
2)本質:靜電作用.
3)表示方法:X—H…Y.
4)形成條件:
①電負性很大的原子(如N、O、F等);
②氫原子.
5)表示形式:X—H…Y,其中“—”是共價鍵,“…”是氫鍵.
1.3 氫鍵的強度
氫鍵介于范德華力與化學鍵之間,強度大小:范德華力<氫鍵<化學鍵.特別強調:氫鍵是特殊的分子間作用力,不屬于化學鍵.
1.4 氫鍵的分類
1)分子間氫鍵(含N、O、F分子間)
分子與分子之間會存在氫鍵的作用,同種分子之間可以存在氫鍵,某些不同種分子之間也可能形成氫鍵,如HF 分子間(如圖1)、NH3分子間(如圖2)、H2O 分子間(如圖3)、對羥基苯甲醛分子間(如圖4).
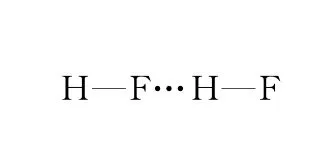
圖1
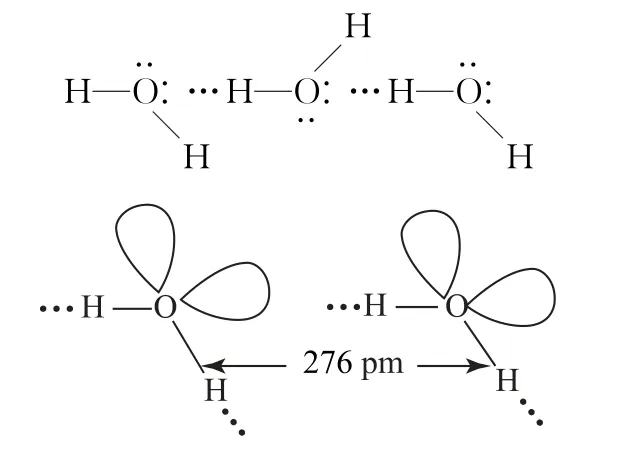
圖3
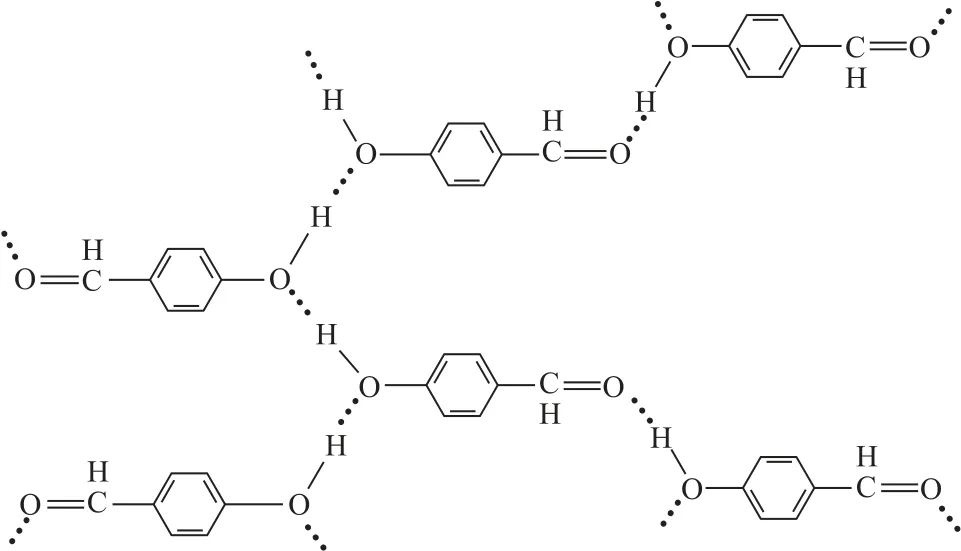
圖4
2)分子內氫鍵
某些分子內,如鄰羥基苯甲醛(如圖5)、HNO3(如圖6)可以形成分子內氫鍵.分子內氫鍵由于受環狀結構的限制,X—H…Y 往往不能在同一直線上.
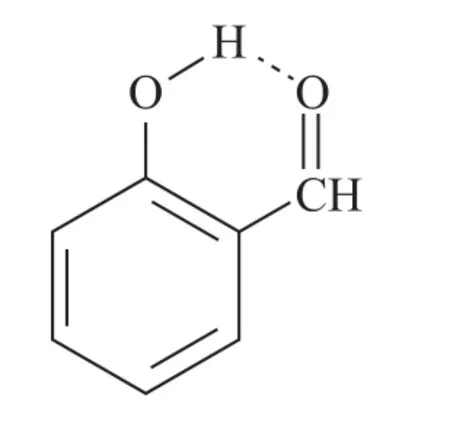
圖5
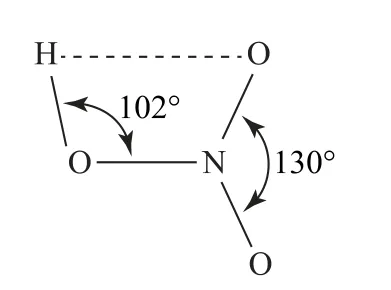
圖6
1.5 氫鍵對物質性質的影響
1)氫鍵對物質熔點、沸點的影響
a)分子間存在氫鍵時,物質在熔化或氣化時,除破壞普通的分子間作用力外,還需要破壞分子間的氫鍵,消耗更多的能量,所以存在分子間氫鍵的物質一般具有較高的熔點和沸點.
例如,第ⅤA~ⅦA 族元素的氫化物中,NH3、H2O 和HF的熔點、沸點比同主族相鄰元素的氫化物的熔點、沸點高,這種反常現象是由于它們各自的分子間形成了氫鍵,第ⅣA~ⅦA 族元素簡單氫化物的沸點變化趨勢如圖7所示.

圖7
b)對于互為同分異構體的物質,能形成分子內氫鍵的物質的熔點和沸點比能形成分子間氫鍵的物質的熔點和沸點低.如鄰羥基苯甲酸能形成分子內氫鍵,而對羥基苯甲酸能形成分子間氫鍵,當對羥基苯甲酸熔化時,需要較多的能量克服分子間氫鍵,所以對羥基苯甲酸的熔點和沸點高于鄰羥基苯甲酸的.
2)氫鍵對物質溶解性的影響
如果溶質與溶劑之間能形成氫鍵,則溶解性增大.氨分子與水分子間能形成氫鍵,且都是極性分子,所以NH3極易溶于水.低級的醇、醛、酮等可溶于水,都與它們的分子能與水分子間形成氫鍵有關.
3)氫鍵的存在引起密度的變化
由于水分子間的氫鍵,水結冰時,體積變大,密度變小,冰融化成水時,體積減小,密度變大.液體分子間若形成氫鍵,有可能發生締合現象.例如液態HF,在通常條件下,除了正常簡單的HF 分子外,還有通過氫鍵聯系在一起的復雜分子(HF)n.其中n可以是2,3,4,….這種由若干個簡單分子連成復雜分子而又不會改變原物質化學性質的現象,稱為分子締合.分子締合會影響液體的密度.
注意:H2O 分子之間也有締合現象.常溫下,液態水中除了簡單 H2O 分子之外,還有(H2O)2,(H2O)3,…,(H2O)n等締合分子存在.降低溫度,有利于水分子的締合.溫度降至0℃時,全部水分子結合成巨大的締合物——冰.
4)氫鍵的存在對分子黏度的影響
分子間有氫鍵的液體,一般黏度較大.例如甘油、磷酸、濃硫酸等多羥基化合物,由于分子間可形成眾多的氫鍵,這些物質通常為黏稠狀液體.
2 氫鍵在2023年高考題中的呈現形式
2.1 判斷氫化物和有機物的熔沸點
2.2 判斷氫鍵的存在與規范表述
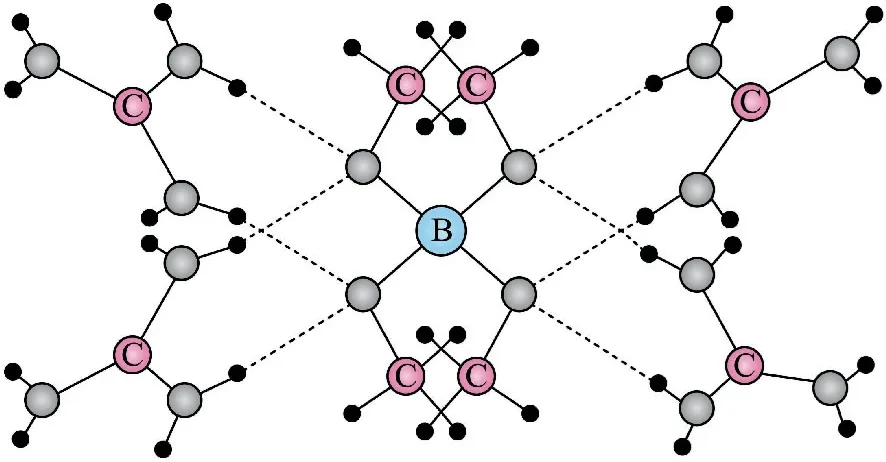
圖8
A.該晶體中存在N—H…O 氫鍵
B.基態原子的第一電離能:C<N<O
C.基態原子未成對電子數:B<C<O<N
D.晶體中B、N 和O 原子軌道的雜化類型相同
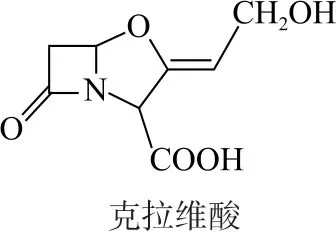
圖9
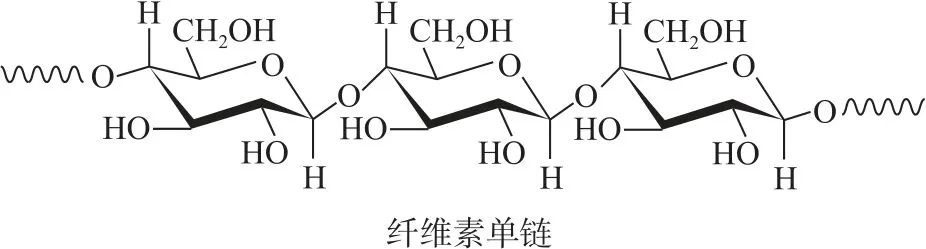
圖10
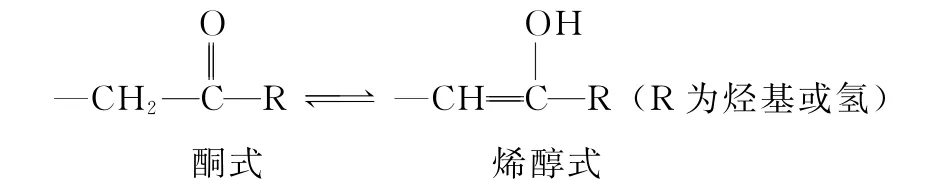
圖11
A.存在順反異構
B.含有5種官能團
C.可形成分子內氫鍵和分子間氫鍵
D.1mol該有機物最多可以和1mol氫氧化鈉溶液反應
2.3 考查氫鍵對物質溶解性的影響
A.纖維素是自然界分布廣泛的一種多糖
B.纖維素難溶于水的主要原因是其鏈間有多個氫鍵
C.NaOH 提供OH-破壞纖維素鏈之間的氫鍵
D.低溫降低了纖維素在NaOH 溶液中的溶解性
2.4 考查有機物分子內氫鍵的形成
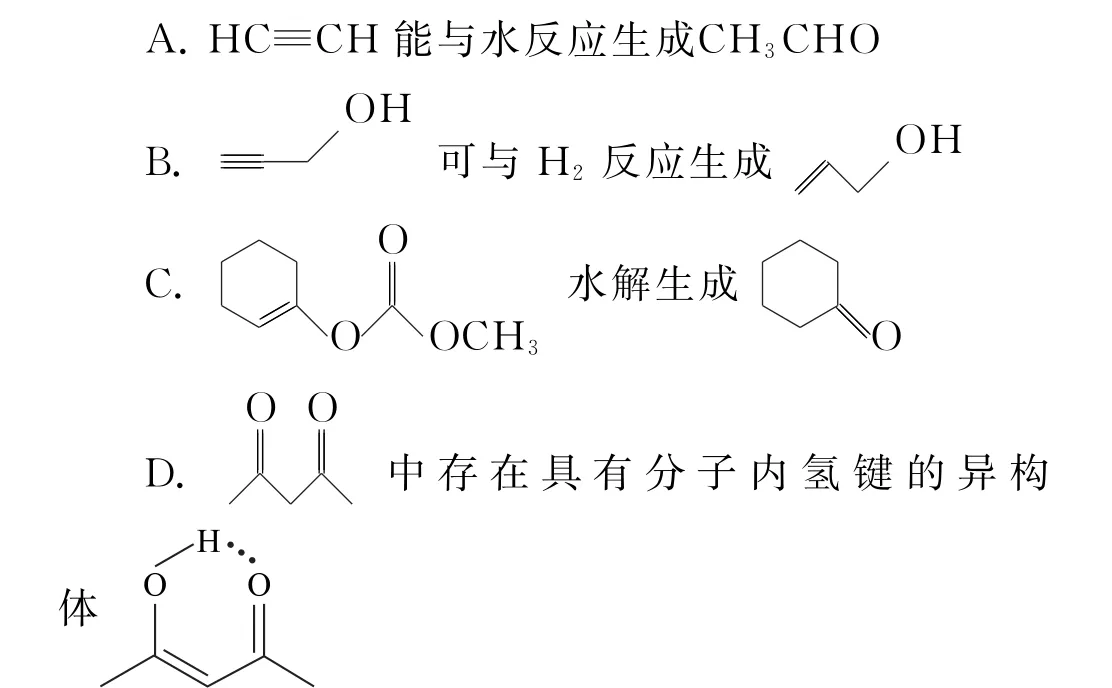
3 氫鍵答題策略與答題模板
3.1 氫鍵與熔、沸點
1)答題策略:分子形成分子間氫鍵會使物質熔沸點升高,而形成分子內氫鍵會使物質熔沸點降低.
2)答題模板:同為分子晶體,×××存在氫鍵,而×××僅存在較弱的范德華力.
例如,乙酸的沸點明顯高于乙醛,其主要原因是:同為分子晶體,CH3COOH 存在分子間氫鍵,而乙醛僅存在較弱的范德華力.
再如,鄰羥基苯甲醛的沸點比對羥基苯甲醛的沸點低,原因是:鄰羥基苯甲醛形成分子內氫鍵,而對羥基苯甲醛形成分子間氫鍵,分子間氫鍵使分子間作用力更大.
3.2 氫鍵與溶解性
1)答題策略:若溶質與溶劑之間能形成氫鍵,則溶解度增大,且氫鍵作用力越大,溶解性越好.
2)答題模板:×××與H2O 或其他溶劑(×××)分子間形成氫鍵.
例如,NH3極易溶于水的原因是:NH3與水分子間形成氫鍵.
(完)

