晶體和配合物中微粒配位數的判斷
賴小海
(江西省新余市第四中學)
在教學的過程中,筆者常常發現學生對配位數的概念和數目判斷總是很困惑,容易出錯.本文從不同類型的晶體和配合物的角度來分析粒子的配位數,引導學生理解并能快速判斷出粒子的配位數.
配位數就是指一個粒子周圍相鄰且最近的粒子個數.物質的配位數與晶體結構或晶胞類型有著密切的關系,且決定了晶體中粒子堆積的緊密程度.粒子排列越緊密,配位數就越大,晶體結構就越穩定.
1 晶體
1.1 分子晶體
在分子晶體中,配位數是指一個分子周圍相鄰且最近的分子數目.
1)如果分子間作用力只有范德華力,則每個分子的周圍最多有12個緊鄰的分子,即“分子密堆積”,因此該晶體中分子的配位數為12.例如,干冰的晶胞結構示意圖如圖1所示.
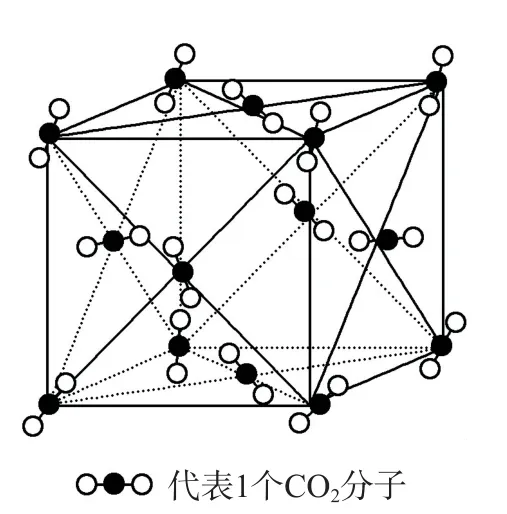
圖1
通過觀察并分析干冰的晶胞結構可知:每個CO2分子周圍緊鄰且等距離的CO2分子有12 個,所以CO2分子的配位數為12.C60、O2、I2、CO、白磷等分子晶體,它們的配位數都是12.
2)如果分子間作用力主要為氫鍵,由于氫鍵具有方向性,會迫使在中心的分子與形成氫鍵方向的分子相互吸引,這一排列使晶體中分子的空間利用率不高,留有相當大的空隙(即分子非密堆積).例如,冰的結構示意圖如圖2所示.
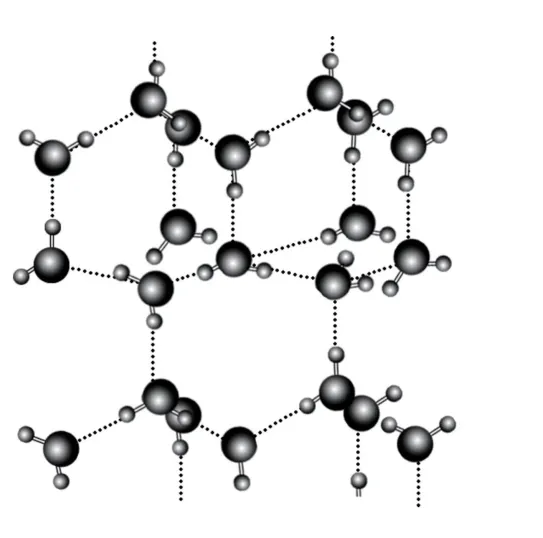
圖2
通過觀察并分析冰的結構可知:處于四面體中心的水分子與四面體頂角方向的4個相鄰的水分子相互吸引,所以水分子的配位數為4.
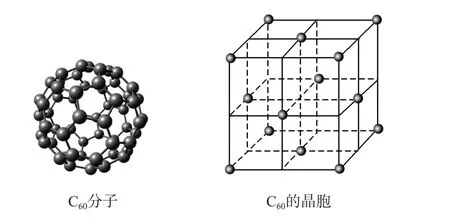
圖3
A.C60晶體可能具有很高的熔、沸點
B.C60晶體可能易溶于四氯化碳中
C.C60晶體的1個晶胞中含有的碳原子為240個
D.C60晶體中C60的配位數為12
1.2 共價晶體
在共價晶體中,配位數是指一個原子周圍相鄰且最近的原子的數目.由于共價鍵具有方向性和飽和性,所以元素的共價數決定了原子的配位數.
1)金剛石型.金剛石(C)的晶體結構和晶胞示意圖如圖4所示.
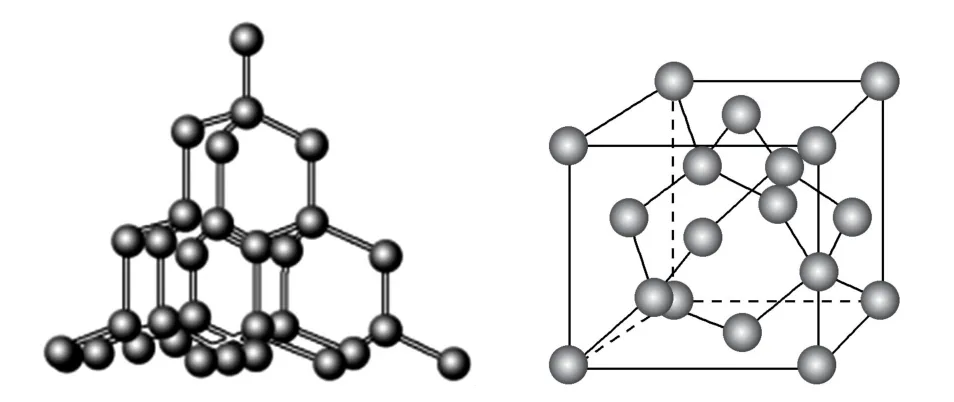
圖4
在金剛石晶體中,每個碳原子以4根共價單鍵與相鄰的4個碳原子相連,所以C原子的配位數是4.類似的還有晶體硅、鍺、灰錫,它們的原子的配位數都是4.
2)二氧化硅型.二氧化硅(SiO2)的晶體結構和晶胞示意圖如圖5所示.
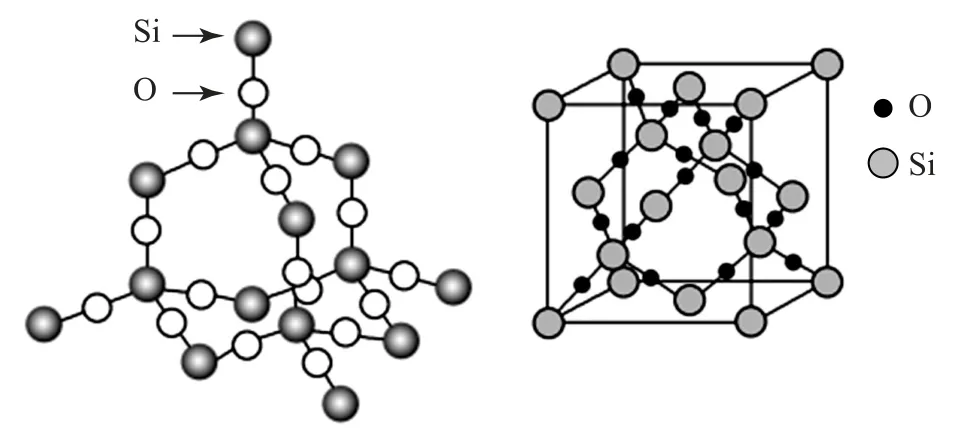
圖5
在二氧化硅晶體中,每個Si原子和4個O 原子相連形成4根共價鍵,所以Si原子的配位數是4.而每個O 原子和2個Si原子相連形成2根共價鍵,所以O 原子的配位數是2.
3)碳化硅型.碳化硅(SiC)的晶胞示意圖如圖6所示.
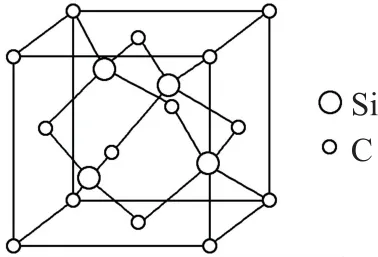
圖6
在SiC 晶體中,每個Si原子和4個C原子相連形成4根共價鍵,所以Si原子的配位數是4.每個C原子和4個Si原子相連形成4根共價鍵,所以C原子的配位數也是4.類似的還有BN、AlN、BP,它們的原子的配位數都是4.
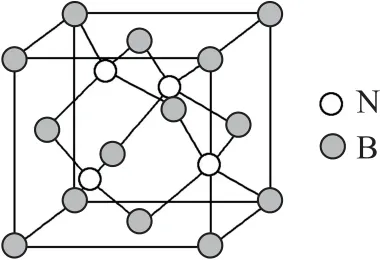
圖7
A.11BN和10BN 的性質無差異
B.該晶體具有良好的導電性
C.該晶胞中含有4個B原子,4個N 原子
D.該晶胞中B和N 的配位數都是4
1.3 金屬晶體
在金屬晶體中,配位數是指一個金屬原子周圍相鄰且最近的金屬原子的數目.金屬單質晶體中金屬原子的配位數主要是與金屬原子的堆積方式有關.
1)簡單立方.其晶胞及配位原子的空間位置示意圖如圖8所示.
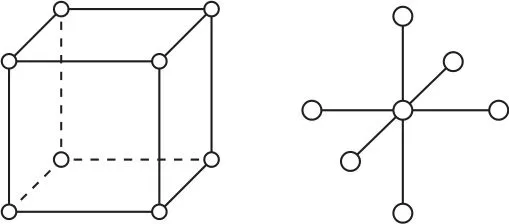
圖8
在簡單立方晶胞中,每個金屬原子周圍相鄰最近且距離相等的金屬原子有6個,所以金屬原子的配位數為6.例如,釙等金屬原子的配位數為6.
2)面心立方.其晶胞及配位原子的空間位置示意圖如圖9所示.
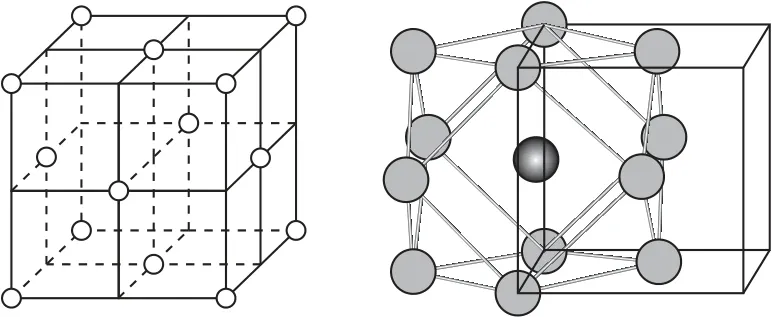
圖9
在面心立方晶胞中,以面心原子為中心分析,上、中、下三層各有4個金屬原子,即每個金屬原子周圍相鄰最近且距離相等的金屬原子有12個,故金屬原子的配位數為12.例如,Cu、Ag等金屬原子的配位數都是12.
3)體心立方.其晶胞及配位原子的空間位置示意圖如圖10所示.
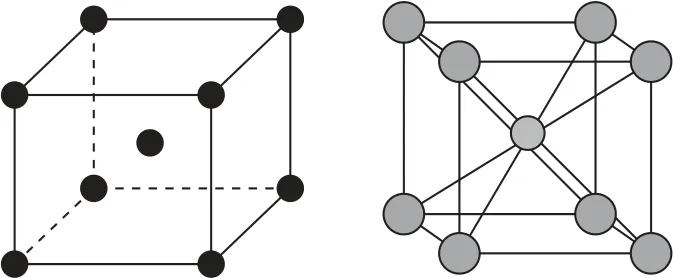
圖10
在體心立方晶胞中,每個金屬原子周圍相鄰最近且距離相等的金屬原子有8個,所以金屬原子的配位數為8.例如,鈉、鉀、鉻等金屬原子的配位數都為8.
4)六方最密堆積.其晶胞及配位原子的空間位置示意圖如圖11所示.
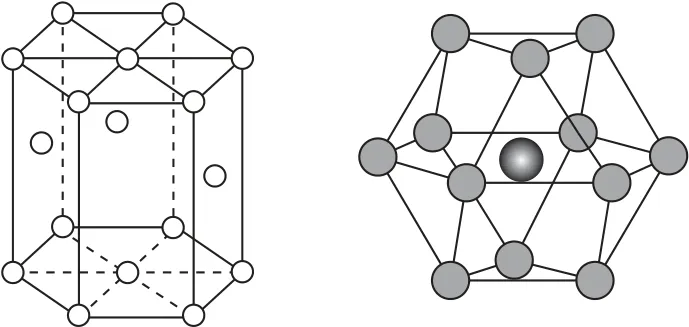
圖11
在六方最密堆積晶胞中,以面心原子為中心分析,上、中、下三層分別有3、6、3個金屬原子,即每個金屬原子周圍相鄰最近且距離相等的金屬原子有12個,所以金屬原子的配位數為12.例如,Zn、Mg、Ti等金屬原子的配位數都是12.
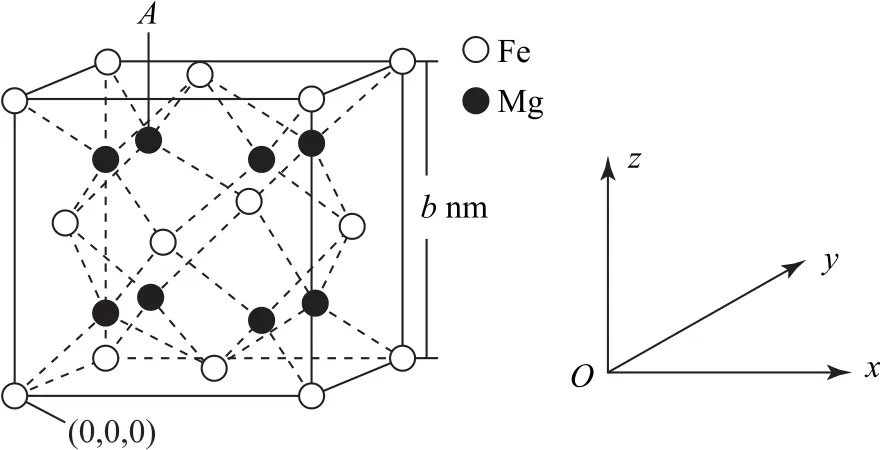
圖12
A.Fe原子的配位數為4
B.A位置原子的坐標為(0.25,0.75,0.75)
D.晶體儲氫時,H2在晶胞的體心和棱的中心位置,若儲氫后化學式為FeMg2H,則儲氫率為100%
1.4 離子晶體
在離子晶體中,配位數是指一個離子周圍相鄰且最近的帶相反電荷離子的數目.
1)氯化鈉型.NaCl的晶胞及配位離子的空間位置示意圖如圖13所示.
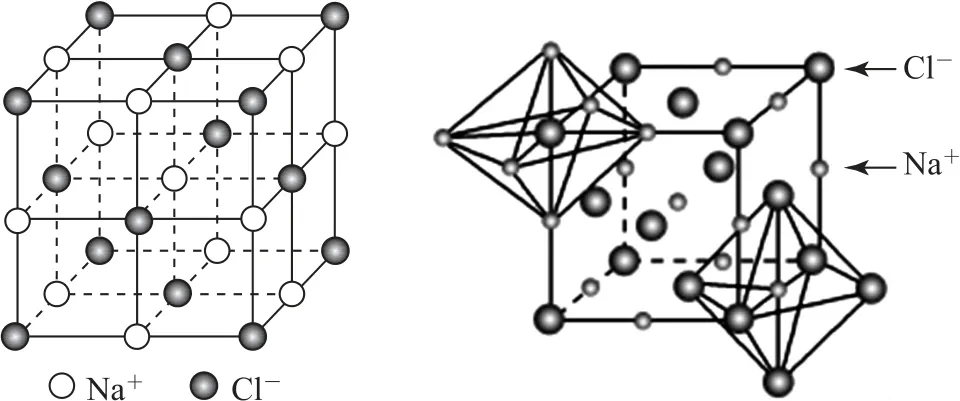
圖13
在NaCl晶體中,與Na+相鄰最近且距離相等的Cl-有6個,所以Na+的配位數為6.與Cl-相鄰最近且距離相等的Na+有6個,所以Cl-的配位數為6.
2)氯化銫型.CsCl的晶胞及配位離子的空間位置示意圖如圖14所示.
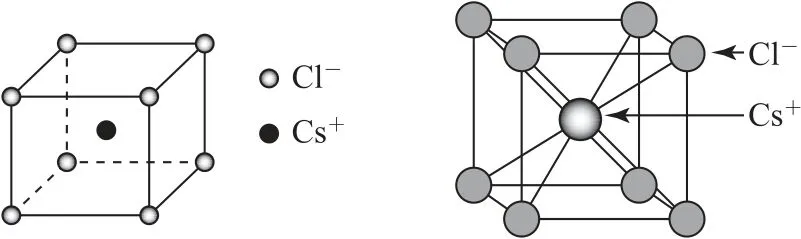
圖14
在CsCl晶體中,與Cs+相鄰最近且距離相等的Cl-有8個,所以Cs+的配位數為8.與Cl-相鄰最近且距離相等的Cs+有8個,所以Cl-的配位數為8.
3)硫化鋅型.ZnS 的晶胞示意圖如圖15所示.
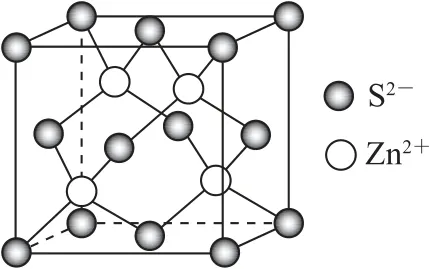
圖15
在ZnS 晶 體 中,與Zn2+相鄰最近且距離相等 的S2-有4 個,所 以Zn2+的配位數為4.與S2-相鄰最近且距離相等的Zn2+有4個,所以S2-的配位數也為4.
4)氟化鈣型.CaF2的晶胞示意圖如圖16所示.
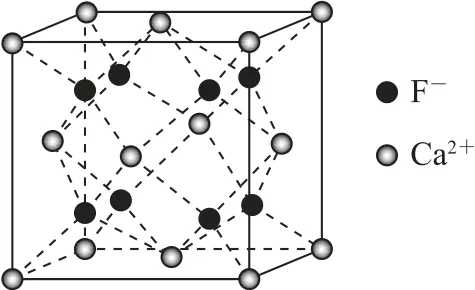
圖16
在CaF2晶體中,與Ca2+相鄰最近且距離相等的F-有8個,所以Ca2+的配位數為8.與F-相鄰最近且距離相等的Ca2+有4個,所以F-的配位數為4.
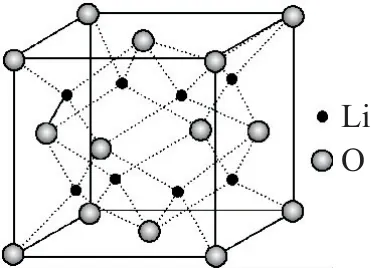
圖17
A.Li+在晶胞中的配位數為8
B.Li+和O2-之間只有靜電引力
C.Li+和O2-的最短距離為
D.阿伏加德羅常數的值為NA,晶胞密度為
1.5 混合型晶體
混合型晶體的結構特點是層狀結構,層與層之間以范德華力維系.每一層的內部通過共價鍵相結合形成平面結構,因此原子的配位數等于該原子的共價數.混合型晶體最典型的代表是石墨晶體,其三維和二維平面結構示意圖如圖18所示.
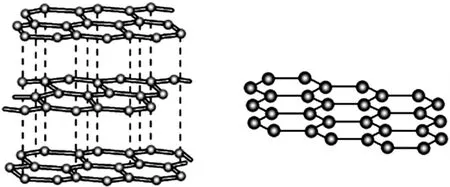
圖18
在石墨晶體中,每一層的內部都是通過共價鍵相結合形成平面六元并環結構,所以每個碳原子與周圍的3個碳原子形成3根共價鍵,碳原子的配位數為3.
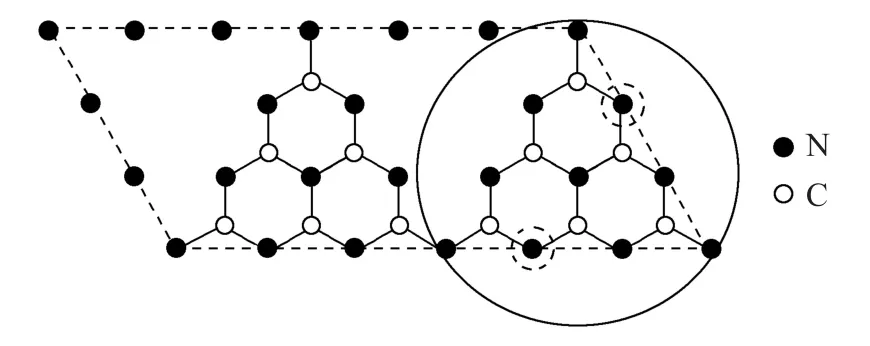
圖19
g-C3N4中,C 原子的雜化軌道類型為_________,N 原子的配位數為________.
2 配合物
在配位化合物中,配位數是指直接同中心離子(或原子)配位的原子數目,也叫中心離子(或原子)的配位數.
中心離子(或原子)配位數的多少與中心離子(或原子)和配體的性質(如電荷數的多少、體積的大小、電子層結構等)以及形成配合物的條件(如溫度、濃度等)有關.因此,不同的金屬離子其配位數往往是不同的,即使是同一價態的金屬離子的配位數也不是固定不變的.在配合物中,配位數由1到14,其中最常見的配位數為2、4、6.
2.1 配位數等于配體的數目
當中心離子(或原子)與單基配體配位時,其配位數等于配體的數目.例如,配合物[Ag(NH3)2]OH、[Ag(CN)2]NO3中Ag+的配位數均為2;配合物[Cu(H2O)4]Cl2、[Cu(NH3)4]SO4中Cu2+的配位數均為4;配合物K3[Fe(CN)6]、K3[Fe(SCN)6]、K3[FeF6]中Fe3+的配位數均為6;Ni(CO)4、Fe(CO)5、Cr(CO)6等羰基化合物中,中心原子Ni、Fe、Cr的配位數分別為4、5、6.
當中心離子(或原子)與多種單基配體配位時,其配位數等于配體數目的總和.例如,配合物[Co(NH3)4(H2O)2]Cl2中Co2+的配位數為6;配合物[CrCl(H2O)5]Cl2中Cr3+的配位數為6.
2.2 配位數等于配體數目的2倍
當中心離子(或原子)與雙基配體配位時,配位數等于配體數目的2倍.例如,配合物[Cu(NH2CH2CH2NH2)2]2+中 NH2CH2CH2NH2屬于雙基配體,每個乙二胺(NH2CH2CH2NH2)分子中有2個N 原子與Cu2+配位,形成2個配位鍵,所以Cu2+的配位數為4.
2.3 特殊情況
在有配位鍵的非配合物中,中心離子(或原子)同時以共價鍵和配位鍵與其他原子(或離子)相結合,其配位數不等于配位鍵的數目.例如,在[B(OH)4]-、[Al(OH)4]-、[BF4]-、[AlCl4]-、Al2Cl6這5種微粒中,中心離子(或原子)都是用3根共價鍵和1根配位鍵與其他原子(或離子)結合的.Al2Cl6的結構式如圖20所示.所以Al的配位數是4.
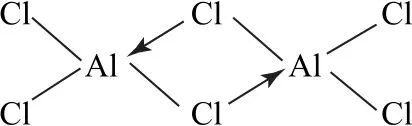
圖20
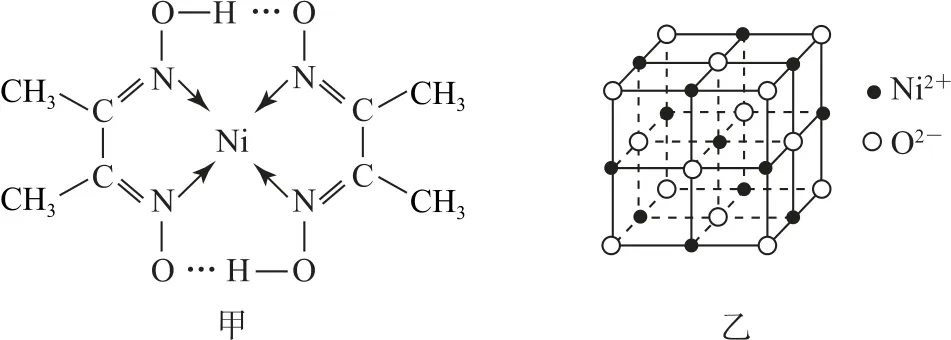
圖21
A.圖乙中離Ni2+最近的Ni2+共有12個
B.圖甲分子中存在的化學鍵有共價鍵、配位鍵、氫鍵
C.圖甲、乙中Ni2+的配位數分別為4和6
D.圖乙表示的可能是氧化鎳(NiO)的晶胞
(完)

