研究新高考真題 探秘共價鍵備考方向
劉艷影 董 順
(1.安徽省渦陽縣第四中學 2.安徽省碭山中學)
2023年新高考(含新教材老高考)地區是使用新教材后的首次高考,這些地區的高考真題為今后的復習備考指明了方向.2023 年高考試題的命題依據是《普通高中化學課程標準(2017 年版2020 年修訂)》(以下簡稱“新課標”).分析2023年新高考地區涉及共價鍵的試題(含新課標卷),我們能夠發現,試題完全依據新課標命題,具體統計如表1所示.
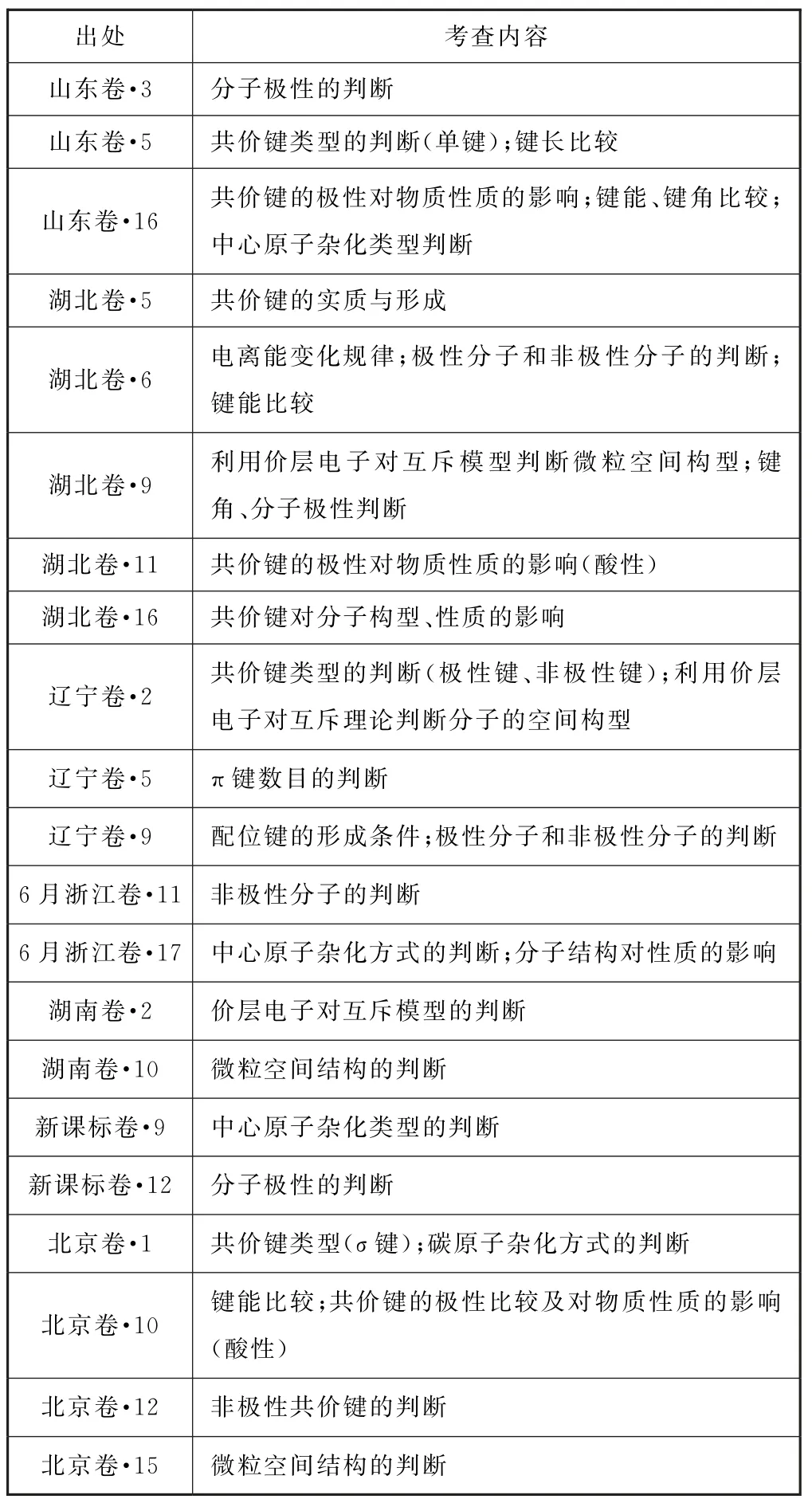
表1

表2
1 共價鍵的實質、形成過程及類型
原子軌道在兩個原子核間重疊,意味著電子出現在核間的概率增大,因此可以說,核間電子好比在核間架起一座帶負電的橋梁,把帶正電的兩個原子核“黏結”在一起了.共價鍵按照電子云重疊方式不同可以分為σ鍵(電子云通過“頭碰頭”方式重疊,常見的有s—sσ鍵、s—pσ鍵、p—pσ鍵及雜化軌道間、雜化軌道與s軌道、p軌道間形成的σ鍵等)和π鍵(電子云通過“肩并肩”方式重疊).其中,π鍵可以分為定域π鍵、大π 鍵(如SO2、O3中的鍵、、SO3中的鍵等)、d—pπ鍵(如H3PO4、H2SO4中非羥基氧原子的p軌道與中心P、S原子3d軌道形成的π鍵)等;按照成鍵兩原子電負性的不同可以分為極性鍵和非極性鍵;按照共用電子對數的不同可以分為單鍵(均為σ鍵)、雙鍵(1個為σ鍵,1個為π鍵)和三鍵(1個為σ鍵,2個為π鍵).
A.(湖北卷·5節選)用電子云輪廓圖表示H—H的s—sσ鍵形成的示意圖(如圖1).

圖1
B.(遼寧卷·5節 選)11.2 L CO2含π 鍵數 目為NA
C.(遼寧卷·2節選)P4中的共價鍵類型:非極性鍵
D.(北京卷·12節選)Na2O2、CaH2中均有非極性共價鍵
E.(湖北卷·11 節選)酸性:CF3COOH(pKa=0.23)遠強于CH3COOH(pKa=4.76),結構因素是羥基極性不同
2 鍵參數的比較與應用
鍵能是指氣態分子中1 mol共價鍵解離成氣態原子所吸收的能量,鍵能的大小可以衡量共價鍵的強弱.
鍵長是構成共價鍵的2個原子的核間距.不過,分子中的原子始終處于不斷振動之中,鍵長只是振動著的原子處于平衡位置時的核間距.成鍵兩原子半徑決定化學鍵的鍵長.原子半徑越小,共價鍵的鍵長越短.對于相同的兩原子形成的共價鍵而言,當2個原子間形成雙鍵、三鍵時,由于原子軌道的重疊程度增大,原子之間的核間距減小,鍵長變短,故單鍵鍵長>雙鍵鍵長>三鍵鍵長.一般來說,鍵長越短,鍵能越大,但也有特殊情況,比如鍵長:F—F<Cl—Cl,但鍵能也是F—F<Cl—Cl,這是由于F原子半徑很小,因此F—F的鍵長短,2個F 原子形成共價鍵時,原子核之間的距離小,排斥力大,因此鍵能小.
另外,鍵能:碳碳單鍵<碳碳雙鍵<碳碳三鍵,但碳碳雙鍵的鍵能小于碳碳單鍵鍵能的兩倍,說明其中的σ鍵鍵能>π鍵鍵能,這也就解釋了烯烴、炔烴性質比烷烴性質活潑的事實.
為什么N2分子不活潑呢? N2分子結構可簡單地寫為,即2個N 原子之間有1個σ鍵,2個π鍵.同時,每個N 原子有1對孤對電子.在N2分子中,每個N 原子有1對孤對電子,N 原子的孤對電子的電子云較集中于N≡N 分子的外側,因而使N 原子上的有效正電荷大,所以對2 個π 鍵的成鍵電子吸引較強,造成N2分子的活性低.
鍵角是指在多原子分子中,2個化學鍵之間的夾角.CO2鍵角為180°,是一種直線形分子;H2O 分子中的H—O—H 鍵角是105°,是一種V 形(或稱角形)分子.多原子分子中的鍵角一定,表明共價鍵具有方向性.
A.(山東卷·5節選)(CF)x中C—C 的鍵長比C—F短
B.(湖北卷·6節選)鍵能:N2<O2<F2
C.(湖北卷·16節選)導致SiCl4比CCl4易水解的因素有Si—Cl鍵鍵能更大,Si—Cl鍵極性更大
D.(北京卷·10節選)不能通過比較氟元素與氯元素的電負性解釋F—F的鍵能小于Cl—Cl的鍵能
3 價層電子對互斥(VSEPR)模型及應用
1)模型要點
a)價層電子對在空間上彼此相距最遠時,排斥力最小,體系的能量最低.
b)孤電子對的排斥力較大,孤電子對數越多,排斥力越強,鍵角越小.
2)用價層電子對互斥理論推測分子的空間結構
價層電子對數包括σ鍵電子對數和孤電子對數,其中σ鍵電子對數等于中心原子結合的原子數.對于ABn型微粒,價層電子對數(中心原子價電子數+配體提供的電子數×n-微粒所帶電荷數).其中,鹵素原子和氫原子作配體時提供1個電子,O、S作配體時不提供電子.
A.(遼寧卷·2節選)BeCl2的空間結構:V 形
B.(湖南卷·2節選)NH3分子的VSEPR 模型:
C.(浙江6 月·2節 選)H2S 分 子 的球棍 模型:
D.(浙江6月·2節選)AlCl3的價層電子對互斥模型:
4 分子極性的判斷
1)化合價法:多原子分子(ABn型).
中心原子化合價的絕對值=該元素的價電子數→該分子為非極性分子→分子的空間結構中心對稱(直線形、平面三角形、正四面體形……).
常見ABn型分子的極性判斷如表3所示.

表3
2)空間結構對稱法(如表4).

表4
A.CS2B.NF3C.SO3D.SiF4
共價鍵是新高考的熱點內容,共價鍵理論在解釋元素化合物及有機化合物性質中發揮著重要的作用.學習共價鍵時要關注其應用,這樣不僅能加深對理論的理解,還會促進對元素化合物及有機物性質的認識.在復習備考中一方面要關注新教材的變化和描述,另一方面要關注新高考地區的試題,明確高考的方向,這樣會使復習備考事半功倍.
(完)

