SETD1A與KDM4A在非小細胞肺癌中的表達及臨床價值
朱小慧,李亞云,張海燕,劉海濤,于志娟
肺癌是最常見的惡性腫瘤,全球每年發病220萬例,死亡180萬例[1]。非小細胞肺癌(non-small cell lung cancer,NSCLC)占所有肺癌類型的85%[2]。對于可切除的早中期NSCLC,手術是首選的治療方案,但仍有術后復發、轉移的風險[3]。組蛋白賴氨酸甲基轉移酶SET結構域包含1A (histone lysine methyltransferase SET domain containing 1A,SETD1A)是組蛋白賴氨酸甲基轉移酶SET1家族成員,能夠特異性催化組蛋白H3賴氨酸4位點3甲基化,促進下游基因的轉錄[4]。研究表明,SETD1A在直腸癌[5]、前列腺癌[6]等惡性腫瘤中表達上調,能誘導插頭框M1的轉錄,促進腫瘤惡性增殖及侵襲。賴氨酸去甲基酶4A (lysine demethylase 4A,KDM4A)具有組蛋白去甲基化功能,參與染色質結構調節、表觀遺傳學信號傳導[7]。研究發現,前列腺癌等腫瘤中KDM4A的表達能誘導腫瘤上皮間質轉化,促進腫瘤侵襲和轉移[8]。目前NSCLC中SETD1A、KDM4A表達及臨床意義尚不明確。本研究通過檢測NSCLC中SETD1A、KDM4A的表達,探討兩者臨床意義,報道如下。
1 資料與方法
1.1 臨床資料 選取2017年1月—2020年1月南通市腫瘤醫院綜合內科收治NSCLC患者116例為研究對象,男65例,女51例,年齡32~83(61.79±6.47)歲;腫瘤直徑:≤5 cm 者66例,>5 cm者50例;病理類型:腺癌78例,鱗癌38例;腫瘤TNM分期:Ⅰ~Ⅱ期81例,Ⅲ期35例;腫瘤分化程度:高中分化70例,低分化46例;合并淋巴結轉移33例;接受術后輔助化療42例。本研究經醫院倫理委員會審核批準通過(LW2023010),患者或家屬知情同意并簽署知情同意書。
1.2 病例選擇標準 (1)納入標準:①所有患者均接受根治性手術切除治療,且術后組織病理檢查確診為NSCLC;②首次診治;③臨床資料完整。(2)排除標準:①確診后合并其他惡性腫瘤;②術后30 d內因并發癥或合并癥死亡;③既往有放化療及靶向藥物治療史;④合并嚴重的肝腎等臟器衰竭。
1.3 觀測指標與方法
1.3.1 SETD1A、KDM4A表達檢測:采用免疫組織化學方法檢測。術中留取部分癌組織和癌旁組織(距離癌組織邊緣2 cm以上),10%多聚甲醛固定12 h,常規石蠟包埋切片。EG1150石蠟包埋機及RM2235切片機購自德國徠卡公司。通用型兩步法免疫組化染色試劑盒購自北京中杉金橋公司,貨號PV9000。梯度水化后檸檬酸鹽溶液中進行抗原熱修復,5%山羊血清室溫封閉2 h,滴加兔抗人SETD1A單克隆抗體(稀釋比1∶200,購自abcam公司,貨號ab243881)和兔抗人KDM4A單克隆抗體(稀釋比1∶100,購自abcam公司,貨號ab191433),4℃過夜,滴加HRP標記二抗,室溫孵育30 min,二氨基聯苯胺顯色4 min,蘇木素復染,梯度脫水后樹膠封片。鏡下觀察染色情況(DX31顯微鏡購自日本奧林巴斯公司),染色強度評分判定:未著色為0分,淺黃色為1分,棕褐色為2分。腫瘤陽性細胞所占面積評分:陽性細胞數≤5%為0分,6%~25%為1分,26%~49%為2分,≥50%為3分。陽性染色判定根據染色強度及陽性細胞所占的面積評分的乘積計算,乘積≥2分為陽性,<2分為陰性。
1.3.2 術后隨訪:NSCLC患者出院后進行定期隨訪,以門診、電話或網絡方式進行,隨訪截止至2023年2月1日。術后第1年每3個月隨訪1次,第2、3年每6個月隨訪1次。隨訪內容為患者生存狀態和生存時間。隨訪終點為患者死亡或隨訪結束。
2 結 果
2.1 NSCLC癌組織和癌旁組織中SETD1A、KDM4A表達比較 NSCLC癌組織中SETD1A棕黃色陽性染色主要位于細胞核,KDM4A陽性染色主要位于細胞漿和細胞膜。見圖1。NSCLC癌組織SETD1A陽性率為61.21%(71/116),高于癌旁組織的6.90%(8/116),差異有統計學意義(χ2=76.546,P<0.001)。NSCLC癌組織中KDM4A陽性率為65.52%(76/116),高于癌旁組織的8.62%(10/116),差異有統計學意義(χ2=80.487,P<0.001)。
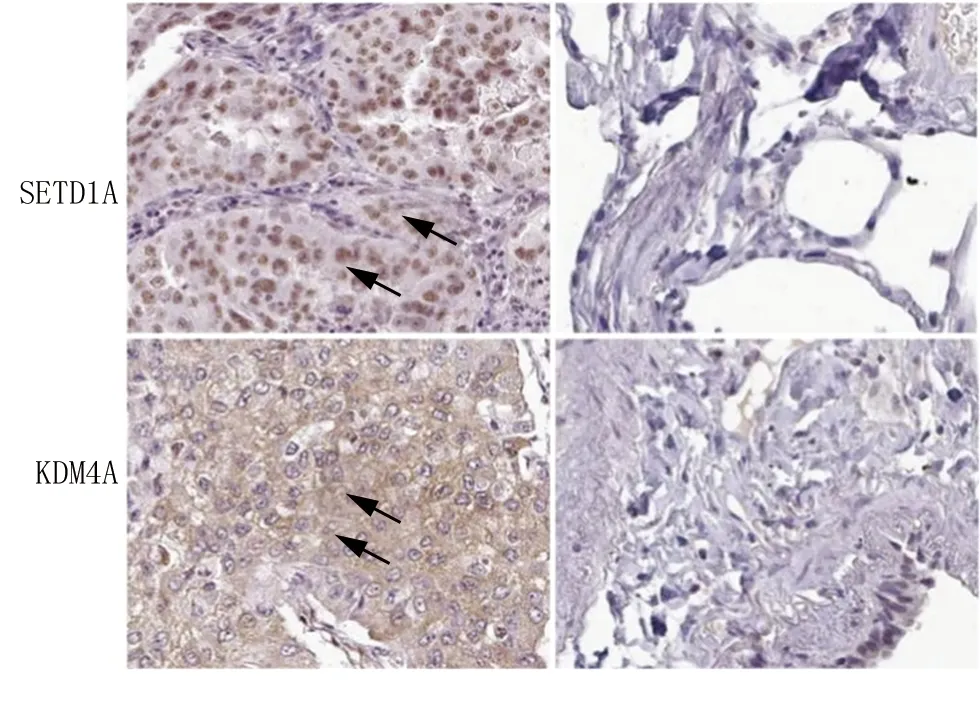
注:箭頭為SETD1A陽性染色定位于細胞核,KDM4A陽性染色位于細胞漿和細胞膜。圖1 NSCLC癌組織和癌旁組織中SETD1A、KDM4A表達比較(免疫組化染色,×200)Fig.1 Comparison of SETD1A and KDM4A expression in NSCLC cancer tissue and adjacent tissues (immunohistochemical staining, × 200)
2.2 NSCLC癌組織中SETD1A、KDM4A表達的相關性 Spearman秩相關分析,NSCLC癌組織中SETD1A與KDM4A表達呈顯著正相關(rs=0.722,P<0.001)。
2.3 癌組織中SETD1A、KDM4A表達在NSCLC患者不同臨床病理特征中比較 TNM分期Ⅲ期、低分化程度、伴淋巴結轉移患者在NSCLC癌組織中SETD1A、KDM4A陽性率高于TNM分期Ⅰ~Ⅱ期、高中分化程度、無淋巴結轉移患者,差異均有統計學意義(P均<0.05),見表1。
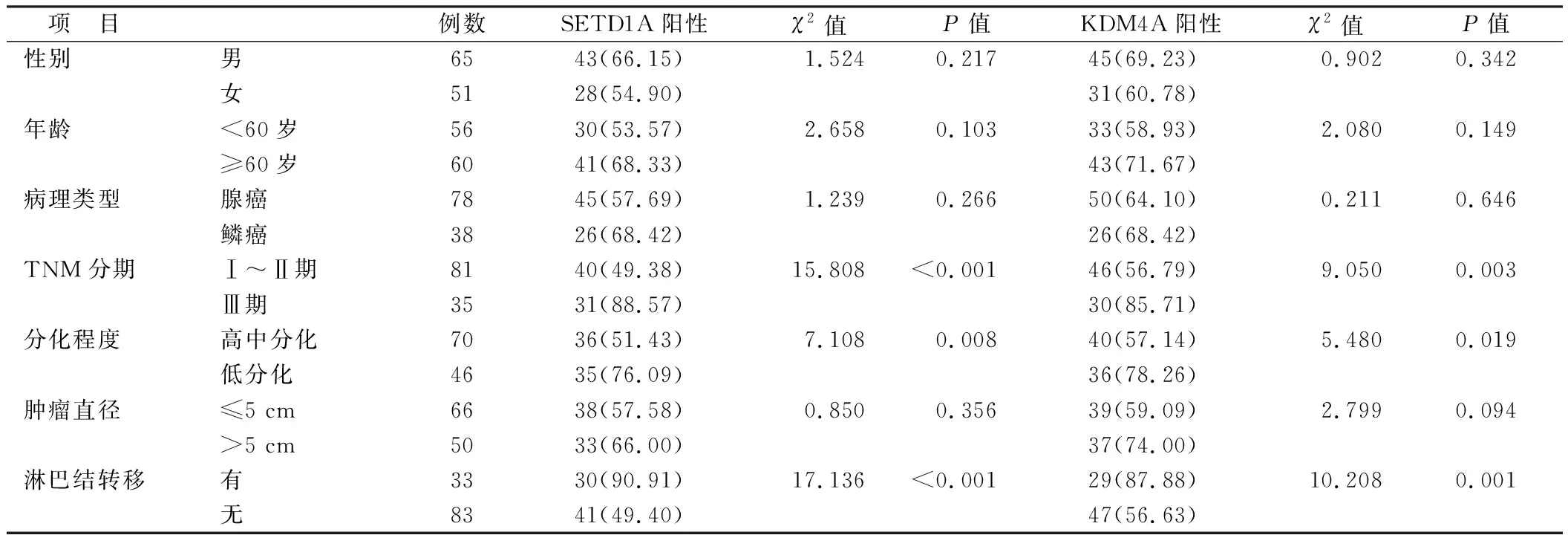
表1 SETD1A、KDM4A表達在NSCLC不同臨床病理特征中比較 [例(%)]Tab.1 Comparison of SETD1A and KDM4A expression in different clinical and pathological features of NSCLC
2.4 癌組織中SETD1A、KDM4A表達與NSCLC患者生存預后關系 116例NSCLC患者隨訪過程中,失訪3例,死亡44例,3年總體生存率為61.21%(71/116)。SETD1A陽性組和陰性組患者3年總體生存率分別為49.28%(34/69)、78.72%(37/47)。Kaplan-Meier分析結果,SETD1A陽性組患者3年累積生存率明顯低于陰性組患者(χ2=12.984,P<0.001)。KDM4A陽性組和陰性組3年總體生存率分別為48.65%(36/74)、83.33%(35/42)。Kaplan-Meier分析結果,KDM4A陽性組患者3年累積生存率明顯低于陰性組患者(χ2=17.175,P<0.001),見圖2。
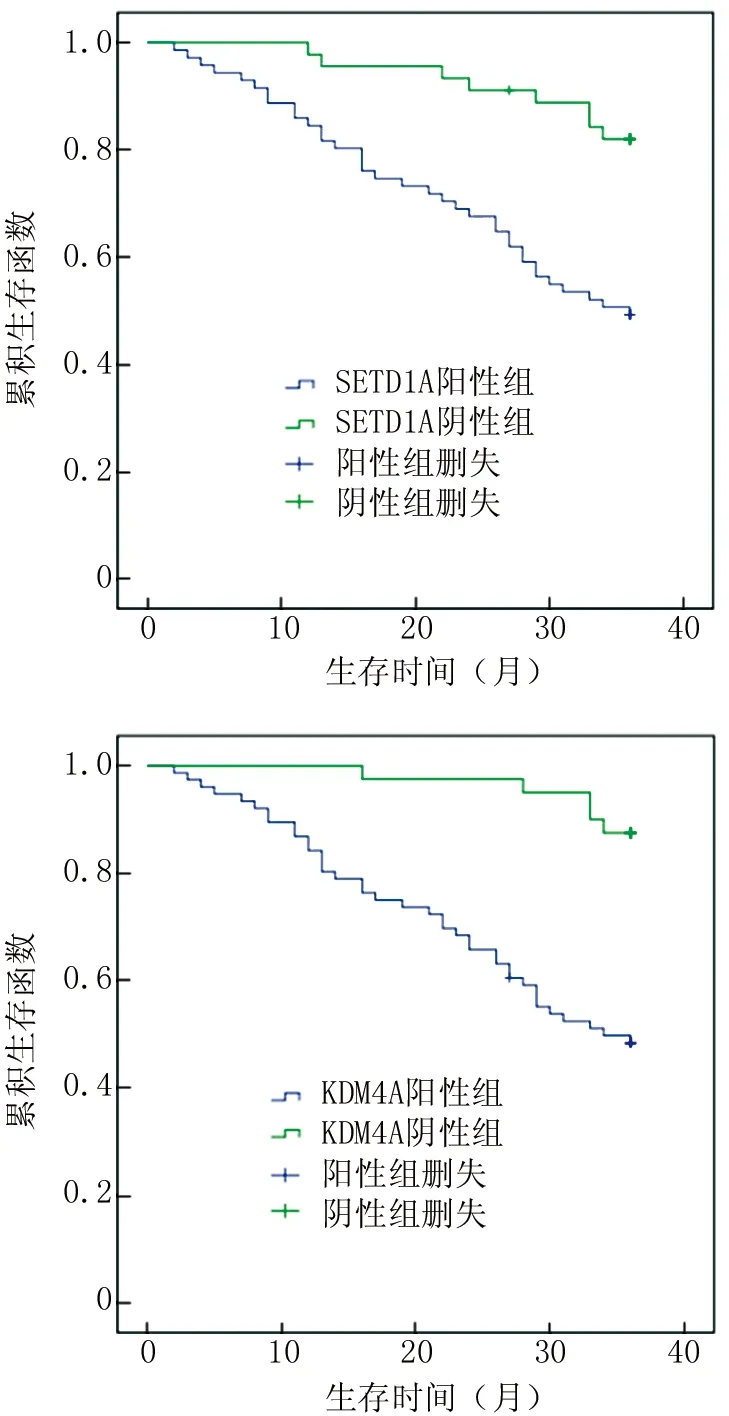
圖2 癌組織中SETD1A、KDM4A表達與NSCLC患者生存預后關系Fig.2 Relationship between the expression of SETD1A and KDM4A in cancer tissue and the survival and prognosis of NSCLC patients
2.5 影響NSCLC預后的多因素Cox回歸分析 以NSCLC預后情況為因變量,以上述結果中P<0.05項目為自變量,進行多因素Cox回歸分析,結果顯示,TNM分期Ⅲ期、合并淋巴結轉移、SETD1A陽性、KDM4A陽性為影響NSCLC患者不良預后的獨立危險因素(P<0.01),見表2。

表2 影響NSCLC預后的多因素Cox比例風險回歸模型比較Tab.2 Comparison of Cox proportional risk regression models with multiple factors affecting the prognosis of NSCLC
3 討 論
NSCLC是最常見的肺癌類型,由于NSCLC早期無特異性臨床癥狀,確診時患者多處于中晚期,生存預后較差,5年生存率僅19%[9]。目前臨床上NSCLC預后評估主要采用TNM分期及病理分型等,但TNM分期忽略機體免疫狀態、健康狀況等其他因素,在評估臨床預后上存在一定的缺陷。因此,深入研究NSCLC疾病機制,尋找能夠有效評估NSCLC患者臨床預后的生物標志物,具有重要的臨床意義。組蛋白的甲基化能夠調節染色質整體的松散及緊密程度,引起基因表達的增強或抑制,參與DNA復制、重組及修復等生物學過程。近年來發現,組蛋白甲基化修飾涉及的甲基化酶和去甲基化酶是組蛋白甲基化修飾的關鍵因子,參與腫瘤等疾病發生發展過程的調節[10]。
SETD1A又稱為SET1,廣泛表達于全身上皮、神經等多種組織中,其作為一種組蛋白賴氨酸甲基化轉移酶,能夠將甲基基團轉移到目標賴氨酸ε-氨基基團上,促進靶基因轉錄活化。研究發現,SETD1A通過激活缺氧誘導因子1α的表達促進糖酵解,促進胃癌細胞增殖及轉移[11]。本研究中,NSCLC組織中SETD1A表達升高,與既往研究中NSCLC中SETD1A mRNA表達升高的結果一致[12],但鑒于蛋白是分子功能的執行者,本研究在蛋白水平檢測SETD1A表達,結果更為準確。NSCLC中SETD1A表達升高可能受非編碼RNA的調節。研究表明,胃癌中長鏈非編碼RNA FOXD2-AS1表達上調,其作為分子海綿結合抑制微小RNA-1913的表達,微小RNA-1913的下游靶基因SETD1A mRNA穩定性增加,導致SETD1A蛋白表達升高,腫瘤增殖及抗凋亡能力增強[13]。本研究中,SETD1A表達與NSCLC患者TNM分期、腫瘤分化程度及淋巴結轉移有關,提示SETD1A促進NSCLC的腫瘤進展。研究發現,NSCLC腫瘤細胞中SETD1A能夠與Zeste同源物增強子2的啟動子結合并誘導其發生組蛋白H3賴氨酸4位點3甲基化,上調Zeste同源物增強子2基因的轉錄,激活Wnt/β-連環蛋白通路,導致腫瘤細胞侵襲和轉移能力增強[12]。本研究發現,癌組織SETD1A陽性是影響NSCLC患者不良生存預后的獨立危險因素,提示SETD1A是新的評估NSCLC患者預后的腫瘤標志物。分析其原因,一方面是SETD1A陽性表達腫瘤細胞存在上皮間質轉化的現象,間質性標志物N-鈣黏素表達升高,而上皮性標志物E-鈣黏素表達下調,腫瘤細胞侵襲和轉移能力較強,腫瘤術中難以徹底清除,術后腫瘤易發生復發轉移,導致患者不良預后[14]。另一方面, SETD1A的表達升高能夠通過促進Yes相關蛋白的磷酸化激活,促進腫瘤細胞對索拉非尼等靶向治療藥物的耐藥性形成,而敲除腫瘤細胞中SETD1A的表達能夠增強索拉非尼對腫瘤的增殖抑制效應[15]。
KDM4A是一種組蛋白去甲基化轉移酶,能夠以二價鐵離子、α-酮戊二酸為共底物,促進賴氨酸去甲基化,參與基因轉錄、細胞周期調控及DNA損傷修復等生物學過程[16]。近年來發現,骨肉瘤中KDM4A能夠促進溶質載體家族7成員11啟動子區的組蛋白H3賴氨酸9位點去甲基化,抑制腫瘤細胞鐵死亡發生,導致腫瘤進展[17]。本研究中,NSCLC中KDM4A表達升高,提示KDM4A參與NSCLC腫瘤的發生,與既往學者在NSCLC腫瘤細胞系中報道結果一致[18]。NSCLC中KDM4A表達上調與腫瘤缺氧微環境有關。研究發現,腫瘤組織缺氧能夠上調KDM4A的表達,進而通過組蛋白H3賴氨酸9位點3甲基化增強缺氧誘導因子1α轉錄,促進血管內皮生長因子及葡萄糖轉運蛋白1的表達,增強腫瘤惡性增殖及轉移能力[19]。此外,KDM4A表達與患者TNM分期、腫瘤分化程度及淋巴結轉移有關,表明KDM4A促進NSCLC腫瘤的惡性進展。有學者在NSCLC腫瘤細胞中發現,KDM4A過度表達能促進遠端缺失同源盒5的去甲基化,增加遠端缺失同源盒5的轉錄活性,激活癌基因Myc的表達和下游Wnt/β-連環蛋白信號通路,促進NSCLC腫瘤細胞的增殖、侵襲及轉移[18]。本研究中,KDM4A陽性表達NSCLC患者生存預后較差,提示KDM4A是一種新的評估NSCLC預后腫瘤標志物。既往亦有學者證實,亞洲人群中KDM4A基因rs586339位點A等位基因多態性能夠增加患者不良生存預后的風險[20]。另外,KDM4A表達升高能夠降低白血病腫瘤細胞中組蛋白H3賴氨酸36位點3甲基化水平,激活DNA損傷修復通路,導致腫瘤對阿糖胞苷等化療藥耐藥性的形成,而應用KDM4A的抑制劑JIB-04處理腫瘤細胞后,能夠重新恢復腫瘤細胞對阿糖胞苷的敏感性[10]。因此,KDM4A作為新的NSCLC預后相關腫瘤標志物,以KDM4A為靶點的治療可能有助于改善患者臨床預后,值得今后進行深入研究。
本研究中,NSCLC中SETD1A與KDM4A表達呈顯著正相關,提示兩者可能在NSCLC中發揮協同作用。SETD1A主要通過組蛋白3賴氨酸4位點的三甲基化,促進下游癌基因的轉錄激活,而KDM4A主要促進組蛋白3賴氨酸9和36位點的去甲基化,重新激活基因起始位點的轉錄,促進癌基因的表達[21]。因此,NSCLC中SETD1A與KDM4A可能存在協同的作用關系,共同加快NSCLC腫瘤的惡性進展。但兩者在NSCLC中的相互作用機制仍有待今后進行深入的實驗研究。
綜上所述,SETD1A、KDM4A在NSCLC中的表達升高,二者與腫瘤TNM分期、腫瘤分化程度及淋巴結轉移有關,均促進NSCLC的腫瘤發生發展過程。SETD1A、KDM4A陽性是影響NSCLC患者不良生存預后的獨立危險因素,臨床醫生可根據NSCLC患者SETD1A、KDM4A的表達,對其生存預后進行評估,對高危患者采取相應的治療及隨訪方案,以改善NSCLC患者的臨床預后。但本研究由于樣本量有限,未對NSCLC中SETD1A、KDM4A具體作用機制進行深入研究,有待今后設計大樣本的臨床研究,深入研究兩者的作用機制及臨床意義。
利益沖突:所有作者聲明無利益沖突
作者貢獻聲明
朱小慧、李亞云:設計研究方案,實施研究過程,論文撰寫;張海燕、于志娟:提出研究思路,分析試驗數據,論文審核;劉海濤:資料搜集整理,實施研究過程,進行統計學分析

