發展模型認知素養 滲透電性效應思想*
——以高三一輪復習課“廣義水解”教學為例
車 耀 錢 勝 吳 軍 劉小玲
(1. 重慶市銅梁一中 重慶 銅梁 402560;2. 重慶市教育科學研究院 重慶 渝中 400000;3. 東北師范大學教育學部 吉林 長春 130024;4.重慶黔江新華中學 重慶 黔江 409099;5. 重慶市銅梁二中 重慶 銅梁 402560)
“模型認知”是研究化學和學習化學的重要方法,被納入化學學科核心素養體系。《普通高中化學課程標準(2017年版2020年修訂)》指出[1]:教學中“通過分析、推理等方法認識研究對象的本質特征、構成要素及其相互關系,建立認知模型,并能運用模型解釋化學現象,揭示現象的本質和規律。”在教學實施建議中明確指出,要利用模型提高教學質量和效率。仔細品味《課程標準》中相關論述的準確性和深刻性,相關論述理所當然地成為指導我們教學的重要依據,無可置疑地成為衡量我們教學質量的重要標準。
高中化學教學中,有許多思想的建立和運用,如氧化還原反應思想、強換弱的思想、平衡思想、守恒思想以及實驗為主的思想等,唯獨“電性效應”思想很容易被人遺忘。[2]本節課把“電性效應”思想滲透到化學反應的教學中去,讓學生更有效地理解化學反應的本質,避免學生機械記憶,提高學生學習化學的效率。
一、課題內容及教學現狀
1.水解知識的教學
在新授課階段,水解知識分布在鹽類的水解和有機物中鹵代烴、酯類和糖類等物質水解這幾個部分。幾個部分之間的邏輯關系在教材上沒有充分的體現;新課教學過程中,因為教學進度等原因,教師較少有意識地建立幾者之間的聯系,至于水解反應的本質原理分析則涉及更少。學生只能機械地記憶水解方程式,形成零散的知識碎片。
在一輪復習過程中,會圍繞某些問題設計合適的微專題,將高中化學各部分的知識有機地聯系在一起,讓學生歸納和整理原有知識,使之條理化、結構化,培養學生的創新能力和知識遷移能力。高三一輪復習教學為水解原理的分析及水解模型的建構提供了機會。
2.“電性效應”思想的教學
“電性效應”是指反應物粒子之間在發生化學反應時,帶異種電荷的兩種粒子相互吸引,帶同種電荷的兩種粒子相互排斥。發生化學反應時一定是帶相反電荷的兩種粒子或是中性粒子之間或帶電粒子與中性粒子之間結合,帶相同電荷的兩種粒子一定不會結合在一起。“電性效應”在化學反應中具有本質性和普遍性,有水參加的絕大多數反應都遵循“電性效應”思想。但是,在日常的教學中,教師往往就某個化學反應進行分析講解,不能有效涉及“電性效應”的本質。[3]在中國知網和百度學術網上以“電性效應”和“化學教學”為關鍵詞檢索文獻,只檢索到三篇文獻,[2-4]可見,一線教師對“電性效應”思想不夠重視。
二、教學思想及創新點
1.廣義水解及思想的滲透
學習既不是碎片化知識的簡單積累,又不是某些“專家結論”的簡單記憶,而是要將所學知識和經驗納入認知結構之中,促進學生知識結構化、網絡化構建,最終目標是學生思維能力和行動能力的深度發展。廣義水解可以理解為水與另一種化合物反應,該化合物分解為兩部分,水中H(H+)結合其中一部分,而-OH(OH-)結合另一部分,得到兩種或兩種以上新的化合物的過程,我們把滿足這些條件的化學反應都叫做水解反應,即從廣義上講,水解反應指水被(任何一種)化學物質分解的一切反應。[2-4]本節課的主要創新點是把高考中經常涉及到的有機化合物(如:鹵代烴、酯類、糖類、蛋白質等)水解反應,無機化合物(如:鹽類、金屬氮化物、碳化物、非金屬氯化物)水解反應等知識碎片融合成“廣義水解”,形成更具統攝力、更具普遍性、解釋功能更強大的學科概念;并把“電性效應”思想滲透到化學反應的教學之中,讓學生理解化學反應的本質。
2.水解模型建立及應用思路
新課改重視開展“素養為本”的教學,要求引導學生開展分類與概括、模型與解釋等具有學科特質的學習活動。學生之間通過協作分析最熟悉的FeCl3水解、乙酸乙酯水解反應,建立水解模型,利用模型解決相關的問題(見圖1),幫助學生形成清晰的問題解決思路。
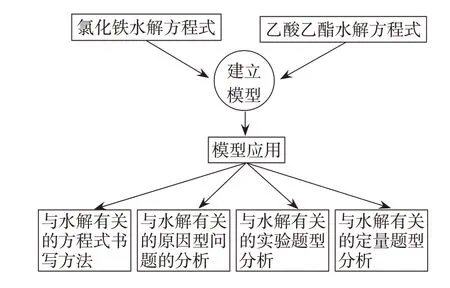
圖1 “廣義水解”設計思路
三、教學目標
依據課程標準的要求和對教材內容的分析,結合學生的實際情況,本節課以“化學反應中的水”為線索,設計如下教學目標:
1.通過對常見復分解反應的規律分析,初步樹立化學反應中的“電性效應”思想。
2.通過對典型水解反應方程式的本質分析,運用電性效應思想,建立水解反應模型。
3.通過對相關高考題型的分析,感受水解模型在解決與水解有關的問題方面的價值,進一步提升模型認知的素養。
四、教學流程設計(見圖2)
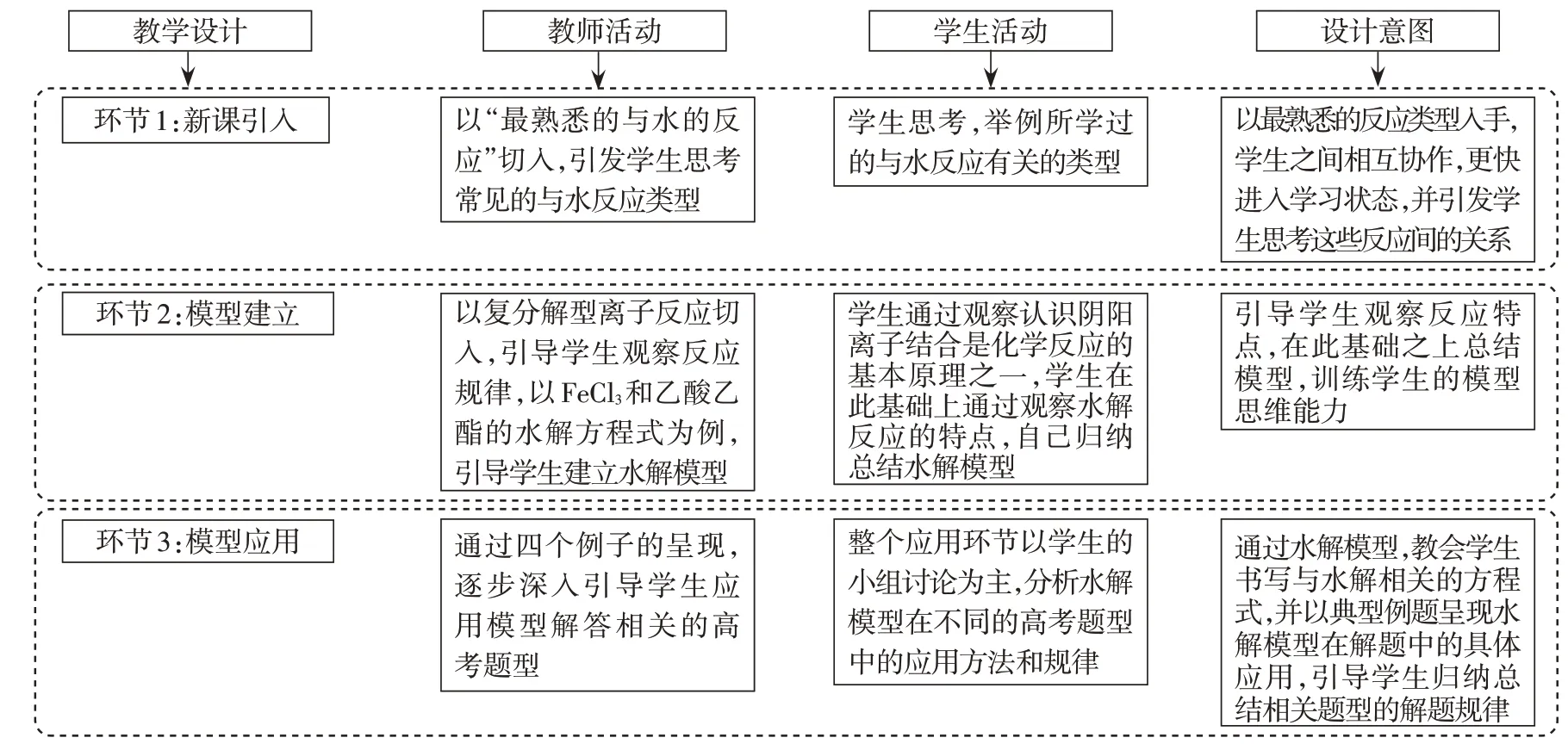
圖2 教學流程設計
五、教學過程
1.環節一:問題導入
【教師】說到水,同學們很熟悉。與水有關的反應很多,其中最基本、最常見的反應大家會想到哪一類?
【學生】水解反應。(復習課不同于新課講授,內容大多是學生學習過的已有知識,如何很好地引入,抓住學生的心是關鍵。本堂課以學生最熟悉的“水”引入,就是要讓學生在印象上建立熟悉感、親近感,拉近學生與教學的心理距離)
【教師】請同學們結合你們所學過的無機化學和有機化學知識,你學過的水解反應有哪些類型?
【小組匯報】
學生1 弱酸或弱堿形成的鹽水解。
學生2 淀粉、纖維素能水解。
學生3 鹵代烴、酯也能水解。
……
【播放PPT】根據學生的描述,展示水解反應的種類,引導學生將狹義的水解進入廣義水解(見圖3)。
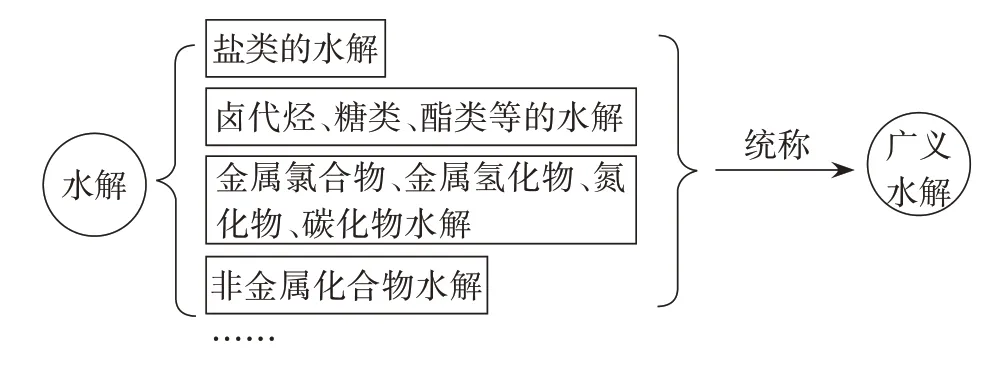
圖3 水解類別
【教師】同學們回答得很好,實際上能發生水解反應的物質,不僅僅是這些,還包括一些我們不熟悉的物質也可以發生水解,比如:非金屬化合物、金屬化合物,金屬氫化物、氮化物、金屬碳化物等。我們把這些水解反應統稱為廣義水解。本節課將結合我們已知的水解反應,將他們整合在一起,試著建立這類反應的基本模型,并運用模型解決相關問題。
【設計意圖】問題導入的環節從學生最熟悉的水解入手,讓學生在頭腦中搜索與水解有關的反應,水解知識會像電影畫面一樣在學生的頭腦中呈現,讓學生迅速進入到學習狀態。
2.環節二:模型建立
【提出問題】這些物質與水的反應有什么共同之處?
【教師】請觀察,下列離子反應有何特點?
【播放PPT】呈現三個常見離子反應,觀察離子間結合的規律(見圖4)。
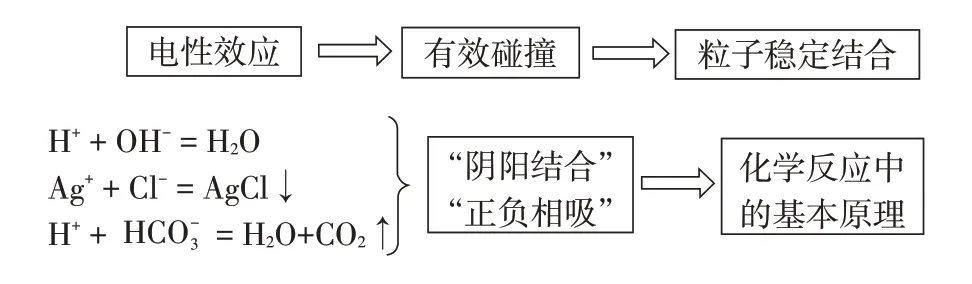
圖4 電性效應
【教師】“正負相吸”的電性效應是這類反應的本質,使不同的電荷的粒子靠近,發生有效碰撞,從而穩定地結合在一起。
【教師】“陰陽結合”、“正負相吸”是化學反應的本質,這是化學反應最基本的原理。
【教師】請觀察典型水解反應的特點
【播放PPT】分析氯化鐵和乙酸乙酯的水解方程式的特點(見圖5)。
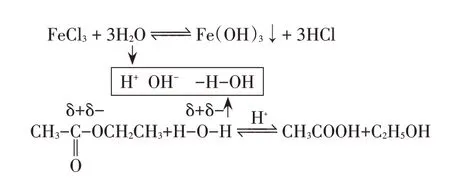
圖5 典型的水解反應
【教師】同學們,我們以大家最熟悉的兩個水解反應為例,看一看它們的反應特點,能水解的鹽存在陰陽離子,乙酸乙酯酯基中心C、O 原子根據電負性(同周期主族元素從左到右電負性增強)可以判斷攜帶正、負電荷,水也能離解出陰、陽離子,同學們試試,借助電性效應構建你心中有關這類反應的水解模型。
【學生活動1】嘗試借助電性效應構建這類反應的水解模型。
【學生展示】在草稿紙上書寫出自己所認為的反應模型(見圖6)。
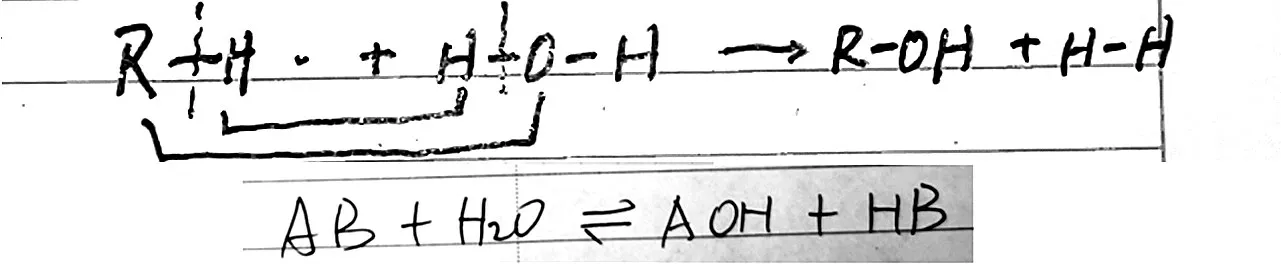
圖6 學生建立的“水解模型”
(學生能根據水解的方程式發現其中的規律,在表達的規范性上仍需要一定的引導)
【播放PPT】展示水解模型(見圖7)

圖7 水解模型
【教師】可以將化合物(包括水)離解成兩部分,其中心原子分別帶上正電荷和負電荷,甚至電離出陰陽離子,分別對應正價和負價,通過陰陽相吸結合成新的物質。接下來,請同學們以此模型為基礎,分析以下各類物質是否滿足該反應模型。
【設計意圖】引導學生分析典型的水解反應,運用電性效應的知識分析其反應的特點。把時間留給學生,相信學生,在課程實踐過程中有相當部分學生都能夠粗略建立水解模型,但是在建立過程中注意引導學生觀察鹽類水解的特點。
3.環節三:模型應用
【學生活動2】已知下列物質能與水劇烈反應,學生在作業本上完成下列物質與水反應的化學方程式:
【學生展示】學生所寫的水解方程式(見圖8)。
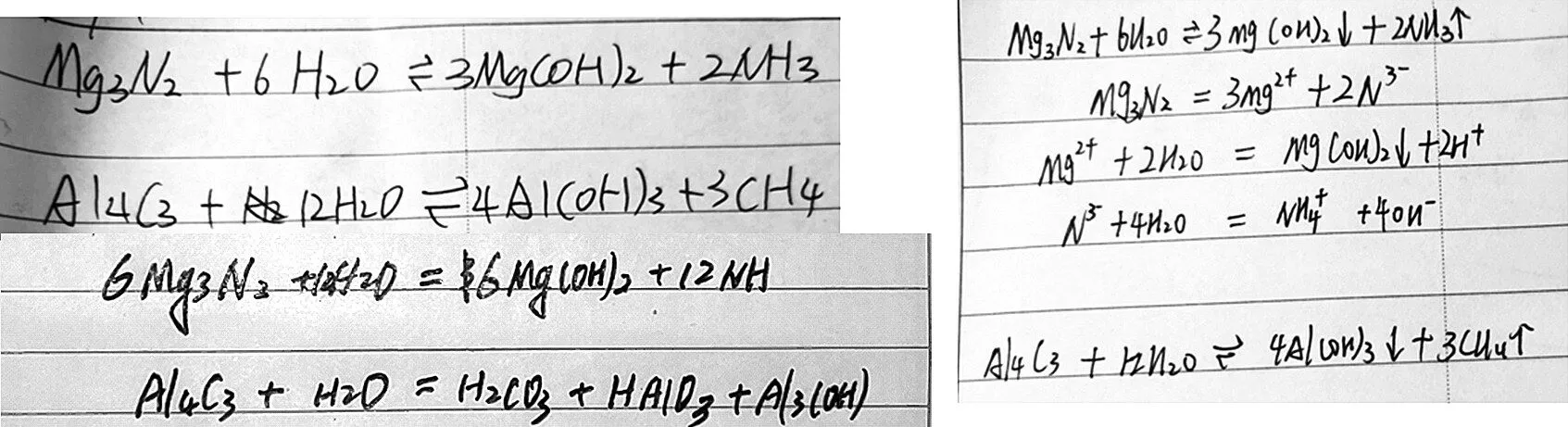
圖8 學生書寫的“水解方程式”
(其中Al4C3的水解書寫相對比較困難,需要引導學生理解CaC2與水的反應,并遷移應用。)
【播放PPT】呈現水解反應方程式和相關規律(見圖9)。
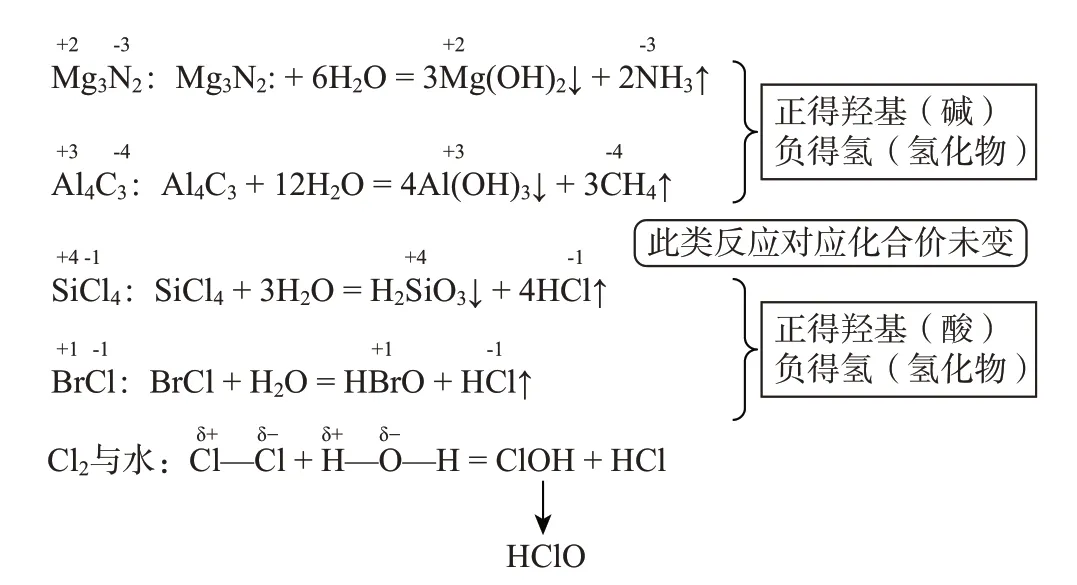
圖9 水解反應書寫規律
【教師】對于金屬化合物,可以從化合價入手,金屬顯正價帶正電荷,非金屬顯負價帶負電荷,與水反應分別生成對應的堿和氫化物,總結為:正得羥基(堿),負得氫(氫化物)。這類反應的特點是:化合價分別一一對應,均未發生變化,這也是書寫此類方程式的重要突破口。接下來,我們再看下一組:
【學生】利用水解模型,完成非金屬化合物與水反應的方程式(見圖10)。

圖10 學生書寫水解方程式
(這一組書寫的難點在BrCl 與水的反應,但正好可以利用這個反應原理給學生解釋HClO的結構式的正確表達方式,同時也可以給學生解釋含氧酸的結構,即為什么有的羥基形成酸而有的羥基形成堿。)
【教師】可以利用電負性大小確定物質中的正負化合價,根據模型寫出相應的化學方程式,BrCl 又叫鹵素互化物,根據剛才的模型,可以得出結論:正得羥基(酸);負得氫(氫化物)。
【設計意圖】模型應用環節,學生能否運用模型正確書寫方程式,關鍵在于能否正確分析化合物中心原子所帶的電荷。在實際教學中,學生完成金屬化合物水解反應書寫的正確率較高,也容易判斷正負電荷(正負價)的情況,但對于非金屬化合物的水解方程式的書寫錯誤率較高,主要原因是對正負電荷(正負化合價)的判斷,這部分知識需要學生理解并運用非金屬性強弱(同周期或同主族,比如BrCl)去判斷,或者通過非金屬元素的電負性大小進行判斷。
4.環節四:題型應用
【播放PPT】例1:高純硅是現代信息、半導體和光伏發電等產業都需要的基礎材料,工業上提純硅有多種路線,其中一種工藝流程示意圖及主要反應如下:
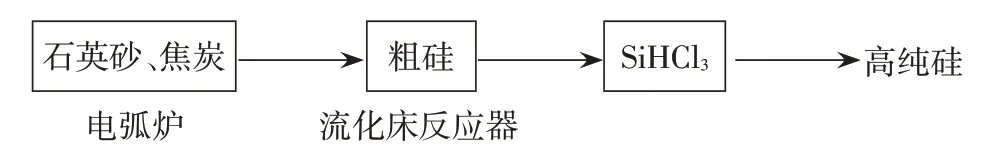
(3)有關物質的沸點數據如下表:
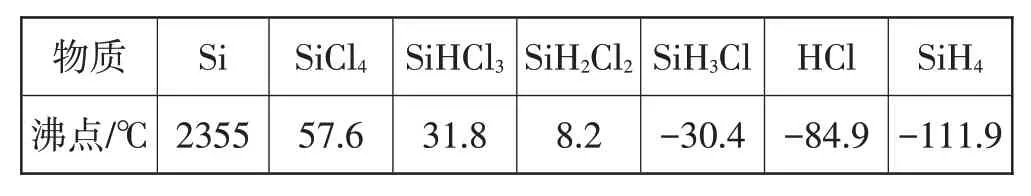
物質沸點/℃Si 2355 SiCl4 57.6 SiHCl3 31.8 SiH2Cl2 8.2 SiH3Cl-30.4 HCl-84.9 SiH4-111.9
SiHCl3極易水解,生成一種白色沉淀,同時有白霧產生,其完全水解的化學方程式為:_____________。
【教師】同學們體驗一下廣義水解在高考試題中的呈現方式。此題以高純硅的制備工藝流程為背景,其中涉及到甲硅烷氯代物的相關信息,根據題設中給出的相關信息,請寫出相關方程式。
【學生活動4】學生相互探討,并上黑板書寫方程式。
【教師】如何判斷相關元素的化合價是關鍵,根據信息應該生成H2SiO3和HCl,里面的氫是怎樣的存在,以SiH4為例,通過投影電負性表(見圖11),學生可以判斷H 為-1 價,根據模型可以判斷還有一種生成物為H2。與此類似的還有一些含H-的化合物如NaH、NaAlH4、NaBH4等,其書寫方法類似。
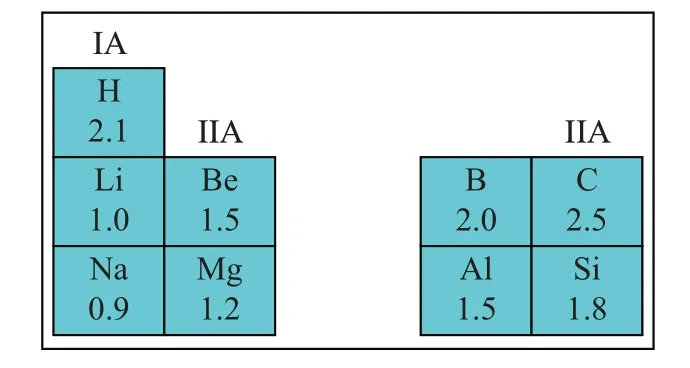
圖11 電負性表
【設計意圖】通過這道題型的演練,進一步明確水解反應的本質,即水解反應指水被(任何一種)化學物質分解的一切反應,[2]在前面的例子中涉及到的水解反應化合價均未發生變化,可能會給學生造成一個誤會,只是兩種異種電荷的粒子相互吸引形成新的物質。而在這幾個例子中,由于H-的存在,其具有的強還原性與H+結合,價態歸中生成H2,因此又將這個模型推廣到了某些氧化還原反應中。
【播放PPT】
例2(2021·浙江卷)Cl2O是很好的氯化劑,實驗室用如圖裝置(夾持儀器已省略)制備高純Cl2O。已知:
①HgO+2Cl2=HgCl2+Cl2O,合適反應溫度為18~25 ℃;副反應:2HgO+2Cl2=2HgCl2+O2。
②常壓下,Cl2沸點-34.0 ℃,熔點-101.0 ℃;Cl2O沸點2.0 ℃,熔點-120.6 ℃。
③Cl2O易與水反應:Cl2O+H2O=2HClO。
請回答:
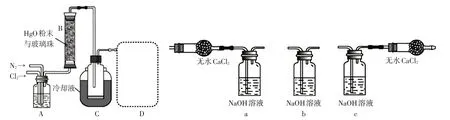
【小題1】①裝置A 的作用是去除原料氣中的少量水分,可用的試劑是___________________。
②將上圖中裝置組裝完整,虛框D中應選用。
【教師】同學們再看這道高考題,易與水反應的物質若在實驗題中出現,該怎么思考裝置的設計和評價(利用模型簡單介紹Cl2O與水反應的原理),對于Cl2O的制備,需要注意什么問題?
【學生活動5】學生思考并以小組為單位匯報結果。
【學生】防止與水反應。
【教師】對!同學們回答題目中的兩個問題,并思考這類實驗在設計時,你需要怎么綜合去考慮問題?
【學生活動6】學生思考并以小組為單位匯報結果。
【學生】濃硫酸和a。
(在這個環節中,問題主要出在第二個空,部分同學選擇了C,注意引導學生分析怎樣防止后面裝置與空氣中的水進入反應裝置。)
【教師】因為Cl2O易水解,如何防止水蒸氣進入制備裝置(B、C)是實驗成敗的關鍵,所以必須保證裝置進口和出口均需要安裝氣體干燥裝置,避免水蒸氣的進入。
【設計意圖】易與水反應的物質制備是高頻考點。在這種題中,如何分析與評價裝置和藥品的作用是考查的重點,同時還可能會考查水解方程式的書寫及相關反應的現象,不僅需掌握其反應原理,也要掌握其分析方法。
【播放PPT】例3:已知聯氨(N2H4)可用作火箭推進劑,其電離類似NH3,屬于二元弱堿(電離平衡常為K1、K2),常溫下將鹽酸滴加到N2H4的水溶液中,混合溶液中微粒的物質的量分數δ(X)隨-lgc(OH-)變化的關系如圖所示。下列敘述錯誤的是( )
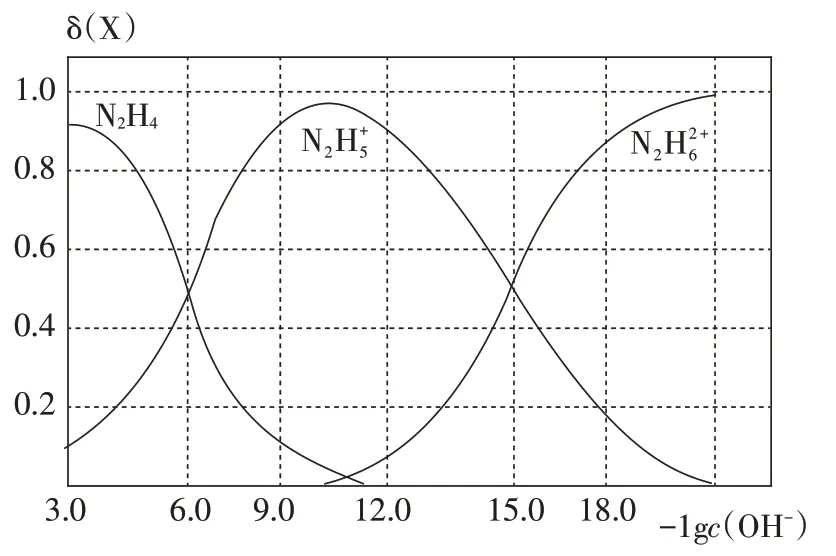
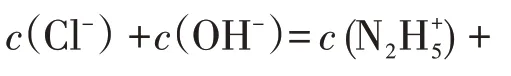
C.N2H5Cl溶液中:c(H+)>c(OH-)
D.Kb1(N2H4)=10-6.0
【教師】前面的各種題都跟水解有一定的關系,這道題可以進一步拓展模型的運用。要求算A、B選項,要寫出其電離方程式,告之N2H4電離方程式與NH3相似,同學們先寫出NH3在水中的電離方程式。
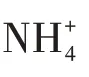
【播放PPT】利用模型書寫出的電離方程并進行分析(如下)。
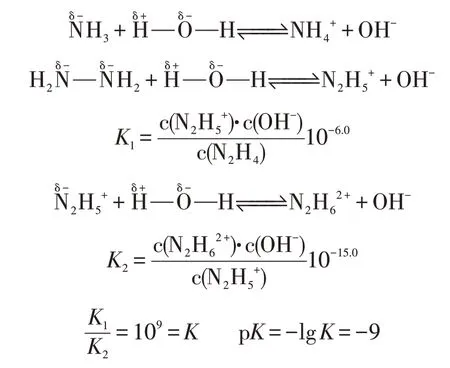
【教師】可以利用模型對N2H4的電離過程進行表達,從而分別表達出二者的電離平衡常數,再利用分布曲線兩個交點對應的pOH,得出K1和K2的數據,再觀察A 選項的平衡常數表達式,只需將K1和K2相比,得出常數,取負對數后等于9。所以D 正確,A 錯誤,選擇A。
【設計意圖】本題型運用水解模型解題,實質已超越了水解,但模型仍然成立,模型還有進一步拓展運用的空間,本題的設計目的也是想將模型應用由定性分析上升到定量分析的層面,去解決更為復雜的問題。
【課堂小結】播放PPT(見圖12)。
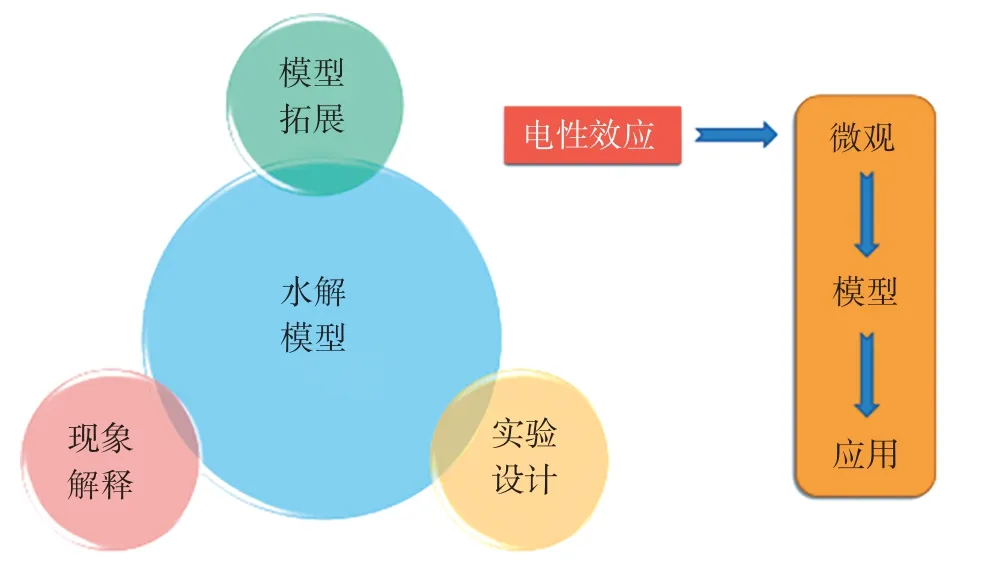
圖12 課程小結
【教師】同學們,本節課從微觀的視角出發建構水解反應的模型,并運用模型判斷化學反應的產物、書寫化學方程式,其關鍵在于利用元素的電負性確定相關元素的化合價。本節課到此結束,謝謝大家!
六、教學效果與反思
課后對一些學生進行了訪談,話題主要是“本堂課你印象最深的地方是什么”“本節課你感覺哪些能力有所提升”等。[5]學生反饋的結果一是認為構建水解模型有助于形成清晰的問題解決思路,切實提高了解決問題的能力;二是認為“電性效應”思想的學習有利于理解化學反應的本質。
筆者在不同層次的班進行了教學體驗,從課程的引入開始,學生總結常見的與水反應的方程式就會有比較大的差異,體現出基礎知識的掌握程度不同,也直接會影響到后面知識的呈現方式。面對不同的學生群體,本節課都是同一個思路:引導學生分析有水參與的化學反應的特點——建立模型——應用模型。從學生的現場表現來看,課堂不能只有一種呈現形式,針對不同層次的學生,需要老師的應變,在實踐中還需要根據學生反饋的情況適時調整教學計劃,從而更好地為學生終身發展服務。

