FOLFOXIRI改良方案姑息化療治療中老年晚期胃癌的效果
侯占國 馮吉林 張萬林 焦克 王爾全 胡小蓮
胃癌在我國高發,其發病率和死亡率均居世界前列,其中男性患病率多于女性[1]。約90%胃癌患者確診時處于中晚期,即便接受外科手術治療,5年存活率仍不超過一半,且接受根治性手術后患者復發概率超過70%[2]。因此臨床多采取術后化療方式預防腫瘤細胞轉移,但由于中老年患者往往基礎疾病較多,身體耐受性差,采用何種化療方案并無定論。隨著研究深入,對于FOLFOXIRI改良方案,即5-氟尿嘧啶/亞葉酸鈣+奧沙利鉑+伊立替康所具效果較為明顯,該方案毒性反應較低的同時復發率也較低[3]。本次研究選取2020年2月至2022年8月我院收治的中老年晚期胃癌患者106例作為研究對象,主要針對FOLFOXIRI改良方案治療中老年晚期胃癌的效果進行探討,報道如下。
1 資料與方法
1.1 一般資料 選取2020年2月至2022年8月我院收治的中老年晚期胃癌患者106例,隨機分為2組,觀察組中,男32例,女24例;年齡45~88歲,平均(60.25±3.18)歲。對照組中,男30例,女20例;年齡46~87歲,平均(61.83±3.47)歲;2組基線資料差異無統計學意義(P>0.05)。
1.2 納入與排除標準
1.2.1 納入標準:①患者符合臨床胃癌診斷標準[4];②年齡≥45歲,具備完整臨床資料;③無手術或放化療病史。
1.2.2 排除標準:①無法耐受研究相關治療方案者;②存在嚴重肝腎等臟器疾病;③存在精神障礙,不能配合研究者。
1.3 方法 2組治療期間,均需要定期接受血常規檢查,出現含量異常結果者需要及時采取相關干預措施。
1.3.1 對照組:接受XELOX方案。奧沙利鉑(江蘇奧賽康藥業有限公司 生產批號:H2006011)靜脈滴注,劑量采取體表面積130 mg/m2標準,與250 ml葡萄糖注射液(5%)混合使用,靜脈輸注2 h,第1天;卡培他濱片[廠商 羅氏(上海)醫藥貿易有限公司,生產批號:SH2668],劑量采取體表面積1 g/m2,口服使用,2次/d,第1~14天,隨后休息7 d,每3周重復,用藥6~8周。
1.3.2 觀察組:接受FOLFOXIRI改良方案。奧沙利鉑劑量采取體表面積85 mg/m2標準,與250ml葡萄糖注射液(5%)混合使用,靜脈滴注2 h,第1天;伊立替康注射液(海南錦瑞制藥有限公司 生產批號:210401):劑量采取120 mg/m2,與250 ml葡萄糖注射液(5%)混合使用,靜脈滴注2 h,第1天;亞葉酸鈣注射液(山西普德藥業有限公司 生產批號:12200401),劑量采取體表面積0.4 g/m2,與250 ml氯化鈉注射液(0.9%)混合使用,靜脈滴注2 h,第1天;5-氟尿嘧啶注射液(上海旭東海普藥業有限公司,生產批號:FA200603)劑量采取體表面積0.4 g/m2,混合適量氯化鈉注射液(0.9%),靜脈推注使用,第1天;然后采取體表面積2.4 g/m2進行靜脈滴注,維持46 h,每2周重復,用藥8~12周期。
1.4 觀察指標 (1)定期進行CT復查,治療后根據WHO《實質性腫瘤療效判定標準》進行短期療效評價:完全緩解(CR):病變完全消失,持續時間至少1個月;部分緩解(PR):腫瘤縮小>50%,持續時間為至少1個月;穩定(SD):腫瘤增加25%,或減少<50%;進展(PD):腫瘤增加>25%。有效(RR)率=CR率+PR率;疾病控制(DCR)= CR+PR+SD[5]。(2)治療前后采取患者空腹靜脈血5 ml做樣本常規處理,取血清,檢測2組血紅蛋白、血小板水平,采用免疫放射法對患者血清內胃泌素-17進行檢測[6]。(3)免疫因子:治療前后采集患者空腹靜脈血,加入紅細胞裂解液,培養0.5 h后離心,依次插入相應的T細胞抗體,用流式細胞儀檢測。指標包括IgG、IgM、IgA、CD4/CD8[7]。(4)觀察2組并發癥發生率。
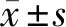
2 結果
2.1 2組臨床療效比較 觀察組治療有效率、疾病控制率均較對照組高(P<0.05)。見表1。

表1 2組臨床療效比較 例(%)
2.2 2組治療后血紅蛋白、血小板和胃泌素水平比較 觀察組治療后血紅蛋白、血小板、胃泌素-17水平高于對照組,差異均有統計學意義(P<0.05)。見表2。
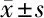
表2 2組治療后血紅蛋白、血小板和胃泌素水平比較
2.3 2組治療前后免疫標水平比較 治療后,觀察組IgG、IgM、IgA、CD4/CD8均高于對照組(P<0.001)。見表3。
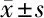
表3 2組治療前后免疫反應指標水平比較
2.5 2組并發癥率比較 觀察組除手足綜合征(P>0.05)外,其他并發癥率均低于對照組,差異有統計學意義(P<0.05)。見表4。

表4 2組不良反應發生率比較 例(%)
3 討論
我國每年胃癌患病人數約40萬,確診時多為晚期,此時已失去手術機會,主要采取全身化療進行治療。鑒于胃癌對于化療有較強的敏感性,采用適當的全身化療方法可改善患者生命質量,對患者生存時間進行延長。化療方法的選擇除了依據患者病情及身體狀況,其有效性及不良反應更是要重點注意的事項[8,9]。胃癌患者的全身化療方法較多,但如何實現治療效果的最優化及毒副作用的最小化依舊是重難點問題[10]。尤其是中老年胃癌晚期患者而言,其基礎合并癥比較多,機體對化療藥物的耐受性較差,所以在選取化療方法時需要進行多方全面性考慮,兼顧有效性及耐受性。
本研究采用的FOLFOXIRI改良化療方案中,伊立替康是細胞毒類藥物家族中一員,屬于喜樹堿類新藥物之一[11]。該藥物屬于選擇性DNA拓撲異構酶I(ToPol)抑制劑,其進入細胞后,可與DNA拓撲異構酶-DNA復合物共價結合形成DNA拓撲異構酶藥物-DNA復合物,能抑制DNA重連步驟,促進DNA不可逆斷裂,引發細胞凋亡,可通過阻滯細胞周期發揮抗腫瘤作用[12-13]。作為第三代鉑類藥物,奧沙利鉑細胞毒性強,抗癌譜較廣,可對DNA錯配修復進行抑制,干預DNA合成,具備較為廣泛的抗腫瘤細胞作用,藥物使用后效果發揮迅速,半衰期較短,同時發生不良反應概率較低[14,15];氟尿嘧啶一直是聯合化療方案的關鍵,屬于胃癌治療的基本用藥之一,聯合奧沙利鉑等藥物治療胃癌晚期在臨床上都取得了滿意的結果。亞葉酸鈣能增加氟尿嘧啶的細胞毒性,作為氟尿嘧啶的增效劑,一般應用亞葉酸鈣與氟尿嘧啶聯合應用,作為胃癌的輔助治療,可延長藥物活性[16]。
本研究顯示,觀察組治療有效率、疾病控制率較對照組高(P<0.05)。觀察組治療后血紅蛋白、血小板、胃泌素-17高于對照組(P<0.05)。說明FOLFOXIRI改良方案更有利于控制患者病情,整體化療效果更優。胃泌素是由胃竇及小腸細胞分泌的一種多肽類激素,其主要作用為促進胃腸運動,刺激胃黏膜細胞生長,胃泌素-17可促進胃腸道的分泌功能,增加胃泌素則可有效保護患者胃黏膜,緩解臨床癥狀[17]。本研究證實,FOLFOXIRI改良方案可以有效提升患者胃泌素水平,效果更優。治療后2組免疫反應指標均有所上升,且觀察組免疫指標水平顯著高于對照組(P<0.01)。中老年晚期胃癌患者多免疫力較低,無法耐受化療后所帶來的不良反應,導致治療中斷,因而在胃癌中晚期患者采取化療方案中,多強調方案不良反應的減少[18]。本研究證實,FOLFOXIRI改良方案可以更有效地改善患者免疫功能狀況,增強患者免疫力與抵抗力,更有利于治療效果提升。本研究結果顯示,觀察組除手足綜合征外,其他并發癥率均較對照組低(P<0.05)。2組手足綜合征差異無統計學意義(P>0.05)。說明FOLFOXIRI改良方案應用后不良反應發生率較低。伊立替康同時和奧沙利鉑聯合應用,通過烷化結合物靶向作用,與 DNA 逐漸形成交叉聯結后,對癌細胞DNA的復制以及轉錄進行有效抑制,從而發揮有效抗腫瘤作用[19]。在研究結果中也發現,2組化療方案實施后患者均有手足綜合征的概率,此時需要指導患者外用紅霉素,內服維生素抗氧化治療,并避免日光直接接觸,控制患者后續不良反應的發生[20]。
綜上所述,中老年晚期胃癌患者,采取FOLFOXIRI改良方案姑息化療治療,其治療效果、病情控制率更為明顯,并增強患者免疫功能,且并發癥更少,值得臨床借鑒。

