丁二酸中雜質含量的分析研究
蘇鳳仙,陳建梅,徐哲峰
(1. 中國石化儀征化纖有限責任公司研究院,江蘇儀征 211900;2. 江蘇省高性能纖維重點實驗室,江蘇儀征 211900)
丁二酸又名琥珀酸,是一種常見的天然有機酸,常被用作聚丁二酸對苯二甲酸丁二醇酯(PBST)和聚丁二酸丁二醇酯(PBS)等新型生物可降解聚酯的合成原料。丁二酸雜質對聚合反應和聚合產物都會產生一定的影響,在二元酸二元醇的酯化縮聚反應階段,雜質的存在可能是導致聚合反應過早終止、聚合物相對分子質量較低和聚合物力學性能較差的主要因素之一[1-2]。
隨著生物可降解聚酯的廣泛使用,作為聚合原料的丁二酸的質量也越來越被重視。丁二酸的生產工藝有許多種,基于生產成本和產品質量考慮,現在使用廣泛的丁二酸生產工藝主要為順酐電解法、順酐加氫法和生物發酵法。不同的廠家和不同的生產工藝會帶來產品雜質的變化,順酐加氫法工藝通常含有雜質酒石酸和丁二酸酐,順酐電解法工藝通常含有雜質酒石酸、富馬酸和馬來酸,生物發酵法工藝通常含有雜質甲酸、乙酸、乳酸、檸檬酸、草酸、酒石酸、蘋果酸、富馬酸和馬來酸等,丁二酸的部分雜質可能對生物可降解聚酯的合成影響較大,不僅會降低聚合物的分子量,而且會增加分子鏈的支化度,所以分析丁二酸雜質含量對生物可降解聚酯的研發和生產至關重要。
丁二酸產品標準如GB/T 34686—2017[3]《工業用丁二酸》推薦采用酸堿滴定法分析丁二酸純度,雖然操作簡便,但是誤差較大,且該標準沒有涉及有機雜質的分析方法和指標要求,所以該標準不能完全適用于丁二酸純度與有機雜質含量的分析。丁二酸的分析在許多文獻資料中也有報道,王訓道等[4]以Cu2+為反離子與丁二酸形成絡合物,再采用反相液相色譜法分析;余作龍等[5]采用C18鍵合液相色譜柱和磷酸二氫鉀水溶液作為流動相分析丁二酸發酵液中的丁二酸含量;嚴勵等[6]采用毛細管電泳儀、磷酸二氫鈉-硼酸鈉為緩沖溶液分離丁二酸發酵液中的有機酸等。雖然文獻資料多次報道有機二元酸的分析,但主要介紹混合液中微量丁二酸的分析,很少涉及丁二酸中有機雜質含量分析的相關內容。
本文主要采用液相色譜法探索丁二酸有機雜質含量的分析方法,進一步評價丁二酸的質量,為生物可降解聚酯的研發與生產進行原料篩選與質量把關。
1 試 驗
1.1 原料及試劑
丁二酸,工業純,市售;甲酸,分析純,國藥集團;乙酸,分析純,國藥集團;草酸,分析純,國藥集團;乳酸,分析純,國藥集團;順丁烯二酸,分析純,國藥集團;反丁烯二酸,分析純,國藥集團;蘋果酸,分析純,國藥集團;酒石酸,分析純,國藥集團;檸檬酸,分析純,國藥集團;氦氣,純度大于99.999%,南京特種氣體廠;氮氣,純度大于99.99%,南京特種氣體廠;氫氣,純度大于99.99%,南京特種氣體廠。
1.2 儀器與設備
氣相色譜儀,7890A型,配有氫火焰離子檢測器,安捷倫科技有限公司;氣質聯用儀,7890B-5977A型,配有電子轟擊離子源、四級桿質量分析器與光電倍增管檢測器,安捷倫科技有限公司;液相色譜儀,e2695型,沃特斯科技有限公司;電子分析天平,XRS105型,梅特勒-托利多儀器有限公司。
1.3 分析方法
Prevail Organic Acid型色譜柱,尺寸為250 mm×4.6 mm×5 μm;柱溫35 ℃,保持10 min;流動相為25 mmol/L磷酸二氫鉀水溶液,流動相pH值:2.5(用磷酸調節);波長為215 nm;流速為1.0 mL/min;稱樣量為1.0 g;進樣量為10 μL。
2 結果與討論
2.1 分析方法的確定
有機物的分析常采用色譜法,色譜法包括氣相色譜法和液相色譜法等,由于氣相色譜法具有高靈敏度、高分離效果、高選擇性等特點,所以被廣泛應用于有機物的分析,而且氣相色譜所用的流動相為氣體,相對液相色譜的化學溶劑流動相,氣相色譜更綠色潔凈,對環境更友好,所以對化工有機物,常常推薦采用氣相色譜法分析。只有當待測組分受熱易分解、沸點較高,氣相色譜法不能滿足分析要求時,才推薦采用液相色譜法分析。
2.1.1 氣相色譜法初探
丁二酸為白色晶體,沸點為236.15 ℃,在235 ℃時易分解,分解產物為丁二酸酐。為了減少丁二酸的受熱分解,將氣相色譜進樣口溫度、檢測器溫度和柱溫都設定在230 ℃以下,并分別探索了不同色譜柱對丁二酸有機雜質的分離情況,如圖1所示。
由圖1可知,不同色譜柱對丁二酸的分離效果差異較大,從分離效果考慮,DB-1柱分析的丁二酸主組分峰面積較大,更適合分析丁二酸。
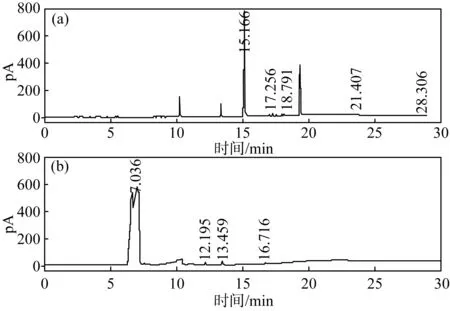
(a):DB-WAX柱;(b):DB-1柱
2.1.2 氣質聯用法定性
采用氣質聯用法對有機組分進行定性分析,發現主組分為丁二酸酐,說明丁二酸在此條件下發生反應生成丁二酸酐,定性結果如圖2所示。根據氣質聯用定性結果,說明圖1中保留時間為7.038 min的組分為丁二酸酐。

(a):丁二酸分析主組分質譜圖;(b):標準譜庫質譜圖
考慮到高溫可能促進丁二酸的反應,所以繼續降低進樣口溫度、檢測器溫度和柱溫,設定在150 ℃以下,再進行分析比較,效果仍然不理想,丁二酸仍然自縮生成丁二酸酐,如圖3所示。雖然氣相色譜設定溫度遠低于丁二酸分解溫度,但是樣品在進樣口是氣化狀態,分子膨脹,且有載氣的壓力作用,丁二酸更容易發生反應。
綜上所述,氣相色譜儀進樣口與柱溫等條件的高溫加速丁二酸的反應,生成丁二酸酐,所以氣相色譜法不適用于分析丁二酸,需要采用液相色譜法分析。
2.2 色譜條件研究
色譜條件是有機物分離分析的關鍵因素,色譜條件合適與否,通常影響分析的分離度、分離效率、響應值、分析速度(時間)以及定量的結果等,所以選擇合適的色譜條件在有機物定量中非常重要。液相色譜的色譜條件包含色譜柱、流動相、檢測器紫外波長、進樣量、流速等,通過摸索以上幾種色譜條件,選擇一個較合適的分析條件,以期達到待測物的完美分離。

(a):230 ℃;(b):150 ℃
2.2.1 色譜柱對丁二酸中有機雜質分離的影響
丁二酸中可能存在的雜質有甲酸、乙酸、乳酸、檸檬酸、草酸、酒石酸、蘋果酸、富馬酸和馬來酸等,對于此類組分的分析常采用有機酸柱和ODS柱,為了進一步比較確定合適的色譜柱,分別采用Aminex HPX-87H柱、Agilent Zorbax ODS柱、Prevail Organic Acid柱,探索不同色譜柱對丁二酸中有機雜質的分離效果,分離效果圖如圖4所示。
由圖4可知,Agilent Zorbax ODS柱和Aminex HPX-87H柱分離效果較差,不能分離丁二酸中有機雜質,Prevail Organic Acid柱分離效果較好,色譜峰響應值較高,分析時間較短,所以色譜柱選擇Prevail Organic Acid有機酸柱。
2.2.2 流動相對丁二酸中有機雜質分離的影響
液相色譜法中,試樣中各組分能被高效的分離,首先在于選擇合適色譜柱,其次是流動相,適當的流動相能改善組分分離效果,提高組分峰響應值。分別采用稀硫酸、磷酸二氫鉀水溶液作為流動相,再在磷酸二氫鉀水溶液中加入甲醇調節流動相極性,探索不同流動相對丁二酸中有機雜質的分離效果,分離效果圖如圖5所示。

(a):Aminex HPX-87H柱;(b):Prevail Organic Acid柱;(c):Agilent Zorbax ODS柱

(a):0.02 mol/L稀硫酸;(b):水,磷酸二氫鉀,甲醇體積比為97∶1∶2;(c):25 mmol/L磷酸二氫鉀水溶液
由圖5可知,作為流動相,磷酸二氫鉀水溶液比硫酸水溶液更能使丁二酸中有機雜質高效分離且色譜峰響應值較高,加甲醇調節流動相極性對丁二酸有機雜質的分離不僅沒有改善,而且影響一些雜質的分離效果,所以磷酸二氫鉀水溶液作為流動相更合適。
2.2.3 pH值對丁二酸中有機雜質分離的影響
丁二酸雜質偏酸性,所以酸性流動相更有利于分離這些組分,用磷酸調節流動相的pH值,調至流動相pH值分別為2.0、2.5、3.0時分析丁二酸中有機雜質,分離效果如圖6所示。
由圖6可知,當pH值為2.5時,丁二酸中各雜質色譜峰響應值最高,所以流動相pH值需要用磷酸調節至2.5。

(a):pH=2.0;(b):pH=2.5;(c):pH=3.0
2.2.4 波長對丁二酸有機雜質響應值的影響
紫外波長是影響樣品響應值的另一個關鍵因素,在合適波長條件下,樣品組分能獲得較高的響應值。分別考察波長條件為196、215和230 nm時丁二酸中有機雜質色譜峰響應值,分析效果如圖7所示。從圖7可以看出,當波長條件為215 nm時,丁二酸中有機雜質分析效果好、色譜峰響應值高,所以選擇波長條件為215 nm。
經過色譜柱、流動相、流動相pH值、波長等條件的探索,最終確定色譜條件:Prevail Organic Acid柱、流動相為25 mmol/L磷酸二氫鉀水溶液、流動相pH值為2.5、波長為215 nm。在此色譜條件下,丁二酸中有機雜質能被有效地分離,色譜峰響應值高、分析效率高。

(a):196 nm;(b):215 nm;(c):230 nm
2.3 丁二酸中有機雜質的定性分析
液相色譜定性方法有許多種,本文采用標準品比照法定性,定性結果如圖8和表1所示。

圖8 丁二酸中有機雜質定性色譜圖
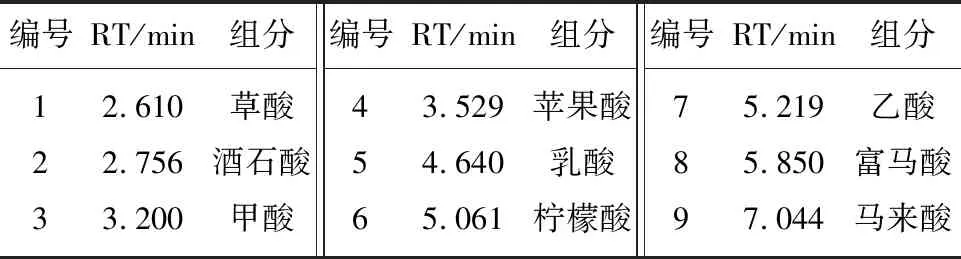
表1 丁二酸中有機雜質定性結果
2.4 丁二酸中有機雜質的定量分析
2.4.1 定量方法的探索
液相色譜的定量方法有多種,廣泛使用的有兩種,分別為外標法與內標法。考慮到丁二酸中有機雜質較多,內標物選擇困難,有可能選擇的內標物會干擾有機雜質的分離度和定量準確性,所以本文采用外標法定量,繪制4級校正曲線,如圖9~17所示。丁二酸中9個有機雜質定量校正曲線的線性范圍寬,說明本方法測試量程大,適用范圍寬;由表2可知,有機雜質定量校正曲線的相關系數都高于0.995,說明校正曲線的相關性高、線性關系好,方法定量準確度高。
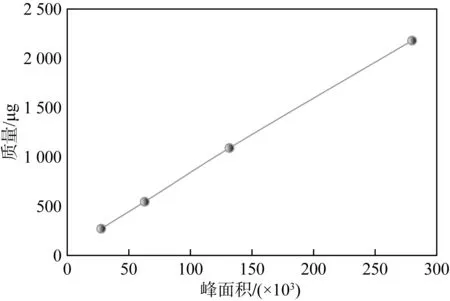
圖9 草酸定量校正曲線

圖10 酒石酸定量校正曲線

圖11 甲酸定量校正曲線
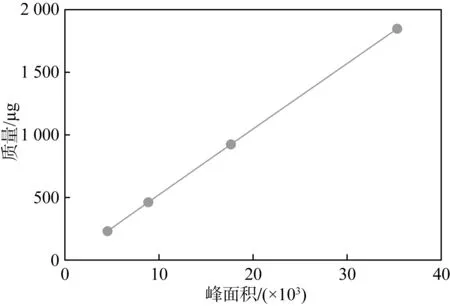
圖12 蘋果酸定量校正曲線
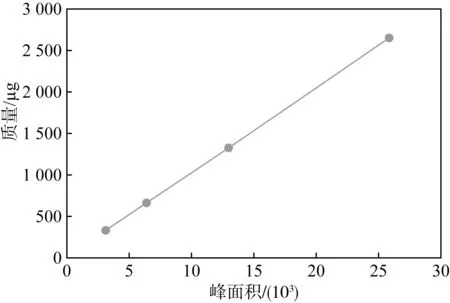
圖13 乳酸定量校正曲線

圖14 檸檬酸定量校正曲線
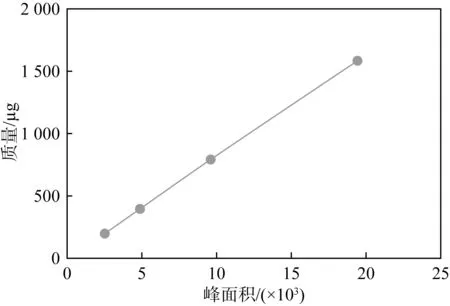
圖15 乙酸定量校正曲線

圖16 富馬酸定量校正曲線
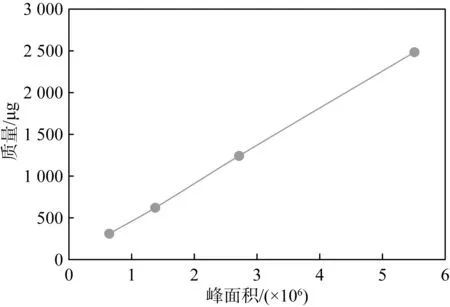
圖17 馬來酸定量校正曲線
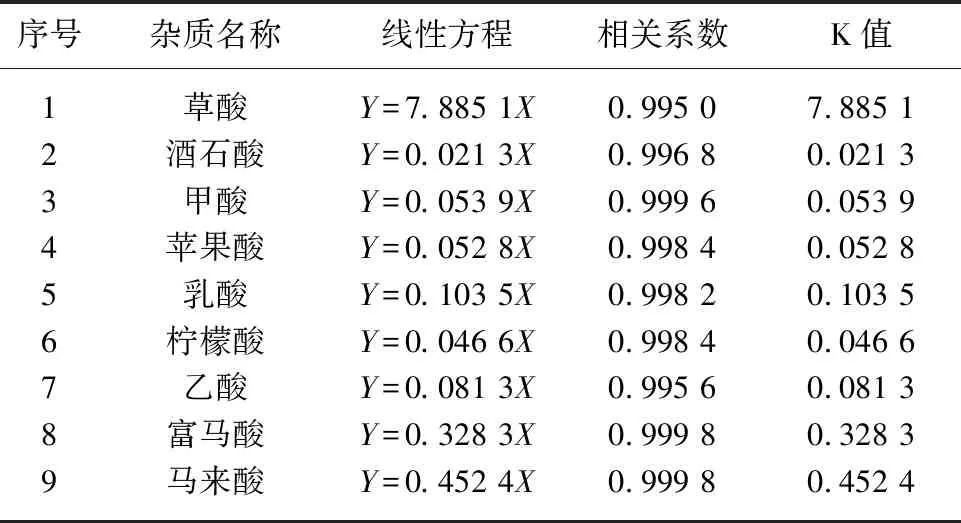
表2 丁二酸中雜質的線性方程
2.4.2 丁二酸中有機雜質含量的分析
稱取1.0 g丁二酸試樣于25 mL容量瓶中,用蒸餾水溶解、定容、搖勻后分析,丁二酸試樣中有機雜質含量按公式(1)計算:
(1)
式中Xi為試樣中雜質組分i的含量,%;Ki為試樣中雜質組分i定量校正曲線的斜率;Ai為試樣中雜質組分i的峰面積;m為試樣的質量,g。
2.4.3 丁二酸純度的分析
丁二酸試樣的純度,以%(質量分數)表示,按式(2)計算:
W=100-∑Xi
(2)
式中W為試樣的純度,%;Xi為試樣中雜質組分i的含量,%。
2.5 方法學考察
2.5.1 精密度的評價
在生產與科研的分析報告中常用相對標準偏差表示精密度,精密度包含重復性和再現性,本文僅考察重復性。對丁二酸分別分析,以雜質富馬酸與酒石酸為考察對象,考察兩個雜質的保留時間和含量的重復性,結果見表3。

表3 丁二酸雜質含量分析方法的重復性
2.5.2 準確度的評價
準確度為真值與測定值差值大小的一種量度,丁二酸雜質含量的真值未知,本方法準確度的評價以雜質酒石酸為考察對象,采用加標回收率的方法檢驗分析方法的準確度。稱取適量丁二酸試樣,分別添加適量的酒石酸標樣,以式(3)計算回收率,結果見表4。
(3)
式中K為回收率,%;X1為樣品原樣量,g;X2為樣品添加量,g;X3為樣品實測量,g。

表4 丁二酸雜質的回收率
2.5.3 線性范圍與檢出限的考察
線性范圍,指響應值(或峰面積)隨組分濃度變化曲線上直線部分所對應的組分濃度變化范圍。在色譜分析中一般將檢出限定義為信噪比(S/N)3∶1時的濃度,以式(4)計算:
(4)
式中D為檢出限,%;S/N為該濃度下的信噪比;Q為進樣濃度,%。
以式(4)計算丁二酸中雜質含量分析方法的檢出限,結果列于表5。由表5可知,該方法具有較寬的線性范圍和良好的線性,相關系數在0.99以上,方法也具有較高的靈敏度,檢出限優于0.001 5%,能滿足丁二酸原料的測試需求。
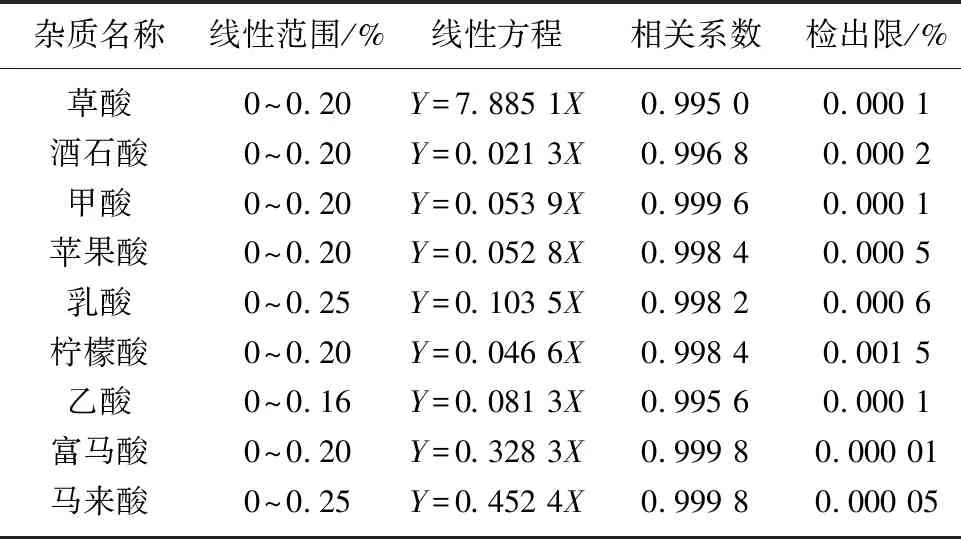
表5 線性范圍與檢出限結果
由表3可知,重復性中丁二酸保留時間的相對標準偏差優于0.65%,丁二酸含量的相對標準偏差優于3.0%;由表4可知,丁二酸分析方法回收率范圍為88.30%~117.24%。說明本方法的重復性好,回收率優,精密度與準確度較高;由表5可知,本方法的線性范圍寬、檢出限低,能用于生物可降解材料原料質量的評價。
3 結 論
a) 建立了丁二酸雜質含量的分析方法:采用Prevail Organic Acid柱、流動相為25 mmol/L磷酸二氫鉀水溶液、流動相pH值為2.5、波長為215 nm的色譜條件下,丁二酸中有機雜質能被有效地分離,色譜峰響應值高、分析效率高。
b) 該方法的精密度與準確度較好,重復性優于3.0%,回收率范圍為88.30%~117.24%,檢測限優于0.001 5%,滿足丁二酸的測試需求。

