生長抑素類似物聯合培維索孟對肢端肥大癥患者治療效果及安全性的Meta分析
張 麗,劉 翔,劉 萍
寧夏醫科大學總醫院內分泌科,寧夏銀川 750004
肢端肥大癥是以生長激素(GH)及胰島素樣生長因子-1(IGF-1)分泌異常增多為特征的內分泌疾病,常由垂體腺瘤引起[1]。過度分泌的GH和IGF-1可對全身多個器官和系統產生廣泛影響,導致全身軟組織、骨和軟骨過度增生,引起面容改變、手足變大、皮膚改變、內臟長大和骨關節病變等一系列表現,同時可能引起呼吸阻塞、高血壓、頭痛、視野缺損、代謝紊亂,部分患者還可出現胰島素抵抗、糖耐量受損,甚至發展為糖尿病。肢端肥大癥患病率為40/100萬至125/100萬,年發病率為3/100萬至4/100萬,好發年齡為40~60歲,發病在性別方面無明顯差異[2]。肢端肥大癥可影響機體多部位的組織器官,所致并發癥較多,可能導致心血管疾病、呼吸系統疾病和腫瘤發生,總體死亡風險約為普通人群的2倍,未得到控制的患者約有一半在50歲前死亡,患者平均壽命約減少10年[3]。肢端肥大癥的治療包括手術及藥物治療,手術治療作為首選治療方式,切除垂體微腺瘤后緩解率高達85%[4],然而并非所有患者均適合手術,對于部分不能行手術切除、術后殘留或復發的患者,藥物治療顯得尤為重要。目前,治療肢端肥大癥的藥物主要包括生長抑素類似物(SSA),如奧曲肽、蘭瑞肽和帕瑞肽,以及多巴胺受體激動劑(如溴隱亭、卡麥角林)和GH拮抗劑,如培維索孟(PEG)等。SSA是肢端肥大癥患者藥物治療的一線用藥,通過與生長抑素受體結合抑制GH分泌,可縮小腫瘤體積、控制血清GH和IGF-1水平、明顯改善臨床癥狀(頭痛、疲勞、多汗、關節痛、感覺異常等)、控制并發癥(心血管獲益、改善呼吸功能障礙)[5]。據文獻報道,在單獨使用SSA的患者中,IGF-1正常率為17%~69%[6-7],部分患者在治療過程中出現SSA抵抗或治療效果不理想,GH及IGF-1無明顯下降的患者,進一步采用PEG單藥治療或與SSA聯合治療通常作為備選方案。本研究旨在評價SSA聯合PEG對肢端肥大癥患者的治療效果及安全性,希望能對臨床工作提供一定幫助。
1 資料與方法
1.1一般資料 中文檢索題名或關鍵詞為肢端肥大癥、生長抑素類似物、奧曲肽、蘭瑞肽、帕瑞肽、培維索孟、聯合治療。英文檢索關鍵詞為acromagely、Somatostatin analogue、Octreotide、Pasireotide、lanreotide、pegvisomant、combination therapy。檢索策略:(Acromegaly) OR (Somatotropin Hypersecretion Syndrome) AND (Octreotide) OR (Pasireotide) OR (lanreotide) OR (Somatostatin analogue) OR (SSA) AND (Pegvisomant) AND (combination therapy) OR (combination treatment)。以上述題名或關鍵詞全面檢索PubMed、Embase、Cochrane library、CNKI、CBM、維普、萬方數據庫中相關文獻并輔以手工檢索。不設置檢索時間限制,末次檢索時間為2022年10月8日。納入標準:(1)確診為肢端肥大癥;(2)同時使用SSA及PEG治療;(3)研究觀察時間至少3個月;(4)研究有效性指標包括聯合治療后IGF-1正常率、安全性結局(治療后轉氨酶升高的患者數量或百分比)。排除標準:(1)文章為綜述、動物研究、個案報道;(2)實驗設計不嚴謹或沒有設立對照的研究;(3)信息不全、數據不完整的研究;(4)文章書寫語言為中、英文以外的研究。
1.2資料提取和質量評價
1.2.1建立表格并提取納入研究的資料 對檢索到的文獻嚴格按照納入和排除標準進行篩選,剔除不符合納入標準的研究,對可能納入的研究閱讀全文。對以下數據進行提取:(1)研究設計;(2)基線特征:患者數量、年齡、性別、以前的治療、研究觀察時間、SSA和PEG中位數劑量;(3)按年齡和性別校正后的標準化IGF-1水平的患者數量或百分比;(4)轉氨酶升高的患者數量或百分比。
1.2.2質量評價 對照試驗采用Cochrane風險偏移運算法則,非對照研究采用修改方法指數進行評價。文獻質量根據NOS標準,針對非隨機對照研究制訂的8個條目,其中研究對象選擇4個條目,4分;組間可比性1個條目,2分;結果測量3個條目,3分;共計9分。評價納入文獻的質量。
1.3統計學處理 采用Rev Man 5.3軟件,以χ2檢驗進行異質性分析,并采用I2定量分析異質性大小,其檢驗水平設定為50%,根據有無異質性選用隨機效應模型或固定效應模型,采用固定效應模型;若I2≥50%,則采用隨機效應模型。以P<0.05為差異有統計學意義。
2 結 果
2.1文獻檢索結果及納入研究特征 共檢索到文獻163篇,均為英文文獻。嚴格按照納入和排除標準,最終納入11項研究[聯合治療組(SSA+PEG治療)377例和單藥治療組(SSA治療)176例],11項研究均為英文文獻,包括7篇前瞻性研究和4篇回顧性研究。納入研究的文獻詳細特征見表1。所有研究中患者均使用大劑量SSA治療,聯合治療組聯合PEG治療,單藥治療組僅使用SSA治療,患者年齡24~81歲,部分患者采用手術治療,部分患者初始治療采用放療或其他藥物治療(如卡麥角林)。研究周期24周至5年。
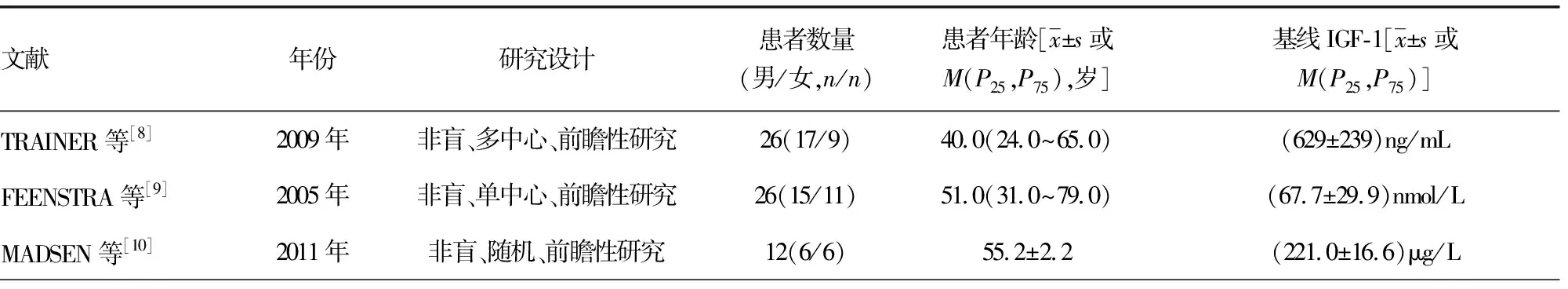
表1 納入11項研究的詳細特征
2.2肢端肥大癥患者使用SSA聯合PEG治療后IGF-1正常率的Meta分析 聯合治療組IGF-1正常率更高,但與單藥治療組比較,差異無統計學意義(OR=1.15,95%CI:0.61~2.19,P=0.66)。見表2。
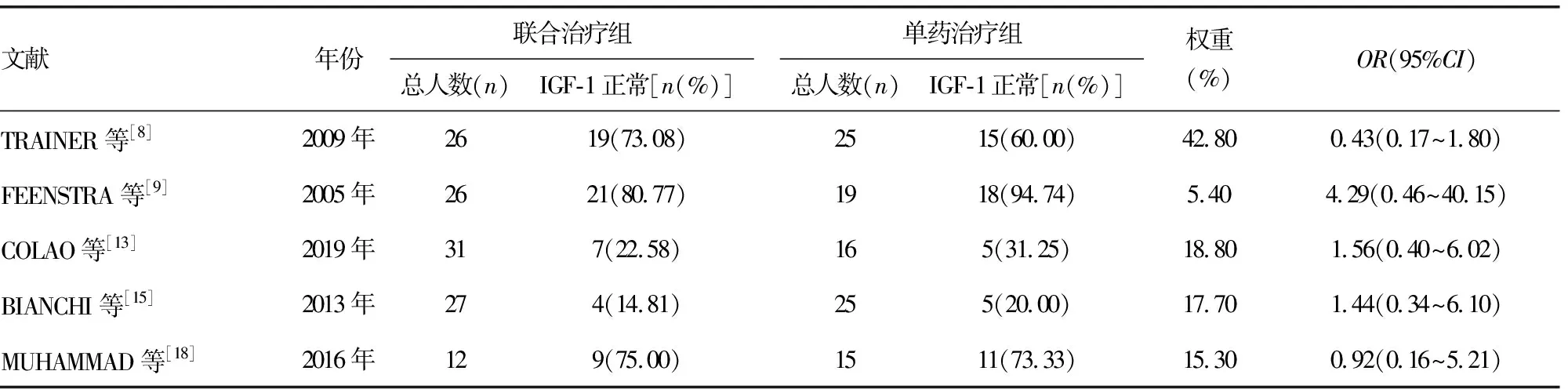
表2 肢端肥大癥患者使用SSA聯合PEG治療后IGF-1正常率
2.3肢端肥大癥患者使用SSA聯合PEG治療后安全性的Meta分析 單藥治療組轉氨酶升高比例更小,安全性更好,但與聯合治療組比較,差異無統計學意義(OR=0.63,95%CI:0.35~1.16,P=0.14)。見表3。
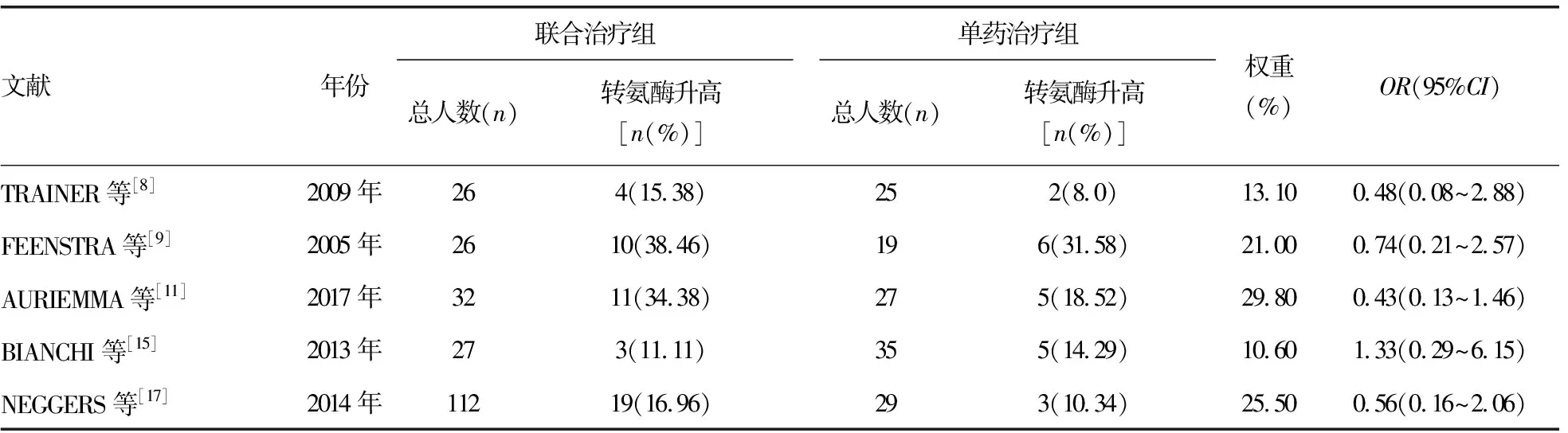
表3 肢端肥大癥患者使用SSA聯合PEG治療的安全性
2.4發表偏倚及敏感性分析 采用漏斗圖法評估發表偏倚,見圖1,各項研究分布較分散,提示所納入研究存在發表偏倚。將效應模型更改進行敏感性分析,所有合并指標的結果與前均一致,說明結果可靠性較好。
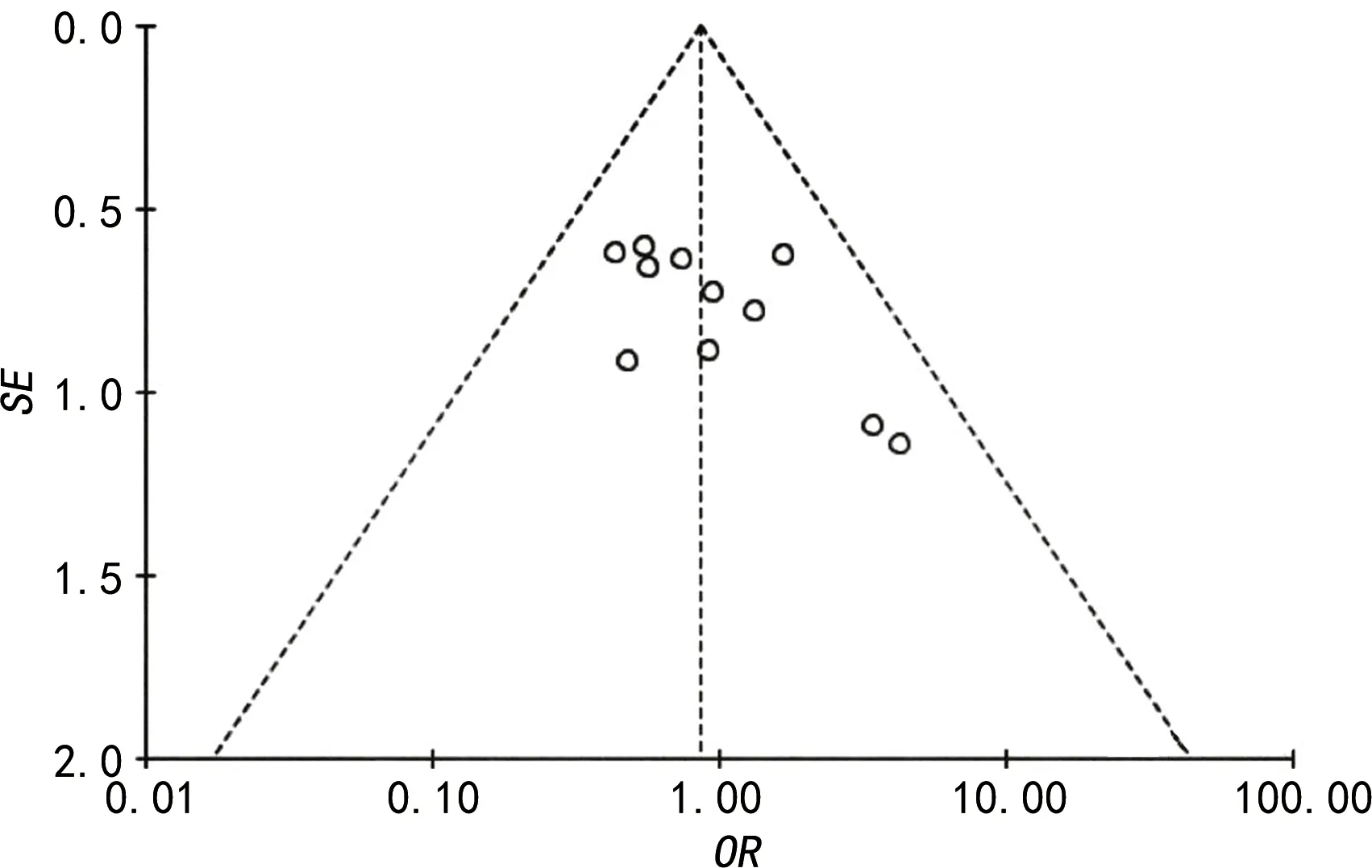
圖1 漏斗圖
3 討 論
目前對于肢端肥大癥患者,手術、藥物或放療的目的主要包括以下幾點:(1)生化控制,即GH、IGF-1降至正常水平;(2)改善癥狀和體征;(3)逆轉并發癥和死亡風險;(4)控制局部腫瘤效應。部分肢端肥大癥患者長期使用SSA治療后,GH及IGF-1水平無明顯下降,患者癥狀和體征無明顯改善,持續高GH、IGF-1水平,增加心血管系統疾病、呼吸系統疾病和腫瘤發生的風險。此類難治性肢端肥大癥患者的治療具有挑戰性,需結合患者IGF-1和GH水平、腫瘤大小和侵襲性、癥狀、患者偏好和治療的成本效益比等因素綜合考慮[19]。
PEG是GH拮抗劑,能夠競爭性地阻斷GH受體,從而阻止與內源性GH結合,降低IGF-1水平。與SSA和多巴胺激動劑比較,PEG并不會減少垂體腫瘤分泌的GH,而是在組織水平上有效阻斷GH。有研究表明,PEG單藥治療可使約70%的肢端肥大癥患者IGF-1水平恢復正常[20],但由于PEG價格昂貴,且治療過程中劑量需要逐漸調整,同時存在轉氨酶升高的風險,故PEG單藥治療方案并未廣泛使用。YAMAGUCHI等[21]在使用PEG治療的有效性及安全性研究中指出,35.6%的患者在治療過程中出現藥物相關不良反應,包括肝功能損害(13.6%)、疾病進展(2.8%)、頭痛(2.4%)、體質量增加(2.0%)及肥胖(2.8%)等。近幾年,有關PEG單藥或聯合SSA治療肢端肥大癥的研究逐漸增多,BONERT等[22]研究表明,在SSA治療的基礎上聯合PEG治療,IGF-1正常率可高達到95.0%,可使20%的患者腫瘤體積縮小,糖代謝異常亦有所改善,藥物安全性總體良好。但不同研究之間相關數據存在差異,不同劑量PEG所產生的治療效果及肝功能損害程度不一致,對糖化血紅蛋白、胰島β細胞功能指數、胰島素抵抗指數等糖代謝指標的影響亦存在差別。
本研究通過對SSA聯合PEG治療肢端肥大癥的相關文獻進行全面檢索,對治療的有效性及安全性進行Meta分析,結果顯示,聯合治療組IGF-1正常率更高,但與單藥治療組比較,差異無統計學意義(OR=1.15,95%CI:0.61~2.19,P=0.66);單藥治療組轉氨酶升高比例更小,安全性更好,但與聯合治療組比較,差異無統計學意義(OR=0.63,95%CI:0.35~1.16,P=0.14)。由此表明,SSA聯合PEG治療可作為SSA治療效果不佳的備選方案,使用PEG治療后會出現轉氨酶短暫、一過性升高,但不影響總體治療的安全性。IGF-1正常率及安全性Meta分析結果差異無統計學意義可能與納入研究樣本量較小、隨機對照研究少、文獻存在發表偏倚等因素有關。
綜上所述,對于難治性肢端肥大癥,SSA聯合PEG治療可作為備選方案之一,能夠有效降低IGF-1水平,總體安全性良好,可能為該病的治療提供新方法。但由于納入高質量研究有限,部分研究樣本量小,存在發表偏倚,導致證據強度不足,聯合治療的有效性及安全性相關結論還需要大樣本、多中心隨機對照試驗予以證實。

