重癥監護室老年重癥患者應用營養支持優化療法的臨床觀察
費榕,顧永梅,王煦
1. 海安市人民醫院重癥醫學科, 江蘇海安, 226600; 2. 海安市人民醫院重癥醫學科中醫康復科, 江蘇海安 226600
重癥監護室(intensive care unit, ICU)又稱為加強監護病房綜合治療室,治療、護理和康復可以同步進行,其提供的護理、治療服務較普通病房更周全[1]。ICU收治患者的病情普遍處于危急狀態,病情較嚴重且免疫力低,患者需要給予全方位密切觀察和處理。ICU重癥患者普遍存在碳水化合物代謝異常、脂肪代謝紊亂、蛋白質分解加速和胃腸道功能受阻等異常變化,這些機能異常均可導致重癥患者出現營養不良,影響患者治療和康復[2-3]。老年患者自身免疫力較弱,同時常伴有慢性基礎病,可導致老年ICU重癥患者營養不良風險更高,因此營養支持是老年ICU重癥患者重要支持手段之一[4]。常規的營養支持主要指腸內營養支持,腸內營養支持療法能夠為危重癥患者給予營養物質補給,有利于維持患者機體代謝正常運轉,調節代謝紊亂[5]。營養支持優化療法是根據患者自身情況進行個性化的營養支持手段,在滿足患者機體基本消耗的同時,還能盡可能降低患者器官負擔,有利于ICU重癥患者的機能恢復和預后改善。淋巴細胞數是血液中淋巴細胞的總數,具有抵抗病毒、細菌等作用,能反映機體的免疫力狀況[6]。白蛋白是由肝臟合成的參與營養物質、代謝廢物運輸的蛋白質,還具有維持血液滲透壓等作用[7]。目前,關于營養支持優化療法對老年ICU重癥患者淋巴細胞計數、血清白蛋白和BMI等影響的研究尚存不足。因此,本研究選取本院ICU收治的老年重癥患者為研究對象,探討老年ICU重癥患者營養支持優化療法對淋巴細胞計數、血清白蛋白、 BMI等的影響,旨在為其臨床診治提供依據。
1 資料與方法

1.2一般資料本研究采取前瞻性、單中心、對照研究設計方案。選取2022年1月—2022年12月于海安市人民醫院ICU收治的老年重癥患者82例,根據數字表法隨機分為:觀察組(n=41)和對照組(n=41)。觀察組中男性22例,女性19例;年齡61~80歲,平均年齡(70.3±5.0)歲;致病原因:重癥肺炎18例,重癥感染14例,嚴重心衰9例。對照組中男21例,女20例;年齡60~80歲,平均年齡(70.5±4.7)歲;致病因素:重癥肺炎15例,重癥感染16例,嚴重心衰10例。2組患者性別構成、年齡和致病因素構成等差異均無統計學意義(P>0.05),具有可比性。
1.3納入和排除標準納入標準: (1)患者年齡≥60歲; (2)住進ICU的患者; (3)發病前無意識、精神障礙疾病史; (4)入院前無合并感染性疾病; (5)患者或其家屬對本研究均知情,簽署知情同意書。符合上述全部標準的病例納入本研究。排除標準: (1)患有先天性疾病; (2)治療期間死亡; (3)預估患者救治后可能出現長期昏迷或意識、精神障礙等; (4)惡性腫瘤; (5)消化道損傷。具備以上任意1項標準的病例即排除。本研究獲得本醫院醫學倫理委員會批準(倫理學批號為HKL2022168)。
1.4治療方法2組患者均給予抗感染、酸堿平衡、電解質糾正和機械通氣等常規治療和對癥治療。(1)對照組患者采取常規腸內營養支持:患者進入ICU后,留置胃管作為營養支持干預方式,根據患者情況(腸內營養耐受性、熱量需求)準備營養液,根據患者情況選取性給予流質食物,流質食物包括米湯、奶等,熱量控制在6.26~12.0 MJ/d,營養液控制在1 000~2 000 mL/d,通過微量泵葡萄糖、氨基酸、維生素、脂肪乳劑等物質靜脈輸送,速度為65~100 mL/h,其余營養物質可以混合加入聚乙烯袋中給予患者靜脈滴注。(2)觀察組患者給予腸內營養支持優化療法,腸內營養方式與對照組相同,腸內營養液給予原則為由稀至濃、由少至多,如入ICU治療前2 d給予低劑量蛋白(<0.8 g/kg·d),待患者病情穩定后可逐漸增加總蛋白攝入量至1.2~2.0 g/kg·d;營養液的溫度控制在35~37 ℃,預防患者腹瀉、痙攣;整個過程采取無菌標準操作,患者床頭上抬45 °,以半臥位進行營養支持以預防誤吸;每2 h觀察一次胃液殘留量,若連續4 h胃液殘留量>50 mL/次,則腸內營養液泵入速度減為原來流速一半,若1 h后仍是胃液殘留量>50 mL/次,采取遵醫囑應用胃動力藥物,胃腸減壓,需要時放置小腸管;早期每隔2 h監測一次血糖,待血糖穩定后降低至每隔2 h監測一次血糖,以確保患者血糖波動范圍為5~12 mmol/L,若患者血糖高出參考范圍時改用低糖營養液或給予胰島素,出現血糖降低時需要緩慢停用要素飲食。
1.5觀察指標與方法于治療前、治療7 d時,進行指標觀察: (1)采取患者清晨空腹靜脈血5 mL,使用血細胞檢測儀監測淋巴細胞計數,使用生化分析儀檢測血清白蛋白、 C反應蛋白(C-reactive protein, CRP)、白介素-6(interleukin-6, IL-6)、腫瘤壞死因子-α(tumor necrosis factor-α, TNF-α); (2)統計患者BMI變化; (3)使用急性生理學及慢性健康狀況(acute physiology and chronic health conditions, APACHE Ⅱ)評分系統[8]評估患者病情恢復情況, APACHE Ⅱ總分范圍0~71分,分值越高患者病情恢復越差; (4)超聲心動圖檢測左室射血分數(left ventricular ejection fraction, LVEF)、左室收縮末期內徑(left ventricular end systolic diameter, LVESD)、左室舒張末期內徑(left ventricular end diastolic diameter, LVEDD); (5)統計患者的機械通氣時間、入住ICU時間和住院時間; (6)記錄患者治療期間并發癥發生情況,并發癥包括腹脹、胃潴留、便秘和吸入性肺炎等。并發癥總發生率=并發癥例數/總例數×100%。
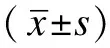
2 結果
2.12組患者淋巴細胞計數、血清白蛋白和BMI比較治療前, 2組患者淋巴細胞計數、血清白蛋白水平和BMI差異均無統計學意義(P>0.05)。治療7 d時, 2組患者淋巴細胞計數高于同組治療前(P<0.05),觀察組血清白蛋白水平高于同組治療前(P<0.05);觀察組患者淋巴細胞計數、血清白蛋白水平和BMI均高于對照組(P<0.05)。見表1。
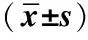
表1 2組患者淋巴細胞計數、血清白蛋白和BMI比較
2.22組患者APACHEⅡ評分比較治療前, 2組患者APACHE Ⅱ評分差異無統計學意義(P>0.05);治療7 d時, 2組患者APACHE Ⅱ評分均低于同組治療前(P<0.05),觀察組患者APACHE Ⅱ評分低于對照組(P<0.05)。見表2。
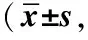
表2 2組患者APACHE Ⅱ評分比較分)
2.32組患者LVEF、LVESD和LVEDD值比較治療前, 2組患者LVEF、 LVESD和LVEDD值差異無統計學意義(P>0.05);治療7 d時, 2組患者LVESD值均低于同組治療前(P<0.05), 2組患者LVEF、 LVESD和LVEDD值差異均無統計學意義(P>0.05)。見表3。
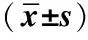
表3 2組患者LVEF、 LVESD和LVEDD值比較
2.42組患者血清CRP、IL-6和TNF-α水平比較治療前, 2組患者血清CRP、 IL-6和TNF-α水平差異均無統計學意義(P>0.05);治療7 d時, 2組患者的CRP、 IL-6和TNF-α水平均低于同組治療前(P<0.05),觀察組患者CRP、 IL-6和TNF-α水平均低于對照組(P<0.05)。見表4。
表4 2組患者血清CRP、 IL-6和TNF-α水平比較
2.52組患者機械通氣時間、入住ICU時間和住院時間比較觀察組患者機械通氣時間、入住ICU時間和住院時間均少于對照組(P<0.05)。見表5。

表5 2組患者機械通氣時間、入住ICU時間和住院時間比較
2.62組患者并發癥比較觀察組患者出現腹脹、胃潴留各1例;對照組患者中腹脹2例、胃潴留3例、便秘1例、吸入性肺炎1例。觀察組并發癥總發生率低于對照組(P<0.05)。見表6。

表6 2組患者并發癥發生比較[例(%)]
3 討論
老年ICU重癥患者由于受到病情影響和身體功能降低,機體處于高代謝水平狀態,導致老年ICU重癥患者在接受治療過程中需要補充足夠的營養物質,改善患者的神經調節,恢復能量代謝平衡,有助于患者的病情緩解,改善患者預后[9-10]。本研究結果顯示, 2種營養支持治療7 d時患者的淋巴細胞計數較治療前呈明顯升高趨勢, APACHE Ⅱ評分較治療前呈明顯降低趨勢,觀察組患者治療7 d時的血清白蛋白水平高于其治療前,與文獻[11]研究結果趨勢相似;此外,觀察組患者治療7 d時的淋巴細胞計數、血清白蛋白水平和BMI均明顯高于對照組,而APACHE Ⅱ評分明顯低于對照組。淋巴細胞是機體免疫應答功能的重要細胞成分,具有調節免疫的作用,淋巴細胞計數偏低提示免疫力降低[12]。白蛋白對血漿膠體滲透壓有維持和調節作用,還對免疫球蛋白有保護作用,能夠增強機體免疫力[13]。APACHE Ⅱ評分是急性生理評分、年齡評分、慢性生理評分構成的評分系統,能夠幫助醫生客觀判斷患者病情和評估患者預后情況,有利于制定更加準確、有效的治療方案[14]。腸內營養支持是依靠患者腸黏膜的吸收功能,將其作為補充營養物質的途徑,不僅能夠給予患者及時補充營養,同時還能夠增加患者腸黏膜的血流量,對腸道進行刺激產生激素、消化液,從而加快患者腸上皮組織的修復,防止患者因營養不良導致疾病進一步出現惡化,營養支持優化根據患者的自身情況進行個性化營養液泵入,由稀到濃、少到多,能夠幫助ICU重癥患者腸胃逐漸適應,從而能夠更好的預防腹脹、感染以及腸功能不全等疾病的發生,能夠在一定程度上增強患者自身的免疫力[15-16]。
腸內營養支持優化能夠幫助ICU患者獲得充分的營養并有效降低住院期間營養不良發生率[17], ICU重癥患者自身病情危重,機體消耗負擔增大,及時給予營養支持可以緩解機體過度消耗,但早期給予過量腸內營養物質,會加重臟器負擔,加重機體炎癥應激反應。本研究結果顯示2種營養支持治療7 d時患者LVESD值、 CRP、 IL-6和TNF-α水平較治療前降低,并且觀察組患者CRP、 IL-6和TNF-α水平降低趨勢更明顯,與文獻[18]研究結果趨勢相似,說明腸內營養支持優化療法能夠緩解ICU重癥患者機體炎癥反應,根據患者自身情況給予優化腸內營養支持,在改善患者營養狀態的同時還可以提高患者的免疫能力,改善體內炎癥代謝和器官損傷,緩解病情[19]。有研究[20]表明在靜脈營養支持增加腸內營養支持能夠有效減緩胃癌患者腹腔化療對患者營養狀況的影響,不僅可以降低不良反應發生率,還能加快患者腸道恢復,縮短住院時間。本研究結果顯示,采取腸內營養支持優化療法的老年ICU重癥患者的機械通氣時間、入住ICU時間和住院時間均明顯短于行常規腸內營養支持的患者,并且治療期間并發癥總發生率也降低,說明給予老年ICU重癥患者腸內營養支持優化法有助于縮短患者住院時間和降低并發癥。
腸內營養支持有利能保證患者所需營養物質得到充分補足,營養物質能有效防止細菌移位,有助于改善患者的免疫功能和胃腸功能恢復[21]。腸內營養支持的應用是有條件的,需要患者的腸道功能沒有太大損傷,而且遠端的腸管沒有梗阻現象,否則不能使用[22]。在給予患者進行腸內營養支持時,應當按照由少到多、慢到快、稀到濃的原則進行營養劑的給予,保證腸道能夠有適應的過程,降低不良事件的發生[23]。在給予患者腸內營養支持時要加強對患者的監測,首先要明確導管在患者體外的位置,并定期進行檢查確定導管無移位現象的出現。如果發現異常要及時進行調整,防止營養劑因管腔折疊、彎曲等因素影響返回進入食管,引起誤吸。ICU重癥患者大部分的胃腸排空功能不良,導致胃潴留的發生率較高,在給予患者腸內營養支持要求患者45 °半臥位,胃腸道耐受性差的患者需要適當的降低營養劑的輸入量以及注入速度等。
綜上所述,給予老年ICU重癥患者腸內營養支持優化療法更能提高患者的免疫力,緩解機體炎癥反應,促進患者病情恢復,還能降低患者治療期間并發癥,縮短老年ICU重癥患者的機械通氣時間、入住ICU時間和住院時間,能夠有效地改善患者的預后情況,因而其具有一定臨床應用價值。但是本研究仍存在著許多不足之處,納入的患者類型不夠全面,具有一定的限制性,所以在后期的研究中將增加觀察指標、擴大樣本量,使其結果更加準確,從而能夠為其臨床治療提供有力的依據。

