低Pt載量PtFeNi@C催化劑制備及其電解水析氫性能
張紫琪,范愛鑫,秦聰麗,王茜,王樹軍
(廊坊師范學院 化學與材料科學學院,河北 廊坊 065000)
隨著社會的不斷進步和發展,人們對能源的需求日益增加,而傳統化石能源儲量減少以及環境污染等問題,人類開始致力于研究可持續發展的、綠色的、清潔的可再生能源[1]。氫能是一種環境友好的清潔高效能源,具有熱值高、可再生等優點,被認為是很有前途的替代化石燃料的清潔能源載體[2]。因此,開發高效、清潔的制氫技術對于人類社會的發展意義重大。目前,工業制氫主要來自甲烷蒸汽重整和煤氣轉化過程,不僅依賴于有限的不可再生的化石燃料,而且制氫過程中還會造成嚴重的環境污染并排放大量的溫室氣體[3]。而電解水制氫技術因其具有成本低、反應物易于獲得、產量穩定并且產物純度較高等優點,引起人們的廣泛關注,被認為是一種理想的大規模制氫方法。電解水制氫反應包括:陰極析氫反應(HER)和陽極析氧反應(OER)兩個半反應,反應過程中涉及多電子轉移,表現出緩慢的反應動力學過程,因此制備高效的催化劑降低反應過電位具有重要意義。目前,具有最小超電勢的鉑基催化劑被認為是電解水析氫的最高效最典型的電化學催化劑[4],但其低儲量、高昂的成本限制了其在實際中的廣泛應用。
近年來,科研工作者致力于研發廉價的、高效的可替代貴金屬的HER催化劑,儲量豐富、價格低廉以及高活性的非貴金屬基磷化物、硫化物、硒化物、碳化物以及金屬合金受到了廣泛關注[5],其中過渡金屬Ni、Co、Fe等合金及其化合物是一類富有前景的高效HER電催化劑。但是,在酸性電解質溶液和高電壓下長時間測試時,裸露的過渡金屬合金催化劑通常會發生溶解和團聚。
為了解決這個問題,研究人員采用碳材料包覆過渡金屬合金策略制備出金屬-碳核殼結構催化劑[6],碳材料在保護金屬顆粒的同時還能提高導電性,從而提升催化劑的電催化性能。新興的由金屬離子和有機配體經自組裝形成的金屬有機框架(MOF)材料通過簡單的碳化過程就可以制得金屬-碳復合材料,被認為是制備碳包覆金屬復合材料的理想前體。然而,盡管金屬-碳核殼結構催化劑取得了一些進展,但這些材料的HER性能仍無法與Pt基催化劑相比。因此,構建低成本、高效、穩定的Pt基電催化劑至關重要。
基于此,本文采用一種簡單的由正己烷(疏水性溶劑)和水(親水性溶劑)組成的“雙溶劑”策略,首先將少量的H2PtCl6溶液浸漬到雙金屬FeNi-MOF的孔道中,經Ar氛圍高溫煅燒成功制備出低Pt載量(質量分數0.7%)的PtFeNi@C催化劑,將PtFeNi合金原位封裝在石墨化碳層內。采用SEM、TEM、XRD和XPS分析所合成材料的形貌和結構,采用電化學工作站測試催化劑的線性掃描伏安曲線(LSV)和Tafel斜率,研究合成材料的電催化析氫性能。
1 儀器與材料
1.1 材料
六水合氯鉑酸,對苯二甲酸,六水合氯化鐵,乙酰丙酮鎳,正己烷,N,N-二甲基甲酰胺,無水乙醇,硫酸,從國藥集團化學試劑有限公司購買。
1.2 實驗設備
電子天平,梅特勒-托利多公司;烘箱,北京陸希科技有限公司;超聲清洗儀,昆山立波超聲波設備有限公司;電化學工作站,上海辰華;管式爐,天津中環;高速離心機,湘儀儀器有限公司。
1.3 催化劑的制備
雙金屬FeNi-MOFs的制備:將270 mg六水合氯化鐵、128 mg乙酰丙酮鎳和166 mg對苯二甲酸加入16 mL DMF中,攪拌均勻后,置于50 mL聚四氟乙烯高壓釜中,120 ℃反應8 h。離心收集沉淀物,并用水-乙醇洗滌3次,120 ℃干燥12 h備用。
H2PtCl6浸漬FeNi-MOFs的制備:取100 mg FeNi-MOFs分散在10 mL正己烷中,超聲分散均勻。將H2PtCl6溶液加入到上述分散液中。離心收集沉淀物,并在60 ℃下干燥12 h。
Pt-FeNi@C的制備:在Ar氛圍下,將上述烘干后的前體置于管式爐中,升溫至600 ℃并維持此溫度2 h后,自然冷卻至室溫,得到PtFeNi@C復合材料。
1.4 分析測試儀器
采用Bruker D8 ADVANCE型X-射線衍射儀表征催化劑的晶相結構,Cu靶,掃描范圍20°~90°。采用掃描電子顯微鏡(Quanta 200F)和透射電子顯微鏡(Tecnai F20)分析催化劑的形貌及結構。用X 射線光電子能譜儀測定分析催化劑表面元素價態,利用電感耦合等離子體發射光譜儀對催化劑元素含量進行測定。所有的電化學測試,均利用CHI-660e(上海辰華)電化學工作站上測得,采用三電極體系:Hg/HgCl2為參比電極,碳棒為對電極,直徑3 mm的玻碳電極為工作電極。
2 實驗結果與討論
2.1 XRD分析
圖1為PtFeNi@C和未摻雜Pt的FeNi@C材料的XRD圖。

圖1 PtFeNi@C和FeNi@C樣品XRD圖
從圖1可以看出,2θ=43.6°,50.8°和74.7°處分別出現歸屬于立方相Fe0.64Ni0.36合金的(111),(200)和(220)晶面(JCPDS:47-1405)。與FeNi@C相比,PtFeNi@C材料的特征衍射峰發生負向偏移,根據布拉格方程,計算出PtFeNi@C材料中Fe0.64Ni0.36合金的晶格參數為0.359 nm,大于FeNi@C中Fe0.64Ni0.36合金的晶格參數(0.357 nm),說明原子半徑較大的Pt原子取代了Fe和/或Ni原子。除此之外沒有其他雜峰,說明制備的催化劑較純。
2.2 SEM分析
PtFeNi@C材料的SEM照片如圖2所示。由圖2可知,PtFeNi@C材料整體呈大小均勻的雙錐體形狀,平均長度為2.5 μm,直徑約為0.6 μm,表面較粗糙。

圖2 PtFeNi@C材料的SEM圖
2.3 TEM分析
圖3為PtFeNi@C材料的TEM圖及高倍TEM照片。從圖3可以清晰地觀察到所合成的棒狀PtFeNi@C材料由許多尺寸相似的小納米顆粒組成,隨機選取100個納米顆粒進行統計,發現小顆粒由平均尺寸約60 nm的金屬內核和約12 nm的碳殼層組成。高倍TEM照片清晰地顯示出金屬顆粒被包裹在碳殼內,0.34 nm的晶格間距是石墨碳的層間距,表明組成棒狀PtFeNi@C材料的單個納米顆粒是由核-殼構成。核-殼結構有利于金屬納米顆粒與石墨碳間的電子傳遞且電化學測試過程中能夠避免金屬納米顆粒的溶解和聚集,提高材料的導電性能及電催化析氫性能。

圖3 PtFeNi@C材料的TEM及HRTEM照片
2.4 XPS分析
為了進一步探究樣品的結構和表面化學組成,對PtFeNi@C材料進行了XPS表征,結果如圖4示。樣品中出現C、Fe、Ni等元素特征峰,Pt元素特征峰較微弱,通過ICP測得Pt的質量含量為0.7%,表明合成的樣品中Pt含量較低。Pt 4f的高分辨率光譜圖位于71.8和75.1 eV處的峰屬于金屬態Pt的特征峰。值得指出的是,與純Pt的兩個峰(Pt 4f:70.9,74.3 eV)相比,PtFeNi@C樣品中Pt特征峰向高結合能方向發生偏移,表明過渡金屬Fe和Ni與Pt之間存在電子相互作用,并且電子向Pt發生轉移。Fe 2p譜圖中位于707.4 eV處的峰屬于單質Fe0,譜圖中位于710.7和712.8 eV處的特征衍射峰分別對應Fe2+和Fe3+。Ni 2p譜圖中位于853 eV和856 eV處的衍射峰分別屬于Ni0+和Ni2+。Fe2+、Fe3+和Ni2+的存在說明樣品表面有一定的氧化。
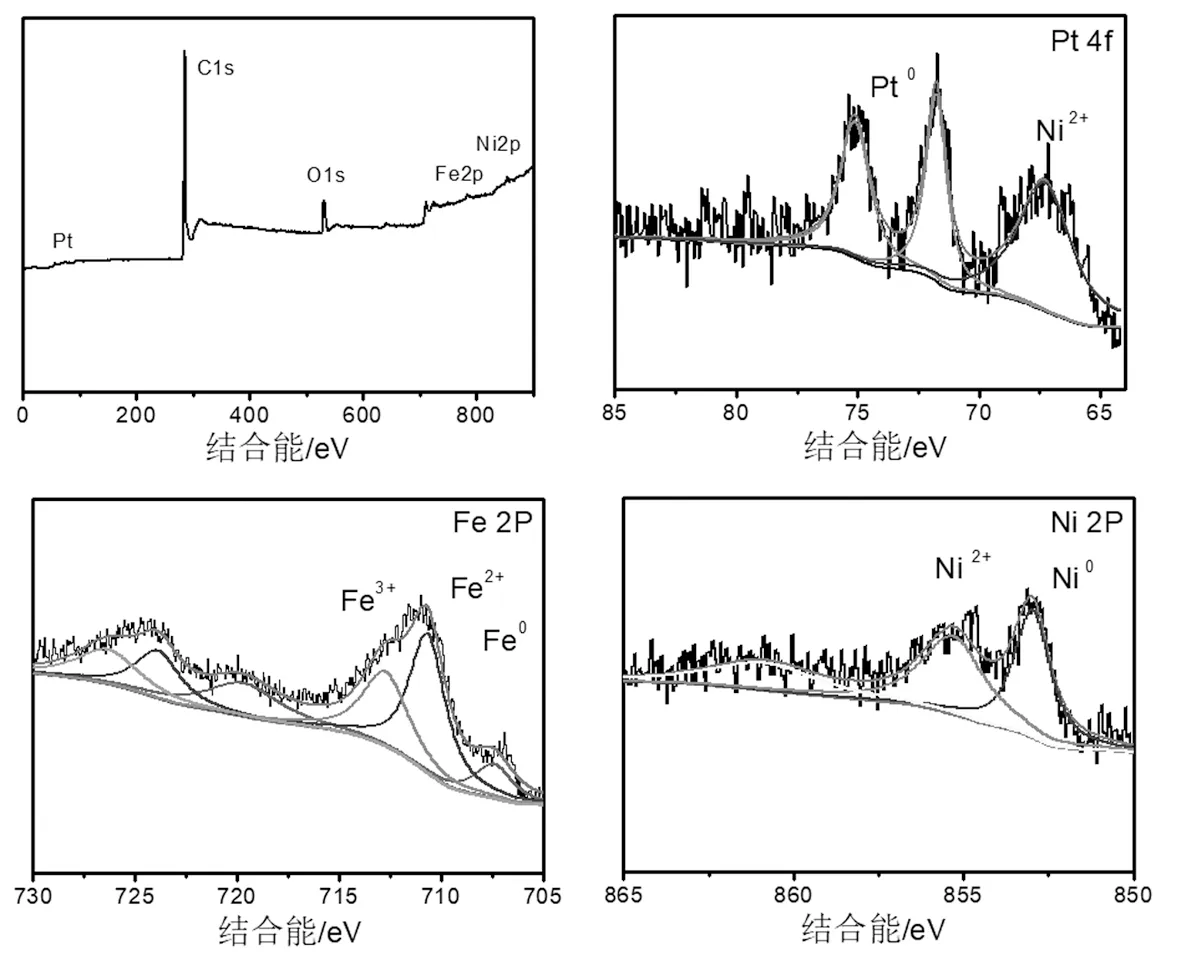
圖4 PtFeNi@C樣品的XPS譜圖
2.5 催化劑電解水析氫性能分析
圖5a為PtFeNi@C、FeNi@C和商業Pt/C催化劑的線性掃描伏安曲線(LSV)圖。通過比較LSV極化曲線同一電流密度下的過電位來評價催化劑的電化學析氫性能。
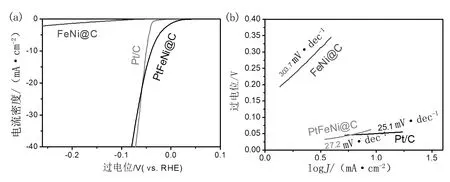
圖5a PtFeNi@C、FeNi@C和商業Pt/C催化劑的線性掃描伏安曲線圖
由圖5a可以看出,在0.5 mol/L H2SO4電解質溶液中,未摻雜的FeNi@C的HER活性很差。當電流密度為-10 mA·cm-2,PtFeNi@C的過電位為-42 mV,商業Pt/C催化劑的過電位為-50 mV,表明PtFeNi@C材料擁有較好的電化學析氫催化活性。
Tafel斜率作為電催化材料的內在特性,能反映電催化材料的動力學特征,是分析電催化性能的一個重要指標,且斜率越小,過電位越小,電催化反應速度越快,析氫性能越好。圖5b為PtFeNi@C、FeNi@C和商業Pt/C催化劑的Tafel曲線圖。從圖5b可以看出,PtFeNi@C的Tafel斜率為27.2 mV·dec-1,而FeNi@C和商業Pt/C的Tafel斜率分別為303.7和25.1 mV·dec-1,表明FeNi@C樣品的速率決定步驟是Volmer步驟,而Pt-FeNi@C和Pt/C的速率確定步驟是Tafel步驟,遵循Volmer-Tafel反應機理。Pt-FeNi@C材料的Tafel斜率與商業Pt/C相當,說明少量Pt摻雜就能達到很好的催化性能。
圖6為PtFeNi@C材料的HER穩定性測試。由圖6a可知,經過1 000圈CV測試后,在電流密度為-10 mA·cm-2下,電壓幾乎沒有衰減。此外,圖6b所示i-t穩定性測試也表明,PtFeNi@C樣品保持電流密度10 mA·cm-2至少10 h而無衰減。以上穩定性測試均證實了PtFeNi@C樣品在0.5 mol/L H2SO4酸性條件下具有良好的HER穩定性。
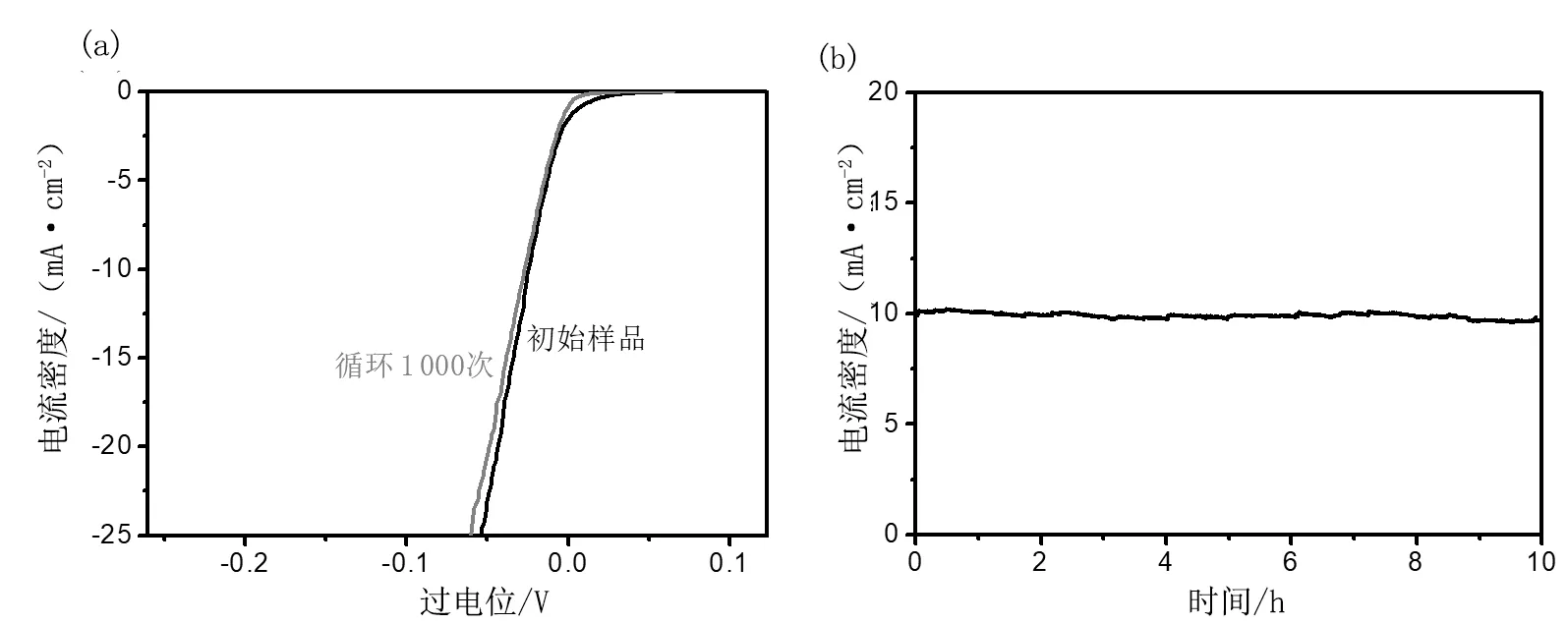
圖6 PtFeNi@C催化劑的(a)循環伏安穩定性測試曲線,(b)計時電流穩定性測試曲線
3 結論
1) 采用“雙溶劑”浸漬、煅燒策略制備出低Pt含量的棒狀PtFeNi@C催化劑。
2) 在電流密度10 mA·cm-2時,PtFeNi@C催化劑析氫過電位為-42 mV,Tafel斜率為27.2 mV·dec-1,HER催化活性較好,且具有良好的HER穩定性。
3) 這種新型催化劑合成策略在其他能量轉換和儲能領域具有廣闊的應用前景。

