基于網絡藥理學初步預測肝素鈉對高血糖的作用
王 儀,陳秀山
(1.山東省中醫藥研究院,山東 濟南 250014 ;2.東營天東制藥有限公司,山東 東營 257100)
近年來,受生活節奏快,工作壓力大,高脂、高鹽、高糖食物攝入量增加等因素的影響,高血糖的發病率逐漸增高[1]。高血糖可通過多種途徑損害機體健康[2-3],嚴重影響患者的生活質量。其臨床治療方法包括改善胰島素抵抗和血糖控制[4]。肝素是一種高度硫酸化帶負電荷的非均一線性糖胺聚糖,屬于天然生物聚合物[5]。其由糖鏈的異質混合物組成[6-7],平均MW 為12 000 ~16 000 Da[8-9]。天然的異質分子可引起相關結構變化,這有利于肝素與各種蛋白質相互作用產生多種生物活性[10]。研究表明,肝素具有抗病毒、抗炎、促進傷口愈合等非抗凝活性[11]。有研究[12-13]證實,肝素具有抑制血管生成的作用,其衍生物sevuparin[14]被報道對抑制惡性瘧原蟲具有輔助作用。肝素在胰島素降血糖機制中也發揮著重要作用[15],負載氧化銅納米酶的肝素水凝膠治療糖尿病創面可取得顯著的療效[16]。針對肝素本身對于高血糖的影響目前臨床上尚無深入的研究,本研究采用數據挖掘、網絡藥理學分析等方法初步探討了肝素與高血糖的聯系。
1 數據與方法
1.1 數據
使用的數據庫及平臺:SwissTargetPrediction ,Uniprot , PubChem, DrugBank, OMIM, GeneCards v5.13,Metascape , STRING v11.5, Cytoscape v3.9.1。
1.2 潛在藥物靶點篩選
在數據庫Uniprot、SwissTargetPrediction、PubChem及DrugBank 中篩選肝素鈉的潛在靶點信息,匯總靶點,去除重復項。
1.3 疾病靶點獲取
在數據庫GeneCards 和OMIM 中,以“hyperglycemia”為關鍵詞查詢疾病靶點,去除重復項,取與1.2 所得肝素鈉靶點的交集。
1.4 蛋白互作(PPI)網絡構建及分析
將1.3 所得成分- 疾病共同靶點導入STRING,選擇Homo sapiens 物種,設置medium confidence 為0.4,斷開隱藏網絡中連接的節點(即游離基因)。各節點的重要性使用“度值(degree)”“介數中心性(betweenness)”表示:度值和介數中心性的大小分別表示此節點在網絡中所具有的直接作用關系的多少及在網絡中所起的橋梁作用的情況。
1.5 基因本體(GO)功能及京都基因與基因組百科全書(KEGG)通路富集分析
在metascape 平臺中導入得到的交集靶點,設置物種為“Homo sapiens”,行富集分析,分析其可能的主要生物學過程與代謝通路。
2 結果與分析
2.1 藥物干預高血糖潛在靶點
將GeneCards 及OMIN 數據庫中檢索到的疾病靶點合并去重,得到1143 個疾病相關靶點。對1143 個疾病靶點與143 個藥物靶點取交集,得到33 個肝素鈉與高血糖交集靶點。
2.2 PPI 網絡
將33 個交集基因置入數據庫String 中,構建了33 個節點、97 條邊、平均度值5.88 的PPI 網絡,利用Cytoscape 軟件對其進行拓撲分析,見圖1a。將度值和介數中心性均大于中位值的6 個靶點確定為肝素鈉干預高血糖的潛在關鍵靶點,得出與藥物干預高血糖關系密切的蛋白主要有TLR4、HIF1A、SERPINE1、CXCR4、FGF2、MTOR 等,見表1。這表明,肝素與高血糖存在聯系,可干預高血糖的治療。


圖1 蛋白互作、GO 和KEGG 富集分析圖
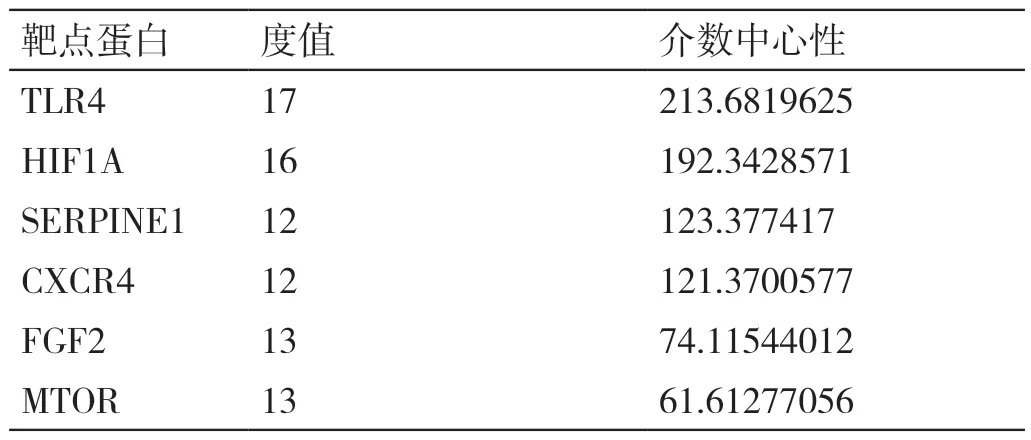
表1 治療疾病重要靶點
2.3 GO 功能及KEGG 通路富集分析
使用DAVID 數據庫對31 個交集靶點進行GO 功能〔生物過程(BP)、分子功能(MF)和細胞成分(CC)〕和KEGG 通路富集分析。分析GO 的BP 20 個條目、CC 5 個條目、MF 8 個條目,發現肝素鈉干預高血糖可能富集在炎癥反應、細胞遷移正調控、傷口愈合調節、細胞對有機氮化合物響應、低氧應答、細胞因子產生正調控和第二信使介導的信號傳導等BP(圖1b),血小板α 粒、細胞膜筏、早期核內體、內吞囊泡及核斑點等CC(圖1c),肝素結合、泛素蛋白連接酶結合、內肽酶活性、磷蛋白結合、絲氨酸型內肽酶抑制劑活性、蛋白質異二聚活性、以醇基為受體的磷酸轉移酶活性、細胞因子受體結合等MF(圖1d)。GO 功能分析表明肝素鈉可能通過影響BP 中炎癥反應、細胞遷移正調控、傷口愈合調節、細胞對有機氮化合物響應、低氧應答、細胞因子產生正調控和第二信使介導的信號傳導等過程,CC 中血小板α 粒、細胞膜筏、早期核內體、內吞囊泡及核斑點等成分,MF 中肝素結合、泛素蛋白連接酶結合、內肽酶活性、磷蛋白結合、絲氨酸型內肽酶抑制劑活性、蛋白質異二聚活性、以醇基為受體的磷酸轉移酶活性、細胞因子受體結合等功能發揮治療作用。KEGG 通路分析顯示,基因主要富集于HIF-1 信號通路、癌癥途徑、鈣信號通路、Apelin 信號通路、鞘氨醇脂質信號通路、流體剪切應力與動脈粥樣硬化、補體和凝血級聯等通路,見圖1e。
3 討論
長期的高血糖一定程度上會損傷機體神經、血管等器官,進而引發諸多疾病。肝素存在于細胞外基質和循環血液中,可抗凝血,并參與機體的免疫調節。研究發現肝素對動物的葡萄糖穩態具有重要的調節作用[17]。葡萄糖穩態是血糖維持穩定的重要因素,因此,本研究假設肝素可干預高血糖,并通過網絡藥理學技術進行預測。網絡藥理學預測表明,肝素鈉與高血糖有多種共同靶點,且GO 和KEGG 分析表明肝素鈉可能通過TLR4、HIF1A、SERPINE1、CXCR4、FGF2、MTOR 等蛋白及HIF-1 信號、鈣信號、Apelin 信號、鞘氨醇脂質信號、流體剪切應力與動脈粥樣硬化、補體和凝血級聯等多種調控通路影響血糖。
綜上所述,本文利用網絡藥理學初步預測得出肝素鈉可能通過作用于TLR4、HIF1A、SERPINE1、CXCR4、FGF2、MTOR 等多個關鍵靶點基因,干預炎癥反應、細胞遷移正調控、血小板α 粒、細胞膜筏、肝素結合、泛素蛋白連接酶結合及絲氨酸型內肽酶抑制劑結合等功能,調控HIF-1 信號通路、癌癥途徑、鈣信號通路、Apelin 信號通路、鞘氨醇脂質信號通路、流體剪切應力與動脈粥樣硬化、補體和凝血級聯等進程干預高血糖,其作用機制涉及多種靶點基因和信號通路。但后續仍需要進行相關實驗,以確定肝素對血糖的作用。

