依帕司他聯合甲鈷胺對2 型糖尿病周圍神經病變的神經功能及不良反應的影響分析
葉長東,孫慶
1. 濟南市第七人民醫院藥劑科,山東濟南 250100;2. 山東省公共衛生臨床中心鄉村振興部,山東濟南 250100
伴隨2 型糖尿病(diabetes mellitus type 2,T2DM)患者病情不斷發展,會導致機體神經、血管等出現病變,對眼睛、臟器等健康造成嚴重的威脅[1-2]。 糖尿病周圍神經病變(diabetic peripheral neuropathy, DPN)屬于糖尿病(diabetes mellitus, DM)中常見的一種并發癥,會對患者運動神經、感覺神經造成損害。DPN 的臨床癥狀有疼痛、肢體木、感覺與運動神經功能產生障礙等[3]。DPN 患者發病較為隱匿,該疾病的進展相對較為緩慢,患者一旦發病即使對其血糖控制較好,也會影響生活質量[4]。如今,臨床通過營養神經、緩解循環藥物對DPN 患者進行治療。依帕司他屬于醛糖還原酶的抑制類藥物,可對山梨醇水上升發揮抑制效果,但是并不能使患者損傷的神經組織得到有效修復;甲鈷胺屬于內源性的維生素B12,能夠對患者神經纖維進行修復,使神經傳導的速度加快;所以聯合治療可相互促進,使其臨床治療效果更佳[5-6]。基于此,本研究選取2021 年4 月—2023 年4 月濟南市第七人民醫院收治的2 型糖尿病周圍神經病變88 例患者以不同方法治療進行分析,現報道如下。
1 資料與方法
1.1 一般資料
選取本院收治的88 例2 型糖尿病周圍神經病變患者,按隨機數表分為兩組,各44 例。對照組男24 例,女20 例;年齡41~80 歲,平均(60.48±5.07)歲;病程3~10 年,平均(6.49±1.21)年。研究組男23 例,女21 例;年齡42~80 歲,平均(61.01±5.09)歲;病程4~10 年,平均(7.01±1.23)年。兩組一般資料比較,差異無統計學意義(P>0.05),具有可比性。本研究已通過醫院醫學倫理委員會批準。
1.2 納入與排除標準
納入標準:①患者的癥狀、臨床表現與《神經內科學》中DPN 診斷的標準相符[7];②能夠正常溝通者;③本研究的患者、家屬均清楚且愿意參與。
排除標準:①對本研究中的藥物有過敏史者;②并發其他嚴重的病變者;③并有腎功能異常者;④有理解、溝通障礙者。
1.3 方法
做好患者的飲食、運動指導,維持空腹血糖(fasting plasma glucose, FPG)指標在4.4~7.0 mmol/L范圍內,餐后2 h 血糖(2-hour postprandial blood glucose, 2 hPG)指標在5.0~9.2 mmol/L 范圍內。
給予對照組甲鈷胺(國藥準字為H20052207;規格:0.5 mg×20 粒)口服治療,用藥0.5 mg/次,3 次/d。研究組在對照組治療基礎上給予依帕司他片(國藥準字H20040012;規格:50 mg/片)口服,0.5 mg/次,3 次/d。兩組均持續治療兩個月。
1.4 觀察指標
治療效果。患者的雙下肢麻木、疼痛、蟻走感全部消除,腱反射也恢復到正常情況表示顯效;患者的雙下肢麻木、疼痛、蟻走感基本緩解,腱反射有所改善表示有效;患者的雙下肢麻木、疼痛、蟻走感、腱反射情況沒有變化表示無效;總有效率=(顯效例數+有效例數)/總例數×100%。
神經傳導的功能。以Nicolet EDX 肌電誘發電位系統對其腓總神經、正中神經的感覺神經傳導速度(sensory nerve conduction velocity, SCV)、運動神經傳導速度(motor nerve conduction velocity, MCV)進行測定。
氧化應激水平。采集患者5 mL 空腹時的靜脈血,以3 000 r/min 的速度對其進行20 min 的離心,以日立7600 全自動的生化分析儀對其血清超氧化物歧化酶、還原性谷胱甘肽指標進行檢測。
不良反應發生情況。包括頭暈、惡心嘔吐、皮疹的發生率[8-9]。
1.5 統計方法
采用SPSS 20.0 統計學軟件進行數據分析,計量資料符合正態分布,以()表示,進行t檢驗;計數資料以例數(n)和率(%)表示,進行χ2檢驗。P<0.05 為差異有統計學意義。
2 結果
2.1 兩組患者治療效果對比
研究組總有效率比對照組更高,差異有統計學意義(P<0.05)。見表1。

表1 兩組患者治療效果對比
2.2 兩組患者神經傳導功能對比
治療后,研究組正中神經與腓總神經的SCV、MCV 指標均比對照組高,差異有統計學意義(P<0.05)。見表2。
表2 兩組患者神經傳導功能對比[(),m/s]
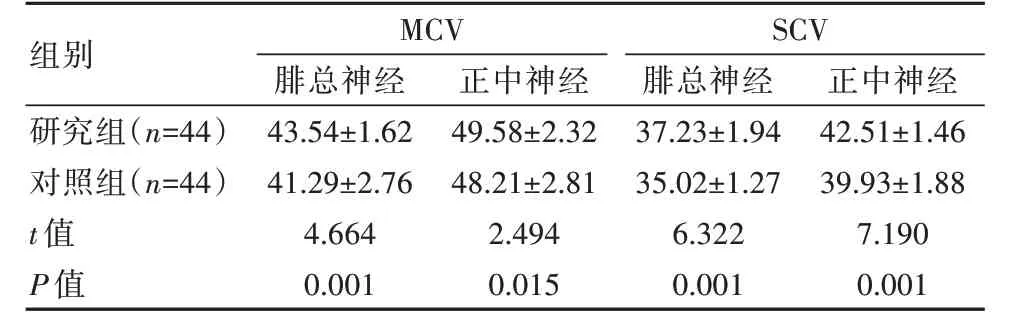
表2 兩組患者神經傳導功能對比[(),m/s]
?
2.3 兩組患者氧化應激情況對比
治療前,兩組患者的氧化應激水平比較,差異無統計學意義(P>0.05);治療后,研究組血清超氧化物歧化酶、還原性谷胱甘肽水平高于對照組,差異有統計學意義(P<0.05)。見表3。
表3 兩組患者氧化應激情況對比()
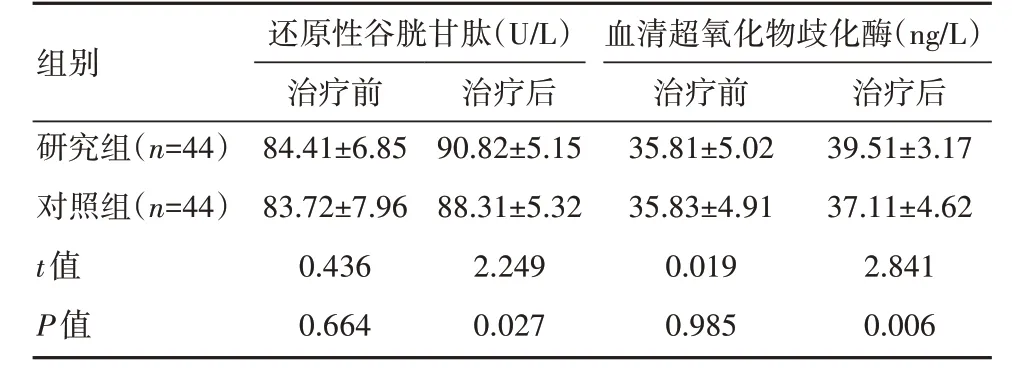
表3 兩組患者氧化應激情況對比()
?
2.4 兩組患者不良反應發生情況對比
兩組不良反應發生率比較,差異無統計學意義(P>0.05)。見表4。

表4 兩組患者不良反應發生率對比
3 討論
DPN 臨床癥狀主要是感覺異常、對稱性的疼痛,在下肢比較常見,疼痛較為劇烈會對患者運動神經造成影響,使人體的肌力衰退,甚至肌肉會萎縮,進而使患者的生活質量下降[10]。所以需及早給予患者針對性、科學的治療方法,以其幫助患者改善神經傳導功能,提升臨床治療效果。
本研究結果顯示:治療之后,研究組總有效率為93.18%,優于對照組的77.27%(P<0.05);說明依帕司他、甲鈷胺共同對2 型糖尿病周圍神經病變患者進行治療的效果較好。究其原因,可能是甲鈷胺是內源性的維生素B12,可經甲基產生轉化反應,可有效改善患者的神經元傳導。依帕司他是一種醛糖還原的抑制劑,可對多元醇的代謝進行有效抑制,且對葡萄糖與山梨醇的轉化給予相應抑制,山梨醇會對患者的神經功能產生影響,依帕司他可減少山梨醇產生,進而改善患者神經傳導的速度[11]。兩種藥物聯合治療能夠相互促進,相互協調,使患者的臨床癥狀得到有效緩解,提升其臨床治療效果。本研究結果顯示:治療后,研究組正中神經與腓總神經的SCV、MCV 指標均比對照組高(P<0.05);研究組的血清超氧化物歧化酶、還原性谷胱甘肽水平與對照組相比更高(P<0.05)。DPN 的發病機制還沒有得到明確,大多情況下則是認為多種原因所導致,比如代謝紊亂、血糖過高、氧化應激反應等,而主要的因素是血糖較高,氧化應激作用也較為關鍵。如果DM 患者的血糖長期處在較高的環境,會減少自由基清除率,抗氧化因子以及氧化因子會隨著失衡,導致患者產生神經元DNA,使其脂肪受損,氧化應激反應還會使神經營養因子水平降低,減弱神經纖維修復、再生的能力,而且氧化應激會與其他的因子產生協同效果,所以幫助患者緩解氧化應激狀態特別關鍵[12]。還原性谷胱甘肽屬于抗氧化的金屬酶,可對氧化進行維持、且具有抗氧化的平衡作用,還原性谷胱甘肽可保障正常的免疫功能,具有抗氧化的作用,所以血清超氧化物歧化酶、還原性谷胱甘肽均能夠對機體的氧化應激情況進行反映。SCV、MCV 可對機體的神經功能給予直接反應。依帕司他能夠對醛糖還原酶的活性給予抑制,使細胞中山梨醇、果糖的含量降低,防止過度堆積,從而使患者體內細胞的肌醇指標提升,使三磷酸腺苷、K+、A+酶的活性得到恢復,進而對DPN 進行有效的治療,幫助患者增強神經傳導速度,有效緩解氧化應激情況[13]。甲鈷胺會參與甲基轉移,為蛋白與核酸的合成發揮促進作用,促進軸索再生、軸索內的輸送以及形成髓鞘,對損傷的神經組織進行修復,使患者恢復神經功能,對依帕司他無法修復損傷的神經進行彌補,使神經傳導功能進一步恢復,并緩解氧化應激情況。本研究結果顯示:治療后,兩組不良反應發生率比較,差異無統計學意義(P>0.05)。依帕司他對DPN患者進行治療的安全性、有效性較高,而且治療的效果比甲鈷胺好。依帕司他與甲鈷胺共同治療的效果比單獨采取依帕司他的更佳,說明甲鈷胺能夠與依帕司發揮協調作用。
綜上所述,給予DPN患者依帕司他與甲鈷胺共同進行治療效果更佳,能夠幫助患者改善神經傳導的功能、氧化應激指標。

