左向右分流減緩肺動脈高壓大鼠心臟重構
紀 爽潘 慧李天騏葉夢婷馬銘婕張學佳王曉建*楊曉敏
(1.內蒙古科技大學包頭醫學院,內蒙古 包頭 014040;2.中國醫學科學院,北京協和醫學院,阜外醫院肺血管醫學重點實驗室,心血管疾病國家重點實驗室,國家心血管病中心,北京 100037;3.包頭醫學院第二附屬醫院心內科,內蒙古 包頭 014030;4.浙江大學醫學院附屬邵逸夫醫院全科醫學科,杭州 310016;5.衢州市柯城區人民醫院,浙江 衢州 324000)
肺動脈高壓(pulmonary arterial hypertension,PAH) 是 第 一 大 類 肺 高 血 壓 ( pulmonary hypertension,PH),根據病因不同可分為先心病相關肺動脈高壓( congenital heart disease-associated pulmonary arterial hypertension,CHD-PAH)、特發性肺動脈高壓(idiopathic pulmonary hypertension,IPAH)、遺傳性肺動脈高壓、藥物和毒素相關肺動脈高壓等多種亞型[1]。 CHD-PAH 和IPAH 是我國排名前兩位的肺動脈高壓類型,分別占第一大類肺動脈高壓43.4%~56.1%、30.8%~35.4%[2-3]。 這兩種肺動脈高壓預后差異很大,CHD-PAH 的1 年、5年和10 年生存率分別是99%、91%和85%,而IPAH只有90%、63%和46%[4]。 為何CHD-PAH 患者的預后優于IPAH,具體機制尚不十分清楚。
本課題組在之前的研究中發現,單純左向右分流手術不會誘導大鼠產生肺動脈高壓,但會在術后1 周誘導大鼠出現快速的左心代償性重構,并在術后8 周持續存在[5]。 有研究表明,嚴重的CHD-PAH患者盡管會產生右心結構的改變,但右心收縮功能卻可以在數十年內保持正常。 這種改變可能是由于分流的存在,導致左心部分分擔了右心的壓力[6]。 在先天性心臟病的早期關閉心臟內左向右的分流,使肺血流動力學和血管回到正常環境,這些患者仍有部分會發展成肺動脈高壓且預后明顯比未進行矯治的CHD-PAH 患者差[7-10]。 所以,我們推斷左向右分流引起的左心代償是心臟整體的“預適應”,可能在先心病合并肺動脈高壓患者的預后中起積極的作用。
本項目中,我們利用大鼠頸部分流手術疊加野百合堿(monocrotaline,MCT)來模擬左向右分流型CHD-PAH,設置單純MCT 組來模擬IPAH,比較兩組肺動脈高壓大鼠在表型差異,進而探究兩種不同類型肺動脈高壓患者預后不同的可能原因。
1 材料和方法
1.1 實驗動物
24 只SPF 級雄性SD 大鼠(150 ~200 g,8 周齡),購買自北京維通利華動物實驗技術有限公司[SCXK(京)2021-0006]。 動物飼養條件為12 h/12 h 的明/暗交替、濕度(50±10)%、溫度(22±1)℃,自由獲取飲食,飼養在清潔環境,飼養于心血管疾病國家重點實驗室[SYXK(京)2022-0052]。 所有動物實驗嚴格遵守3R 原則,本項目研究方案通過阜外醫院動物倫理委員會批準(FW-2022-0028)。
1.2 主要試劑與儀器
異氟烷(廣州碩恒生物科技有限公司,批號:20221001);野百合堿(MCT)(美國Sigma 公司,批號:mfcd00084656);4%多聚甲醛溶液(北京雷根生物技術有限公司,批號:0111A23);EVG 染色試劑盒(上海碧云天生物技術有限公司,批號:GR3382140-1)。 小動物超聲儀(加拿大VisualSonics 公司,序列號:041QPR);小動物氣麻醉機(美國Matrx 公司,序列號:V1643859);多導生理記錄儀(Powerlab 8/30)及其配套的壓力換能器(北京華睿寶科技有限公司,序列號:DB763);全景玻片掃描系統(廈門精藝興業科技有限公司,序列號:17490957)。
1.3 實驗方法
1.3.1 動物分組
將大鼠隨機分為3 組:對照組(control,n=8);單純野百合堿組(simple MCT,n=8),皮下注射MCT(50 mg/kg);手術+MCT 組(operation+MCT,n=8),頸部動靜脈吻合術的同時注射MCT(50 mg/kg)。造模后3 周為實驗終點,各組大鼠進行超聲心動圖檢查、右心導管檢測和肺組織病理學分析。
1.3.2 頸部動靜脈吻合術
吸入異氟烷麻醉后,大鼠仰臥固定于手術臺,頸部剃毛備皮后,做一斜形切口。 分離頸部動、靜脈,腹腔注射肝素200 U,夾住動、靜脈近端,綁扎遠端,剪斷動、靜脈,吻合動、靜脈殘端。動靜脈吻合后,拔除血管夾,立即可見靜脈搏動,吻合口無漏血,手術成功。 縫合頸部皮膚,消毒傷口表面。
1.3.3 MCT 皮下注射
在大鼠后頸背部皮下注射MCT(50 mg/kg)。
1.3.4 超聲心動圖檢查
將大鼠吸入異氟烷麻醉,仰臥于測量臺上,暴露胸部皮膚并涂抹耦合劑,使用小動物超聲裝置(Vevo 2100 成像系統)檢測主動脈短軸切面上右心室流出道寬度,在多普勒模式下的主動脈短軸圖像上測量肺動脈血流量,在四腔切面上觀察三間瓣環收縮期位移,舒張期右心室游離壁厚度和管腔直徑是在胸骨旁右心短軸切面上測量的。
1.3.5 左右心導管檢查
當大鼠吸入異氟烷麻醉后,在胸骨上方1 cm 處切開皮膚,暴露頸外靜脈。 剝離并切斷頸外靜脈,結扎遠端,近端打松結,拉緊近端結扎線以防止出血。 用針刺破頸外靜脈,將導管插入血管,將近心端結扎線扎緊以固定導管。 導管緩慢推進,導管穿過右心進入肺動脈。 用波形驗證導管位置,并記錄右心室和肺動脈壓力。 取3 個穩定波形,每個波形由10 個心動周期組成,記錄平均肺動脈壓和右心室收縮壓。 保存3 組數據的平均值作為大鼠的壓力值,并采用相同的方法測量左心。
1.3.6 病理檢查
取出完整的大鼠左葉肺組織,在室溫下用4%多聚甲醛固定2 周,然后脫水并包埋在石蠟中。 HE和EVG 染色后計算肺小動脈(<50 μm 和50 ~100 μm)中膜厚度(肌層厚度/血管外徑)的百分比。 每組至少計數5 只大鼠,每只大鼠至少有15 只血管。
1.4 統計學方法
采用GraphPad Prism 8.0 軟件進行分析,連續變量表示為平均數±標準差(±s)。 多組間均值比較采用單因素方差分析,兩組間均值比較采用獨立樣本t檢驗兩組比較,P<0.05 認為差異有統計學意義。
2 結果
2.1 手術+MCT 組大鼠的左心室重構優于單純MCT 組大鼠
與對照組相比,單純MCT 組和手術+MCT 組的舒張期右室前壁厚度(right ventricular wal,RVAW;d) 和 舒 張 期 右 室 腔 徑(right ventricular internal diameter,RVID;d)顯著增加(表1,P<0.01);三尖瓣環收縮期位移(tricuspid annular plane systolic excursion,TAPSE)和肺動脈血流加速時間/肺動脈射血時間(acceleration time of pulmonary blood flow/pulmonary ejection time,PAT/PET)均降低,提示兩組大鼠均出現右心重構和右心功能障礙(表1,P<0.01)。 單純MCT 組與手術+MCT 組兩組之間在右心重構指標上無明顯差異。 單純MCT 組大鼠的左心受擴張的右心室壓迫,舒張期左室腔徑(left ventricular internal diame, LVID;d)減小,左心射血分數(ejection fraction, EF)升高,顯著高于對照組(圖1,P<0.05)。 與單純MCT 組相反,手術+MCT組大鼠雖然右心室也發生重構,但是LVID;d 未降低,EF 值未升高,總體上更接近正常對照組,提示左向右分流手術部分緩解了MCT 引起的左心重構。

注:A:對照組(n =5);B:單純MCT 組(n =8);C:手術+MCT 組(n =8);D:舒張期左室腔徑統計圖;E:左心射血分數統計圖。 與對照組相比, *P<0.05, **P<0.01。圖1 實驗終點大鼠胸骨旁右心短軸切面M 模式檢測圖及結果統計圖Note.A, Control group(n =5).B, Simple MCT group (n =8).C, Operation+MCT group (n =8).D, Statistical diagram of left ventricular cavity diameter in diastole.E, Statistical diagram of left ventricular ejection fraction.Compared with control group, *P<0.05, **P<0.01.Figure 1 M-mode detection diagram and result statistics of parasternal right heart short-axis section in rats at the end of the experiment

表1 實驗終點三組大鼠超聲結果Table 1 Ultrasonic results of rats in three groups at the end of the experiment
2.2 手術+MCT 組大鼠的右心室功能處于代償期
與對照組相比,其余兩組的平均肺動脈壓(mean pulmonary artery pressure,mPAP)和右室收縮壓(right ventricular systolic pressure,RVSP)均升高(表2,P<0.01),提示兩組大鼠均發生肺動脈高壓。與單純MCT 組相比,手術+MCT 組的mPAP 和RVSP 稍低,左室收縮壓(left ventricular systolic pressure,LVSP) 顯 著 升 高(71.2 vs 105.1,P<0.05)(表2,P<0.01),在右心功能方面,單純MCT 大鼠的右心等容收縮期心室內壓上升最大速率(maximal ventricular pressure rising rate,dp/dt Max) 和等容舒張期心室內壓下降最大速率(maximal rate of decrease of ventricular pressure,dp/dt Min)均顯著高于對照組,提示肺動脈壓力升高使該組大鼠右心室處于功能代償期。 如圖2所示,MCT+分流組大鼠右心代償雖然高于對照組,但顯著低于單純MCT 組,提示該組大鼠右心后負荷和代償反應明顯低于單純MCT 組(P<0.05)。 這與MCT+分流組大鼠肺血管壓力稍低于單純MCT 組相一致。
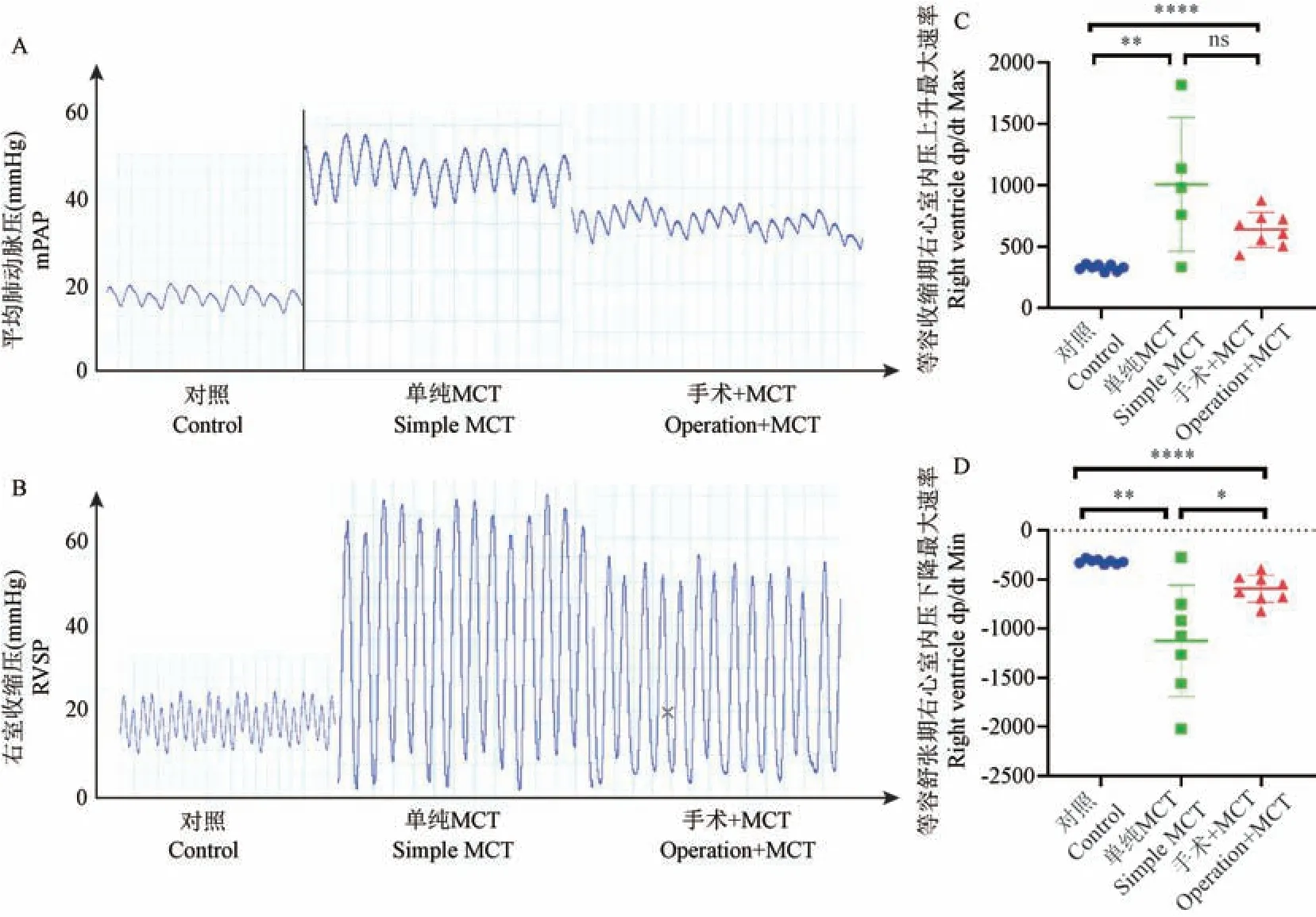
注:A:各組大鼠平均肺動脈壓力波形圖(n=8);B:各組大鼠右室收縮壓波形圖(n=8);C:右心等容收縮期心室內壓力上升最大速率(dp/dt Max)統計圖;D:右心等容舒張期心室內壓下降最大速率(dp/dt Min)統計圖。 與對照組相比, *P<0.05, **P<0.01, ****P<0.0001。圖2 各組大鼠右心導管測壓波形圖Note.A, Waveform of mean pulmonary artery pressure of rats in three groups (n=8).B, Right ventricular systolic pressure waveform of rats in three groups (n=8).C, Statistical diagram of the maximum rate of ventricular pressure rise (dp/dt Max) during isovolumic contraction of the right heart.D,Maximum rate of decrease of ventricular internal pressure (dp/dt Min) of right heart during isovolumic relaxation.Compared with control group, *P<0.05, **P<0.01, ****P<0.0001.Figure 2 Waveform of right ventricular catheter pressure measurement of rats in each group
2.3 MCT 注射誘導嚴重肺血管重構
在明確右室重構和肺動脈壓力變化的前提下,對三組大鼠肺組織病理學染色,分析肺血管病變程度(圖3)。將肺小動脈分為直徑<50μm和直徑50 ~100 μm 兩組,分別統計中膜厚度百分比。 與對照組相比,單純MCT 組和手術+MCT 組肺小動脈中膜增厚,肺血管明顯重構(表3,P<0.001)。 單純MCT 組和手術+MCT 組兩組之間肺小動脈重構程度沒有明顯差異(圖3G、3H,P<0.05),提示左向右分流不影響肺血管重構,主要影響心臟重構,進而影響預后。
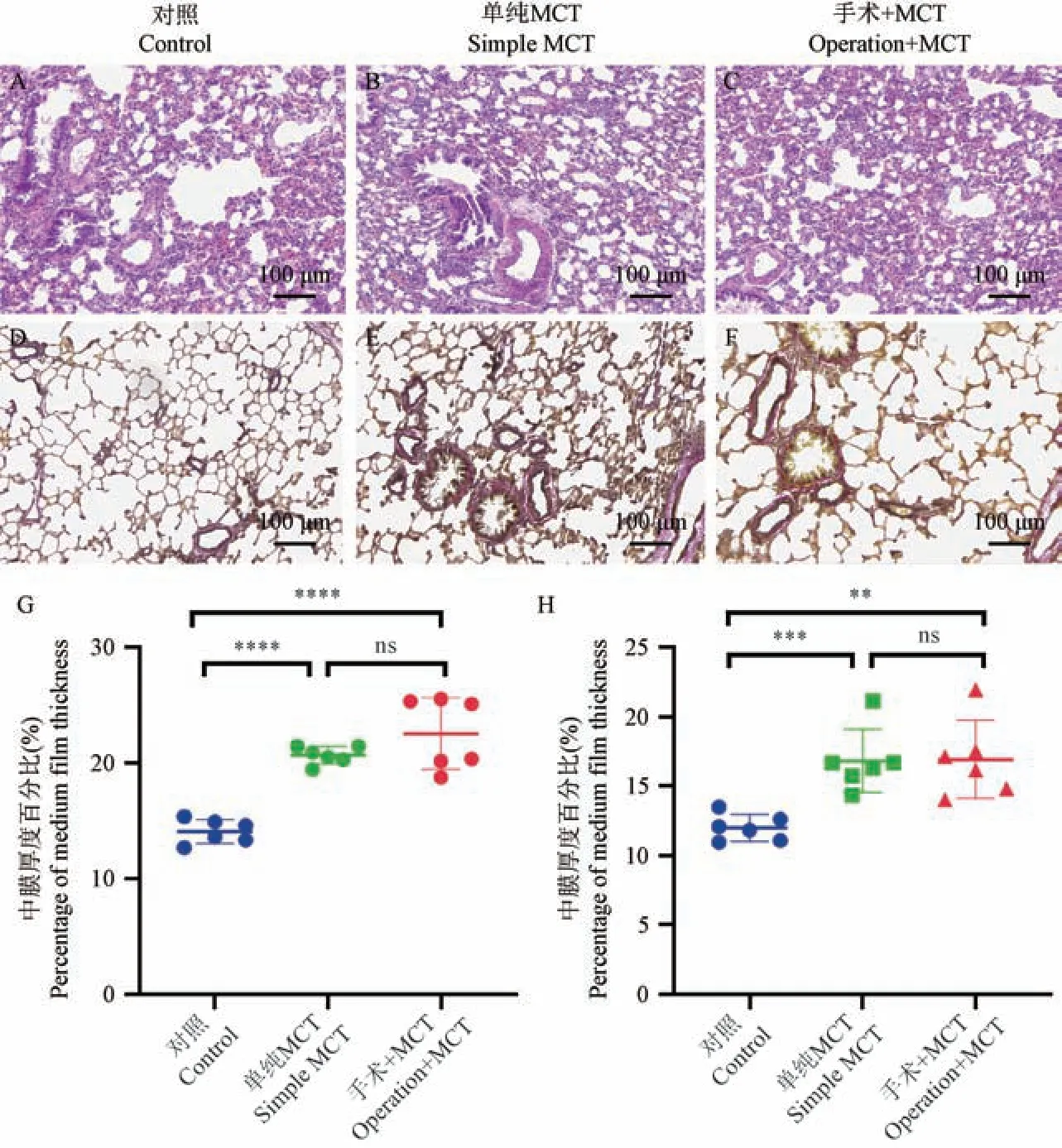
注:A~C:對照組、單純MCT 組、手術+MCT 組大鼠肺小動脈HE 染色圖;D~F:對照組、單純MCT 組、手術+MCT 組大鼠肺小動脈EVG 染色圖;G:直徑50 μm 以下血管中膜厚度百分比統計圖(n =8);H:直徑50~100 μm 血管中膜厚度百分比統計圖(n=8)。 與對照組相比, **P<0.01, ***P<0.001, ****P<0.0001。圖3 各組大鼠肺組織病理染色及統計圖Note.A~C, HE staining of pulmonary arterioles of rats in control group, simple MCT group and operation+MCT group.D~F, EVG staining of pulmonary arterioles in rats of control group, simple MCT group and operation +MCT group.G, Statistical chart of percentage of vascular media thickness below 50 μm (n =8).H, Statistical chart of the percentage of vascular media thickness 50~100 μm (n =8).Compared with control group, **P<0.01, ***P<0.001, ****P<0.0001.Figure 3 Pathological staining and statistical diagram of lung tissue of rats in each group

表3 實驗終點三組大鼠肺小動脈中膜厚度百分比結果Table 3 Percentage results of pulmonary arteriolar media thickness of rats in three groups at the end of the experiment
3 討論
本研究中,單純MCT 組和手術+MCT 組大鼠術后3 周均出現肺動脈高壓和右心室重構,且兩組大鼠之間無明顯差異。 但對更多表型數據進行分析后,發現手術+MCT 組大鼠的LVID;d、EF、右心dp/dt Max 和dp/dt Min 均明顯優于單純MCT 組,提示CHD-PAH 與IPAH 在心臟重構方面有很大的不同。
注射MCT 是制造肺動脈高壓動物模型的經典方法,單次皮下注射劑量范圍為40 ~80 mg/kg 體重,最常用的的劑量為60 mg/kg 體重[11-12]。 本研究中,我們將MCT 的注射量從常規的60 mg/kg 體重降低到50 mg/kg 體重,更好地展示了左向右分流在CHD-PAH 中所起的作用。 與腹主動脈-腔靜脈分流術模型相比[13-14],本研究采用的頸部分流更靠近大鼠心臟,所產生的分流也更加強烈,更加符合患者的臨床特征。 本研究所模擬的CHD-PAH 在肺動脈壓力、右室重構、肺血管病理重構等多方面與IPAH 大鼠沒有明顯差別,但CHD-PAH 大鼠的左室功能更好,右室因肺動脈壓力升高引起的代償性反應性更低。 這些發現與臨床研究相一致。 2013 年一項針對不同類型肺動脈高壓患者臨床特征的研究表明,CHD-PAH 患者肺動脈壓力和肺血管阻力最高,但患者肺動脈高壓功能分級(WHO-FC)和運動耐量較好,提示CHD-PAH 患者心功能與肺動脈壓力和肺血管阻力并不一致[15]。 關于中國肺動脈高壓特征的多中心人群隊列研究結果顯示,與IPAH患者相比CHD-PAH 組患者更容易延誤診斷導致肺動脈壓力更高,但心臟的性能更好,生存率明顯優于其他病因組[16-17]。
真實世界中,CHD-PAH 與IPAH 患者病程很長。 本次實驗時間較短,僅觀察了造模后3 周的表型變化,并且未設計多個實驗終點對各組大鼠進行超聲心動圖、左右心導管和肺組織病理學檢測,觀察左心代償作用產生的時間點。 后續我們將做更多研究,明確這兩個模型在長期預后和各個時間點心肺功能的改變。
肺動脈高壓患者的病灶部位在肺血管,但預后主要取決于心臟整體功能和代償能力。 本研究比較了IPAH 和CHD-PAH 兩種不同病理情況大鼠模型心臟結構、肺動脈壓力和肺小動脈病理變化,發現先心病合并肺動脈高壓與特發性肺動脈高壓的心臟重構有著很大不同,在肺血管重構相似的情況下,左向右分流的先心病顯著改變了心臟整體對肺動脈壓力升高的代償反應。 我們的初步實驗結果為后續研究這兩種不同肺動脈高壓亞型的病理機制打下基礎。

