肝硬化發生骨量丟失的臨床特征及其與肌少癥的相關性
金 秋, 楊 婧, 馬紅琳, 孫正豪, 劉清清, 胡紹山, 李蘋菊
昆明醫科大學第二附屬醫院消化內科, 昆明 650000
骨質疏松癥(osteoporosis,OP)是一種全球性的影響健康的隱匿性疾病,由于骨礦物質和骨量減少、骨小梁與皮質骨微觀結構的改變導致骨脆性增加,骨折風險隨之上升。骨量減少是指介于正常骨量和OP 之間的狀態,通常認為骨量減少是OP 的前階段,若不能早期發現和干預則易逐步發展為OP,骨量丟失包括OP和骨量減少。肝硬化人群中OP的發生率為20%~43%[1],骨量減少發生率為50.3%[2],顯著高于普通人群,肝硬化本身和低骨密度(bone mineral density,BMD)相關。目前,肝硬化患者發生骨量丟失的危險因素尚未完全明確,研究認為肌肉-骨骼-脂肪三者之間相互影響,關于合并肌少癥對骨量丟失影響的相關研究主要集中于原發性骨質疏松、2 型糖尿病和風濕免疫系統疾病的患者中,針對肝硬化患者的研究甚少,且當前尚無肝硬化人體成分分析和骨密度相關性的報道。本研究旨在探討肝硬化患者發生骨量丟失的影響因素,探討人體成分分析和骨密度的相關性,為防治肝硬化患者骨量丟失提供依據。
1 資料與方法
1.1 研究對象 選取2022年4月—2022年12月于本院住院治療并確診的肝硬化患者為研究對象。納入標準:(1)肝硬化診斷符合2019年《肝硬化診治指南》[3];(2)病例資料齊全者。排除標準:(1)年齡<18歲、妊娠、哺乳期患者;(2)伴有惡性腫瘤、血液系統疾病、腎衰竭、心臟衰竭患者;(3)長期使用雙膦酸鹽、鈣片、維生素D 和性激素患者;(4)甲狀腺功能亢進、甲狀腺功能減退病史患者;(5)癱瘓、截肢者;(6)風濕免疫系統疾病患者;(7)肝硬化病因2種及以上者;(8)具有心臟起搏器者;(9)未絕經女性。
1.2 資料收集 收集患者住院期間的一般資料[包括年齡、性別、BMI、握力、肝硬化病因、Child-Pugh 分級、糖皮質激素使用史、富馬酸替諾福韋二吡呋酯(TDF)服用史、吸煙史、飲酒史、高血壓史、糖尿病史],實驗室指標[包括Alb、ALT、AST、ALP、GGT、膽堿酯酶、TBil、TC、TG、鈣、磷、PT、活化部分凝血活酶時間(APTT)、INR、25 羥基維生素D、Ⅰ型膠原羧基末端肽交聯(β-C-terminal telopeptide of type 1 collagen,β-CTX)、骨 鈣 素N 端 中 分 子 片 段(N-terminal mid-fragment of osteocalcin,N-MID)、甲狀旁腺激素(parathyroid hormone,PTH)、降鈣素(calcitonin,CT)]、影像學資料[包括雙能X 線吸收骨密度檢測(dual energy X-ray absorptiometry,DXA)、腹部CT]和人體成分分析。
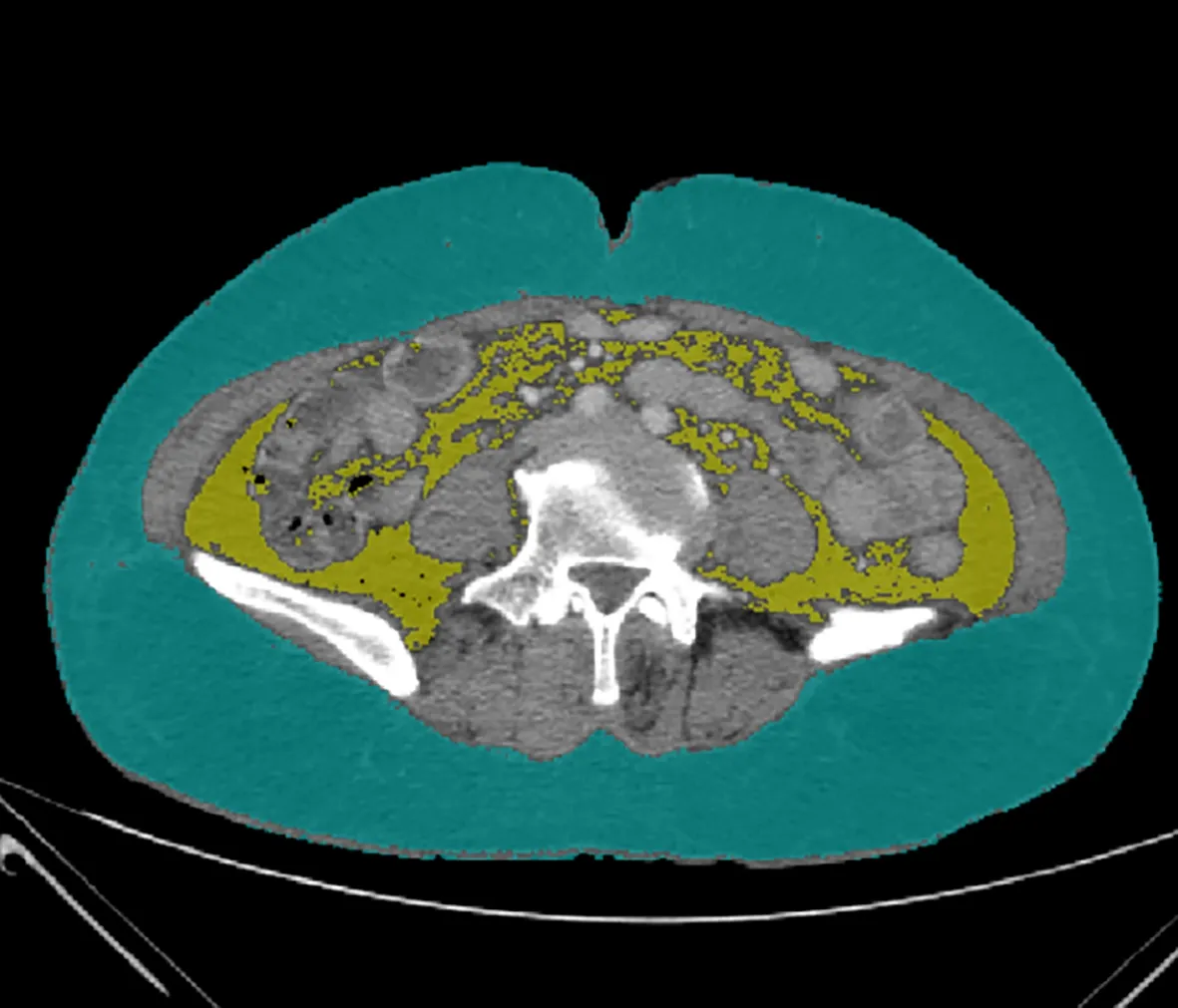
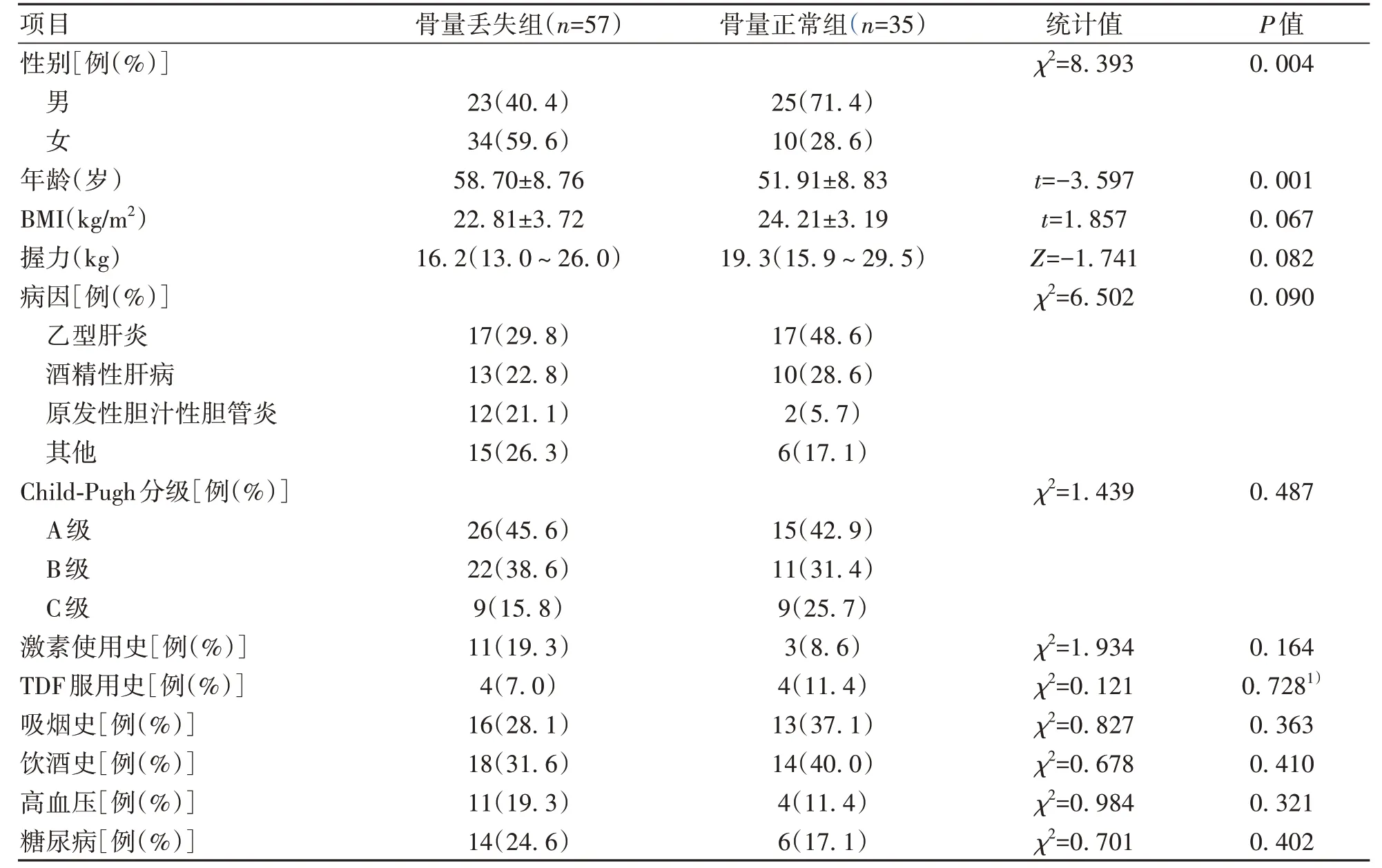
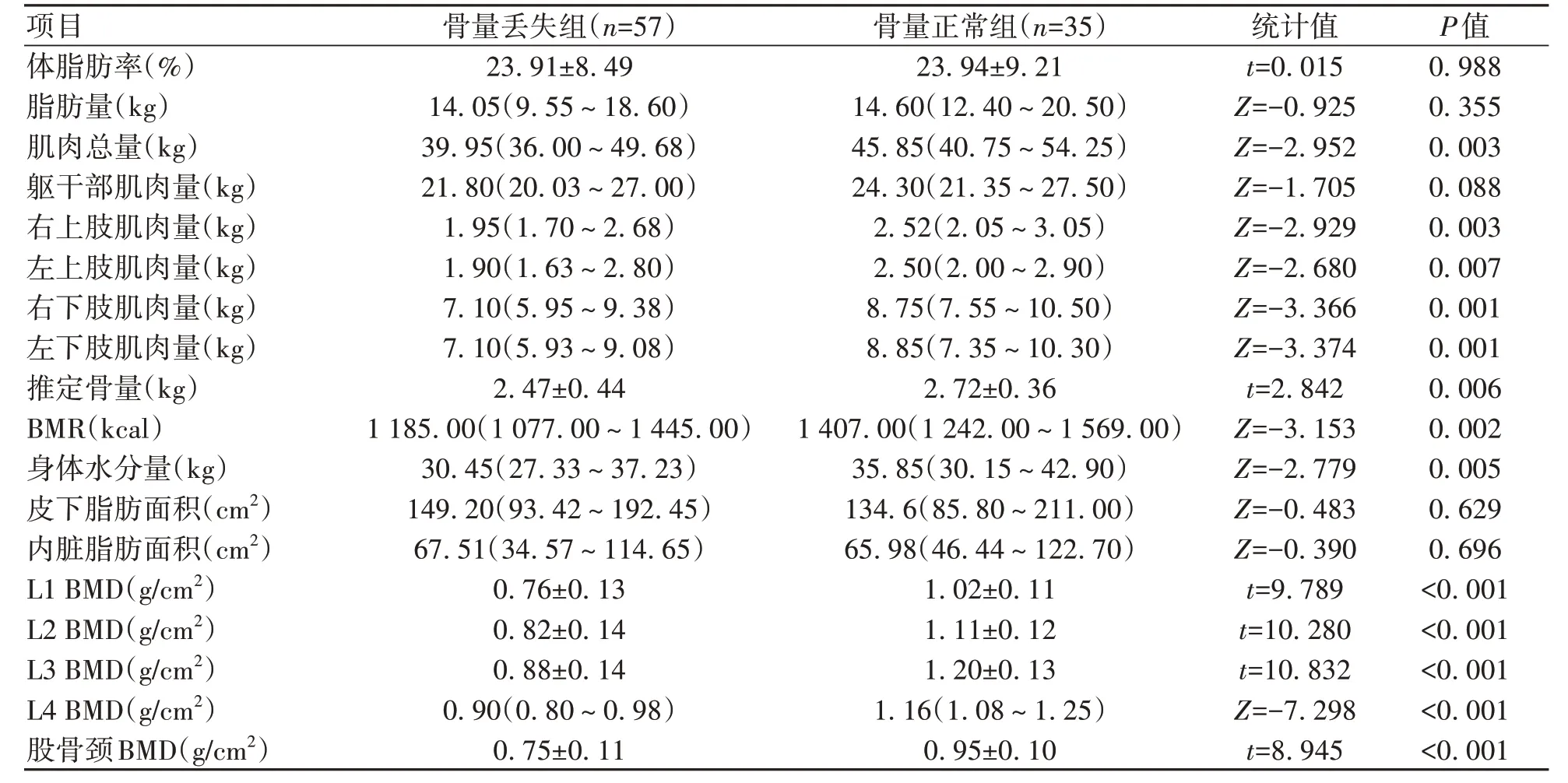
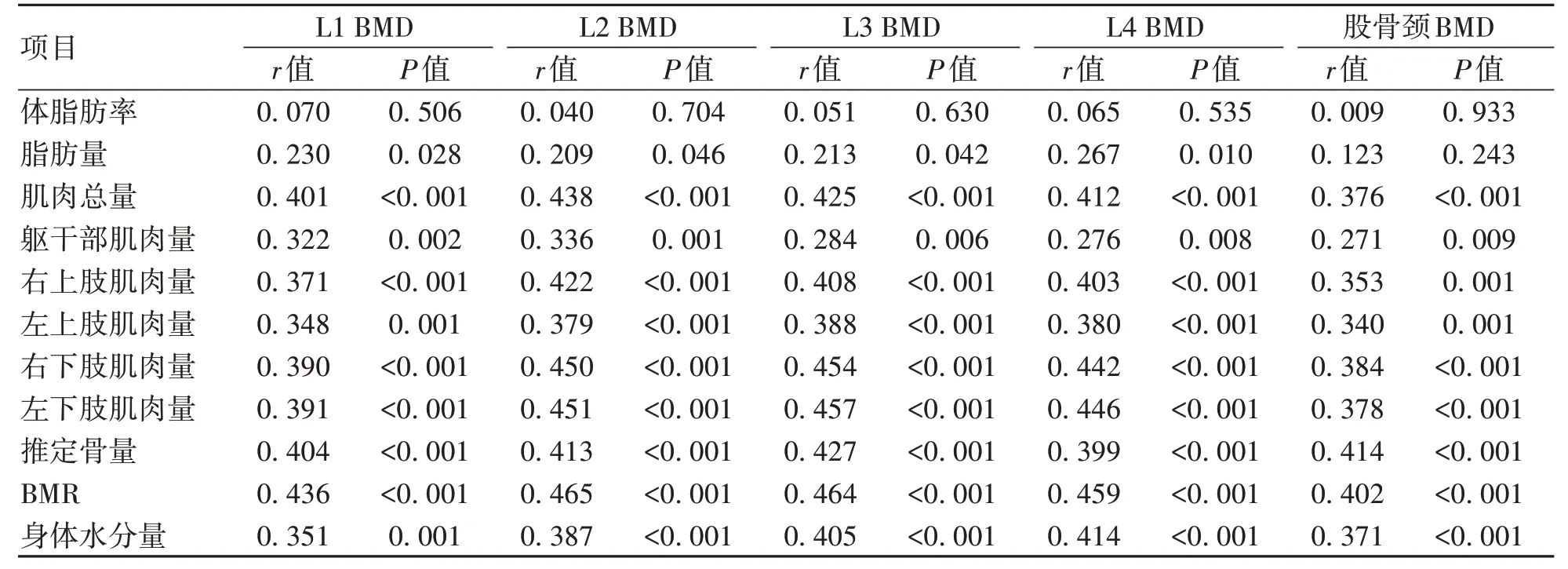
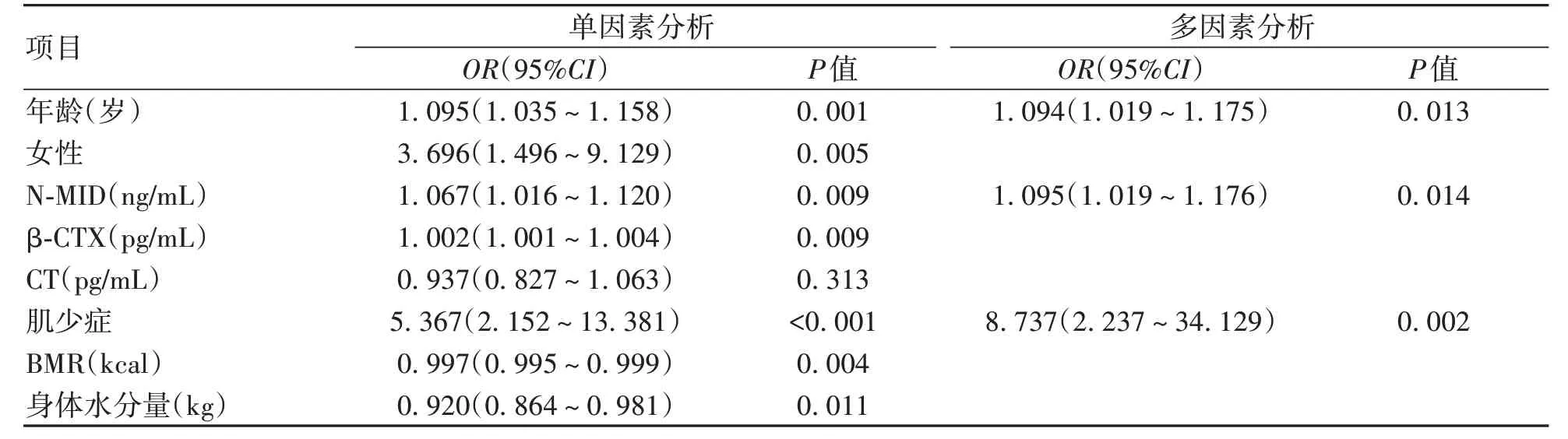
1.3 骨密度檢測 由固定專業醫生使用GE Health care13.31 的雙能X 射線骨密度儀進行檢測。受試者在檢查前避免使用影響射線的藥物、移除首飾等。指導受試者擺放正確體位,將測量部位暴露在X 線能夠照射范圍內。測定L1~L4 和股骨頸BMD(g/cm2),記錄BMD、T-值和Z-值,根據我國《原發性骨質疏松癥診療指南(2017)》[4],結合T-值、Z-值和脆性骨折史,對于≥50 歲的男性以及絕經后女性,T-值≥-1.0 診斷骨量正常,-2.5 1.4 L3-骨骼肌指數(SMI)測量 所有肝硬化患者均進行腹部CT 掃描,由同一名醫生截取L3 水平橫截面的圖像,使用sliceOmatic 5.0 Rev-9 Alberta Protocol 軟件進行圖像處理,手動勾畫L3 橫截面CT 值在-29~150 的骨骼肌區域,由軟件自動計算該區域面積即得L3-骨骼肌面積(圖1),L3-SMI=L3-骨骼肌面積(cm2)/身高2(m2)。肝硬化患者肌少癥的診斷:根據2019 年北美專家意見聲明[5],推薦診斷肝硬化肌少癥的L3-SMI臨界值為男<50 cm2/m2,女<39 cm2/m2。 圖1 L3-骨骼肌面積Figure 1 L3-skeletal muscle area 1.5 腹部脂肪面積測量 對肝硬化患者進行腹部CT 掃描,由同一名醫生截取臍水平的橫截面圖像,使用sliceOmatic 5.0 Rev-9 Alberta Protocol 軟件分別手動勾畫出CT 值在-190~-30的皮下脂肪區域和CT 值在-150~-50 的內臟脂肪區域,通過軟件自動計算皮下脂肪面積以及內臟脂肪面積(圖2)。 圖2 腹部脂肪面積Figure 2 Abdominal fat area 1.6 人體成分分析 由經驗豐富的臨床營養科醫生使用百利達公司(TANITA Corporation)生產的型號MC-180身體成分分析儀,通過生物電阻抗法分析測量人體成分。具體方法為:測試開始前需明確患者體內未放置金屬避免對結果產生干擾,交代患者排空尿液、脫去金屬飾品、厚重衣物以及鞋襪,于系統上輸入患者的基本信息(包括姓名、性別和身高等),在受試者安靜狀態下,受試者將雙足分別站立在不銹鋼電極材料上,根據系統提示,雙手分別握住兩個測量把手,雙上肢自然下垂,保持身體站立,待測量完畢后獲得人體成分相關數據,記錄體脂肪率、脂肪量、肌肉總量、軀干部肌肉量、右上肢肌肉量、左上肢肌肉量、右下肢(含臀部)肌肉量、左下肢(含臀部)肌肉量、推定骨量、基礎代謝率(basal metabolic rate,BMR)和身體水分量。 1.7 統計學方法 應用SPSS 25.0統計學軟件進行數據分析。計量資料服從正態分布的以xˉ±s表示,兩組間比較采用成組t檢驗;計量資料服從偏態分布的以M(P25~P75)表示,兩組間比較采用Mann-WhitneyU檢驗;計數資料兩組間比較采用χ2檢驗、連續性修正χ2檢驗。Pearson 相關性分析用于服從雙變量正態分布的計量資料,Spearman 相關性分析用于不服從雙變量正態分布的計量資料。二元Logistic 回歸分析骨量丟失的危險因素。P<0.05為差異有統計學意義。 2.1 一般資料 共納入肝硬化患者92例,其中,骨量丟失組57例,男23例,女34例,平均(58.70±8.76)歲;骨量正常組35例,男25例,女10例,平均(51.91±8.83)歲。骨量丟失組患者的年齡、女性占比明顯大于骨量正常組(P值均<0.05)。兩組間BMI、握力、病因、Child-Pugh 分級、糖皮質激素使用史、TDF 服用史、吸煙史、飲酒史、高血壓史、糖尿病史差異無統計學意義(P值均>0.05)(表1)。 表1 兩組間一般資料比較Table 1 Comparison of general data between the two groups 2.2 骨量丟失組和骨量正常組實驗室指標比較 與骨量正常組相比,骨量丟失組的N-MID、β-CTX 水平較高(P值均<0.05),CT水平較低(P<0.05),其余指標差異無統計學意義(P>0.05)(表2)。 表2 兩組間實驗室資料比較Table 2 Comparison of laboratory data between the two groups 2.3 骨量丟失組和骨量正常組發生肌少癥的情況對比 骨量丟失組的L3-SMI 低于骨量正常組(P<0.05),合并肌少癥的比例高于骨量正常組(P<0.05)(表3)。 2.4 骨量丟失組和骨量正常組人體成分分析、腹部脂肪面積和骨密度對比 骨量丟失組的肌肉總量、四肢肌肉量、推定骨量、BMR、身體水分量、L1~L4 BMD、股骨頸BMD均低于骨量正常組(P值均<0.05),兩組間體脂肪率、脂肪量、軀干部肌肉量、皮下脂肪面積以及內臟脂肪面積差異均無統計學意義(P值均>0.05)(表4)。 表4 兩組間人體成分分析、腹部脂肪面積和骨密度比較Table 4 Comparison of body composition analysis, abdominal fat area and bone mineral density between the two groups 2.5 人體成分分析和骨密度的相關性分析 相關性分析顯示,肌肉總量、軀干部肌肉量、四肢肌肉量、推定骨量、BMR、身體水分量均與L1~L4 BMD和股骨頸BMD 呈正相關(P值均<0.05),脂肪量與L1~L4 BMD呈正相關(P值均<0.05)。未發現體脂肪率和BMD 的相關性(P值均>0.05)(表5)。 表5 人體成分和骨密度的相關性分析Table 5 Correlation analysis between body composition and bone mineral density 2.6 肝硬化骨量丟失的危險因素 根據肝硬化患者是否發生骨量丟失為因變量,以年齡、女性、N-MID、β-CTX、CT、肌少癥、身體水分量和BMR 作為自變量納入單因素Logistic 回歸分析,因肌肉量和肌少癥為同一類指標,故未納入單因素Logistic 回歸分析。進一步將單因素Logistic 回歸分析中有意義的指標納入多因素Logistic 回歸分析,結果顯示年齡、N-MID 和肌少癥是肝硬化患者發生骨量丟失的獨立危險因素(P值<0.05)(表6)。 表6 肝硬化骨量丟失危險因素的Logistic回歸分析Table 6 Logistic regression analysis of risk factors for bone mass loss in cirrhosis 骨量丟失呈慢性起病,常因發生骨質疏松性骨折和慢性疼痛才引起患者重視。Zheng 等[6]研究證明,肝硬化患者的腰椎和股骨頸骨密度[分別為(1.02±0.16)g/cm2和(0.88±0.14)g/cm2]均明顯低于健康同齡人[分別為(1.06±0.16)g/cm2和(0.93±0.11)g/cm2],且肝硬化患者低骨密度發生率較高[7]。增齡是公認導致低骨密度的危險因素之一,本研究結果顯示,年齡是肝硬化患者發生骨量丟失的獨立危險因素,提示隨著年齡增長應注意防范骨量丟失的發生。本研究結果顯示,女性更容易發生骨量丟失。 肝硬化營養不良發生率為50%~90%[8],這將導致患者的人體成分發生改變,具體表現為脂肪和肌肉組織含量隨著肝硬化嚴重程度增加而降低[9]。肌肉對骨骼的機械附著有助于保護骨骼,肌少癥和增齡密切相關,一項Meta 分析[10]表明我國社區老年男性和女性肌少癥發生率分別為12.9%和11.2%。肝硬化患者肌少癥發生率高于普通人群,為40%~70%[11],肝硬化發生肌少癥存在其特殊的發病機制,涉及的機制包括促炎因子增加、胰島素樣生長因子1 水平降低、門體分流和氨基酸代謝改變導致血氨升高等[12]。肌細胞分泌的肌肉生長抑制素和鳶尾素等均對骨密度產生影響[13],肌肉與骨骼緊密聯系。本研究發現,肌肉總量、軀干部及四肢肌肉量均和L1~L4 BMD、股骨頸BMD 呈正相關,證明了高肌肉質量對肝硬化患者的骨密度具有積極的作用,進一步研究表明肌少癥是肝硬化發生骨量丟失的獨立危險因素(OR=8.737,95%CI:2.237~34.129),和張靜怡等[14]對慢性乙型肝炎患者的研究結論一致。 脂肪組織對骨骼的影響尚存爭議,皮下脂肪可分泌芳香化酶促進成骨,內臟脂肪則能上調炎癥因子的表達促進破骨細胞分化。瘦素和脂聯素作為脂肪因子均具促骨形成和骨吸收的雙重作用,但具體以哪一種作用為主尚無定論[15-16]。本研究發現皮下脂肪面積和內臟脂肪面積的組間差異不具有統計學意義。Fan 等[17]對絕經后女性的研究發現總脂肪質量和骨密度呈正相關,本研究同樣證明脂肪量和骨密度呈正相關,但相關性較弱,表明脂肪組織可能具有保護骨密度的作用,未來仍需進一步研究。 BMR是人體維持心跳、呼吸等基本生命所需最低的能量消耗。Hsu等[18]研究發現,BMR和中老年女性股骨頸骨密度呈正相關。和上述研究結果相似,本研究中骨量丟失組BMR 顯著低于骨量正常組,BMR 和L1~L4 BMD 以及股骨頸BMD 呈正相關,表明低BMR可能是肝硬化患者骨量丟失的預測因子。肌少癥和衰弱的存在與BMR 降低相關[19],本研究骨量丟失患者中合并肌少癥的人數較多,患者因衰弱以及長期久坐導致活動減少,以上因素可能導致骨量丟失組的BMR顯著降低。 人體水分約占體質量的40%~60%。針對健康中年男性體成分的研究[20]表明,身體水分量隨著增齡而逐漸降低,骨量減少組的身體水分量低于骨量正常組。本研究結果同樣顯示,肝硬化骨量丟失組的身體水分量明顯降低,相關性分析顯示身體水分量和骨密度呈正相關,對于身體水分量減少的患者需警惕骨量丟失的發生。 N-MID 和β-CTX 分別作為骨形成和吸收的指標,不僅能夠反映OP患者的療效,還能夠預測骨質疏松性骨折的發生[21-23]。本研究結果顯示,骨量丟失組N-MID和β-CTX 均高于骨量正常組,且N-MID 是骨量丟失的獨立危險因素。本研究證明骨量丟失患者的骨形成和骨吸收均增加,提示肝硬化骨量丟失和高骨轉換密切相關,可能的原因是骨吸收大于骨形成而逐步導致骨量丟失,和江雅平等的研究結果一致[24]。本研究中,骨量丟失組降鈣素低于骨量正常組,值得注意是,25羥基維生素D 的組間差異雖無統計學意義,但兩組均處于缺乏狀態。骨密度僅能反應骨骼強度,而測定骨代謝標志物有助于了解當前骨代謝變化情況。 長期使用糖皮質激素可致低骨密度,本研究未發現糖皮質激素使用史是骨量丟失的獨立危險因素,可能系本研究中自身免疫性肝炎患者和有糖皮質激素使用史的人數較少,部分患者既往使用激素時長較短尚未對骨骼帶來不利影響。 綜上,高齡、女性與合并肌少癥者更易發生骨量丟失,N-MID 和β-CTX 水平升高,CT、肌肉量、推定骨量、BMR和身體水分量降低者同樣易骨量丟失。肌少癥、年齡和N-MID 是肝硬化骨量丟失的獨立危險因素。人體成分和骨密度具有相關性,通過生物電阻抗法測定人體成分的變化有助于評估患者骨骼狀態,優化人體成分利于保護骨骼健康。本研究存在一定局限性,這是一項單中心的橫斷面研究,仍存在樣本量較小的問題,未能將患者按照性別分組單獨分析男性和女性發生骨量丟失的臨床特征。由于Child-Pugh C級患者病情重,考慮患者外出檢查的安全性,納入該類患者的人數較少,未來仍需多中心、大樣本的研究給予驗證。 倫理學聲明: 本研究方案于2022年4月8日經由昆明醫科大學第二附屬醫院倫理委員會審批,批號:審-PJ-科-2022-66,所有入組對象均已簽署知情同意書。 利益沖突聲明: 本文不存在任何利益沖突。 作者貢獻聲明:金秋負責課題設計,數據收集,文章構思并撰寫論文;馬紅琳、孫正豪、李蘋菊、胡紹山、劉清清參與數據收集,查閱分析文獻;楊婧負責指導論文撰寫與定稿。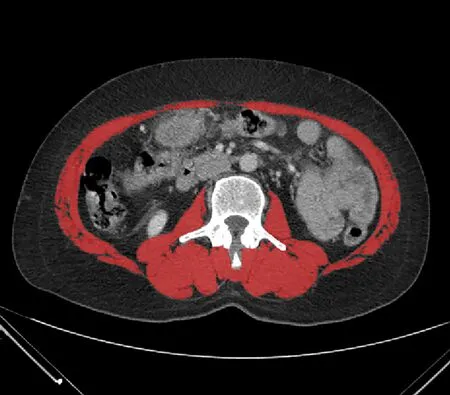
2 結果

3 討論

