PBL和POE融合下的元素化合物教學(xué)
隆路詩 宋來強
摘要:元素化合物是化學(xué)知識的核心部分,同樣也是落實化學(xué)學(xué)科核心素養(yǎng)的重要知識載體。以硝酸的重要性質(zhì)———與金屬的反應(yīng)為例,呈現(xiàn)以PBL方法為驅(qū)動、POE策略為學(xué)習(xí)主線的融合教學(xué),深化學(xué)生對元素化合物性質(zhì)及相關(guān)理論的思考,培養(yǎng)學(xué)生科學(xué)探究精神和證據(jù)意識,為高中元素化合物教學(xué)提供借鑒。
關(guān)鍵詞:高中化學(xué);元素化合物;PBL方法;POE策略
《普通高中化學(xué)課程標(biāo)準(zhǔn)(2017年版2020年修訂)》中倡導(dǎo)“素養(yǎng)為本”的有效課堂教學(xué)模式和策略,提倡設(shè)計和開展多種形式的實驗探究活動,有目的、有計劃地引導(dǎo)學(xué)生運用化學(xué)科學(xué)思維方式和方法學(xué)習(xí)化學(xué)知識[1]。元素化合物作為中學(xué)化學(xué)的核心內(nèi)容,其教學(xué)著重通過化學(xué)實驗,從宏微結(jié)合、變化守恒的視角,運用證據(jù)推理與模型認(rèn)知的思維方式,使學(xué)生獲得結(jié)構(gòu)化的核心元素化合物知識,提升學(xué)生的創(chuàng)新和實踐能力[2]。因此,在元素及其化合物教學(xué)設(shè)計和實施中,科學(xué)制定具體可行、基于化學(xué)學(xué)科核心素養(yǎng)發(fā)展的教學(xué)策略尤為重要。
一、PBL教學(xué)方法和POE教學(xué)策略的意義
PBL教學(xué)方法(Problem-Based-Learning)是基于問題導(dǎo)向的教學(xué)方法,旨在創(chuàng)設(shè)的情境中提出復(fù)雜、有意義、真實的問題,進(jìn)而尋找證據(jù)進(jìn)行解釋,充分發(fā)揮教師主導(dǎo)作用,體現(xiàn)學(xué)生主體性,培養(yǎng)學(xué)生發(fā)現(xiàn)、解決問題及合作探究的能力[3]。POE教學(xué)策略包括三個環(huán)節(jié):Predict(預(yù)測)、Observe(觀察)、Explain(解釋),旨在使學(xué)生學(xué)會搜集各種證據(jù),對物質(zhì)的性質(zhì)及其變化做出假設(shè)且能從問題和假設(shè)出發(fā),設(shè)計相應(yīng)的實驗方案,對實驗信息進(jìn)行加工并獲得結(jié)論,從而強化學(xué)生的證據(jù)推理能力,培養(yǎng)學(xué)生的科學(xué)探究精神[4]。
PBL教學(xué)方法和POE教學(xué)策略均著重于學(xué)生學(xué)習(xí)的主體性,強調(diào)在多角度、不斷的探究過程中獲取知識,并形成對知識的深度理解,均與元素化合物教學(xué)相契合。二者相融合,以PBL方法為驅(qū)動,提出復(fù)雜、有意義、真實的問題作為學(xué)生思維的起點,充分激發(fā)學(xué)生探索新知的欲望,再以POE策略為學(xué)習(xí)主線,引導(dǎo)學(xué)生運用性質(zhì)預(yù)測———實驗觀察———解釋的科學(xué)探究方法逐步解決問題,使學(xué)生積極主動地參與探究知識的過程,形成科學(xué)的思維方式,促進(jìn)其核心素養(yǎng)的全面發(fā)展。
二、教學(xué)分析
(一)教學(xué)內(nèi)容及學(xué)情
“硝酸與金屬的反應(yīng)”一課位于人教版(2019)化學(xué)教材必修二第五章第二節(jié)“氮及其化合物”,是體現(xiàn)硝酸強氧化性的重要部分。通過本節(jié)內(nèi)容的學(xué)習(xí),學(xué)生已經(jīng)了解了有關(guān)N2、NO、NO2、NH3、銨鹽的內(nèi)容,初步建構(gòu)了氮元素在不同化合價物質(zhì)間轉(zhuǎn)化的知識體系;通過以往內(nèi)容的學(xué)習(xí),學(xué)生了解了實驗室制備氯氣的方法、硫酸的性質(zhì),知道濃度、溫度對酸的性質(zhì)有影響,已具備氧化性、還原性等知識。雖然學(xué)生初步具備了分析問題、解決問題和實驗探究的能力,但仍缺乏對證據(jù)的有效使用,很難獨自根據(jù)已有知識對實驗現(xiàn)象進(jìn)行合理的解釋,以致于課堂上的問題無法得到實際意義上的解決。因此,通過真實有效的問題,在預(yù)測、觀察、解釋各個環(huán)節(jié)中不斷引導(dǎo)學(xué)生通過已知進(jìn)行深度思考,實現(xiàn)知識的靈活運用、融會貫通十分重要。
(二)教學(xué)目標(biāo)
1.能從價態(tài)角度合理預(yù)測硝酸的強氧化性及其與銅的反應(yīng)產(chǎn)物,能聯(lián)系已知合理分析處理實驗現(xiàn)象,形成實驗結(jié)論,提升發(fā)現(xiàn)、解決問題的能力。掌握從問題和假設(shè)出發(fā)進(jìn)行實驗到形成結(jié)論的科學(xué)探究方法,樹立對物質(zhì)性質(zhì)及實驗現(xiàn)象分析推理后,證實或證偽問題的證據(jù)意識。
2.能依據(jù)氧化還原反應(yīng)的原理及實驗事實歸納硝酸的強氧化性、不同濃度的還原產(chǎn)物、與金屬的反應(yīng)模型,提升根據(jù)研究對象的本質(zhì)特征建立模型的能力。
3.能運用硝酸與金屬反應(yīng)模型預(yù)測不同濃度硝酸與鐵的反應(yīng)現(xiàn)象,揭示現(xiàn)象的本質(zhì)和規(guī)律。能從理論角度深入分析實驗異常,敢于提出自己的見解,樹立實事求是的科學(xué)精神。
三、教學(xué)過程
PBL教學(xué)方法和POE教學(xué)策略融合教學(xué)的流程以問題為主線,最終目的在于引發(fā)學(xué)生的深度思考(見圖1)。
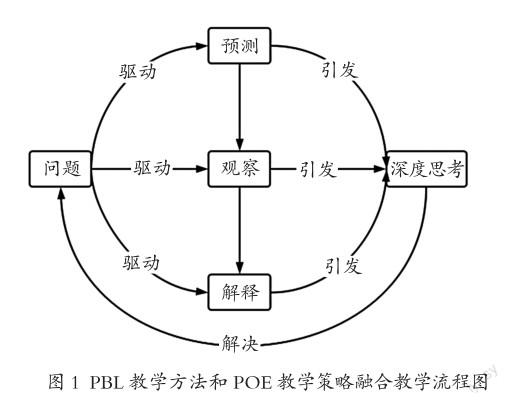
(一)問題———預(yù)測———思考———解釋
教學(xué)初始,教師利用學(xué)生原有認(rèn)知,提出問題:“活潑金屬與酸反應(yīng)制備氫氣,是H+作為氧化劑,而硝酸作為強電解質(zhì),在水溶液中可完全電離出H+,同樣都是H+,為什么硝酸中的H+沒有氧化金屬產(chǎn)生氫氣呢?”學(xué)生做出“或許有氧化性比H+強的物質(zhì)先和金屬反應(yīng)了”的假設(shè),教師繼續(xù)追問假設(shè)的根據(jù),逐漸引導(dǎo)學(xué)生認(rèn)識到HNO3中N為+5價,為N最高價,氧化性可能強于H,形成初步的解釋。
設(shè)計意圖:利用制備氫氣的離子反應(yīng)實質(zhì)與所需反應(yīng)物之間的矛盾制造認(rèn)知沖突,激發(fā)學(xué)生對硝酸性質(zhì)的探索欲望。
(二)問題———預(yù)測———觀察———解釋
化學(xué)是一門以實驗為基礎(chǔ)的科學(xué),實踐是檢驗真理的唯一途徑。為了避免H+可以氧化金屬的干擾,引導(dǎo)學(xué)生設(shè)計硝酸與H+無法氧化的金屬銅進(jìn)行反應(yīng),從而驗證解釋。實驗開始前,根據(jù)氧化還原反應(yīng)的特征,提出問題,驅(qū)動學(xué)生預(yù)測,稀硝酸與銅反應(yīng)可能會生成什么?會伴隨著什么現(xiàn)象?學(xué)生帶著自己的猜測觀看教師演示實驗,教師將銅絲下端繞成螺旋狀,插入裝有稀硝酸的試管中,無明顯現(xiàn)象。學(xué)生通過觀察,思考原因,不難得出反應(yīng)或許過慢,加熱再觀察。加熱后,學(xué)生通過實驗現(xiàn)象以及之前的預(yù)測不難得出產(chǎn)物硝酸銅和一氧化氮。進(jìn)而引導(dǎo)學(xué)生根據(jù)實驗事實,進(jìn)行理論解釋:硝酸氧化性比較強,體現(xiàn)在N元素上,能氧化H氧化不了的金屬。
設(shè)計意圖:引導(dǎo)學(xué)生從元素價態(tài)的角度分析反應(yīng)的產(chǎn)物,并根據(jù)產(chǎn)物性質(zhì)預(yù)測反應(yīng)現(xiàn)象,培養(yǎng)學(xué)生的證據(jù)意識。通過實驗預(yù)測與現(xiàn)象的不符引發(fā)學(xué)生對化學(xué)反應(yīng)及其現(xiàn)象的全面思考,培養(yǎng)學(xué)生面對意外情況的應(yīng)變能力。通過稀硝酸與銅的反應(yīng)事實,初步體會硝酸的強氧化性及體現(xiàn)氧化性的元素。
(三)遷移問題———預(yù)測———觀察———解釋
以問題“稀硝酸能與銅反應(yīng),濃硝酸能與銅反應(yīng)嗎?如果反應(yīng),相比稀硝酸,反應(yīng)現(xiàn)象會有什么不同?”為引,繼續(xù)驅(qū)動學(xué)生思考,利用知識的遷移,對濃硝酸的性質(zhì)進(jìn)行預(yù)測。學(xué)生通過觀察教師演示實驗,得出反應(yīng)后有NO2生成,不是NO,溶液變?yōu)榫G色,與預(yù)測性質(zhì)相比產(chǎn)生很大出入。教師提示學(xué)生回顧學(xué)習(xí)銅在氯氣中燃燒,最后用蒸餾水驗證氯化銅時的現(xiàn)象,點明藍(lán)色和黃色混合變?yōu)榫G色的事實。學(xué)生再通過聯(lián)系NO2和水合銅離子的顏色,得出溶液顯綠色的原因。需要注意的是,關(guān)于濃硝酸與銅反應(yīng)溶液顏色的解釋眾說紛紜,沒有形成統(tǒng)一認(rèn)識,教師從中選取易于理解的解釋用于教學(xué)即可。
設(shè)計意圖:利用學(xué)生慣性思維與實驗現(xiàn)象的不同,引發(fā)認(rèn)知沖突,突出不同濃度硝酸不僅反應(yīng)劇烈程度不同,還原產(chǎn)物也不同。通過思考遷移將原有認(rèn)知與當(dāng)前認(rèn)知建立聯(lián)系,實現(xiàn)學(xué)生認(rèn)知的意義建構(gòu),培養(yǎng)學(xué)生證據(jù)推理的思維方式。
(四)總結(jié)問題———解釋———思考
教師結(jié)合上述內(nèi)容歸納出問題,不同濃度硝酸與銅反應(yīng)有什么不同?學(xué)生解釋:稀硝酸還原產(chǎn)物是NO,濃硝酸還原產(chǎn)物是NO2,濃硝酸反應(yīng)更劇烈、更容易。教師繼續(xù)提問,引發(fā)思考,硝酸還可以和哪些金屬反應(yīng)?學(xué)生利用原有知識解決問題,并得到結(jié)論,按照金屬活動性順序表,Cu之前的金屬都可以發(fā)生反應(yīng)。
設(shè)計意圖:通過氧化還原反應(yīng)規(guī)律和不同濃度硝酸反應(yīng)事實,延伸為硝酸與金屬的反應(yīng)模型,提升學(xué)生的建模能力。
(五)遷移問題———預(yù)測———觀察———解釋———思考
教師提出:“利用已有結(jié)論,提出新的問題,那鐵和稀、濃硝酸反應(yīng),分別有什么現(xiàn)象呢?”學(xué)生按照思維慣性,預(yù)測鐵和稀硝酸反應(yīng),會產(chǎn)生無色氣體NO,在空氣中被氧化成紅棕色氣體NO2,和濃硝酸直接就會產(chǎn)生紅棕色氣體NO2,而溶液不確定,可能是淡綠色的Fe(NO3)2,也有可能是淡黃色的Fe(NO3)3。教師演示鐵與稀硝酸的反應(yīng)實驗,學(xué)生觀察并發(fā)現(xiàn)下端繞成螺旋狀的鐵絲插入到稀硝酸當(dāng)中,有無色氣體生成,并在試管上端變?yōu)榧t棕色,溶液變黃。教師提出問題,引導(dǎo)學(xué)生解釋該現(xiàn)象,這個反應(yīng)能說明硝酸的哪些性質(zhì)?學(xué)生不難答出,硝酸的氧化性強,可直接將Fe氧化為Fe3+。
問題再遷移,引導(dǎo)學(xué)生根據(jù)鐵和稀硝酸的反應(yīng),預(yù)測鐵與濃硝酸反應(yīng)會產(chǎn)生怎樣的現(xiàn)象。教師可以適時點撥,帶領(lǐng)學(xué)生回憶上一章“硫及其化合物”學(xué)習(xí)時遇到的類似情況,即銅與濃硫酸反應(yīng)可以生成SO2;換成了鐵,卻沒有現(xiàn)象,是因為鐵遇濃硫酸發(fā)生鈍化,瞬間被氧化生成一層致密的氧化物薄膜,阻止鐵與硫酸接觸。進(jìn)而提出課后思考問題:其實鐵遇濃硝酸也發(fā)生了鈍化,生成了一層氧化物保護(hù)層。那么如何讓鐵與濃硝酸持續(xù)反應(yīng)?利用鐵遇濃硝酸鈍化在生產(chǎn)生活中有什么用呢?
設(shè)計意圖:通過不同濃度硝酸與金屬的反應(yīng)模型及鐵常見的氧化態(tài)推測鐵與不同濃度硝酸的反應(yīng),鞏固學(xué)生對硝酸性質(zhì)的認(rèn)識,鍛煉學(xué)生的知識遷移能力。通過鐵與稀硝酸的反應(yīng)事實,突出硝酸氧化性強,一般將金屬氧化為高價態(tài),完善硝酸與金屬的反應(yīng)模型。通過鐵和濃硫酸發(fā)生反應(yīng)現(xiàn)象形成認(rèn)知沖突,引導(dǎo)學(xué)生在事物本身性質(zhì)和知識理論相結(jié)合的基礎(chǔ)上綜合分析并解決問題,培養(yǎng)學(xué)生證據(jù)推理意識,樹立探索求知的科學(xué)精神。
四、教學(xué)反思
教師利用“酸與金屬制備氫氣”的問題沖突牽動整節(jié)課,在探究不同濃度硝酸與銅、鐵的反應(yīng)過程中,學(xué)生利用物質(zhì)性質(zhì)及實驗事實尋求理論和實際雙方面證據(jù),形成并不斷深化對硝酸的認(rèn)識,構(gòu)建不同濃度硝酸與金屬反應(yīng)的思維模型,面對“異常”現(xiàn)象敢于提出自己的見解,體會問題發(fā)現(xiàn)———已知推測———實驗探究———形成結(jié)論的科學(xué)研究方式,達(dá)成了科學(xué)探究、證據(jù)推理、模型認(rèn)知等方面的素養(yǎng)要求。
新時代拔尖創(chuàng)新人才的培養(yǎng),需要突破當(dāng)下的應(yīng)試、競賽等常規(guī)方式,加快指向現(xiàn)實情境下問題解決的綜合性課程研發(fā),建立一套科學(xué)、具體、行之有效的培養(yǎng)模式,以培養(yǎng)出適應(yīng)新時代發(fā)展要求、德才兼?zhèn)涞囊慌咚刭|(zhì)人才[5]。在化學(xué)學(xué)科當(dāng)中,元素化合物是體現(xiàn)化學(xué)研究特點的核心內(nèi)容,其內(nèi)容呈現(xiàn)的方式方法不僅直接影響學(xué)生對知識的理解,更對學(xué)生科學(xué)研究思維的培養(yǎng)至關(guān)重要。PBL與POE融合教學(xué)以教材內(nèi)容為基礎(chǔ),在真實情境中創(chuàng)設(shè)有效、復(fù)雜的驅(qū)動問題,在激發(fā)學(xué)生學(xué)習(xí)興趣和動機的同時,引導(dǎo)學(xué)生以預(yù)測———觀察———解釋的科學(xué)學(xué)習(xí)方法,環(huán)環(huán)相扣,從而使學(xué)生在深度思考的過程中,完成對知識的理解和認(rèn)知結(jié)構(gòu)的完善,最終實現(xiàn)關(guān)鍵能力的發(fā)展和素養(yǎng)的提升。
參考文獻(xiàn):
[1] 中華人民共和國教育部.普通高中化學(xué)課程標(biāo)準(zhǔn)(2017年版2020年修訂)[M].北京:人民教育出版社,2020:2.
[2] 李靖軒.基于化學(xué)學(xué)科核心素養(yǎng)發(fā)展的元素化合物教學(xué)案例研究[J].化學(xué)教育(中英文),2022,43(16).
[3] 任瑞潔,馬娜,朱雪芳,等.PBL教學(xué)模式在化學(xué)教學(xué)中的應(yīng)用[J].中學(xué)化學(xué)教學(xué)參考,2022(6).
[4] 胡佳,王祖浩.基于POE教學(xué)策略的線上教學(xué)設(shè)計:以探究含氯消毒劑的性質(zhì)和應(yīng)用為例[J].中小學(xué)數(shù)字化教學(xué),2021(8).
[5] 蘆詠莉.全面建設(shè)社會主義現(xiàn)代化國家呼喚新時代人才[J].
中國教育學(xué)刊,2022(11).
見習(xí)編輯/張婷婷

