多囊卵巢綜合征大鼠和小鼠模型的生殖與代謝特點(diǎn)及選擇應(yīng)用
林梓欣, 曾國(guó)美, 林穎, 方潔妮, 胡芳遠(yuǎn), 李潔, 鄭汝群, 胡敏, 李娟
(1. 廣州醫(yī)科大學(xué)第一臨床學(xué)院, 廣東 廣州 510120; 2. 廣州醫(yī)科大學(xué)附屬第一醫(yī)院中醫(yī)科, 廣東 廣州 510120)
多囊卵巢綜合征(polycystic ovary syndrome,PCOS)是育齡期婦女常見的生殖內(nèi)分泌疾病,以稀發(fā)排卵或持續(xù)性無排卵、高雄激素血癥、卵巢多囊樣改變、不孕及胰島素抵抗等為主要臨床特征,嚴(yán)重影響女性患者的身心健康。關(guān)于PCOS發(fā)病機(jī)制的研究也在不斷深入。良好的動(dòng)物模型對(duì)PCOS的研究十分重要。目前PCOS動(dòng)物模型造模方法繁多,但尚缺少針對(duì)PCOS動(dòng)物模型表型的整理以及大鼠和小鼠模型對(duì)比的綜述。PCOS除具有生殖異常的特征外,還可能存在糖脂代謝的異常特征。在實(shí)際實(shí)驗(yàn)操作中,根據(jù)不同的實(shí)驗(yàn)?zāi)康?需要選擇不同的動(dòng)物模型。通過實(shí)踐及文獻(xiàn)分析發(fā)現(xiàn),雖然是同一種造模方法,在大鼠和小鼠上給予相同的藥物,或者不同階段給藥,都可能會(huì)產(chǎn)生不同的表型。因此,為了方便實(shí)驗(yàn)研究者選取最佳的造模方式,本綜述對(duì)目前常用的PCOS大鼠和小鼠經(jīng)典模型及其臨床表現(xiàn)進(jìn)行總結(jié)歸類、對(duì)比分析,旨在指導(dǎo)研究者有針對(duì)性地選擇最適宜的模型。
1 生殖異常的PCOS大鼠和小鼠模型
通過文獻(xiàn)研究發(fā)現(xiàn),采用來曲唑灌胃的成年大鼠和小鼠、雌激素造模的小鼠、米非司酮造模的大鼠和小鼠、睪酮造模的Swiss小鼠,以及給予妊娠期C57BL/6J小鼠雙氫睪酮的子代僅明確表明具有生殖異常的表現(xiàn),對(duì)于代謝異常的表現(xiàn)仍缺少有力的證據(jù)。
1.1 來曲唑造模法
來曲唑是一種口服的非甾體高效選擇性的第三代芳香化酶抑制劑,為人工合成的芐三唑類衍生物。來曲唑一方面抑制雌激素對(duì)下丘腦的負(fù)反饋?zhàn)饔?從而導(dǎo)致垂體促性腺激素分泌增加;另一方面可以阻止體內(nèi)雄激素向雌激素轉(zhuǎn)化,導(dǎo)致雄激素堆積,兩方面同時(shí)作用可以誘導(dǎo)卵巢呈多囊樣改變。
Kafali等[1]首次采用來曲唑建立PCOS大鼠模型,給予6周齡大鼠不同劑量來曲唑灌胃,21 d后發(fā)現(xiàn)不同劑量誘導(dǎo)的模型均表現(xiàn)為卵巢囊腫比例升高、卵巢包膜增厚和黃體數(shù)量減少。盡管對(duì)卵巢重量沒有顯著影響,但它能劑量依賴性地抑制子宮重量。此外,孕酮水平降低,睪酮和促黃體生成素(luteinizing hormone,LH)均升高,促卵泡刺激激素(follicle-stimulating hormone,FSH)水平在高、中劑量組(0.5和1.0 mg/kg)升高,在低劑量組(0.1 mg/kg)輕微下降,尤其卵巢的病理改變與人類PCOS非常相近。Kirici等[2]選取10~12周齡SD大鼠采用來曲唑誘導(dǎo)建立PCOS模型,將來曲唑(1 mg·kg-1·d-1)在1%羧甲基纖維素鈉和0.9%生理鹽水中溶解,連續(xù)灌胃21 d后發(fā)現(xiàn)PCOS組與其他組相比,表現(xiàn)為囊泡數(shù)量明顯增加,閉鎖卵泡數(shù)量增加,且PCOS組血清睪酮水平明顯高于其他各組,而各組間的LH、FSH和胰島素水平均無差異。
Torres等[3]分別給予4周齡和8周齡C57BL/6NHsd小鼠皮下埋植來曲唑緩釋劑(50 μg/d)連續(xù)5周,5周后發(fā)現(xiàn)青春期和成年雌性小鼠均具有PCOS的生殖特征,包括高雄激素血癥、LH升高、無排卵和卵巢多囊樣改變。然而,與青春期小鼠不同的是,成年雌性小鼠無明顯的卵巢重量增加、體重增加和腹部肥胖,空腹血糖和胰島素水平輕微升高,但無胰島素抵抗。說明其代謝特征與來曲唑干預(yù)的節(jié)點(diǎn)有關(guān),青春期接受來曲唑干預(yù)更易造成小鼠代謝異常,而成年期接受來曲唑干預(yù)小鼠仍維持正常的胰島素敏感性。
1.2 雌激素造模法
高雌激素誘導(dǎo)PCOS模型的機(jī)制為可誘導(dǎo)出PCOS垂體內(nèi)分泌環(huán)境的典型特征,雌激素通過正反饋調(diào)控LH分泌,高雌激素刺激使垂體對(duì)促性腺激素釋放激素(gonadotropin-releasing hormone,GnRH)刺激的敏感性增加,GnRH致使LH水平升高,另一方面雌激素的持續(xù)刺激通過負(fù)反饋調(diào)節(jié)抑制垂體FSH的分泌。
Chapman等[4]對(duì)雌性(C57BL/6J×A/J)F1(B6A)小鼠在5~7日齡時(shí)連續(xù)3 d皮下注射20 μg戊酸雌二醇,發(fā)現(xiàn)100日齡時(shí)成年小鼠表現(xiàn)出卵巢多囊樣改變以及黃體減少,且通過進(jìn)一步研究發(fā)現(xiàn),胸腺切除的小鼠注射雌二醇后并不能導(dǎo)致卵巢多囊樣改變,因而提出了卵巢囊腫是由類固醇治療后引起的自身免疫性疾病的觀點(diǎn)。Moayeri等[5]對(duì)4周齡的NMRI小鼠每天皮下注射4 mg/100 g戊酸雌二醇,誘導(dǎo)20 d后與正常小鼠相比,模型組小鼠初級(jí)卵泡減少,竇前卵泡增多,囊性卵泡增多,黃體數(shù)減少;顆粒細(xì)胞厚度明顯減少,卵母細(xì)胞直徑變小,而膜厚度異常增加;血清FSH水平降低,而LH顯著升高。Falahatian等[6]給8周齡的NMRI小鼠單次肌內(nèi)注射戊酸雌二醇(40 mg/kg),隨訪8周后小鼠出現(xiàn)動(dòng)情周期紊亂,睪酮、孕酮、雌激素水平較對(duì)照組增加,同時(shí)HE染色發(fā)現(xiàn)PCOS模型的卵巢中初級(jí)和原始卵泡數(shù)量顯著減少,竇前卵泡數(shù)量顯著增加,黃體數(shù)減少,卵巢囊腫數(shù)量增加。
1.3 米非司酮造模法
米非司酮是一種口服墮胎藥,屬于對(duì)孕酮受體具有很強(qiáng)親和力的類固醇。健康婦女在卵泡期服用米非司酮可破壞卵泡的正常發(fā)育,減少LH增加,且抑制排卵。
楊艷東[10]對(duì)6~8周的昆明種小鼠連續(xù)給予米非司酮灌胃(0.065 mg米非司酮溶于0.1 mL麻油中)24 d,發(fā)現(xiàn)長(zhǎng)期小劑量的米非司酮可抑制小鼠卵泡發(fā)育,但隨停藥時(shí)間的延長(zhǎng)這種損傷會(huì)逐漸恢復(fù),在停藥24 d動(dòng)情周期消失,停藥48 d動(dòng)情周期明顯延長(zhǎng),96 d動(dòng)情周期逐漸恢復(fù)規(guī)律。但該方法同樣缺少對(duì)小鼠代謝方面的研究,也沒有反映小鼠激素水平的變化。
因此,米非司酮造模法在大鼠和小鼠模型中,對(duì)代謝方面的研究仍十分有限。針對(duì)代謝紊亂的PCOS研究,不建議選擇該模型。
1.4 雄激素造模法
高雄激素血癥是PCOS的顯著特征,體內(nèi)循環(huán)雄激素水平的升高可阻礙卵泡發(fā)育成熟及導(dǎo)致囊腫形成。因此采用外源性雄激素造模是目前應(yīng)用最多的造模方法。其中,睪酮是生殖激素中的主要雄激素,由男性的睪丸或女性的卵巢分泌,腎上腺亦分泌少量睪酮。在體內(nèi),睪酮通過雄激素受體的介導(dǎo)直接促進(jìn)卵泡的早期發(fā)育,而在排卵前則作為前體合成雌激素,通過雌激素受體介導(dǎo)而發(fā)揮作用。過量睪酮使垂體對(duì)下丘腦刺激的敏感性降低、LH持續(xù)性分泌并導(dǎo)致排卵性LH峰消失,同時(shí)抑制FSH的促排卵作用,最終導(dǎo)致不排卵[11]。
Edwards[12]在新生Swiss小鼠出生后的前3天里每天給予100 μg的睪酮或者丙酸睪酮,發(fā)現(xiàn)可以導(dǎo)致小鼠不排卵和卵巢多囊樣改變,但該研究未檢測(cè)代謝方面的變化。
1.5 雙氫睪酮造模法
除睪酮外,還存在雙氫睪酮、脫氫表雄酮等其他雄激素。為模擬PCOS狀態(tài),脫氫表雄酮、雙氫睪酮等雄激素均常用于誘發(fā)動(dòng)物體內(nèi)的高雄激素血癥。
雙氫睪酮是一種可以由睪酮經(jīng)過5-α還原酶催化產(chǎn)生且不能被轉(zhuǎn)化為雌激素的雄激素。脫氫表雄酮造模無法排除高雄激素血癥是由雌激素轉(zhuǎn)化而來還是雄激素過高直接引起的,而雙氫睪酮造模法更具有針對(duì)性。實(shí)驗(yàn)中常通過皮下注射雙氫睪酮或埋置雙氫睪酮緩釋片的方法來誘導(dǎo)構(gòu)造PCOS動(dòng)物模型。
胡巧云等[13]選擇6~8周齡C57BL/6J小鼠,在其妊娠16~18 d時(shí)皮下注射雙氫睪酮(250 μg/d),將雙氫睪酮母鼠產(chǎn)下的雌性子代小鼠作為研究對(duì)象,結(jié)果顯示小鼠體重不受母鼠產(chǎn)前高雙氫睪酮暴露的影響,但卵巢重量及卵巢與體重的比值上升,動(dòng)情周期尤其是動(dòng)情間期時(shí)程明顯延長(zhǎng)。卵巢內(nèi)出現(xiàn)大的空泡,同時(shí)閉鎖卵泡數(shù)量增加,竇狀卵泡、成熟竇狀卵泡和黃體均減少,提示小鼠生育能力下降。血清中雌二醇、孕酮和FSH水平降低,而睪酮、LH水平、LH/FSH比值明顯升高,血清中呈現(xiàn)明顯的“高雄低雌”的典型癥狀。
2 生殖和代謝異常的PCOS大鼠和小鼠模型
雖然采用了同種藥物,在對(duì)不同的動(dòng)物,如大鼠或小鼠,不同的品系,或者在不同的年齡階段或妊娠期,不同的給藥方式等,均可能帶來不一樣的模型特征。
2.1 來曲唑造模法
為了誘導(dǎo)出同時(shí)具有代謝和生殖表型的PCOS大鼠模型,Maliqueo等[14]給予21日齡的青春期Wistar大鼠皮下植入不同劑量來曲唑緩釋劑,90 d后發(fā)現(xiàn)100或200 μg/d兩種來曲唑劑量均導(dǎo)致大鼠體重增加,腹股溝脂肪堆積,無排卵、卵巢增大伴卵泡閉鎖和多發(fā)囊腫,內(nèi)源性高雄激素血癥以及雌激素水平降低。此外,每天服用200 μg的大鼠還存在胰島素抵抗,腹股溝和腸系膜脂滴中的脂肪細(xì)胞增大,LH循環(huán)水平升高,FSH水平降低,卵巢17α-羥化酶(Cyp17A1)mRNA表達(dá)增加。表明從青春期開始,連續(xù)給予雌性大鼠來曲唑200 μg/d,持續(xù)90 d,可產(chǎn)生具有生殖和代謝特征的PCOS模型。
Kauffman等[15]給予4周齡青春期雌性C57BL/6N小鼠皮下植入來曲唑(50 μg/d)5周后,小鼠表現(xiàn)為血清睪酮水平升高,雌二醇水平正常,與PCOS患者相似。與對(duì)照組相比,來曲唑誘導(dǎo)的小鼠卵巢更大、多囊樣改變且黃體減少,動(dòng)情周期消失,并且不孕。血清LH水平升高,而血清FSH水平顯著降低。與對(duì)照組相比,來曲唑組小鼠體重增加更多,腹部肥胖增多,脂肪細(xì)胞大小增加,脂肪炎癥水平升高,糖耐量受損,反映了類似PCOS患者的代謝表型。Bhattarai等[16]選取21日齡ICR雌性小鼠和C57BL/6雌性小鼠給予來曲唑1 μg/g,連續(xù)灌胃21 d,PCOS組均出現(xiàn)不規(guī)則的動(dòng)情周期,表現(xiàn)為動(dòng)情期縮短,間期延長(zhǎng),且來曲唑喂養(yǎng)的小鼠體重在第3周顯著增加。
尹萍等[17]選取3周齡雌性大鼠喂養(yǎng)45%高脂飼料16周,于第6周齡開始灌胃來曲唑直至造模結(jié)束。結(jié)果顯示,模型組大鼠體重增加,卵巢、腹股溝脂肪質(zhì)量增加,子宮、垂體質(zhì)量及臟器指數(shù)顯著減少,卵巢呈多囊樣改變,顆粒細(xì)胞層減少,白膜增加。此外,三酰甘油和低密度脂蛋白升高,糖耐量曲線下面積增加,血清睪酮水平上升,空腹胰島素水平升高,胰島素敏感性降低。Zhang等[18]給予8周齡SD大鼠高脂飼料聯(lián)合來曲唑灌胃(1.0 mg·kg-1·d-1)21 d后,模型組表現(xiàn)出動(dòng)情間期明顯延長(zhǎng)的不規(guī)則周期,體重和血糖顯著升高,FSH顯著降低,LH、睪酮顯著升高。此外,Zheng等[19]通過給予8周齡C57BL/6J小鼠皮下注射來曲唑(50 μg/d)聯(lián)合高脂飲食喂養(yǎng)6周,同樣成功獲得了PCOS合并胰島素抵抗的小鼠模型。表明來曲唑聯(lián)合高脂飼料可以建立典型的生殖代謝異常的PCOS模型,且伴有明顯的肥胖,為常用的PCOS造模方法。
2.2 雌激素造模法
雌激素造模多選用SD大鼠,較少使用Wistar大鼠。邵華[20]給予8~12周齡雌性SD大鼠肌內(nèi)注射戊酸雌二醇,結(jié)果顯示,30 d后與對(duì)照組和空白組相比,高劑量(4 mg)、低劑量(2 mg)戊酸雌二醇組的大鼠出現(xiàn)動(dòng)情周期紊亂、卵巢表面蒼白,可見較多囊狀卵泡;組織學(xué)檢查顆粒細(xì)胞層明顯減少;激素水平上,睪酮與雄烯二酮的水平并無明顯升高,推測(cè)戊酸雌二醇誘導(dǎo)的PCOS模型與高雄激素?zé)o明顯關(guān)系。且注射4 mg戊酸雌二醇30 d后卵巢多囊性改變最為典型。Fazel等[21]對(duì)有3個(gè)連續(xù)規(guī)則動(dòng)情周期的SD大鼠連續(xù)皮下注射戊酸雌二醇(4 mg),4周后發(fā)現(xiàn)PCOS大鼠體重明顯增加,卵巢重量顯著增加,子宮重量明顯降低;血清LH、睪酮和雌二醇水平升高,而FSH和孕酮水平下降,高密度脂蛋白降低,三酰甘油水平和三酰甘油/高密度脂蛋白的比值升高;血糖和胰島素水平、胰島素抵抗指數(shù)(homeostasis model assessment insulin resistance,HOMA-IR)、胰島素樣生長(zhǎng)因子-1均升高。卵巢形態(tài)學(xué)表現(xiàn)與邵華[20]的模型一致。
2.3 雙氫睪酮造模法
嚴(yán)曉南[22]在SPF級(jí)SD大鼠妊娠第16~19 d頸背部皮下注射0.5 mL雙氫睪酮油劑(10 mg/mL)或0.5 mL溶劑,子代雌鼠出生后第4~8周的研究結(jié)果顯示,子代雌鼠在青春期體重增長(zhǎng)明顯加快,卵巢內(nèi)有大量卵泡成囊狀改變,卵泡總數(shù)、囊狀卵泡和閉鎖卵泡的數(shù)量均明顯增多,但卵巢重量和卵巢重量/體重的比值兩組間均無顯著差異。血清睪酮和雌二醇水平與對(duì)照組比較無顯著差異。空腹血糖、胰島素和瘦素水平均明顯升高,HOMA-IR亦顯著增高。8周齡時(shí)體內(nèi)游離脂肪酸明顯升高。
Manner?s等[23]對(duì)21日齡Wistar雌性大鼠皮下埋置雙氫睪酮緩釋片(7.5 mg/90 d),結(jié)果顯示雙氫睪酮組大鼠體重增加,脂肪增多,體脂率上升,動(dòng)情周期紊亂,卵巢面積和重量下降,囊性卵泡和閉鎖卵泡數(shù)量增加,血漿睪酮、雌二醇濃度無明顯變化,孕酮水平下降。同時(shí),PCOS模型大鼠瘦素水平升高,總膽固醇、三酰甘油、高密度脂蛋白無明顯變化,平均葡萄糖輸注率、胰島素敏感指數(shù)均下降,表明PCOS模型大鼠出現(xiàn)胰島素抵抗。說明21日齡的青春期大鼠皮下埋植含7.5 mg的雙氫睪酮緩釋片飼養(yǎng)到90 d具備了PCOS樣的生殖障礙和代謝紊亂特征。Pruett等[24]對(duì)4周齡SD雌性大鼠皮下埋植雙氫睪酮緩釋片(7.5 mg/90 d),8周后與對(duì)照組相比,同樣發(fā)現(xiàn)PCOS大鼠模型出現(xiàn)體重明顯增加,體重指數(shù)增加,脂肪量/肌肉量的比值增加。
van Houten等[25]對(duì)出生19 d的青春期前雌性小鼠皮下植入雙氫睪酮緩釋藥丸90 d(含2.5 mg雙氫睪酮,27.5 μg/d)后,發(fā)現(xiàn)小鼠出現(xiàn)動(dòng)情周期不規(guī)則,體重增加,卵巢閉鎖卵泡增加,多數(shù)閉鎖卵泡具有囊腫樣結(jié)構(gòu),脂肪細(xì)胞體積增大,瘦素水平升高,脂聯(lián)素水平下降,同時(shí)伴有葡萄糖不耐受。脂聯(lián)素具有抗炎、抗動(dòng)脈粥樣硬化和增加胰島素敏感性等作用,其血清水平降低易致胰島素抵抗[26]。
2.4 脫氫表雄酮造模法
脫氫表雄酮是孕烯醇酮轉(zhuǎn)化為雄烯二酮的中間產(chǎn)物,通過外源性提高脫氫表雄酮水平使雄烯二醇水平升高,進(jìn)而導(dǎo)致睪酮、雌酮水平升高,造成PCOS高雄激素血癥。升高的雌酮通過負(fù)反饋調(diào)節(jié)抑制FSH分泌釋放,使其相對(duì)不足而導(dǎo)致卵泡發(fā)育停滯,出現(xiàn)排卵障礙及卵巢多囊樣改變。
該法1991年由Lee等[27]提出,國(guó)內(nèi)外眾多學(xué)者對(duì)此模型進(jìn)行了更深一步的研究。王娜梅[28]選取23日齡SD雌性大鼠,每日于頸背部皮下注射脫氫表雄酮(6 mg/100 g體重+0.2 mL油劑),20 d后大鼠失去規(guī)律的動(dòng)情周期,卵巢體積增大,呈多囊樣改變;FSH、LH、睪酮水平明顯高于對(duì)照組;糖耐量異常,空腹胰島素及HOMA-IR明顯高于對(duì)照組。膽固醇、脂肪濕重、脂體比明顯高于對(duì)照組。Yu等[29]連續(xù)給予6周齡SD大鼠皮下注射脫氫表雄酮(60 mg·kg-1·d-1)共21 d,3周后檢測(cè)血糖和血清激素水平,模型組與對(duì)照組相比血清葡萄糖、睪酮、LH水平明顯升高,血清雌二醇、性激素結(jié)合球蛋白(sex hormone binding globulin,SHBG)、FSH水平明顯降低,游離睪酮指數(shù)和LH/FSH比值明顯升高。Zheng等[30]也同樣發(fā)現(xiàn)SD大鼠注射脫氫表雄酮(6 mg/100g)20 d后,大鼠出現(xiàn)周期紊亂,HOMA-IR顯著升高,子宮和卵巢重量增加,子宮內(nèi)膜腺體增生和卵巢形態(tài)改變,模型組卵巢皮質(zhì)層原始卵泡數(shù)量正常,閉鎖卵泡數(shù)量增加,有多個(gè)黃體化的囊性卵泡,卵泡在光鏡下未見卵母細(xì)胞或輻射冠。此外睪酮、雌二醇、LH、LH/FSH比值增加。這些研究均表明脫氫表雄酮可誘導(dǎo)SD大鼠出現(xiàn)與PCOS患者相似的生殖和代謝異常的改變,是研究PCOS生殖及代謝異常的較理想動(dòng)物模型[31]。
Solano等[32]用21日齡的Balb/c小鼠,連續(xù)注射脫氫表雄酮(60 mg·kg-1·d-1)20 d以誘導(dǎo)PCOS小鼠模型。該模型小鼠出現(xiàn)卵巢多囊樣改變,多囊樣卵泡膜和顆粒細(xì)胞層變薄,血清中雌二醇水平升高,體重增加,空腹胰島素、空腹血糖及HOMA-IR升高。Lai等[33]選用21日齡C57BL/6J雌性小鼠,以脫氫表雄酮(6 mg/100 g)連續(xù)處理20 d,同時(shí)給予高脂飲食。實(shí)驗(yàn)結(jié)果顯示,小鼠卵巢出現(xiàn)明顯多囊樣改變,顆粒細(xì)胞層變薄、閉鎖卵泡增加、黃體數(shù)量減少;動(dòng)情周期紊亂,血清睪酮明顯升高,體重增加,糖耐量異常以及存在胰島素抵抗。
2.5 胰島素聯(lián)合人絨毛膜促性腺激素造模法
人絨毛膜促性腺激素(human chorionic gonadotropin,HCG)可抑制卵泡顆粒細(xì)胞有絲分裂使顆粒細(xì)胞數(shù)量變少,胰島素刺激卵巢卵泡膜細(xì)胞和間質(zhì)細(xì)胞合成雄激素,降低血中SHBG含量,從而使雄激素的濃度升高,在二者共同作用下,可誘導(dǎo)出高雄激素血癥及卵泡閉鎖,形成多囊樣改變[34]。
本方法最早由Poretsky等[35]創(chuàng)建,其在前人基礎(chǔ)上發(fā)現(xiàn)高胰島素環(huán)境可促使類LH樣作用下的囊性卵泡和卵巢體積增長(zhǎng),同時(shí)注射胰島素及雌激素可使實(shí)驗(yàn)動(dòng)物(85日齡SD雌性大鼠)出現(xiàn)卵巢多囊樣和無排卵。徐曉娟等[36]采用6周齡SD雌性大鼠,胰島素聯(lián)合HCG模型組于大鼠頸背部連續(xù)皮下注射諾和靈30R(2 IU/d)和HCG(3 IU/d)28 d。研究結(jié)果表明,該造模方法可使SD大鼠出現(xiàn)動(dòng)情周期紊亂,無排卵前的成熟卵泡,卵巢臟器指數(shù)、睪酮、LH、三酰甘油、HOMA-IR升高,總膽固醇降低,同時(shí)具有胰島素抵抗和卵巢多囊樣改變的特點(diǎn)。
Hong等[37]選用8周齡C57BL/6雌鼠,采用胰島素聯(lián)合HCG造模法,皮下注射胰島素(劑量從0.5 IU/d開始,每天增加0.5 IU,直至6.0 IU/d),以誘導(dǎo)小鼠高胰島素血癥和胰島素抵抗。同時(shí)每日2次皮下注射HCG(6.0 IU/d),誘導(dǎo)小鼠高雄激素血癥,共注射21 d。小鼠經(jīng)胰島素和HCG干預(yù)后,與對(duì)照組相比,子宮和卵巢重量、子宮和卵巢臟器系數(shù)均增加,同時(shí)血清雌二醇、FSH、LH水平,LH/FSH比值,以及空腹血糖、空腹胰島素均顯著升高。模型組小鼠卵巢呈囊性竇泡,竇腔增大,顆粒細(xì)胞層減少,排列松散,卵母細(xì)胞消失,黃體減少。子宮直徑較大,說明小鼠生殖器官存在廣泛炎癥。同時(shí),模型組子宮腔內(nèi)上皮細(xì)胞和細(xì)胞層數(shù)減少。
2.6 雄激素造模法
Demissie等[38]對(duì)懷孕的成年雌性大鼠在妊娠第16~19天進(jìn)行游離睪酮或溶劑注射,雌性后代被喂予常規(guī)或高脂肪飲食。在60日齡時(shí),產(chǎn)前雄激素化(prenatelly androgenized,PA)大鼠的體重、子宮旁脂肪和皮下脂肪、血清胰島素、膽固醇和三酰甘油水平以及肝臟的三酰甘油含量與對(duì)照組相比顯著增加。該實(shí)驗(yàn)結(jié)果表明,在成年雌性大鼠中,短暫的產(chǎn)前雄激素暴露會(huì)產(chǎn)生代謝綜合征的特征,而高胰島素血癥可能是PA的直接結(jié)果。給予9日齡SD大鼠皮下注射丙酸睪酮(1.25 mg)造模,于70日齡開始陰道涂片,連涂10 d后發(fā)現(xiàn)大鼠出現(xiàn)囊性卵泡,卵巢顆粒細(xì)胞數(shù)量減少,無黃體,體重增加,雌二醇和瘦素水平升高,FSH降低,但同時(shí)存在LH水平的不升反降與PCOS相反的情況[39]。
3 結(jié)語(yǔ)
以上為現(xiàn)階段國(guó)內(nèi)外大鼠、小鼠較為常用的PCOS造模方法,各模型的生殖及代謝特征見表1。
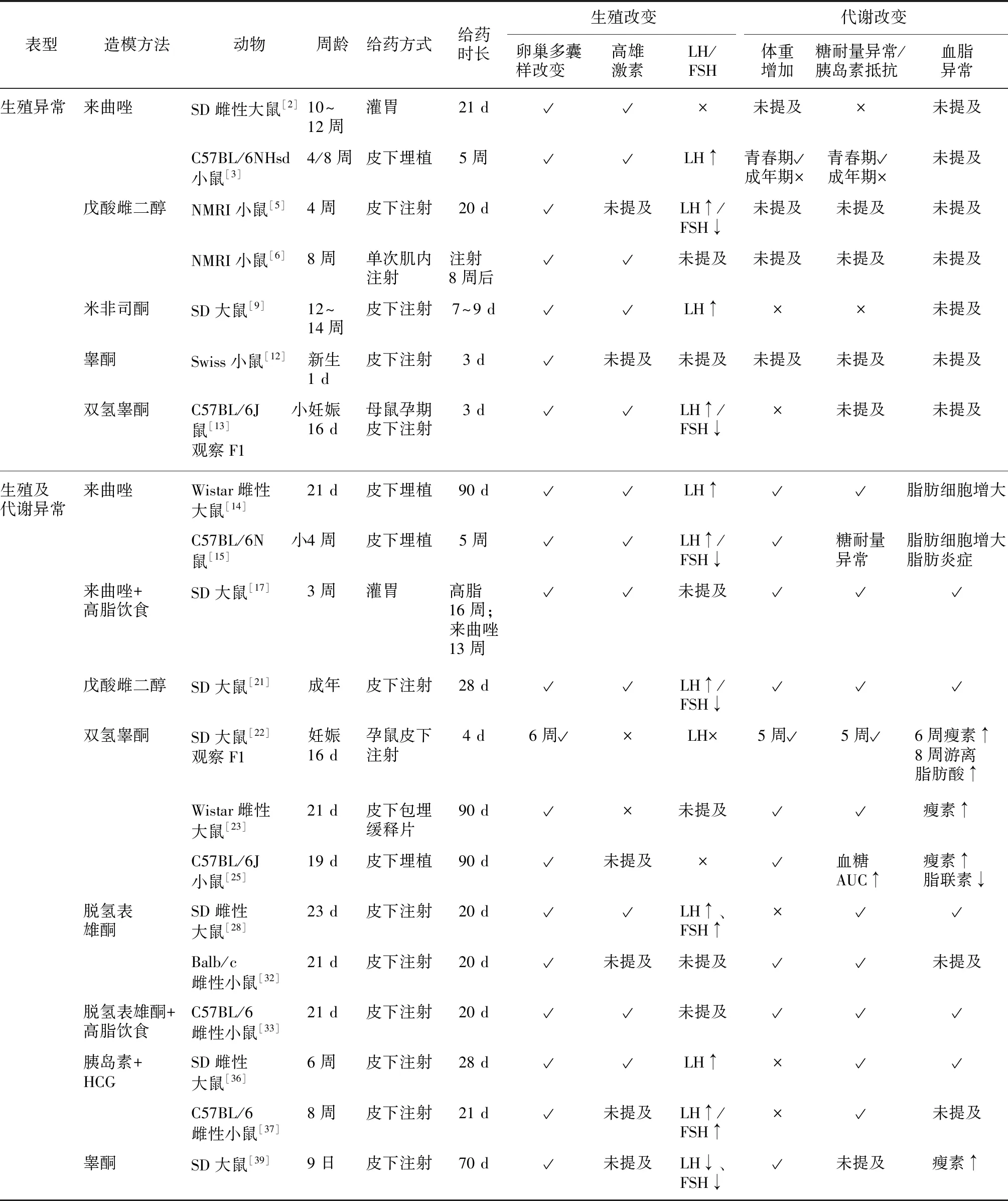
表1 PCOS大鼠和小鼠模型的生殖與代謝特點(diǎn)
來曲唑誘導(dǎo)的PCOS模型在卵巢改變方面與人類PCOS表現(xiàn)相似,均表現(xiàn)為卵巢體積明顯增大,具有大量典型囊狀卵泡,同時(shí)伴有睪酮水平升高,體重增加,是較為成功的卵巢多囊樣改變的PCOS模型。并且青春期給予來曲唑可誘導(dǎo)出同時(shí)具有生殖和代謝表型的PCOS大鼠和小鼠模型。而成年期給予大鼠和小鼠來曲唑,僅可誘導(dǎo)出生殖異常的PCOS大鼠和小鼠模型。
雌二醇誘導(dǎo)的PCOS模型激素分泌水平與人類PCOS相似,但由于不同研究報(bào)道存在差異,該模型缺乏穩(wěn)定性,且形成的囊性卵巢體積減小,雌激素干擾下丘腦-垂體軸,不適于PCOS形態(tài)學(xué)和治療效果的相關(guān)研究。
雙氫睪酮誘導(dǎo)的PCOS模型是最常用的造模方法之一,具有典型、多元化且成功率高的優(yōu)點(diǎn)。通過皮下注射或埋置雙氫睪酮緩釋片建立PCOS模型對(duì)大鼠和小鼠都適用,同時(shí)具備生殖和代謝異常改變。PCOS模型大鼠卵巢重量減少,而PCOS模型小鼠卵巢重量趨于增加,但與正常組小鼠相比無顯著差異。此外,小鼠模型卵巢囊性卵泡數(shù)量增加,但卵泡分布并不完全類似PCOS女性,同時(shí)LH水平有降低趨勢(shì)但與對(duì)照組相比無差異[25]。此外,雙氫睪酮作為動(dòng)物體內(nèi)自身活性的部分,外源性給予雄激素可能無法反映PCOS患者相關(guān)激素合成和代謝的真實(shí)狀態(tài)。因此,這類模型不建議用于探索PCOS高雄激素血癥發(fā)病機(jī)制,而只適用于研究高雄激素血癥的繼發(fā)癥狀,具有一定的局限性。
脫氫表雄酮誘導(dǎo)的PCOS動(dòng)物模型選用未性成熟的雌性大鼠和小鼠,可出現(xiàn)持續(xù)和穩(wěn)定的無排卵現(xiàn)象,但該模型的囊性卵泡膜細(xì)胞層較薄,不同于PCOS患者的囊性卵泡膜細(xì)胞層較厚[40]。同雙氫睪酮一樣,大鼠和小鼠均具有生殖和代謝的異常改變,但需要注意的是,因造模藥物為脫氫表雄酮,存在模型體內(nèi)升高的脫氫表雄酮難以區(qū)分是內(nèi)源性還是外源性的雄激素不足。
雙氫睪酮、脫氫表雄酮和胰島素聯(lián)合HCG的PCOS模型,除具有卵巢多囊樣改變外,還具有胰島素抵抗、血糖升高等代謝異常的表型。但由于胰島素聯(lián)合HCG造模法加入了外源性胰島素,因而不適用于胰島素抵抗的研究[41]。
綜上,來曲唑誘導(dǎo)的PCOS模型是較為成功的卵巢多囊樣改變的模型,為研究PCOS卵巢特征的優(yōu)選模型,但需要注意的是,雖然來曲唑誘導(dǎo)的大鼠和小鼠PCOS模型均會(huì)有生殖異常的典型改變包括動(dòng)情周期紊亂、卵巢多囊樣改變,但成年期模型缺少代謝方面的表征。采用雌激素誘導(dǎo)的PCOS大鼠和小鼠模型,均有卵巢多囊樣改變,但該模型缺乏穩(wěn)定性。而雄激素造模的方法,卵巢體積并未見明顯改變,因此這兩種方法不適用于PCOS形態(tài)學(xué)研究。對(duì)于發(fā)病機(jī)制的研究,因無法區(qū)分是內(nèi)源性還是外源性的因素,不建議選擇同類激素干預(yù)的造模方法。此外,如需觀察同時(shí)具有生殖和代謝異常的PCOS模型,除給予青春期大鼠和小鼠來曲唑或聯(lián)合高脂飲食外,還可選用雙氫睪酮、脫氫表雄酮及胰島素聯(lián)合HCG的造模方法。
由于PCOS是一種多因素造成的異質(zhì)性疾病,這些模型都無法完全模擬臨床上PCOS患者的特征。因此,當(dāng)考慮選用哪種模型進(jìn)行研究時(shí),十分重要的一點(diǎn)是要明確研究目的是什么,再根據(jù)研究目的選擇適宜的模型。
本文總結(jié)了常用PCOS模型的生殖和代謝特點(diǎn),根據(jù)不同的研究目的,可更直觀地為研究者在動(dòng)物模型的選擇上提供幫助。近年來國(guó)內(nèi)外學(xué)者對(duì)于PCOS的機(jī)制研究不斷深入,相信隨著實(shí)驗(yàn)動(dòng)物學(xué)的發(fā)展,未來更理想的PCOS動(dòng)物模型將會(huì)建成,推動(dòng)PCOS基礎(chǔ)研究的同時(shí),為臨床研究及應(yīng)用發(fā)展提供更可靠的實(shí)驗(yàn)依據(jù)。
 江蘇大學(xué)學(xué)報(bào)(醫(yī)學(xué)版)2024年1期
江蘇大學(xué)學(xué)報(bào)(醫(yī)學(xué)版)2024年1期
- 江蘇大學(xué)學(xué)報(bào)(醫(yī)學(xué)版)的其它文章
- 中性粒細(xì)胞與淋巴細(xì)胞比值對(duì)缺血性卒中相關(guān)性肺炎的預(yù)測(cè)價(jià)值
- 消化道腫瘤的中藥治療及機(jī)制研究新手段
- 用于炎癥治療的磷脂酰絲氨酸修飾胞外囊泡納米遞藥系統(tǒng)的初步構(gòu)建與評(píng)價(jià)
- hnRNPA2B1通過抑制轉(zhuǎn)鐵蛋白受體增強(qiáng)胰腺癌細(xì)胞對(duì)鐵死亡的抵抗
- ELP-SOD融合蛋白的純化及其脂質(zhì)體制備
- 系統(tǒng)性炎癥指標(biāo)對(duì)下肢動(dòng)脈硬化閉塞癥患者發(fā)生肌少癥的預(yù)測(cè)價(jià)值
