基于16S rRNA測序分析銀屑病小鼠皮膚及腸道微生態菌群
張雨婷 趙慧霞 孟 欣 趙佳樂 何曉園
1長治醫學院,山西長治,046000;2長治醫學院附屬和濟醫院皮膚科,山西長治,046000
皮膚和腸道菌群參與機體免疫的建立,是許多促炎疾病的重要驅動因素[1,2]。銀屑病和微生態菌群變化之間有著密不可分的聯系,菌群紊亂可能是導致銀屑病發生的關鍵因素[3,4]。與正常人群相比,銀屑病患者皮膚及腸道菌群多樣性改變,進一步支持了腸-免疫-皮膚軸[5,6]的存在。為探討銀屑病皮膚及腸道菌群變化,我們造模銀屑病小鼠模型,收集皮膚、糞便樣本,采用16S rRNA高通量基因測序方法,檢測并分析菌群變化。皮膚及腸道菌群與宿主之間的相互作用將有助于探討銀屑病的發病機制,并為今后銀屑病微生態研究提供新的理論基礎。
1 材料和方法
1.1 構造銀屑病小鼠模型 雄性BALB/c小鼠(SPF級,5周齡,體重16~18 g,北京斯貝福生物技術有限公司)置于隔離環境中飼養。溫度23℃,濕度50%。所有動物操作均通過長治醫學院倫理委員會批準。
適應環境1周后將小鼠隨機分為實驗組和對照組,每組納入6只。使用脫毛膏將全部小鼠背部毛發脫除。實驗組小鼠背部皮膚涂抹咪喹莫特乳膏[IMQ,四川明欣藥業有限責任公司,3 g/支,(批準文號)國藥準字H20030129]62.5 mg/日,連續7天[7];對照組小鼠接受相同體積的凡士林(山東德州利康醫藥科技有限公司,300 g/盒),連續7天,見圖1。在此期間,實驗組及對照組在相同條件下飼養,飼料、水、飼養溫度、濕度均無明顯差異。第8日麻醉后處死小鼠。
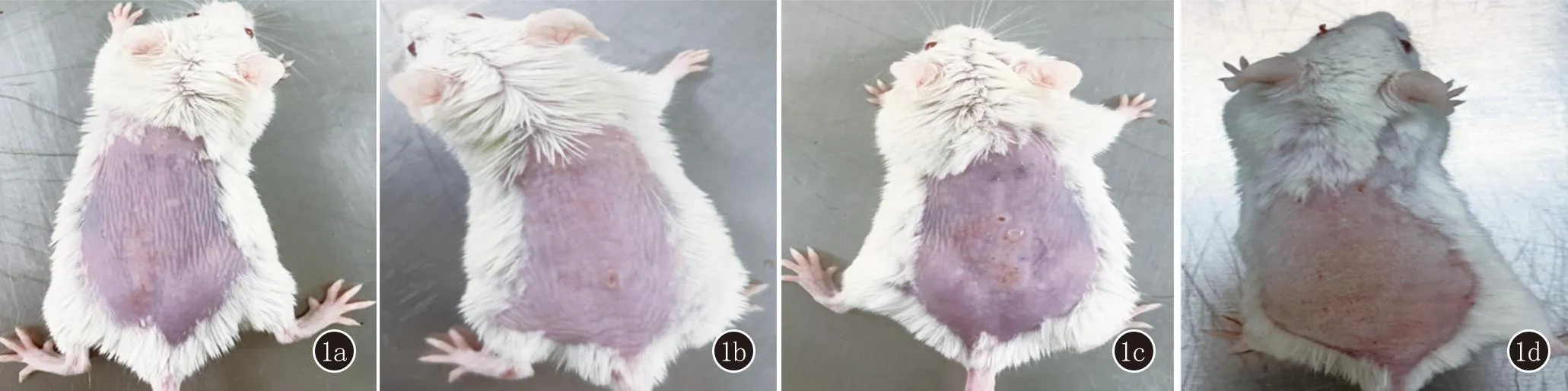
1a、1b:對照組;1c、1d:實驗組
1.2 皮膚組織樣本采集 造模第8日,使用二氧化碳氣體麻醉機(PerkinElmer)將小鼠麻醉后,取背部皮膚組織,大小約1 cm×1 cm×2份,標記為1號樣本、2號樣本。取樣后即刻將1號樣本放入無菌福爾馬林溶液固定,2號樣本放入無菌凍存管,置入-80℃冰箱內凍存備用。所有樣本均由同一實驗人員采集,嚴格遵守無菌原則,避免實驗標本在采集過程中受其他菌群污染。
1.3 糞便樣本采集 造模第8日,采集兩組小鼠新鮮糞便,取樣后即刻分裝2 g糞便樣本于無菌凍存管,置入-80℃冰箱內凍存備用。采集過程及要求同前。
1.4 樣本處理 1號樣本送至長治醫學院附屬和濟醫院病理科,經固定、脫水、包埋、切片、染色等步驟,制作成石蠟切片,結果回報后閱片。
2號樣本及糞便樣本送至上海寶藤生物醫藥科技股份有限公司進行檢測,提取樣本中的細菌總DNA,對V3~V4可變區行聚合酶鏈反應擴增,使用Illumina NovaSeq平臺行高通量測序,分類學分析得到代表序列的物種注釋結果。選用SILVA138數據庫比對,并在門、綱、目、科、屬、種分類水平上統計每個樣本的群落組成,分析兩組小鼠菌群多樣性、群落差異、組間物種及功能差異等[8]。
1.5 統計學方法 使用SPSS 25.0軼件進行統計學分析,計量資料以(X±S)表示,正態分布樣本采用t檢驗,非正態分布樣本采用Wilcoxon秩和檢驗,組間差異分析采用χ2檢驗、Anosim檢驗分析,以P<0.05為差異有統計學意義。
2 結果
2.1 小鼠皮膚組織病理 對照組、實驗組小鼠局部皮膚組織病理結果見圖2。
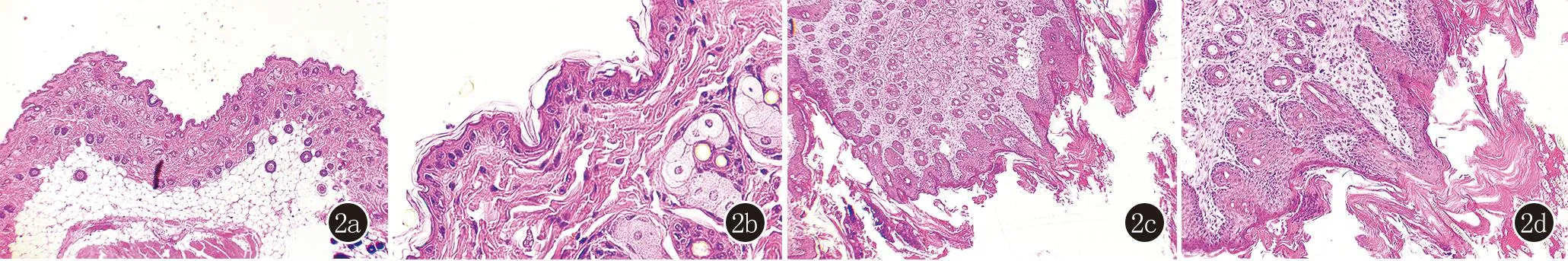
2a、2b:對照組;2c、2d實驗組
實驗組病理顯示:角化過度,顆粒層變薄或消失,棘層增厚,表皮突規則下延,真皮淺層毛細血管擴張,周圍炎細胞浸潤。符合銀屑病病理改變,造模成功。
2.2 小鼠皮膚組織菌群
2.2.1 α多樣性分析 通過計算每個樣本的α多樣性指數,可以反映樣本內微生物群落的豐富度、多樣性和均勻度。與對照組相比,實驗組Shannon指數(P=0.1)、Simpson指數(P=0.1)、ACE指數(P=0.1)降低,而Chao 1指數(P=0.7)、goods_coverage(P=0.1)升高,如表1所示。各指數均P>0.05,差異無統計學意義,但這些指數的數值表明銀屑病小鼠皮膚群落豐度和物種多樣性均略低。

表1 對照組與實驗組皮膚微生態菌群α多樣性指數分析
2.2.2 β多樣性分析 β多樣性分析關注樣本間的菌群組成差異。結果顯示,加權距離Anosim檢驗結果R=1,P=0.1。R>0,說明組間差異大于組內差異,但P>0.05,差異無統計學意義。我們基于Bray-Curtis距離進行PCoA分析,計算得不同分組因素對樣本差異的解釋度R=0.5767,分組顯著性P=0.1。分析結果,雖然P>0.05,差異無統計學意義,但仍能說明菌群多樣性差異較大。
2.2.3 菌群組成分析 實驗結果顯示,實驗組皮膚菌群豐度較對照組變化顯著。與對照組相比,實驗組中擬桿菌門、彎曲桿菌門、腸桿菌門、紅蝽菌綱、脫鐵桿菌綱、脫硫弧菌綱、梭狀芽孢桿菌目_UCG-014、毛螺菌目、理研菌科、瘤胃球菌科、副桿菌屬、丁酸桿菌屬、沙門氏菌種、耐久腸球菌種等的相對豐度降低,而厚壁菌門、芽孢桿菌綱、葡萄球菌目、巴斯德氏菌科等的相對豐度升高,乳桿菌目無明顯變化。因此,在門、綱、目、科、屬、種水平上,實驗組與對照組相比,菌群豐度顯示有明顯差異。兩組樣本在各分類水平上的物種相對豐度柱狀圖、兩組間屬水平物種的聚類熱圖見圖3。
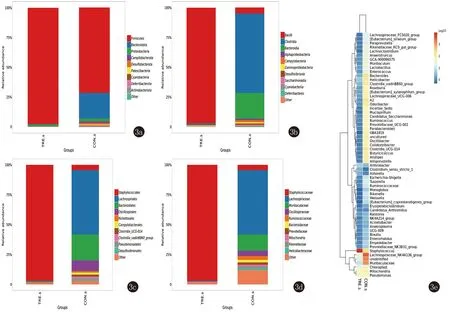
圖3 3a:門水平物種相對豐度柱狀圖;3b:綱水平物種相對豐度柱狀圖; 3c:目水平物種相對豐度柱狀圖; 3d:科水平物種相對豐度柱狀圖; 3e:兩組間屬水平物種的聚類熱圖
2.2.4 兩組群落差異分析(LefSe) 采用LefSe分析兩組的皮膚菌群組成、樣本所含菌群種類及各分類群的相對豐度差異,辨別對兩組間差異起決定作用的的物種。結果顯示小鼠皮膚菌群中,在綱水平,紅蝽菌綱、擬桿菌綱、彎曲桿菌綱、脫鐵桿菌綱、脫硫弧菌綱、芽孢桿菌綱在兩組樣本菌群的差異中起主要作用,在目水平,紅蝽菌目、擬桿菌目、黃桿菌目、彎曲菌目、脫鐵桿菌目、脫硫弧菌目、無膽甾原體目、丹毒絲菌目、乳桿菌目、葡萄球菌目起主要作用。見圖4。
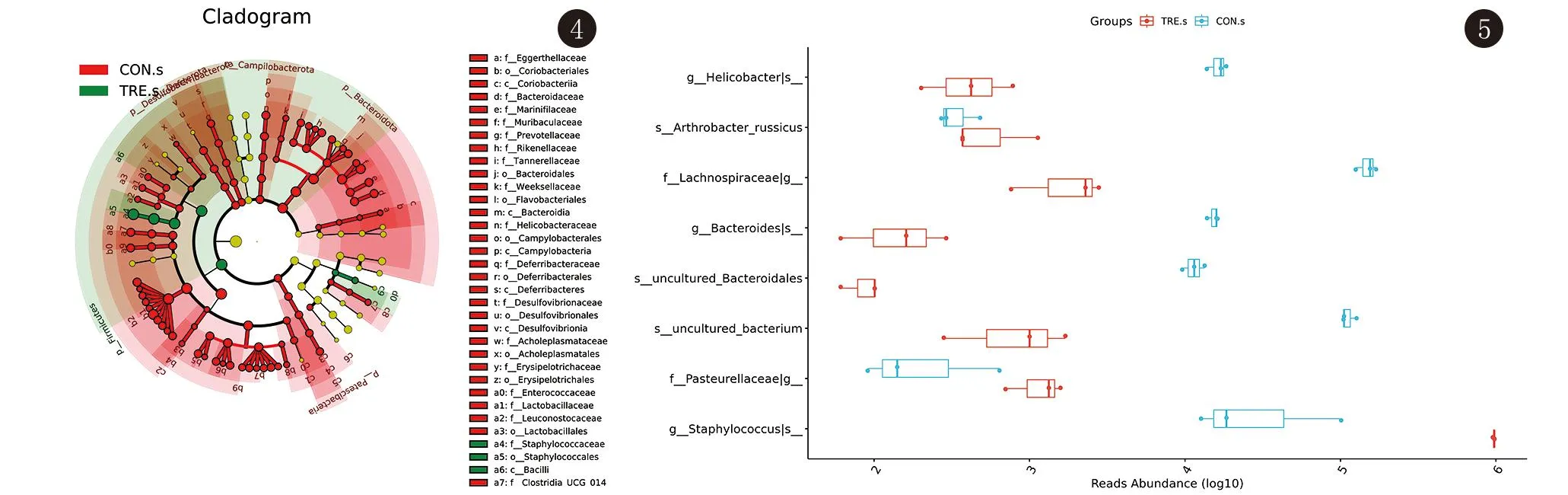
圖4 皮膚菌群LefSe進化分支圖
2.2.5 組間物種及功能差異分析(MetagenomeSeq) MetagenomeSeq利用線性模型找到對照組與實驗組菌群差異所在,結果顯示,χ2=16.069,P=0.003,95%CI[0.098,0.393],兩組菌群在門、綱、目、科、屬、種水平均存在差異,有統計學意義。較為顯著的是,小鼠皮膚菌群中,實驗組中巴斯德菌科、葡萄球菌屬、關節桿菌科占優勢,而對照組中螺桿菌屬、擬桿菌屬、毛螺菌科占優勢。見圖5。
2.3 小鼠腸道菌群
2.3.1 α多樣性分析 實驗組腸道菌群Shannon指數(P=0.2)、Chao 1指數(P=0.4)、ACE指數(P=0.3)、goods_coverage(P=0.3)均降低,Simpson指數(P=0.2)無變化,如表2所示。各指數均P>0.05,差異無統計學意義,但結果仍能顯示出銀屑病小鼠腸道群落豐度略高,而物種多樣性均略低。
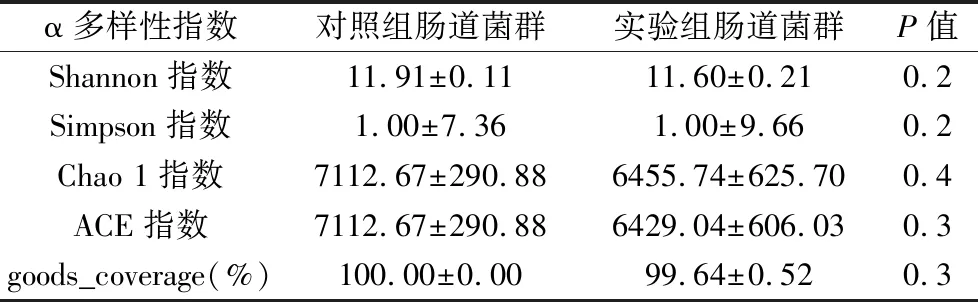
表2 對照組與實驗組腸道微生態菌群α多樣性指數分析
2.3.2 β多樣性分析 實驗結果顯示,加權距離Anosim檢驗結果R=0.778,P=0.1。R>0,說明組間差異大于組內差異,但P>0.05,差異無統計學意義。基于Bray-Curtis距離的PCoA分析結果R=0.2712,分組顯著性P=0.1。雖然P>0.05,差異無統計學意義,但菌群多樣性仍有差異。
2.3.3 菌群組成分析 實驗結果顯示,實驗組腸道菌群豐度較對照組變化顯著。一些細菌的相對豐度降低,如擬桿菌門、腸桿菌門、變形菌門、α-變形菌綱、乳桿菌目、理研菌科、紫單胞菌屬、瘤胃球菌屬等,而其他細菌,如彎曲桿菌門、藍藻菌門、厚壁菌門、梭狀芽孢桿菌綱、毛螺菌目、念珠藻目、消化鏈球菌目、脫鐵桿菌科、脫硫弧菌科、瘤胃球菌科、丁酸桿菌屬、沙門氏菌種、埃希氏菌種等的相對豐度增加,而真桿菌科、螺桿菌屬等變化存在矛盾。因此,實驗組與對照組相比在各水平上菌群豐度均有差異。兩組在各分類水平上的物種相對豐度柱狀圖、兩組間屬水平物種的聚類熱圖。見圖6。

圖6 6a:門水平物種相對豐度柱狀圖; 6b:綱水平物種相對豐度柱狀圖; 6c:目水平物種相對豐度柱狀圖; 6d:科水平物種相對豐度柱狀圖; 6e:兩組間屬水平物種的聚類熱圖
2.3.4 兩組群落差異分析(LefSe) LefSe分析結果顯示,小鼠腸道菌群中,在綱水平,擬桿菌綱、脫鐵桿菌綱、脫硫弧菌綱、梭狀芽孢桿菌綱、α-變形菌綱在兩組樣本菌群的差異中起主要作用,在目水平,擬桿菌目、脫鐵桿菌目、脫硫弧菌目、乳桿菌目、梭狀芽孢桿菌目_vadinBB60群、毛螺菌目、念珠藻目、消化鏈球菌目、腸桿菌目起主要作用。見圖7。
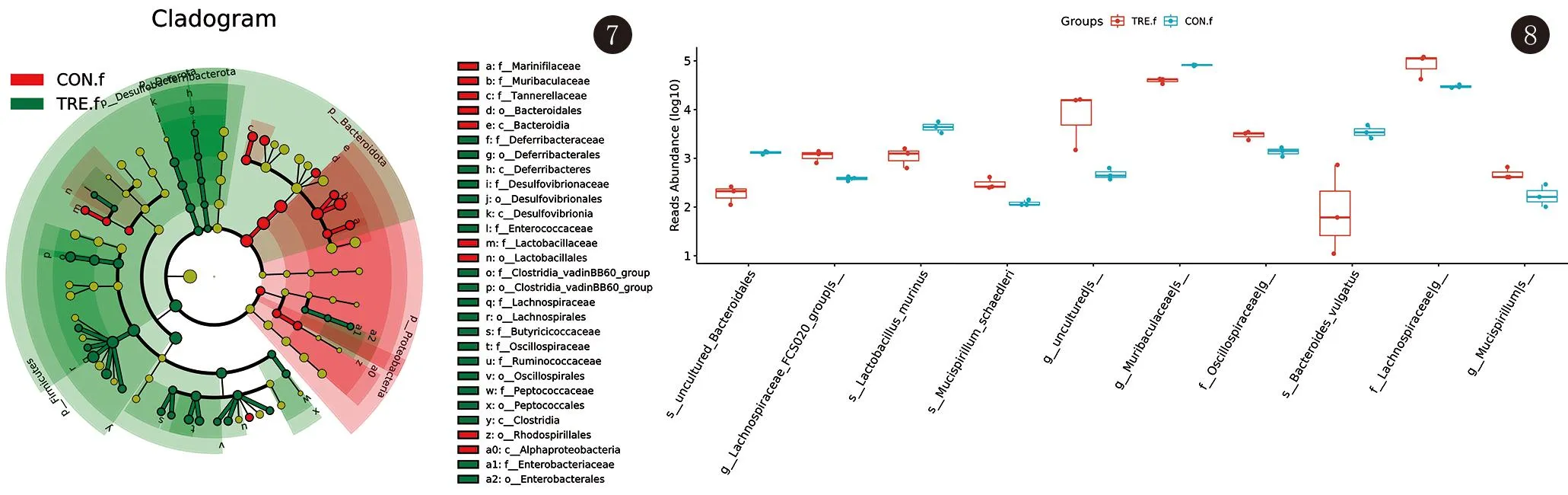
圖7 腸道菌群LefSe進化分支圖
2.3.5 組間物種及功能差異分析(MetagenomeSeq) MetagenomeSeq結果顯示,χ2=16.069,P=0.003,95%CI[0.098,0.393],兩組菌群在門、綱、目、科、屬、種水平均存在差異,有統計學意義。結果顯示小鼠腸道菌群中,實驗組中顫螺旋菌科、毛螺菌科、毛螺菌屬_FCS020群、黏液螺旋菌屬、舍氏小螺菌種占優勢,而對照組中擬桿菌屬、鼠乳桿菌種占優勢。見圖8。
3 討論
綜上所述,實驗組與對照組相比,皮膚和腸道菌群的相對豐度均存在明顯差異,提示銀屑病小鼠存在微生態菌群失調。目前學者普遍認為,正常情況下微生態菌群處于動態平衡的狀態,具有維持機體穩定、抵御病原微生物入侵、調節免疫應答、調控營養代謝等多種功能。菌群失調會使代謝產物釋放入血,引發免疫炎癥反應,進而參與銀屑病的進程[9-10]。
近年來多項研究報道,銀屑病患者存在不同程度的皮膚及腸道微生物群紊亂,提示菌群變化可能在銀屑病的發病機制中起關鍵作用[11-12]。本研究中,實驗組與對照組相比,在門、綱、目、科、屬、種水平上,皮膚和腸道菌群相對豐度均存在顯著差異,有統計學意義。LefSe分析表明,小鼠皮膚菌群中紅蝽菌綱、擬桿菌綱、乳桿菌目、葡萄球菌目等起主要作用,腸道菌群中擬桿菌綱、梭狀芽孢桿菌綱、腸桿菌目、毛螺菌目等起主要作用。MetagenomeSeq分析結果顯示,銀屑病小鼠皮膚菌群中巴斯德菌科、葡萄球菌屬、關節桿菌科等占優勢,而腸道菌群中顫螺旋菌科、毛螺菌科、毛螺菌屬_FCS020群、黏液螺旋菌屬、舍氏小螺菌種等占優勢。我們的實驗結果與之前多項關于銀屑病菌群研究的結果基本一致。Hidalgo-Cantabrana等[13]的研究顯示,銀屑病患者腸道中厚壁菌門的比例顯著升高,而擬桿菌門、嗜黏蛋白阿克曼菌屬、瘤胃球菌屬、普拉梭菌種降低,同時,厚壁菌門/擬桿菌門比值與銀屑病的嚴重程度呈正相關[14]。我們的實驗中銀屑病小鼠腸道厚壁菌門、擬桿菌門、瘤胃球菌屬的變化與Hidalgo-Cantabrana等的研究結果相同,但普拉梭菌屬在銀屑病小鼠腸道中無明顯變化。Wang等[15]對27例銀屑病樣本和54例對側非皮損皮膚及健康皮膚樣本進行了菌群成分的測序和分析,結果顯示,銀屑病皮膚樣本菌群α多樣性和β多樣性顯著低于健康人群,且不動桿菌、假單胞菌、沙門氏菌、芽孢桿菌的豐度較健康人群皮膚明顯降低,本實驗中也顯示出相似的結果,但銀屑病小鼠皮膚中不動桿菌的變化不明顯。Zhang等[16]的研究結果也相似,且與我們的實驗結果一致。這些結果差異可能與銀屑病患者容易受到外界環境影響或與飲食結構不同有關,導致部分菌群受干擾,而小鼠在相同環境下飼養,受干擾的因素較少。但總體而言,我們的實驗結果和之前的研究基本一致,進一步驗證了實驗的可信度。
我們通過成功構建咪喹莫特誘導的銀屑病小鼠模型,采用16S rRNA高通量測序比較并分析了銀屑病小鼠與正常小鼠皮膚及腸道中菌群差異,并與目前已公開發表的關于銀屑病患者菌群變化的結果進行聯合分析,提示銀屑病患者存在明顯的皮膚及腸道菌群變化,菌群相對豐度及多樣性發生改變。其原因可能與銀屑患者皮膚屏障受損有關,動態平衡被破壞,增加了致病菌感染的風險,通過腸道進入機體,進而腸道微生態環境紊亂,影響相關炎癥因子釋放和免疫應答,導致疾病的發生,但具體發生機制還有待進一步研究證實。
然而,我們的實驗也存在不足之處,一是實驗樣本量較小,二是檢測的菌群數量有限。在后續實驗中,皮膚及腸道微生態菌群對銀屑病的影響仍需更深入剖析。菌群變化對銀屑病慢性炎癥反應的發生發展具有重要意義,調節皮膚、腸道菌群可能成為銀屑病的替代治療方式。我們將繼續進一步探索皮膚、腸道菌群與銀屑病的關聯,為今后研究銀屑病、研發新型治療藥物提供新的策略,皮膚及腸道菌群作為治療銀屑病新的靶點,可能將在銀屑病的診療中發揮舉足輕重的作用。

