不同抗凝方案在接受連續腎臟替代療法的急診膿毒癥患者中的應用效果
師延剛,于曉琳,耿玉安,劉瑞芳
(河南省直第三人民醫院 急重癥醫學科,河南 鄭州 450000)
膿毒癥患者病情進展較快,且易并發急性腎損傷,連續替代腎臟療法(continuous renal replacement therapy, CRRT)可以代替患者機體的腎臟功功能,幫助其清除炎癥介質,糾正內環境紊亂,為膿毒癥患者的救治提供了重要的內穩定平衡[1-2]。但是在血液凈化的過程中,抗凝不充分容易造成患者血管通路及濾器堵塞,從而加劇炎癥反應,降低治療效果。而過度抗凝則容易引起患者出血。低分子肝素與枸櫞酸均是臨床常用的抗凝劑,均有一定的抗凝效果,但是何種抗凝劑可以在保證CRRT順利進行的同時也不引起出血及并發癥,成為膿毒癥患者治療順利的關鍵,需要臨床重點考慮。基于此,本研究對110例接受CRRT治療的急診膿毒癥患者進行回顧性研究,分析患者采用不同抗凝方案對其炎癥狀態和出血風險的影響。
1 資料與方法
1.1 一般資料
采用回顧性研究,選擇2020年1月至2022年12月醫院收治的110例接受CRRT治療的急診膿毒癥患者作為研究對象,根據抗凝方案的不同進行分組,將接受低分子肝素抗凝的58例患者資料納入對照組,將接受局部枸櫞酸抗凝的52例患者資料納入觀察組。對照組男31例,女27例;年齡42~71歲,平均(56.84±6.79)歲;病程3~6 d,平均(4.26±0.61)d;急性生理與慢性健康評分系統[3]評分為17~25分,平均(21.24±2.36)分;合并基礎疾病高血壓14例,糖尿病10例,高脂血癥5例。觀察組:男27例,女25例;年齡40~72歲,平均(57.42±6.59)歲;病程3~5 d,平均(4.13±0.40)d;急性生理與慢性健康評分系統評分為18~25分,平均(21.69±1.92)分;合并基礎疾病高血壓12例,糖尿病9例,高脂血癥7例。兩組患者一般資料均衡可比(P>0.05)。
1.2 入選標準
(1)納入標準:滿足《中國膿毒癥/膿毒性休克急診治療指南(2018)》[4]中膿毒癥診斷標準;接受CRRT治療;血管通路功能正常;臨床資料完整。(2)排除標準:凝血功能障礙;有抗凝治療史;肝、腎功能不全或障礙;存在嚴重活動性出血;合并患有血液系統性疾病;治療前存在心動過緩或低血壓;存在其他感染性疾病;妊娠或哺乳期婦女。
1.3 方法
1.3.1對照組
接受低分子肝素抗凝方案。CRRT治療后,給予患者低分子肝素(昆明積大制藥股份有限公司,國藥準字H20053199),采用皮下注射的方式,注射速度為4~5 s,注射完畢后停留約10 s,初始劑量為15~20 IU·kg-1·h-1,追加劑量為5~10 IU·kg-1·h-1。臨床需動態監測患者凝血指標、血管路動脈壓的變化以及濾器等情況,合理調整患者的使用劑量;置換液流量控制在2~3 L·h-1,血液流量為150~200 mL·min-1,血液置換時間為每日8~10 h,在CRRT治療結束前1~2 h停用。
1.3.2觀察組
采用局部枸櫞酸抗凝:給予患者枸櫞酸鈉抗凝劑(四川綿竹鴻基制藥有限責任公司,國藥準字H20073117),經血管動脈端輸入質量濃度為40 g·L-1的枸櫞酸鈉,以血流速率的2.5%持續輸注,控制濾器后的游離鈣離子濃度為0.25~0.35 mmol·L-1;在靜脈端注射0.056 mmol·L-1的氯化鈣生理鹽水(100 g·L-1的氯化鈣80 mL溶入到1 000 mL生理鹽水中),速率為40 mL·h-1,控制患者體內游離鈣離子濃度為1.0~1.35 mmol·L-1,直至CRRT治療結束。
1.4 評價指標
1.4.1炎癥因子水平
于1次透析治療前后采集患者的空腹靜脈血3 mL,設置離心機速率為3 500 r·min-1,離心處理10 min,取上層血清,采用全自動特定蛋白分析儀(深圳湃爾生物科技有限公司,型號PR-880)檢測患者的血清腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α)、白細胞介素-6(interleukin-6,IL-6)水平。
1.4.2凝血功能指標
于1次透析治療前后采集兩組患者上肢淺靜脈血4 mL,通過凝血分析儀(企晟醫療器械有限公司,京械注準2062220177,型號SF-8000)檢測患者的凝血酶原時間(prothrombin time,PT)、活化部分凝血活酶時間(activated partial thromboplastin time,APTT),以及纖維蛋白原(fibrinogen,Fib)。
1.4.3出血風險評估
采用房顫抗凝治療出血評分系統[5]評估兩組患者接受抗凝CRRT治療后的出血風險。該量表包含高血壓、肝腎功能、年齡等7項內容共9個條目,每個條目各計1分,總分為0~9分,房顫抗凝治療出血評分系統評分越高,則表示患者出血風險越大。
1.5 統計學方法

2 結果
2.1 炎癥因子水平
治療前,兩組患者血清TNF-α、IL-6水平差異無統計學意義(P>0.05);治療后,兩組患者血清TNF-α、IL-6水平較前下降,且觀察組水平低于對照組低,差異有統計學意義(P<0.05)。見表1。

表1 兩組患者炎癥因子水平比較
2.2 凝血功能指標
治療前,兩組患者PT、APTT、Fib差異無統計學意義(P>0.05);治療后,兩組患者PT、APTT較前下降,Fib水平較前升高,且觀察組患者PT、APTT低于對照組,Fib水平高于對照組(P<0.05)。見表2。
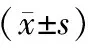
表2 兩組患者凝血功能指標比較
2.3 出血風險評估
治療前,兩組房顫抗凝治療出血評分系統評分差異無統計學意義(P>0.05);治療后,兩組患者房顫抗凝治療出血評分系統評分均降低,且觀察組評分低于對照組,差異有統計學意義(P<0.05)。見表3。

表3 兩組患者出血風險比較分)
3 討論
CRRT治療是急診膿毒癥患者重要的治療措施之一,不僅可以幫助患者清除體內多余的炎癥介質、毒素等,還具有維持患者機體內環境穩定的作用[6]。但因膿毒癥患者常伴器官功能障礙而引起凝血功能障礙,常需輔以抗凝治療來保證CRRT治療的順利進行,可減輕患者體內的炎癥反應,降低出血風險,改善患者預后[7]。目前,臨床常用的抗凝劑主要包括低分子肝素與枸櫞酸,但具體哪一種抗凝方案更為有效尚未明確,故對此展開研究。
炎癥反應是膿毒癥患者的癥狀表現之一,TNF-α、IL-6是常見的炎癥反應指標,且在患者體內多呈現為高表達[8]。本研究結果顯示,兩組膿毒癥患者治療后血清TNF-α、IL-6水平均降低,表明兩種抗凝劑均可以改善患者的炎癥反應。分析其原因,低分子肝素可以通過降低白細胞黏附和激活速度來抑制補體系統的激活,可較好地保護患者血管內皮細胞的連續性和完整性,抑制炎癥介質的釋放[9]。枸櫞酸屬于人體生理性物質,具有較好的生物相容性,不僅可以降低鈣離子的濃度,還可以抑制補體激活,抗炎作用更具優勢[10]。同時,采用枸櫞酸方案治療時,枸櫞酸進入人體后會迅速發揮作用,使得濾器內與患者血液內的二價鈣離子濃度下降,以此來下調膜介導的炎癥反應,從而降低炎癥細胞因子的水平,達到減輕炎癥反應的目的。因此,與低分子肝素相比,枸櫞酸的抗炎效果更強。
凝血功能異常是導致膿毒癥患者出血的因素之一,PT、APTT與Fib均是臨床檢測凝血功能與抗凝治療的重要監測指標,既可用于評估患者是否有凝血障礙,也可用于出血風險評估。本研究發現,治療后兩組PT、APTT均降低,Fib升高,且觀察組患者PT、APTT更低,Fib水平更高,且本研究還通過評分系統發現,治療后兩組患者房顫抗凝治療出血評分系統評分均降低,且觀察組患者評分更低,表明觀察組患者出血風險更小,這就說明膿毒癥患者采用低分子肝素與局部枸櫞酸的抗凝方案均可以達到較好的抗凝作用,但顯然后者對患者凝血功能的改善更好,出血風險也更低。具體分析其原因,低分子肝素是通過酶解與抗凝血酶結合形成復合物來阻斷凝血連鎖反應,但其也會產生肝素相關的白細胞、血小板降低,在一定程度上會增加出血風險。而枸櫞酸是通過動脈端進入患者循環管路內,能夠與血液中鈣離子結合形成一種穩定的枸櫞酸鈣復合物,以降低血管通路中的鈣離子濃度,從而抑制機體凝血級聯反應,抑制血小板激活,達到改善凝血功能、實現抗凝的作用[11-12]。另外,枸櫞酸可以在患者體內轉化為碳酸根離子,且有一部分會從透析液中清除,剩余的枸櫞酸鈣會被運轉至肝腎進行代謝;同時通過輸入含鈣溶液,幫助患者血液中鈣離子濃度維持正常。因此,采用局部枸櫞酸的抗凝方案可以在保證凝血效果的同時不會損傷患者的凝血功能。同時,楊皓瑩等[13]在比較局部檸檬酸鈉抗凝與低分子肝素抗凝在膿毒癥患者CRRT治療過程中的應用效果時也指出,與低分子肝素相比,檸檬酸鈉抗凝可降低出血風險,與本研究結果有相似之處。由此可見,與低分子肝素相比,采用局部枸櫞酸抗凝的方式更具優勢。
4 結論
與低分子肝素抗凝相比,采用局部枸櫞酸抗凝方式可更好地降低急診膿毒癥患者炎癥反應,改善凝血功能,且出血風險更低。

