體外物理震動排石機在輸尿管軟鏡碎石術后患者殘石排出中的應用效果
顏靚倩(通信作者),林珍珍,韓子華,陳衛英,梁林佳
浙江省臺州醫院 (浙江臺州 318050)
泌尿系結石是泌尿科常見的梗阻性疾病,其發病率呈逐年增高的趨勢。輸尿管軟鏡碎石術(retrograde intrarenal surgery,RIRS)是目前臨床治療上尿路結石的主要方式之一,但術后難免會有結石殘留,如不及時處理可引起輸尿管梗阻、感染和疼痛等并發癥,因此RIRS 術后需輔助排石以提高殘石清除率[1]。以往臨床上對腎內殘石主要依靠如多飲水、倒立體位、口服擴張輸尿管藥等傳統的被動排石法進行排石,但效果不甚理想,缺乏簡單、主動和無創的主動排石手段[2]。體外物理震動排石機是目前我國自主研發的一款主動輔助排石儀器,能將高能振動波傳導至腎和輸尿管,利用簡諧波產生的推動力促進結石主動下移并排出,但用于RIRS 術后殘石排出的報道較少[3-4]。基于此,本研究探討體外物理震動排石機促進RIRS 患者術后殘石排出的效果,現報道如下:
1 臨床資料
1.1 一般資料
選取2022 年1 月至2023 年4 月我院泌尿科結石門診就診的90 例RIRS 術后殘石患者,采用隨機數字表法分為對照組和試驗組,每組45 例。對照組男22 例,女23 例;年齡21~84 歲,平均(45.02±3.72)歲;術后時間8~19 d,平均(12.73±2.91)d;殘石直徑1.8~5.0 mm,平均(3.66±0.71)mm。試驗組男24 例,女21 例;年齡22~85 歲,平均(45.58±3.89)歲;術后時間7~18 d,平均(12.42±2.65)d;殘石直徑2.1~5.0 mm,平均(3.72±0.72)mm。兩組性別、年齡、術后時間和殘石直徑等比較,差異無統計學意義(P>0.05),有可比性。本研究已獲得醫院醫學倫理委員會的審核批準,患者均自愿參與研究且已簽署知情同意書。
納入標準:術前均經泌尿系CT 或超聲檢查證實為上尿路結石,并行RIRS 治療;RIRS 均一次碎石成功且留置D-J 管位置良好,影像學檢查示單個殘石直徑≤6 mm;結石以下輸尿管無明顯梗阻。排除標準:合并輸尿管狹窄或尿路梗阻;泌尿系畸形或重度腎積水。
1.2 方法
對照組采用傳統排石措施治療:口服擴張輸尿管藥、多飲水(>2 L/d))、增加活動量(督促患者進行快走、跳躍或爬樓梯等運動)和健側臥位休息,囑腎下盞結石患者倒立等。
試驗組在對照組基礎上采用體外物理震動排石機(鄭州富健達公司,Friends-I 型)治療:囑患者排石前飲水后憋尿,超聲檢查腎盞內殘石情況和腎積水程度。術前0.5 h,口服呋塞米片40 mg,囑患者平臥于治療床上,調整排石床角度為45°、頭低足高位,振動頻率為2 800 次/min,振幅5 mm。期間以實時超聲檢查結石位置,取健側臥位或俯臥位,連續給予機械振蕩15 min,待患者感下腹部脹痛難忍、憋尿困難時排空尿液。
兩組均2 周后復查泌尿系平片,如仍有較大的結石殘留,予以再次排石治療。兩組治療時間均為4 周。
1.3 觀察指標
(1)治療當日見石率和開始排石時間;(2)治療2、4 周后復查泌尿系平片,檢測殘石率和殘石直徑;(3)治療前及治療4 周后血清炎癥因子水平:超敏C 反應蛋白(hypersensitive C-reactive protein,hs-CRP)和腫瘤壞死因子-α(tumor necrosis factor-α,TNF-α),分別采用免疫比濁法和酶聯免疫吸附法測定血清hs-CRP 和TNF-α 水平。(4)治療期間并發癥發生情況:包括腎絞痛、發熱、嚴重血尿及尿路感染等。
1.4 統計學處理
2 結果
2.1 兩組治療后當日見石率和開始排石時間比較
試驗組當日見石率高于對照組,開始排石時間短于對照組,差異有統計學意義(P<0.05),見表1。

表1 兩組治療后當日見石率和開始排石時間比較
2.2 兩組血清hs-CRP 和TNF-α 水平比較
治療前,兩組血清hs-CRP 和TNF-α 水平比較,差異無統計學意義(P>0.05)。治療4 周后,兩組血清hs-CRP 和TNF-α 水平低于治療前,且試驗組低于對照組,差異有統計學意義(P<0.05),見表2。
表2 兩組血清hs-CRP 和TNF-α 水平比較(±s)
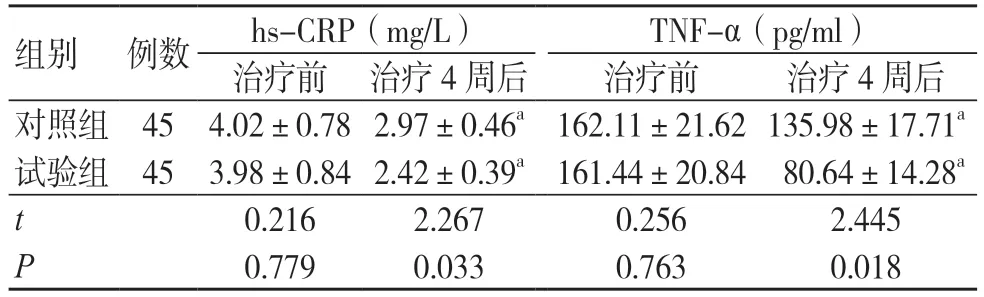
表2 兩組血清hs-CRP 和TNF-α 水平比較(±s)
注:與同組治療前相比,aP<0.05;hs-CRP 為超敏C 反應蛋白,TNF-α 為腫瘤壞死因子-α
組別 例數 hs-CRP(mg/L) TNF-α(pg/ml)治療前 治療4 周后 治療前 治療4 周后對照組 45 4.02±0.78 2.97±0.46a 162.11±21.62 135.98±17.71a試驗組 45 3.98±0.84 2.42±0.39a 161.44±20.84 80.64±14.28a t 0.216 2.267 0.256 2.445 P 0.779 0.033 0.763 0.018
2.3 兩組殘石率和殘石直徑比較
治療2 周和4 周后,試驗組殘石率均低于對照組,殘石直徑均小于對照組,差異有統計學意義(P<0.05),見表3。
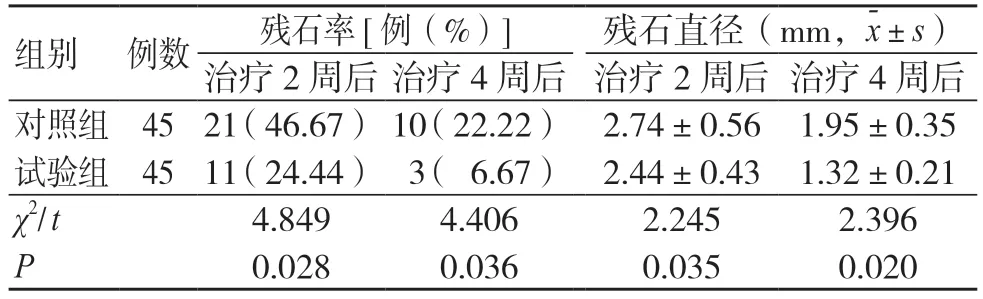
表3 兩組殘石率和殘石直徑比較
2.4 兩組治療期間并發癥發生率比較
試驗組并發癥發生率低于對照組,差異有統計學意義(P<0.05),見表4。

表4 兩組治療期間并發癥發生率比較 [例(%)]
3 討論
RIRS 是目前治療腎及輸尿管上段結石常用的方法,但術中使用的鈥激光只能將結石擊碎成微小結石碎粒,后通過尿液的沖刷將結石排凈,患者往往難以于短時間內將結石碎粒徹底排出體外,結石的排凈率并不理想,甚至部分患者結石難以排出,可引發梗阻、感染或形成石銜,甚至需再次手術治療[5-6]。腎內殘石不僅會誘發患者出現腎絞痛、發熱或血尿等癥狀,且殘石長時間停留在腎內,易被凝血塊或絮狀物包裹更難排出,殘石逐漸融合增大,會導致結石復發。因此,降低術后的殘石率是RIRS 手術目前急需解決的難點[7-8]。以往臨床常采用口服擴張輸尿管藥、飲水、運動和自主體位排石等方法輔助排石,但均屬于被動排石措施,排石療效不甚理想,并可增加排石過程中輸尿管梗阻、腎絞痛和尿路感染的發生風險[9]。對腎下盞的殘石采用“倒立”排石,患者往往難以掌握體位,且又缺乏的輔助排石儀器設備,往往難以通過被動的排石方式排出體外。
體外物理震動排石機是一種新型的高效輔助排石儀器,將以往被動排石轉變為主動排石[11-12]。體外物理震動排石機使用多方位物理簡諧振動慣性引導技術,其中下置振動器可產生橫向簡諧波,上置振動器可產生定點和定向簡諧波,推動結石前行和下移,促使分離擊碎后的小結石與體腔分離,引導并促進殘余小結石、血凝塊等沿著尿路通道逐漸排出,提高排石的效果,降低結石殘留及結石復發風險[13-14]。本研究結果發現,試驗組當日見石率高于對照組,開始排石時間短于對照組,治療2、4 周后殘石率均低于對照組,殘石直徑均小于對照組。提示體外物理震動排石機用于RIRS 術后患者的排石效果優于傳統排石措施,可加快殘石排出,提高結石排凈率。同時本研究結果還發現,治療4 周后,試驗組血清hs-CRP 和TNF-α 水平低于對照組,試驗組治療期間并發癥發生率低于對照組。提示體外物理震動排石機用于RIRS 術后患者可降低體內相關炎癥因子水平,減少術后并發癥發生。其原因可能與傳統的排石措施不能進行主動排石相關[15-16]。而體外物理震動排石機是一種主動排石儀器,可依據結石的部位調整排石床的傾斜角及患者體位,使結石所在腎盞的盞頸處于開口向下的相對高位,利用體位排石原理,再結合主、副振子產生的簡諧波及縱向加速度促進結石向下移動,加快殘石排出,提高結石排凈率,特別是腎下盞結石的排石效果[17-18];同時使結石和體腔分離形成間隙,為排石移動及下排形成滑動空間,減少排石中腎和輸尿管黏膜的損傷,不僅可減輕炎癥反應,且可降低腎絞痛和血尿的發生率,減少并發癥發生[19-20]。
綜上所述,體外物理震動排石機用于RIRS 術后患者,不僅可加快殘石排出,提高結石排凈率,且可減輕炎癥反應,減少術后并發癥的發生。

