深圳市鹽酸利托君不良反應報告分析和風險信號挖掘*
肖 霄,唐碧雨,吳建茹,魏芬芳,李麗敏,吳文宇
(廣東省深圳市藥物警戒和風險管理研究院,廣東 深圳 518024)
先兆流產是婦產科臨床常見生殖疾病[1],若孕婦在第12~28孕周出現下腹疼痛或墜脹、陰道少量流血、妊娠物未排出等現象,即可認為是晚期先兆流產[2],如不及時治療,可能發展至流產,甚至出現繼發不孕[3]。臨床對晚期先兆流產患者主要采用藥物療法,常用藥物包括硫酸鎂、鹽酸利托君[4]等。有研究表明,鹽酸利托君治療先兆早產起效快,能明顯延長妊娠時間,且對新生兒出生體質量的提高等均較硫酸鎂好,但母體使用后發生副反應的風險明顯高于硫酸鎂[5]。此外,國家藥品審評中心臨床試驗備案信息顯示,國產鹽酸利托君生物等效性試驗仍缺少妊娠期女性的數據。為此,本研究中分析了深圳市2017年至2021年收集到的鹽酸利托君藥品不良反應(ADR)監測數據,挖掘妊娠人群使用的風險信號,結合相關文獻、藥品說明書進行風險提示,為臨床安全用藥提供參考。現報道如下。
1 資料與方法
1.1 數據來源
通過廣東省藥物警戒與風險管控系統收集國家藥品不良反應監測中心2017年1月1日至2021年12月31日接收到的深圳市藥品不良反應(ADR)監測數據。
1.2 數據規整
剔除重復報告后,共獲得140 387 條數據記錄(因同一患者可能有多種懷疑藥品,故報告編碼有重復)。刪除其中非妊娠期用藥、流產用藥、產前預防用藥、產后用藥,以及同一份報告中同一種藥物不同劑量/頻次數據,共得到775 條數據記錄,涉及患者698 例,共發生ADR 1 389 例次,其中鹽酸利托君相關的分別為51 例、147 例次。根據2015年版《世界衛生組織不良反應術語集》(WHOART)統計ADR累及系統/器官。
1.3 信號挖掘方法
采用比例報告比(PRR)法、報告比值比(ROR)法和綜合標準(MHRA)法[6],依據經典四格表對相關ADR信號進行挖掘。詳見表1和表2。

表1 比例失衡法四格表Tab.1 Fourfold table of disproportionality measurement

表2 PRR,ROR,MHRA法的計算公式及閾值Tab.2 Calculation formulas and thresholds of PRR,ROR and MHRA methods
1.4 統計學處理
采用Microsoft Excel 2013 軟件和R 語言對數據進行描述性分析和統計學分析。計數資料以率(%)表示,行χ2檢驗或采用Fisher確切概率法。檢驗水準α=0.05,P<0.05為差異有統計學意義。
2 結果
2.1 人口特征、報告類型及轉歸
698例患者的年齡主要集中于21~34歲,鹽酸利托君相關ADR 報告類型主要為一般報告,其次為新的一般報告。超70%患者的ADR痊愈及好轉。詳見表3。
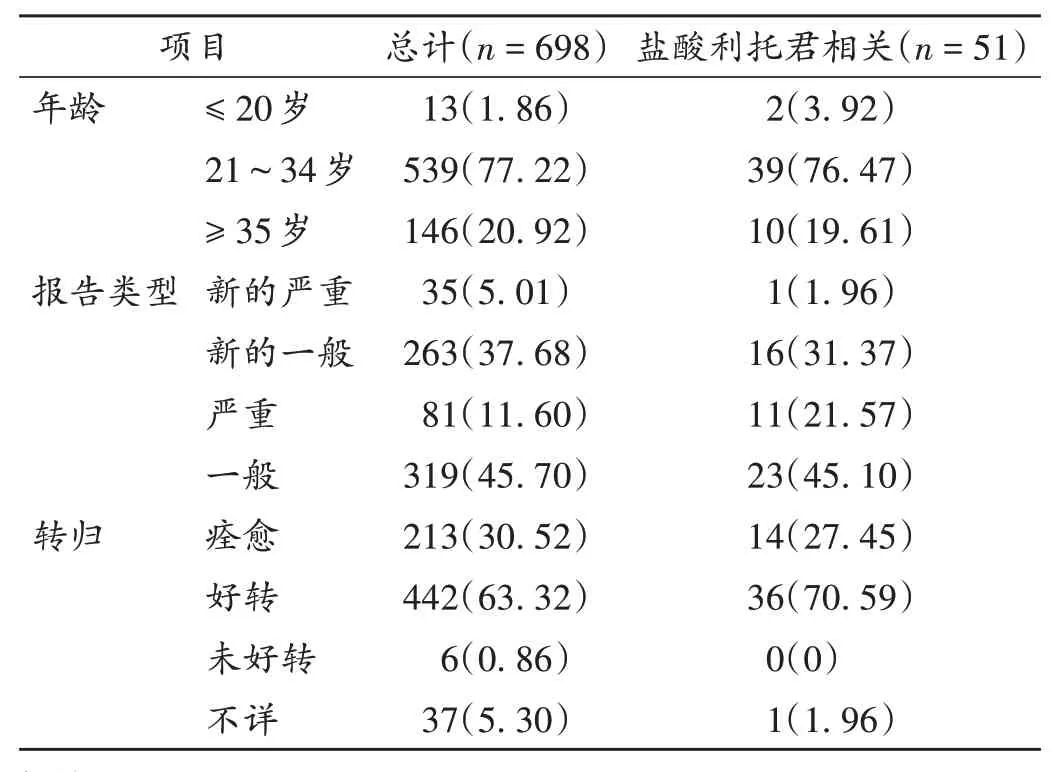
表3 患者年齡、報告類型及轉歸情況[例(%)]Tab.3 Age,reporting type and outcome of patients[case(%)]
2.2 孕周分布
698 例患者中有明確孕周信息的有372 例,共涉及ADR 754例次,與鹽酸利托君相關的有40例,孕周分布見圖1。可見,總的及與鹽酸利托君相關的ADR 例次和患者數孕周分布趨勢基本一致,以第32孕周最多。

圖1 ADR的孕周分布Fig.1 Relationship between the occurrence of ADRs and gestational weeks
2.3 ADR 累及系統/器官及臨床表現
1 389 例次ADR 涉及21 種系統/ 器官,249 種臨床表現,按累計系統/ 器官分類,排前3 的分別為胃腸道疾病(425例次、30.60%),皮膚及其附件疾病(244例次、17.57%),全身疾病(187 例次、13.46%)。147 例次鹽酸利托君相關ADR 已知累及12 種系統/器官,54 種臨床表現。詳見表4。
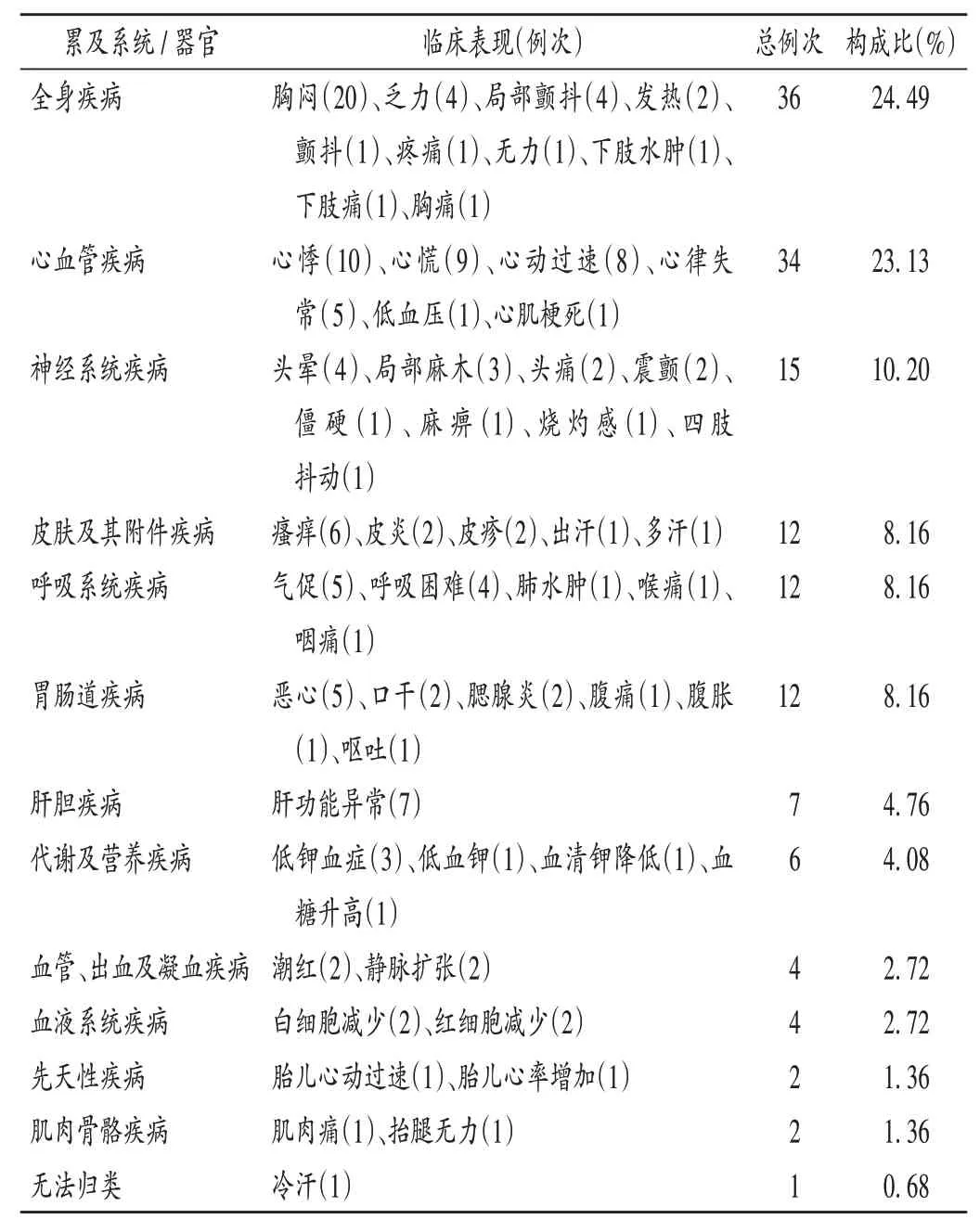
表4 鹽酸利托君相關ADR累及系統/器官及臨床表現(n=147)Tab.4 Systems / organs and clinical manifestations involved in ritodrine hydrochloride - related ADRs(n = 147)
2.4 風險信號挖掘
147 例次鹽酸利托君相關ADR 中,胸悶、心悸、心慌、心動過速、氣促、心律失常、局部顫抖、低鉀血癥、局部麻木9 類ADR 信號的檢測結果有統計學意義(P<0.05),主要ADR 信號(≥3例次)見表5(其中-表示無法計算,*表示新的ADR)。
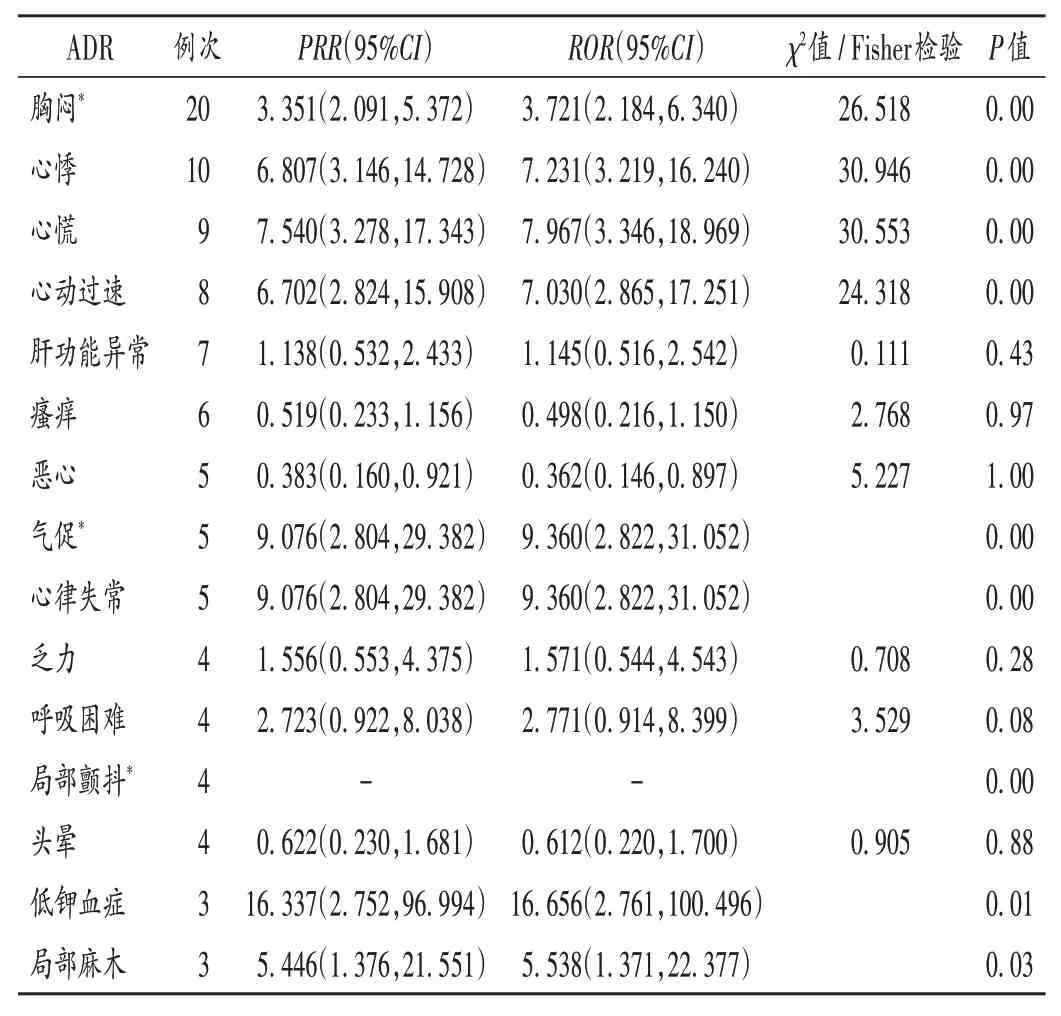
表5 鹽酸利托君主要相關ADR風險信號挖掘結果Tab.5 Results of risk signal mining of ritodrine hydrochloride -related major ADRs
3 討論
鹽酸利托君注射液為高特異性β2受體激動劑,也是唯一被美國食品和藥物管理局(FDA)批準和推薦使用的早產預防藥[7]。其ADR 可能與受體興奮有關。β2受體分布于骨骼肌、平滑肌和肝臟,興奮后可舒張子宮,緩解宮縮,同時增加糖原分解和骨骼肌收縮,導致血糖升高和肢體顫抖。鹽酸利托君相關ADR 臨床表現和檢出信號多與心血管系統相關,可能與β2受體激動劑過度激活β受體有關,可引起心律失常及中樞神經系統反應。選擇性β2受體激動劑既可選擇性激動支氣管平滑肌β2受體,也可激動心臟β2受體,劑量大時對心臟β 受體無選擇性,可增強心肌收縮力,加快心率,甚至引發室性期前收縮和二聯律等心律失常[8]。
嚴重ADR 中,胸悶、心悸、呼吸困難、氣促、肺水腫等的例次較多,如不及時干預,對母體和胎兒的負面影響較大。胸悶、心悸等可能為利托君對心臟的激動作用導致。呼吸困難、氣促、肺水腫可能為利托君對腎素-醛固酮系統的激活疊加妊娠期機體生理變化有關。妊娠人群的循環血容量比平時增加35%~40%,多胎妊娠時增加更明顯[9],利托君可激動腎素- 血管緊張素-醛固酮系統,引起水鈉潴留,妊娠期血容量增加,心輸出量增加,心臟負荷較非妊娠期增加,提高了肺水腫的潛在風險。若用氯化鈉作溶劑,可增加電解質,進一步擴大血容量[10]。本研究中收集到鹽酸利托君ADR 的報告類型以新的一般ADR 為主,對比信東生技股份有限公司2020年8月13 日修改的藥品說明書【不良反應】項,其新的ADR 包括胸悶、氣促、心律失常、乏力、局部顫抖、頭暈、紅細胞減少、靜脈擴張、口干、皮炎、腮腺炎、顫抖、低血壓、腹痛、腹脹、喉痛、僵硬、燒灼感、四肢抖動、下肢水腫、下肢痛、心肌梗死和咽痛,其中乏力為嚴重ADR,追溯原始報告發現患者同時出現低血鉀(為藥品說明書中已知ADR),給予補鉀后緩解,故乏力可能與低血鉀有關。此外,根據藥品說明書,鹽酸利托君用于預防孕晚期(妊娠22 周后)的早產,51 例患者中有5 例屬超藥品說明書用藥(1 例為孕18 周出現僵硬和顫抖等新的一般ADR;4 例為孕21 周出現胸悶、肝功能異常等),患者轉歸良好,但不能排除超藥品說明書用藥的潛在風險。國際婦產科聯盟將分娩年齡≥35 歲的妊娠定義為高齡妊娠[11],COOKE 等[12]的研究顯示,高齡孕婦隨著年齡的增加,機體的過氧化脂質水平增加,血管內皮功能損傷加重,血管活性物質大量釋放,引起血管收縮,增加心臟負荷,導致血壓升高。本研究中20.92%的妊娠患者為高齡妊娠,疊加藥物的β 受體激動效應可能更易使其出現心血管疾病ADR 或加重ADR。同時,由于地塞米松可促胎肺成熟,硫酸鎂對胎兒有腦保護作用,在早產治療中可能會出現多藥聯用或序貫療法,經查閱藥品說明書,硫酸鎂有致孕婦肺水腫的風險。且有案例報告[13-15]三藥聯用時出現妊娠期肺水腫。因此,建議藥品上市許可持有人后續關注藥物安全性,將高齡妊娠注意事項及聯合用藥有潛在肺水腫的風險提示列入藥品說明書。
為減少妊娠人群臨床用藥ADR 的發生,提出以下建議。1)孕5~6 周和孕31~32 周患者ADR 多發,建議對相應時期用藥患者加強ADR 監測。2)胃腸道系統是相應ADR 最常累及的系統,用藥后如有相關異常,建議仔細對比患者用藥前后的狀態,并與妊娠反應加以區別,及時給予干預措施。3)控制鹽酸利托君劑量,嚴格按藥品說明書給藥,并監測患者的心率、呼吸頻率、血壓、血糖、血鉀等指標,尤其是高齡妊娠人群及與硫酸鎂、糖皮質激素聯合用藥患者,出現心悸、胸悶、呼吸困難時及時調整患者為側臥位,必要時吸氧、給予利尿劑等。
本研究的不足為患者孕周信息不全,無法從孕周方面對所有妊娠人群進行分析;所有使用藥品數據無法獲得,故無法計算ADR 發生率;鹽酸利托君數據較少,可能存在多重共線性。
綜上所述,鹽酸利托君的ADR 多與其對腎素- 血管緊張素-醛固酮系統的激活疊加妊娠期人體生理變化有關,臨床使用時需嚴格控制劑量與時機(孕周),加強監測,關注高齡孕婦的用藥情況,以減少嚴重ADR 的發生。

