基因多態性對腹腔鏡術后舒芬太尼用量的預測效能*
張 奕,韓 強,阿卜杜拉·阿卜迪艾尼,賈蔓箐
(新疆醫科大學第七附屬醫院,新疆 烏魯木齊 830028)
術后疼痛控制欠佳不僅會導致患者主觀感受痛苦,還可引起機體多個系統/器官出現反應,延緩術后康復,延長住院時間,增加醫療費用。腹腔鏡圍術期鎮痛能減輕患者術后的疼痛,但仍難以滿足需求,因為外科手術復雜程度高,術后并發癥多,且人們對術后鎮痛的需求也越來越高[1]。目前臨床用于術后鎮痛的一線藥物為以舒芬太尼為代表的阿片類藥物。影響患者術后疼痛的因素眾多,如術前精神狀態、手術創傷大小、遺傳因素等[2]。相關研究表明,基因表達的差異對于疼痛敏感性和術后鎮痛效果影響較大[3]。已有研究發現,CYP3A4,COMT,OPRM1、ABCB1等多個基因的單核苷酸多態性(SNP)與疼痛敏感性及阿片類藥物術后鎮痛效果密切相關[4][如CYP3A4(rs2242480)[5]、COMT(rs4680)[6]、OPRM1(rs1799971)[7]、ABCB1(rs1045642)[8]]。基于此,本研究中探討了上述4個基因的SNP 位點對腹腔鏡術后舒芬太尼用量的影響,以期為術后鎮痛的個體化用藥及降低藥品不良反應發生率提供參考。現報道如下。
1 資料與方法
1.1 一般資料
納入標準:擇期行腹腔鏡手術(包括胃大部切除術、結直腸癌根治術);漢族;年齡18~65 歲;能正確使用患者自控鎮痛(PCA)泵且術后接受48 h 舒芬太尼PCA 鎮痛;認知和自我評估功能良好;癌癥術前未接受放射治療和化學藥物治療(簡稱放化療)。本研究符合《赫爾辛基宣言》且經醫院醫學倫理委員會批準(審批號K-20210305),患者及其家屬均簽署知情同意書。
排除標準:對本研究擬用藥物過敏;既往存在慢性疼痛,接受過長期鎮痛治療;嚴重的心、肝、肺、腎功能障礙;精神類疾病;不適合進行此研究的其他情況。
資料收集:收集醫院2021年4月至2023年3月收治的行腹腔鏡手術治療患者的資料,包括性別、年齡、體質量指數(BMI)、美國麻醉醫師協會(ASA)麻醉分級、手術時間、蘇醒時間、手術類型;術前1 天的空腹血糖(FBG)、白蛋白(Alb)、天門冬氨酸氨基轉移酶(AST)、白細胞計數(WBC)、血清肌酐(SCr)、血尿素氮(BUN)、白細胞介素6(IL - 6)、腫瘤壞死因子- α(TNF-α)水平。
1.2 方法
患者完成術前準備后,嚴格按腹腔鏡手術操作指南手術,嚴格按胃腸外科護理流程予圍術期治療及護理。術后均予PCA:首先予枸櫞酸舒芬太尼注射液(宜昌人福藥業有限責任公司,國家準字H20054171,規格為50 μg∶1 mL;下同)5 μg 負荷劑量,靜脈緩慢注射,然后連接PCA 泵。PCA 泵配方為,枸櫞酸舒芬太尼注射液150 μg + 鹽酸托烷司瓊注射液(海南靈康制藥有限公司,國藥準字H20060287,規格為每瓶5 mg)10 mg,用0.9%氯化鈉注射液稀釋至150 mL,背景輸液速率為1.0 mL/h,PCA劑量為每次0.4 mL,鎖定時間為15 min,控制疼痛數字評價量表(NRS)評分<3分(即維持在輕度疼痛)。記錄患者術后24 h 內的舒芬太尼用量。
1.3 基因多態性分析
采集患者術前禁食12 h 后肘靜脈血2 mL,乙二胺四乙酸(EDTA)抗凝,采用酚- 氯仿抽提法提取DNA。采用聚合酶鏈式反應-限制性片段長度多態性分析法測定SNP。1)應用Primer 3 軟件設計CYP3A4(rs2242480)、COMT(rs4680)、OPRM1(rs1799971)、ABCB1(rs1045642)4 個基因位點的引物(美國AB 公司設計及合成),詳見表1。2)PCR 反應體系:25 μL,包括10 pmol/ L 引物1 μL,DNA模板約2 μL,200 μmol/L dNTPs 20 μL,1 U Taq 聚合酶1 μL,1.5 mmol/ L MgCl21 μL。反應條件,96 ℃預變性6 min;94 ℃40 s,52 ℃60 s,72 ℃50 s,共35 個循環;72 ℃延伸7 min。3)采用瓊脂糖凝膠電泳鑒別。4)擴增結束后用限制性內切酶MspI和CviQI 酶解。5)采用瓊脂糖凝膠電泳鑒別基因型。6)采用紫外成像儀拍照。采用Bio - Rad C FX manager 3.0 軟件進行基因型分析。采用Apaman 探針實時熒光定量PCR技術檢測4個位點的基因型。

表1 引物序列Tab.1 Primer sequences
1.4 統計學處理
采用SPSS 22.0 統計學軟件分析。計數資料以率(%)表示,組間比較行χ2檢驗;計量資料以±s或M(P25,P75)表示,行單因素方差分析。采用有序Logistic回歸分析評估腹腔鏡患者術后舒芬太尼用量的相關影響因素;使用R 軟件建立列線圖模型,計算C-指數,繪制校準曲線,采用受試者操作特征(ROC)曲線評估模型的早期預測價值。P<0.05為差異有統計學意義。
2 結果
2.1 患者臨床資料
共納入患者300 例,其中男170 例、女130 例,平均年齡(44.82 ± 8.94)歲,術后舒芬太尼用量[30.35(18.33,47.92)]μg。按舒芬太尼用量的區間范圍采用四分位法,將患者分為A 組(總用量≤25%)、B 組(總用量26%~50%)、C 組(總用量51%~74%)、D 組(總用量≥75%),各75例。4組患者的臨床資料中僅手術時間、FBG的差異有統計學意義(P<0.05)。詳見表2。
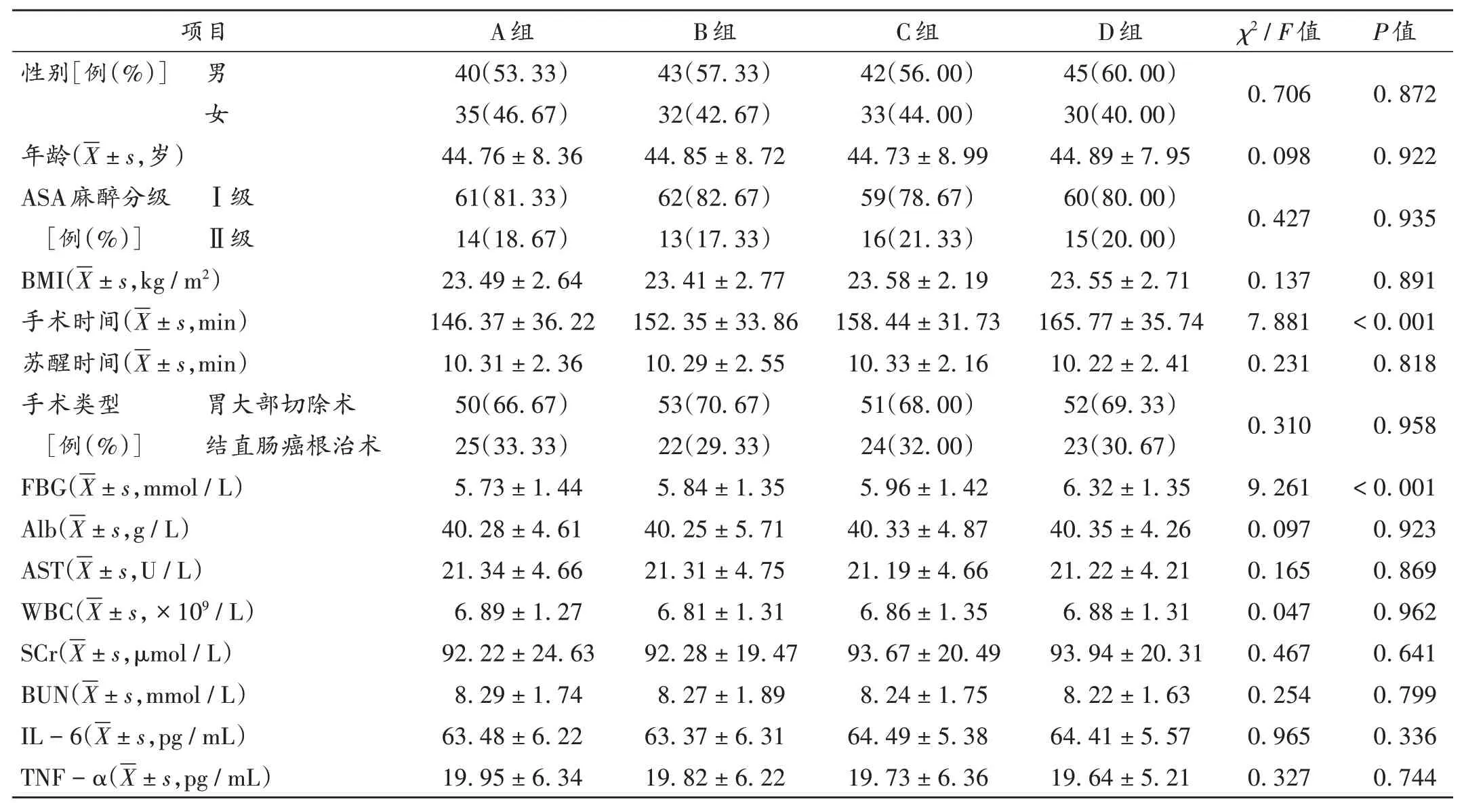
表2 4組患者臨床資料比較(n=75)Tab.2 Comparison of clinical data among the four groups(n = 75)
2.2 不同基因位點的SNP 比較
所有基因位點均經Hardy - Weinberg 平衡定律檢驗,達到遺傳平衡(P> 0.05)。4 組患者CYP3A4(rs2242480)、ABCB1(rs1045642)、COMT(rs4680)、OPRM1(rs1799971)不同基因型比例比較,差異均有統計學意義(P<0.05)。詳見表3。

表3 4組患者不同基因位點單核苷酸多態性比較(例)Tab.3 Comparison of SNP at different gene loci among the four groups(case)
2.3 舒芬太尼用量的相關影響因素分析
有序Logistic 回歸分析顯示,手術時間、FBG、CYP3A4(rs2242480)CT 基因型是腹腔鏡術后舒芬太尼用量的獨立影響因素(P<0.05)。詳見表4。

表4 有序Logistic回歸分析結果Tab.4 Results of the ordinal Logistic regression analysis
2.4 列線圖模型的構建與驗證
以獨立影響因素構建舒芬太尼用量的早期預測的列線圖模型(見圖1),總分0~200分,對應使用高用量舒芬太尼的概率為0.05~0.95。經過計算得出C-指數為0.915[95%CI(0.889,0.984)],且模型校準曲線(見圖2)與理想模型接近。ROC曲線分析顯示,列線圖模型在早期評估舒芬太尼用量的藥-時曲線下面積(AUC)為0.909,敏感性為82.67%,特異性為86.67%,詳見圖3。
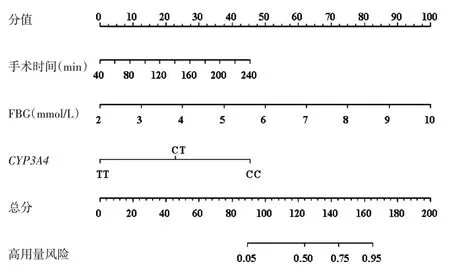
圖1 腹腔鏡術后舒芬太尼高用量評估列線圖模型Fig.1 Alignment diagram model for evaluating the high dosage of sufentanil after laparoscopic surgery
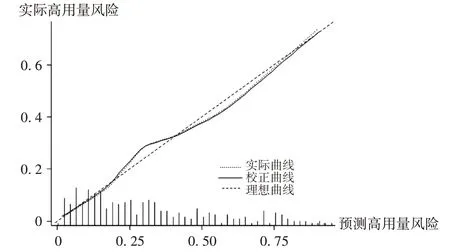
圖2 列線圖模型的內部校正曲線Fig.2 Internal calibration curve of the alignment diagram model

圖3 列線圖模型的早期預測效能的ROC曲線Fig.3 ROC curve of early prediction efficacy of alignment diagram model
3 討論
舒芬太尼為阿片類制劑中鎮痛效果較強的藥物,臨床廣泛用于術中麻醉、重癥監護室鎮靜鎮痛和術后鎮痛,具有起效迅速、清除率高且對呼吸系統影響小的優勢。有研究發現,不同個體之間舒芬太尼的有效鎮痛的血藥濃度差異可達50 倍[9]。這一發現提示遺傳學因素可能影響阿片類制劑在體內的作用發揮。相關研究表明,基因表達的差異能影響機體對疼痛的敏感性及術后鎮痛效果[10]。目前,臨床關于影響舒芬太尼鎮痛效應基因因素的研究較少,因此通過術前評估患者遺傳學差異進而預測患者對舒芬太尼鎮痛劑量的使用,對于指導臨床實踐具有積極意義。
本研究結果發現,患者手術時間越長,術前FBG 水平越高,術后24 h 內舒芬太尼總用量越大;多數情況下手術時間長意味著手術本身操作難度較大,術中造成的創傷就越大,術后就需更大劑量的鎮痛藥物緩解疼痛。相關研究也表明,手術時間長短與術后疼痛存在明顯相關性[11]。血糖方面,相關研究表明,高血糖可增強機體的痛覺敏感度,其機制可能是通過促炎、促氧化作用,上調機體傷害感受性離子通道,下調γ-氨基丁酸(GABA)神經元活性,減弱疼痛信號的傳遞,進而產生雙重痛覺過敏[12]。動物實驗發現,血糖急劇升高的模型大鼠對嗎啡的鎮痛作用反應遲鈍[13]。
在基因多態性方面,本研究結果顯示,4 組患者CYP3A4(rs2242480)、ABCB1(rs1045642)、COMT(rs4680)、OPRM1(rs1799971)的SNP均存在顯著差異,有序Logistic回歸分析顯示,僅CYP3A4(rs2242480)CT 基因型比例是腹腔鏡術后舒芬太尼用量的獨立影響因素。分析原因為:1)國外一項大規模測序研究發現,CYP3A4(rs2242480)是該基因SNP 突變頻率最高的位點,中國人群中突變頻率為22.1%~37%[14]。研究發現,舒芬太尼的體內代謝均由CYP3A4(rs2242480)所表達的蛋白酶負責,直接影響舒芬太尼在體內的清除率,同時發現,CYP3A4(rs2242480)的基因型突變可降低CYP3A4蛋白酶活性,降低舒芬太尼在體內代謝速率[15]。CYP3A4(rs2242480)的野生型純合子(CC)表達的酶活性明顯高于突變型雜合子(CT)和突變型純合子(TT)。許多臨床研究也指出,CYP3A4(rs2242480)TT基因型或CT 基因型的患者術后24,48 h 舒芬太尼消耗量明顯降低[16-17]。COMT 是體內兒茶酚胺代謝的主要作用酶類,主要調控體內兒茶酚胺的產生和腦啡肽水平。
COMT編碼區有6個SNP,其中COMT(rs4680)的突變率最高可達40%[18]。研究表明,COMT(rs4680)的突變可降低COMT蛋白酶的熱穩定性,導致體內兒茶酚胺代謝失衡,使患者疼痛敏感性增加,耐受力降低[6]。也有研究將此基因的突變情況作為評估患者對疼痛承受力和反應方式的一項指標[19]。韓國的一項研究表明,ABCB1的SNP 與舒芬太尼的鎮靜效應之間存在相關性,特別是ABCB1(rs1045642)的C > T 突變能明顯降低術后舒芬太尼用量[20]。有研究指出,ABCB1(rs1045642)的C > T突變可能通過影響舒芬太尼的轉運、吸收、清除,進而引起藥物效能的差異,同時也指出這種作用機制仍待進一步研究[7]。OPRM1(rs1799971)是該基因最常見的突變位點,有研究指出,該位點的突變能降低阿片類藥物的效能,且攜帶GG 基因型的患者需更多的阿片類藥物鎮痛才能達到效果[8]。但本研究結果顯示,ABCB1(rs1045642)、COMT(rs4680)、OPRM1(rs1799971)的SNP與舒芬太尼用量之間不存在獨立相關性,考慮可能與樣本量較小且僅針對漢族人群有關,具有一定的局限性。
ROC 曲線分析顯示,列線圖模型在早期評估舒芬太尼用量的AUC為0.909,敏感性為82.67%,特異性為86.67%。這一結果給臨床早期評估術中、術后舒芬太尼用量提供了科學的參考依據。
綜上所述,CYP3A4(rs2242480)的SNP 與腹腔鏡術后舒芬太尼鎮痛用量有關,術前檢測患者的基因分型對于指導臨床個體化使用舒芬太尼具有重要意義。

