PD-1抑制劑聯合白蛋白結合型紫杉醇、鉑類藥物治療晚期食管癌的臨床研究
張文兵 劉潔 何文霞 陳敬 曹輝
【摘要】 目的:探討程序性死亡受體1(PD-1)抑制劑聯合白蛋白結合型紫杉醇、鉑類治療晚期食管癌的臨床效果。方法:選取2020年12月—2022年12月淮南東方醫院集團總醫院收治的晚期食管癌患者82例,依照隨機數字表分為研究組和常規組,各41例。常規組采用白蛋白結合型紫杉醇、鉑類治療,研究組在常規組的基礎上另給予PD-1抑制劑治療。比較兩組臨床療效、不良反應、細胞角蛋白19片段(Cyfra 21-1)與鱗狀細胞癌抗原(SCCA)水平,隨訪1年,比較兩組無進展生存期(PFS)。結果:研究組的疾病控制率(DCR)、客觀緩解率(ORR)均高于常規組(P<0.05);與治療前相比,兩組Cyfra 21-1、SCCA均降低,且研究組較常規組均更低(P<0.05);兩組不良反應發生率比較,差異無統計學意義(P>0.05);研究組中位PFS長于常規組(P<0.05)。結論:PD-1抑制劑聯合白蛋白結合型紫杉醇、鉑類治療晚期食管癌患者的效果顯著,可降低Cyfra 21-1、SCCA水平,改善預后。
【關鍵詞】 晚期食管癌 程序性死亡受體1抑制劑 白蛋白結合型紫杉醇 鉑類
Clinical Study of PD-1 Inhibitor Combined with Albumin Bound Paclitaxel, Platinum in the Treatment of Advanced Esophagus Cancer/ZHANG Wenbing, LIU Jie, HE Wenxia, CHEN Jing, CAO Hui. //Medical Innovation of China, 2024, 21(11): 0-101
[Abstract] Objective: To investigate the clinical effect of programmed death-1 (PD-1) inhibitor combined with Albumin Bound Paclitaxel, Platinum in the treatment of advanced esophagus cancer. Method: A total of 82 patients with advanced esophagus cancer admitted to General Hospital of Huainan Oriental Hospital Group from December 2020 to December 2022 were selected and divided into study group and conventional group according to random number table, with 41 cases in each group. The conventional group was treated with Albumin Bound Paclitaxel and Platinum, and the study group was treated with PD-1 inhibitor on the basis of the conventional group. Clinical efficacy and adverse reactions, cytokeratin 19 fragment (Cyfra 21-1) and squamous cell carcinoma antigen (SCCA) levels were compared between the two groups, progression free survival (PFS) was compared between the two groups after 1 year of follow-up. Result: The disease control rate (DCR) and objective remission rate (ORR) in the study group were higher than those in the conventional group (P<0.05). Compared with before treatment, Cyfra 21-1 and SCCA were decreased in both groups, and those in study group were lower than those in conventional group (P<0.05). There was no significant difference in the incidence of adverse reactions between the two groups (P>0.05). The median PFS in study group was longer than that in conventional group (P<0.05). Conclusion: PD-1 inhibitor combined with Albumin Bound Paclitaxel, Platinum have a significant effect in the treatment of advanced esophagus cancer patients, which can reduce Cyfra 21-1 and SCCA levels and improve prognosis.
[Key words] Advanced esophagus cancer Programmed death-1 inhibitor Albumin Bound Paclitaxel Platinum
First-author's address: Department of Medical Oncology, General Hospital of Huainan Oriental Hospital Group, Huainan 232001, China
doi:10.3969/j.issn.1674-4985.2024.11.022
食管癌是一種臨床上較為多見的消化系統惡性腫瘤,調查結果顯示,我國食管癌死亡率居于惡性腫瘤第4位,發病率居于第6位,死亡病例數與新發例數約占全球50%,嚴重威脅患者的生命安全[1-2]。食管癌具有癥狀隱匿、復發率高、轉移率高等特點,大部分患者確診時已為中晚期,加之中老年人合并基礎疾病較多、身體功能較差,造成多數中老年局部晚期食管癌患者難以進行手術治療[3]。由于鉑類化療藥物臨床副作用較多,且療程較長,患者在治療期間容易出現耐藥性,因此臨床療效有限[4]。局部控制率不理想是晚期食管癌患者死亡率居高不下的重要原因[5],故如何提高晚期食管癌的局部控制率仍然是臨床工作者的研究熱題。白蛋白結合型紫杉醇具有良好的水溶性,可在一定程度上減少不良反應[6]。信迪利單抗通過抑制免疫檢查點分子程序性死亡受體1(PD-1)與其配體[程序性死亡受體配體1(PD-L1)]的結合,從而增強患者自身免疫系統對癌細胞的攻擊能力[7]。然而,PD-1抑制劑聯合白蛋白結合型紫杉醇、鉑類的治療效果尚不清楚,鑒于此,本研究選取晚期食管癌患者進行對照分析,以探究其療效。
1 資料與方法
1.1 一般資料
選取2020年12月—2022年12月淮南東方醫院集團總醫院收治的晚期食管癌患者82例。(1)納入標準:①參照文獻[8]《食管癌規范化診治指南》,符合食管癌診斷標準,且經病理學確診;②生存期>6個月。(2)排除標準:①意識不清;②主動放棄治療;③依從性差;④合并其他惡性腫瘤。依照隨機數字表分為兩組,各41例。本研究通過本院醫學倫理委員會審批。患者或家屬簽署知情同意書。
1.2 方法
常規組給予白蛋白結合型紫杉醇、鉑類治療。靜滴注射用奈達鉑(生產廠家:江蘇奧賽康藥業股份有限公司,批準文號:國藥準字H20143132,規格:100 mg)80~100 mg/m2,每個周期的第1天用藥;靜滴白蛋白結合型紫杉醇(生產廠家:石藥集團歐意藥業有限公司,批準文號:國藥準字H20183044,規格:100 mg)260 mg/m2,每個周期的第1天用藥。21 d為1個周期,治療3個周期。
研究組在常規組基礎上另給予PD-1抑制劑信迪利單抗[生產廠家:信達生物制藥(蘇州)有限公司,批準文號:國藥準字S20180016,規格:100 mg(10 mL)/瓶],200 mg/次,每個周期1次,21 d為1個周期,用藥至疾病進展或毒性不耐受。
1.3 觀察指標及判定標準
(1)比較兩組患者客觀緩解率(ORR)和疾病控制率(DCR)。治療3個周期后1個月,參照修訂的實體瘤療效評價標準(RECIST)指南(1.1版)評估。完全緩解(CR):所有病灶完全消失;部分緩解(PR):基線病灶長徑總和縮小30%以上;疾病穩定(SD):基線病灶長徑總和縮小但未達到PR或病灶增大但未達到PD;疾病進展(PD):基線病灶長徑總和增大20%以上或出現新病灶[9]。ORR=(CR+PR)例數/總例數×100%,DCR=(CR+PR+SD)例數/總例數×100%。(2)比較兩組患者血清細胞角蛋白19片段(Cyfra 21-1)和鱗狀細胞癌抗原(SCCA)水平。治療前后空腹采集靜脈血3 mL,離心分離血清,采用酶聯免疫吸附試驗(ELISA)測定。(3)不良反應。記錄患者治療期間出現的不良反應。(4)比較兩組無進展生存期(PFS)。所有患者自首次用藥開始,隨訪12個月,治療結束后每3個月定期復查1次,對患者的PFS進行統計。
1.4 統計學處理
用SPSS 22.0軟件分析。以(x±s)表示計量資料,組間比較用獨立樣本t檢驗,組內比較用配對t檢驗;計數資料以率(%)描述,以字2檢驗;采用Kaplan-Meier法繪制生存曲線。P<0.05表示差異有統計學意義。
2 結果
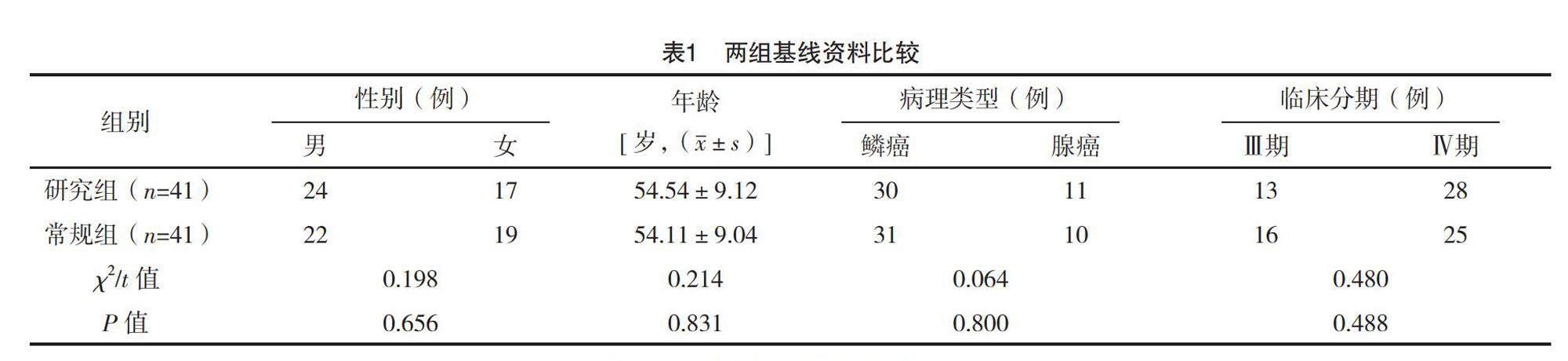
2.1 兩組基線資料比較
兩組性別、年齡等基線資料比較,差異均無統計學意義(P>0.05),具有可比性,見表1。
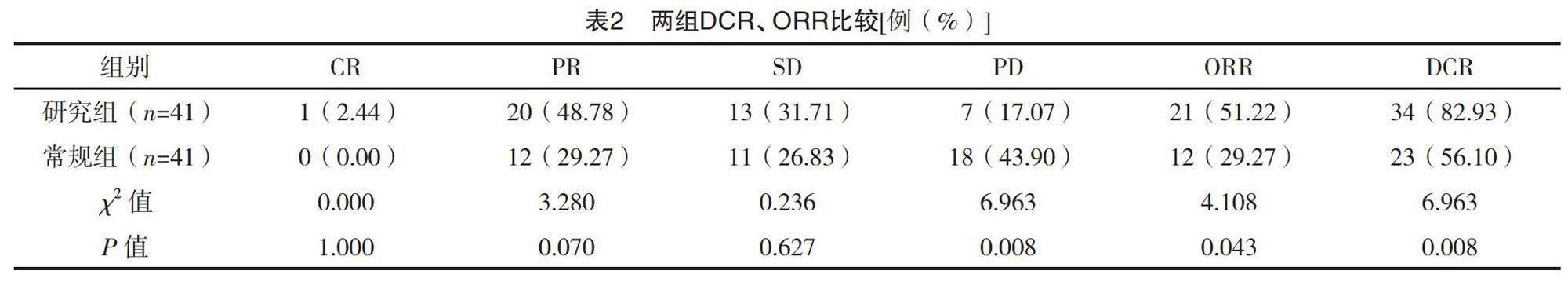
2.2 兩組DCR、ORR比較
研究組的DCR、ORR均高于常規組(P<0.05),見表2。
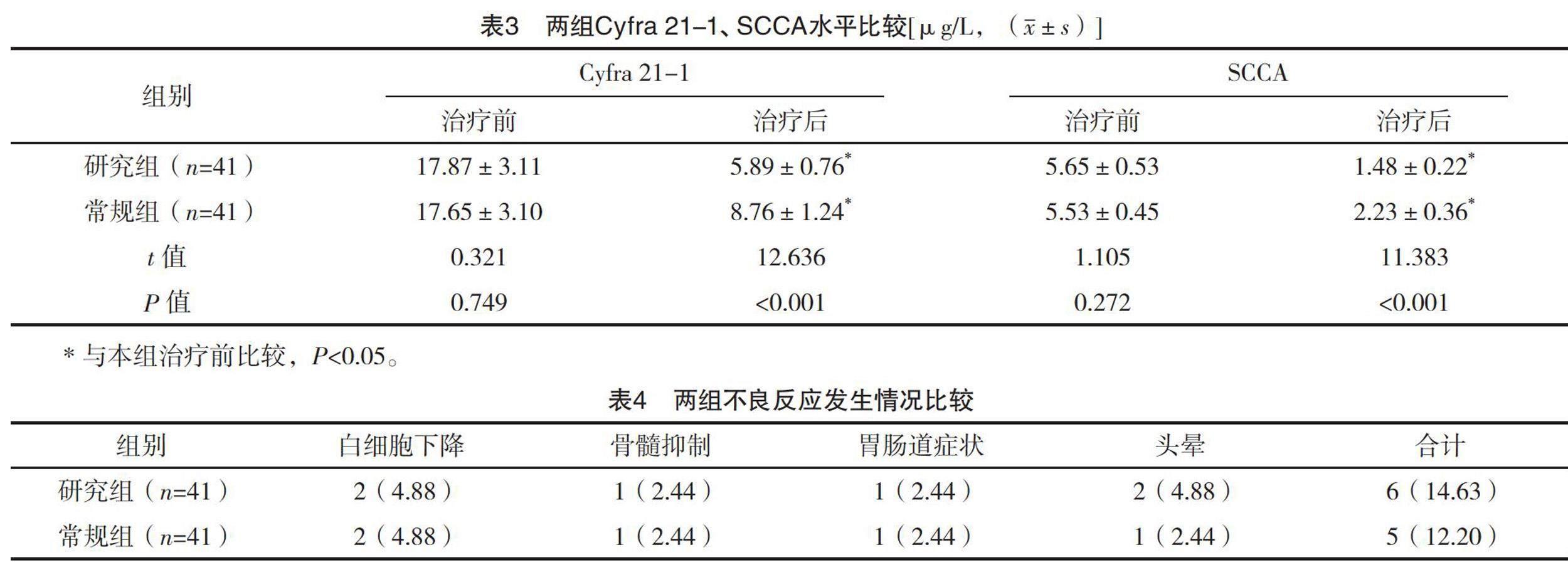
2.3 兩組Cyfra 21-1、SCCA水平比較
治療前,兩組Cyfra 21-1、SCCA比較,差異均無統計學意義(P>0.05);與治療前相比,兩組Cyfra 21-1、SCCA均降低,且研究組較常規組均更低(P<0.05)。見表3。
2.4 兩組不良反應發生情況
兩組不良反應發生率比較,差異無統計學意義(字2=0.105,P=0.746),見表4。
2.5 兩組PFS比較
研究組和常規組中位PFS分別為8.09個月[95%CI(7.12,9.23)]和6.12個月[95%CI(5.87,7.89)],研究組中位PFS長于常規組(P<0.05),見圖1。
3 討論
目前,食管癌病因尚不明確,遺傳、長期飲酒吸煙、飲食習慣不良等都可能導致該病發生。近年來,隨著生活水平的提升,食管癌發生率也不斷增加,且臨床死亡率較高,嚴重威脅患者生命健康[10]。化療是臨床不能進行手術治療食管癌患者的首選療法,但長期用藥不良反應較多,且容易產生耐藥性。PD-1是一種可抑制免疫應答激活的蛋白,可表達于活化T細胞、B細胞、自然殺傷細胞、單核細胞等細胞表面[11]。信迪利單抗是PD-1抑制劑,通過抑制PD-1與其配體結合,促進免疫應答作用,增強免疫功能,從而促進T細胞對腫瘤細胞的殺傷作用[12]。
本研究發現,研究組的DCR、ORR均高于常規組,提示PD-1抑制劑聯合白蛋白結合型紫杉醇、鉑類治療晚期食管癌患者的效果確切。PD-1是一種免疫檢查點受體,可以通過與其配體PD-L1或PD-L2結合,抑制活化的自然殺傷細胞、T細胞、巨噬細胞和B細胞的免疫反應,增強機體對自身抗原的耐受性[13-14]。鑒于藥物能夠通過白蛋白的引導進入腫瘤細胞區域,白蛋白結合型紫杉醇因而能夠實現更為精確的腫瘤細胞靶向,從而顯著減輕對健康細胞的潛在傷害[15-20]。因此,PD-1抑制劑聯合白蛋白結合型紫杉醇、鉑類能夠增強抗腫瘤作用,提高化療效果。本研究治療后研究組血清SCCA、Cyfra 21-1水平均低于常規組,且患者不良反應未明顯增加,說明PD-1抑制劑聯合白蛋白結合型紫杉醇、鉑類治療晚期食管癌患者能夠降低SCCA、Cyfra 21-1水平,且安全可靠。本研究研究組PFS較長,說明聯合用藥治療晚期食管癌患者能夠改善預后。
綜上,晚期食管癌患者采用PD-1抑制劑聯合白蛋白結合型紫杉醇、鉑類治療能夠緩解臨床癥狀,提高臨床療效,安全可靠,且能延長PFS。
參考文獻
[1] HE F,WANG J,LIU L,et al.Esophageal cancer: trends in incidence and mortality in China from 2005 to 2015[J].Cancer Med, 2021,10(5):1839-1847.
[2] FAN J,LIU Z,MAO X, et al.Global trends in the incidence and mortality of esophageal cancer from 1990 to 2017[J].Cancer Med,2020,9(18):6875-6887.
[3] MORAL G I,VIANA MIGUEL M,VIDAL DOCE ?,et al.
Postoperative complications and survival rate of esophageal cancer: two-period analysis[J].Cir Esp (Engl Ed),2018,96(8):473-481.
[4]何小平,曾小飛,陸宇海,等.西妥昔單抗配合化療方案治療老年晚期食管癌療效及對患者PI3K/AKT信號通路的干預作用[J].中國老年學雜志,2022,42(13):3162-3166.
[5] ILIC M,KOCIC S,RADOVANOVIC D,et al.Trend in esophageal cancer mortality in Serbia, 1991-2015 (a population-based study): an age-period-cohort analysis and a join point regression analysis[J].J BUON,2019,24(3):1233-1239.
[6] ZHAO W,ZHAO J,KANG L,et al.Fluoroscopy-guided salvage photodynamic therapy combined with Nanoparticle Albumin-Bound Paclitaxel for locally advanced esophageal cancer after chemoradiotherapy: a case report and literature review[J].Cancer Biother Radiopharm,2021,33(5):945-949.
[7] SANTOMASSO B D,NASTOUPIL L J,ADKINS S,et al.
Management of immune-related adverse events in patients treated with chimeric antigen receptor T-cell therapy: ASCO guideline[J].
J Clin Oncol,2021,39(35):3978-3992.
[8]中國抗癌協會食管癌專業委員會.食管癌規范化診治指南[M].2版.北京:中國協和醫科大學出版社,2013:104-107.
[9] EISENHAUER E A,THERASSE P,BOGAERTS J,et al.New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[10] SUNG H,FERLAY J,SIEGEL R L,et al.Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2021,71(3):209-249.
[11] SALAS-BENITO D,CONDE E,TAMAYO-URIA I,et al.The mutational load and a T-cell inflamed tumour phenotype identify ovarian cancer patients rendering tumour-reactive T cells from PD-1+ tumour-infiltrating lymphocytes[J].Br J Cancer,2021,124(6):1138-1149.
[12] SONG H,LIU X L,JIANG L,et al.Current status and prospects of Camrelizumab, a humanized antibody against programmed cell death receptor 1[J]. Recent Pat Anticancer Drug Discov,2021,16(3):312-332.
[13] IWAMA S,KOBAYASHI T,YASUDA Y,et al.Immune checkpoint inhibitor-related thyroid dysfunction[J].Best Pract Res Clin Endocrinol Metab,2022,36(3):101660.
[14]張康梅,鄭智,朱偉.PD-1抑制劑治療終止后晚期食管癌患者后續治療的臨床研究[J].實用癌癥雜志,2021,36(12):1974-1976.
[15] TAN H,HU J,LIU S.Efficacy and safety of nanoparticle Albumin-bound Paclitaxel in non-small cell lung cancer: a systematic review and meta-analysis[J].Artif Cells Nanomed Biotechnol,2019,47(1):268-277.
[16] QIAO Y,CHEN C,YUE J,et al.Tumor marker index based on preoperative SCCA and CYFRA 21-1 is a significant prognostic factor for patients with resectable esophageal squamous cell carcinoma [J].Cancer Biomark,2019,25(3):243-250.
[17]許雨柔,鄒宜豐,蔡寧,等.晚期食管癌PD-1/PD-L1免疫檢查點抑制劑療法的Cochrane Meta分析[J].復旦學報(醫學版),2023,50(5):660-669,682.
[18]馬聰,陳慧靜,聶新,等.放療與否對一線應用PD-1抑制劑聯合化療治療Ⅳ期食管癌的影響[J].現代消化及介入診療,2022,27(9):1166-1170.
[19] TRAMONTANO L,CAVALIERE C,SALVATORE M,et al.
The role of non-gaussian models of diffusion weighted MRI in hepatocellular carcinoma: a systematic review[J].J Clin Med,2021,10(12):2641.
[20]季德林,馮克海, 謝韜.卡瑞利珠單抗+白蛋白紫杉醇+奈達鉑/順鉑治療老年晚期食管癌的臨床療效觀察[J].中國現代醫學雜志,2022,32(23):6-10.
(收稿日期:2024-02-03) (本文編輯:陳韻)

