山西省2024年普通高中學業水平考試模擬試題 化學(一)
李娜 閆曉曉
本試題分第玉卷和第域卷兩部分,第玉卷為選擇題,第域卷為非選擇題。滿分100分,考試時間60分鐘。
可能用到的相對原子質量:H 1 C 12 N 14 O 16 Na 23 Al 27 S 32 Cl 35.5 Mn 55
第玉卷選擇題(共60分)
一、選擇題:本題共15小題,每小題4分,共60分。在每小題給出的四個選項中,只有一項符合題目要求。
1.為了社會的可持續發展,“綠色化學”理念已經滲透到生產、生活的各個方面中。下列做法遵循“綠色化學”原則的是
A.化肥能使糧食增產,使用時多多益善
B.為降低成本,將化石燃料直接燃燒
C.開發高效氫能、太陽能等新型電動汽車,減少城市機動車尾氣污染

7.現代生活離不開方便實用的化學能源,有許多的化學能源是根據原電池的原理制造的。如圖為某小組為探究原電池原理所設計的裝置,下列說法錯誤的是

15.某化學小組為探究二氧化硫的制備與性質,設計了如下的實驗裝置,下列相關解釋正確的是
A.裝置D中酸性高錳酸鉀溶液紫紅色褪去,說明二氧化硫具有漂白性
B.裝置A中體現了濃硫酸的強氧化性
C.裝置Ⅰ名稱為:長頸漏斗
D.裝置C中澄清石灰水會變渾濁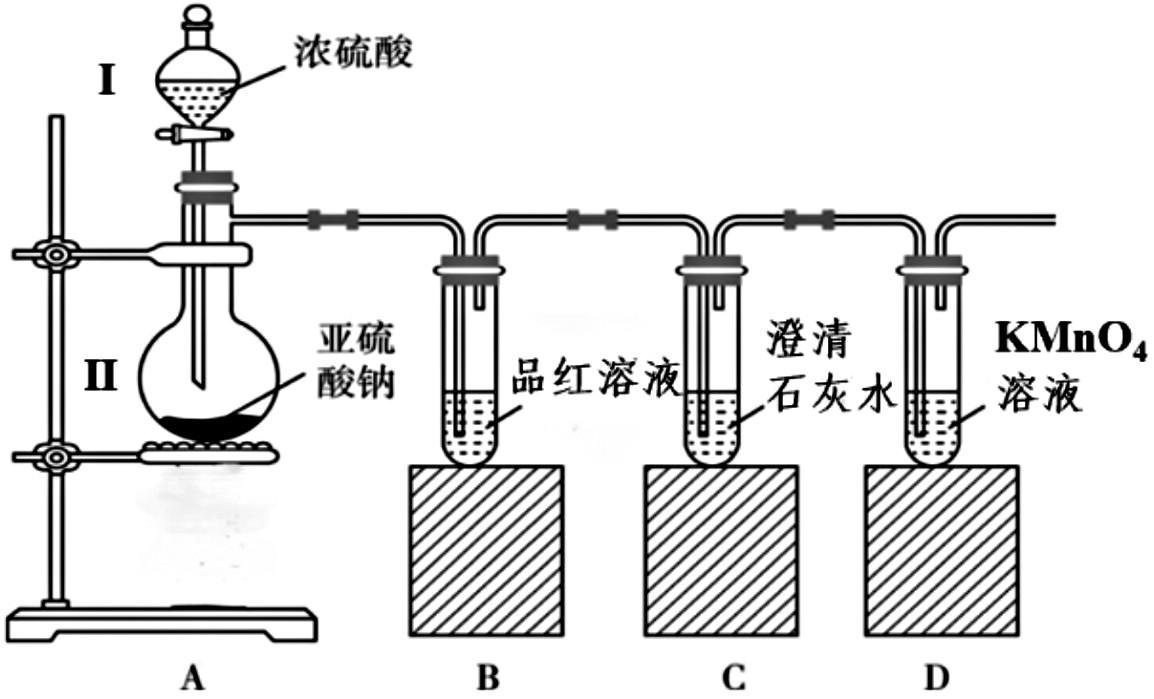
第域卷非選擇題(共40分)
二、非選擇題:本題共4小題,共40分。
16.(10分)元素周期表反映了元素之間的內在聯系,是學習、研究、應用化學的一個重要工具。下表為元素周期表的一部分,請回答下列問題。
(1)⑦元素的原子結構示意圖。
(2)⑤和⑥元素最高價氧化物對應水化物之間反應的離子方程式:。
(3)③、④、⑤和⑥元素的簡單離子半徑由大到小的順序:(填離子符號)。
(4)④和⑧分別與氫元素形成的簡單氫化物的熱穩定性大小為:(填化學式)。
(5)⑤和①形成的離子化合物可在野外用作生氫劑,請用化學方程式表示出原理:。
17.(10分)氯氣是一種重要的化工原料,大量用于制造鹽酸、有機溶劑、農藥、染料和藥品等。如圖為氯氣的制備與性質探究實驗。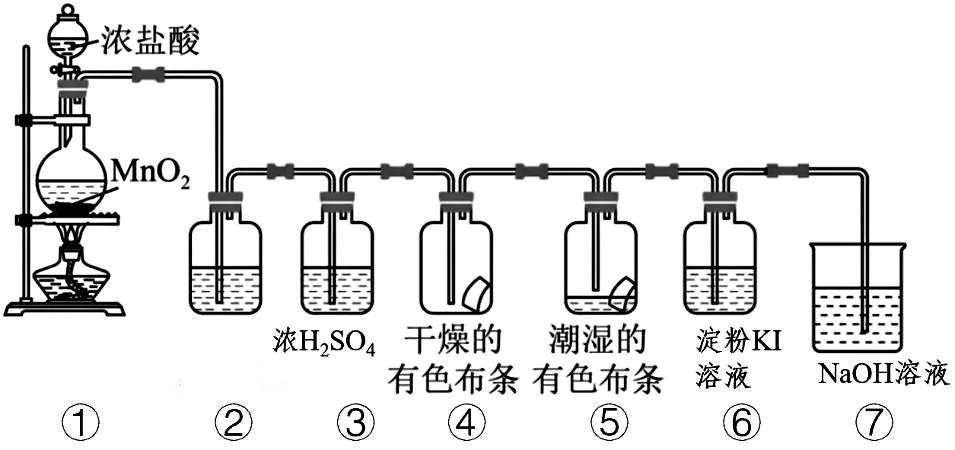
(1)裝置淤用來實驗室制備氯氣,請寫出離子方程式;盛放濃鹽酸的儀器名稱為。
(2)于中溶液為;盂中溶液的作用是;
(3)榆、虞的現象說明了。
(4)裝置愚的現象。
(5)0.87 g二氧化錳與足量的濃鹽酸混合加熱制取氯氣,則生成的氯氣在標準狀況下的體積是。
18援(10分)已知A物質是衡量一個國家石油化學工業發展水平的標志,也可用作催熟劑,在一定條件下能發生下圖所示的轉化關系。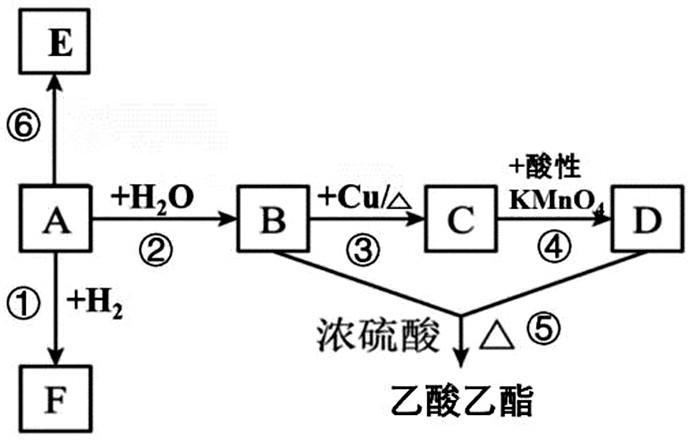
(1)寫出分子D的官能團名稱:;反應淤的反應類型:;
(2)C的結構簡式。

