基于SIRT1/PGC.1α信號(hào)通路探討抑眩寧顆粒干預(yù)缺血性眩暈的作用機(jī)制
王福榮 李明坤 劉志廣 馬金波
摘要 目的: 探討抑眩寧顆粒對(duì)沉默信息調(diào)節(jié)因子1(SIRT1)/過(guò)氧化物酶體增殖物激活受體γ輔激活因子1α(PGC.1α)信號(hào)通路的調(diào)控作用及對(duì)缺血性眩暈大鼠眩暈癥狀的改善作用。 方法: 對(duì)清潔級(jí)SD大鼠進(jìn)行電刺激逃避反射訓(xùn)練3 d后建立缺血性眩暈?zāi)P汀⒋笫蠓譃槟P徒M、抑眩寧顆粒組(6 g/kg)、SIRT1抑制劑(EX527)組(5 mg/kg)、抑眩寧顆粒+EX527組(抑眩寧顆粒6 g/kg+EX527 5 mg/kg),各組給予相應(yīng)藥物干預(yù)7 d;另取16只清潔級(jí)SD大鼠作為假手術(shù)組(進(jìn)行造模前訓(xùn)練,僅穿線不結(jié)扎)。采用跳臺(tái)逃避實(shí)驗(yàn)測(cè)定跳臺(tái)逃避潛伏期;多普勒激光血流儀測(cè)量大鼠前庭神經(jīng)核組織血流量,計(jì)算血流量下降率;蘇木精.伊紅染色觀察大鼠腦組織病理特征;酶聯(lián)免疫吸附法檢測(cè)大鼠腦組織丙二醛(MDA)、超氧化 物歧化酶(SOD)活性、一氧化氮(NO)、白細(xì)胞介素.1β(IL.1β)、 腫瘤壞死因子.α(TNF.α) 含量;蛋白免疫印跡法檢測(cè)大鼠腦組織SIRT1、PGC.1α、B淋巴細(xì) 胞瘤.2相關(guān)X蛋白(Bax)、B淋巴細(xì)胞瘤.2(Bcl.2) 蛋白表達(dá)水平。 結(jié)果: 與假手術(shù)組比較,模型組大鼠腦組織神經(jīng)細(xì)胞變形、固縮和凋亡,跳臺(tái)逃避潛伏期、 給藥后血流量下降率、腦組織MDA、NO、IL.1β、 TNF.α含量、Bax蛋白表達(dá)水平升高( P <0.05),SOD活性、SIRT1、PGC. 1α和Bcl.2蛋白表達(dá)水平降低( P <0.05)。 與模型組比較,抑眩寧顆粒組大鼠腦組織凋亡變異的細(xì)胞數(shù)量減少,膠質(zhì)周?chē)恼<?xì)胞數(shù)量增多,跳臺(tái)逃避潛伏期、給藥后血流量下降率、腦組織MDA、NO、IL.1β、TNF.α含量及Bax蛋白表達(dá)水平降低( P <0.05),SO D活性、SIRT1、PGC.1α和Bcl.2蛋白表達(dá)水平升高( P <0.05); EX527組大鼠腦組織神經(jīng)細(xì)胞嚴(yán)重變形,固縮和凋亡現(xiàn)象明顯,跳臺(tái)逃避潛伏期、給藥后血流量下降 率、腦組織MDA、NO、IL.1β、 TNF.α含量及Bax蛋白表達(dá)水平升高( P <0.05),SOD活性、SIRT1、PGC.1α和Bcl.2蛋白表達(dá)水平降低( P <0.05)。EX527可逆轉(zhuǎn)抑眩寧顆粒對(duì)缺血性眩暈大鼠的改善作用( P <0.05)。 結(jié)論: 抑眩寧顆粒可能通過(guò)激活SIRT1/PGC.1α通路、抑制氧化應(yīng)激和炎癥反應(yīng),進(jìn)而改善缺血性眩暈大鼠眩暈癥狀。
關(guān)鍵詞 ?缺血性眩暈;抑眩寧顆粒;沉默信息調(diào)節(jié)因子1/過(guò)氧化物酶體增殖物激活受體γ輔激活因子1α,SIRT1/PGC.1α;大鼠;實(shí)驗(yàn)研究
doi: ?10.12102/j.issn.1672.1349.2024.10.010
Mechanism of Yixuanning Granules on Ischemic Vertigo ?Based on SIRT1/PGC.1α Signaling Pathway
WANG Furong, LI Mingkun, LIU Zhiguang, MA Jinbo
Zhaogezhuang Hospital Kailuan General Hospital, Tangshan 063000, Hebei, China
Corresponding Author ?MA Jinbo, E.mail: 605088130@qq.com
Abstract Objective: To investigate the regulatory effect of Yixuanning granules on silencing information regulatory factor 1(SIRT1)/peroxisome proliferator.activated receptor γ.coactivator 1α(PGC.1α) signaling pathway and its improvement effect on vertigo symptoms of ischemic vertigo in rats. ?Methods: After 3 days of escape reflex training of electrical stimulation,rat model of ischemic vertigo was established,a nd the rats were divided into model group,Yixuanning granules group(6 g/kg),SIRT1 inhibitor(EX527) group (5 mg/kg), Yixuanning granules+EX527 group(Yixuanning granules 6 g/kg+EX527 5 mg/kg).Each group was given drug for 7 days.Another 16 rats were selected as sham group(pre.modeling training,only threading without ligature).The stage escape latency of rats was measured by the stage escape experiment.The blood flow in vestibular nucleus of rats was measured by Doppler laser blood flow analyzer,and the decreasing rate of blood flow was calculated.Hematoxylin.eosin staining was used to observe the pathological characteristics of rat brain.The activities of malondialdehyde(MDA),superoxide dismutase(SOD),nitric oxide(NO),interleukin.1β(IL.1β) and tumor necrosis factor.α(TNF.α) were detected by enzyme.linked immunosorbent assay(ELISA).The expressions of SIRT1 ,PGC.1α, B.lymphoblastoma.2.associated X protein(Bax) and B.lymphoblastoma.2(Bcl.2) in rat brain were detected by Western Blot. ?Results: Compared with sham group,brain nerve cells in the model group were deformable,constricted and apoptotic,stage escape latency blood flow rate decreased after administration,the activity of MDA,NO,IL.1β,TNF.α content and Bax protein expressions in cerebral tissue ?increased( P <0.05).SOD activity,SIRT1,PGC.1α and Bcl.2 protein expressions decreased( P <0.05).Compared with model group,the number of apoptotic cells in brain tissue of Yixuanning granules group decreased,the number of normal cells around glia increased significantly,the latency of stage escape,the decrease rate of blood flow after administration,the activity of MDA,NO,IL.1β,TNF.α content and Bax protein expressions in cerebral tissue ?decreased( P <0.05).SOD activity,SIRT1,PGC.1α and Bcl.2 protein expressions increased( P <0.05).Cerebral nerve cells in the EX527 group deformated severely,with obvious signs of contraction and apoptosis,and the activity of MDA,NO,IL.1β,TNF.α content and Bax protein expressions in brain tissue ?increased( P <0.05),SOD activity,SIRT1,PGC.1α and Bcl.2 protein expressions decreased( P <0.05).EX527 could reverse the improvement effect of Yixuanning granules on ischemic vertigo in rats( P <0.05). ?Conclusion: Yixuanning granules might improve vertigo symptoms of ischemic vertigo in rats by activating the SIRT1/PGC.1α pathway and inhibiting oxidative stress and inflammatory responses.
Keywords ?ischemic vertigo; Yixuanning granules; silencing information regulatory factor 1/peroxisome proliferator.activated receptor γ.coactivator 1α, SIRT1/PGC.1α; ?rats; experimental study
缺血性眩暈是臨床的常見(jiàn)病和多發(fā)病,具有多病因、多病機(jī)、病位廣、難診斷、難根治等特點(diǎn),中醫(yī)藥治療效果顯著且作用持久 ?[1] 。其中抑眩寧顆粒是治療缺血性眩暈的常用藥物,主要功效為平肝潛陽(yáng)、降火滌痰、養(yǎng)血健脾、祛風(fēng)清熱;主要適應(yīng)證為肝陽(yáng)上亢、氣血兩虛型眩暈癥,但其中的藥理機(jī)制尚未明確。沉默信息調(diào)節(jié)因子1(silent information regulator 1,SIRT1)在較多神經(jīng)退行性疾病中發(fā)揮神經(jīng)保護(hù)作用,過(guò)氧化物酶體增殖物激活受體γ輔激活因子1α(peroxisome proliferator activated ?receptor γ coactivator.1α,PGC.1α) 水平升高,可減輕氧化應(yīng)激、炎癥反應(yīng),消除活性氧,同時(shí)使SIRT1和PGC.1α蛋白表達(dá)增加,激活SIRT1及其下游抗氧化防御機(jī)制,減輕糖尿病大鼠心肌病變 ?[2] 。激活SIRT1可提高PGC.1α去乙酰化,降低腦缺血再灌注大鼠死亡率,改善行為學(xué)障礙和神經(jīng)元凋亡 ?[3] 。其中,褪黑素通過(guò)激活SIRT1/PGC.1α通路減輕鉻誘導(dǎo)的肺損傷 ?[4] ,姜黃素通過(guò)激活SIRT1/PGC.1α通路減輕異煙肼誘導(dǎo)的肝毒性 ?[5] 。抑眩寧顆粒是否通過(guò)SIRT1/PGC.1α通路改善缺血性眩暈大鼠眩暈癥狀的研究較少。本研究通過(guò)構(gòu)建缺血性眩暈大鼠模型,使用抑眩寧顆粒和SIRT1抑制劑(EX527)干預(yù),旨在從SIRT1/PGC.1α通路揭示抑眩寧顆粒對(duì)缺血性眩暈大鼠眩暈癥狀的改善作用,為抑眩寧顆粒在臨床應(yīng)用于缺血性眩暈的治療提供實(shí)驗(yàn)依據(jù)。
1 材料與方法
1.1 實(shí)驗(yàn)材料
1.1.1 實(shí)驗(yàn)動(dòng)物
清潔級(jí)SD大鼠,雌雄各半,5~7周齡,體質(zhì)量180~200 g,購(gòu)自長(zhǎng)沙市天勤生物技術(shù)有限公司,許可證號(hào):SCXK(湘)2019.0027。飼養(yǎng)條件:溫度22 ℃,濕度55%,12 h光暗循環(huán)。本研究經(jīng)開(kāi)灤總醫(yī)院趙各莊醫(yī)院倫理委員會(huì)批準(zhǔn)。
1.1.2 實(shí)驗(yàn)藥物與試劑
抑眩寧顆粒(批號(hào)20220127)購(gòu)自通化茂祥制藥有限公司,SIRT1抑制劑(EX527,批號(hào)49843.98.3)購(gòu)自美國(guó)Selleck公司;蘇木精.伊紅(HE)染液、二喹啉甲酸(BCA)蛋白檢測(cè)試劑盒、電化學(xué)發(fā)光(ECL)顯色試劑盒(批號(hào)分別為SW.2398、SW.3783、SW.2387)均購(gòu)自北京中山金橋生物科技有限公司;蛋白提取試劑盒、超氧化物歧化酶(SOD)、丙二醛(MDA)、一氧化氮 (NO)、白細(xì)胞介素.1β(IL.1β)、腫瘤壞死因子.α(TNF.α) 酶聯(lián)免疫吸附(ELISA)試劑盒(批號(hào)分別為ML91627、ML012634、 ML012784、ML034782、ML047392、ML013476) 均購(gòu)自上海酶聯(lián)生物科技有限公司;兔源β.肌動(dòng)蛋白(β.actin)、SIRT1、PGC.1α、B淋巴細(xì)胞瘤.2相關(guān)X蛋白(Bax)、B淋巴細(xì)胞瘤.2(Bcl.2)、羊抗兔二抗(批號(hào)分別為ZM1016、ZM2390、ZM2493、ZM3489、ZM2479、ZM3478)均購(gòu)自北京四正柏生物科技有限公司。
1.1.3 實(shí)驗(yàn)儀器
跳臺(tái)記錄儀(型號(hào)YLS.3Tb)購(gòu)自上海軟隆科技發(fā)展有限公司;腦立體定位儀(型號(hào)ALC.H)、多普勒激光血流儀(型號(hào)LDI2)、離心機(jī)(型號(hào)5418R)均購(gòu)自上海玉研科學(xué)儀器有限公司;光學(xué)顯微鏡(型號(hào)ML11)、酶標(biāo)儀(型號(hào)EnVision)均購(gòu)自北京瑞宇科技有限公司;蛋白凝膠成像系統(tǒng)(型號(hào)JY.04)購(gòu)自上海菲特科學(xué)器材有限公司。
1.2 方法
1.2.1 造模前訓(xùn)練
造模前對(duì)大鼠進(jìn)行電刺激逃避反射訓(xùn)練,將大鼠置入跳臺(tái)儀中,適應(yīng)3 min后給予強(qiáng)度為30 V、50 Hz的電刺激,當(dāng)大鼠跳上跳臺(tái)并保持30 s為訓(xùn)練成功,每日訓(xùn)練2次 ,連續(xù)3 d,建立穩(wěn)定的逃避刺激條件反射。
1.2.2 缺血性眩暈大鼠模型的建立、分組及給藥
第4天選取訓(xùn)練成功的大鼠,采用結(jié)扎右側(cè)頸總動(dòng)脈和右側(cè)鎖骨下動(dòng)脈構(gòu)建缺血性眩暈大鼠模型 ?[6] :大鼠腹腔注射戊巴比妥鈉麻醉,在腦立體定位儀上仰臥固定,切開(kāi)頸部皮膚,暴露右側(cè)頸總動(dòng)脈并穿線備用。沿右側(cè)頸總動(dòng)脈近心端找到右側(cè)鎖骨下動(dòng)脈分叉處,剝離周?chē)M織,穿線備用。平顱頭位,定位大鼠右側(cè)前庭神經(jīng)核,切正中頭皮1.5 cm切口,過(guò)氧化氫灼皮暴露前囟,用牙科鉆鉆孔,使之可容納激光探頭;采用多普勒激光血流儀測(cè)定大鼠右前庭神經(jīng)核組織血流量,待血流平穩(wěn)后,結(jié)扎右側(cè)頸總動(dòng)脈和鎖骨下動(dòng)脈,術(shù)后肌肉注射抗生素預(yù)防感染。大鼠腦血流量明顯下降且次日仍存活視為造模成功 ?[6] 。
將造模成功的64只大鼠按照隨機(jī) 數(shù)字表法分為模型組、抑眩寧顆粒組(6 g/kg) ?[7] 、EX527組(5 mg/kg) ?[8] 、 抑眩寧顆粒+EX527組(抑眩寧顆粒6 g/kg+EX527 5 mg/kg),每組16只。另取16只大鼠作為假手術(shù)組(進(jìn)行造模前訓(xùn)練,僅穿線不結(jié)扎)。造模成功后開(kāi)始給藥,抑眩寧顆粒組給予大鼠6 g/kg的抑 眩寧顆粒灌胃(將抑眩寧顆粒和蒸餾水配制成濃度為0.6 g/mL的混懸液,灌胃體積10 mL/kg) ?[7] ?;EX527組給予大鼠腹腔注射5 mg/kg的EX527 ?[8] ;抑眩寧顆粒+EX527組給予大鼠6 g/kg的抑眩寧顆粒灌胃給藥,同時(shí)腹腔注射5 mg/kg的EX527;模型組和假手術(shù)組灌胃等量蒸餾水。每日1次,連續(xù)給藥7 d。給藥期間,EX527組2只大鼠死亡,其余各組所有大鼠均存活。
1.2.3 跳臺(tái)逃避實(shí)驗(yàn)測(cè)定大鼠跳臺(tái)逃避潛伏期
給藥周期結(jié)束后,大鼠置入500 r/min的離心機(jī)勻速轉(zhuǎn)動(dòng)30 s,立即放入跳臺(tái)儀中,記錄從大鼠受到強(qiáng)度為30 V、50 Hz的電刺激到第1次跳上平臺(tái),且30 s內(nèi)不跌落所需的時(shí)間(不包含在平臺(tái)上的時(shí)間),即為跳臺(tái)逃避潛伏期。
1.2.4 多普勒激光血流儀測(cè)定大鼠前庭神經(jīng)核組織血流量
使用多普勒激光血流儀測(cè)量各組大鼠結(jié)扎前20 min、結(jié)扎后20 min(給藥前)、給藥7 d后(給藥后)的前庭神經(jīng)核組織血流量,計(jì)算血流量下降率。給藥前血流量下降率(%)=(結(jié)扎前20 min血流量-結(jié)扎后20 min血流量)/結(jié)扎前20 min血流量×100%;給藥后血流量下降率(%)=(結(jié)扎前20 min血流量-給藥7 d后血流量)/結(jié)扎前20 min血流量×100%。
1.2.5 HE染色觀察大鼠腦組織病理變化
隨機(jī)取EX527組7只大鼠,其余各組分別隨機(jī)取8只大鼠,處死大鼠,獲取腦組織標(biāo)本,采用10%甲醛中性緩沖液固定,分別用75%、85%、95%和100%濃度梯度的乙醇脫水(每次5 min),之后用二甲苯清洗3次(每次5 min),石蠟包埋,切成4 μm厚的薄片,置于60 ℃培養(yǎng)箱中孵育1 h,冷卻后再次使用不同濃度梯度的乙醇脫水,蘇木精染色7 min,洗滌,鹽酸乙醇分化5 s,伊紅浸泡1 min,使用中性樹(shù)脂固定后通風(fēng),將切片置于光學(xué)顯微鏡下觀察腦組織的病理變化。
1.2.6 ELISA法檢測(cè)大鼠腦組織MDA、SOD活性、NO、IL.1β、TNF.α含量
將EX527組剩余的7只大鼠,其余各組剩余的8只大鼠,斷頭取腦,將右側(cè)半腦的腦組織清洗干燥后,稱(chēng)重0.5 g(剩余部分迅速置入-80 ℃冰箱中用于后續(xù)實(shí)驗(yàn)),制成組織勻漿,離心分離上清液按相關(guān)指標(biāo)的ELISA試劑盒說(shuō)明書(shū),分別測(cè)定SOD活性、MDA、NO、IL.1β、TNF.α含量。
1.2.7 ?蛋白免疫印跡法檢測(cè)大鼠腦組織SIRT1、PGC.1α、 Bax、Bcl.2蛋白表達(dá)水平
取-80 ℃保存的剩余大鼠腦組織,解凍勻漿,蛋白提取試劑盒提取腦組織總蛋白,定量蛋白濃度, 進(jìn)行電泳、轉(zhuǎn)膜,加入兔源SIRT1(1∶750)、PGC.1α(1∶700)、 Bax(1∶1 750)、Bcl.2(1∶1 350)、β.actin(1∶730)一抗,4 ℃過(guò)夜孵育,加入羊抗兔二抗(1∶2 150)室溫孵育1.5 h,使用ECL試劑盒顯色,Image.J軟件分析蛋白相對(duì)表達(dá)水平。
1.3 統(tǒng)計(jì)學(xué)處理
采用SPSS 26.0統(tǒng)計(jì)學(xué)軟件對(duì)數(shù)據(jù)進(jìn)行分析,符合正態(tài)分布的定量資料以均數(shù)±標(biāo)準(zhǔn)差( x ?± s )表示,多組間比較采用單因素方差分析,兩組間比較采用SNK. q 檢驗(yàn)。以 P <0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié) 果
2.1 各組大鼠跳臺(tái)逃避潛伏期比較
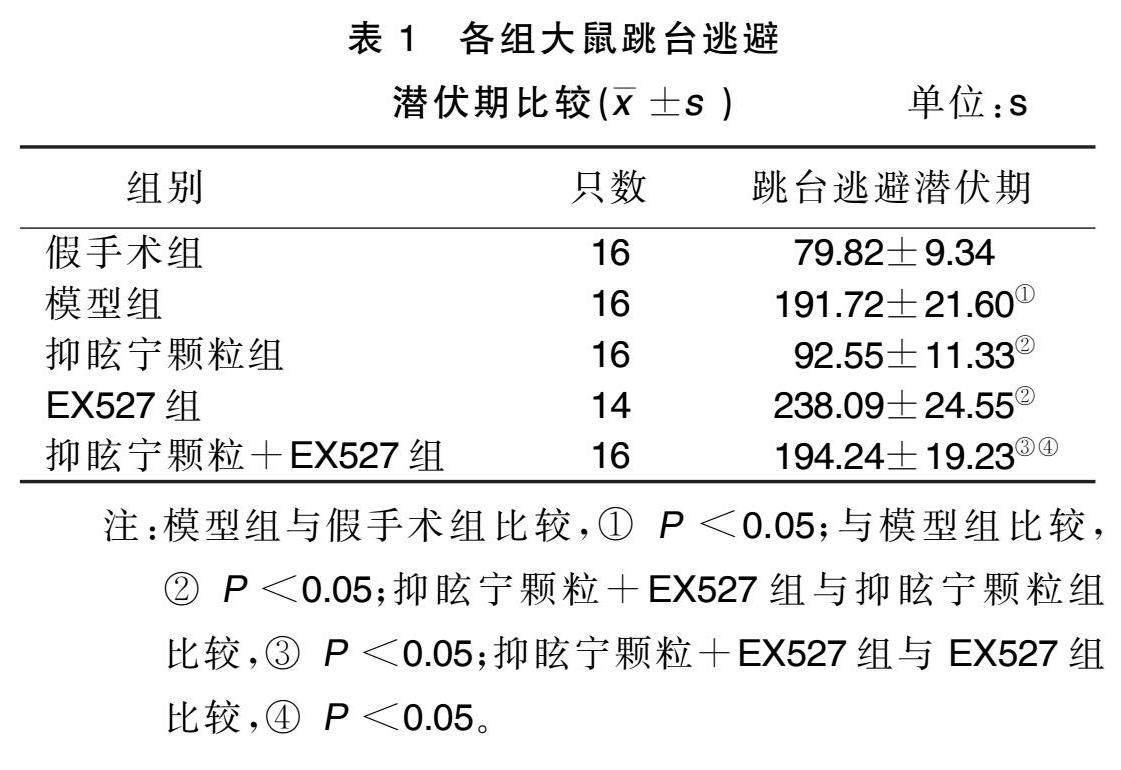
與假手術(shù)組比較,模型組大鼠跳臺(tái)逃避潛伏期延長(zhǎng)( P <0.05);與模型組比較,抑眩寧顆粒組大鼠跳臺(tái)逃避潛伏期縮短( P <0.05),EX527組大鼠跳臺(tái)逃避潛伏期延長(zhǎng)( P <0.05);與抑眩寧顆粒組比較,抑眩寧顆粒+EX527 組大鼠跳臺(tái)逃避潛伏期延長(zhǎng)( P <0.05); 與EX527組比較,抑眩寧顆粒+EX527組大鼠跳臺(tái)逃避潛伏期縮短( P <0.05)。詳見(jiàn)表1。
2.2 各組大鼠前庭神經(jīng)核組織血流量下降率比較
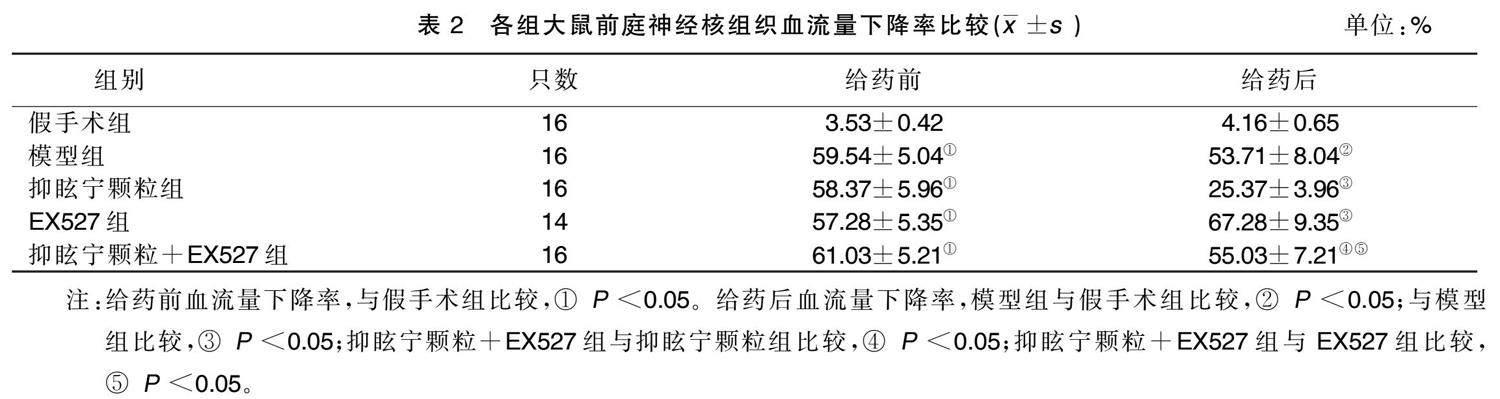
與假手術(shù)組比較,模型組和各給藥組給藥前血流量下降率升高( P <0.05)。與假手術(shù)組比較,模型組大鼠給藥后血流量下降率升高( P <0.05);與模型組 比較,抑眩寧顆粒組大鼠給藥后血流量下降率降低 ( P <0.05),EX527組大鼠給藥后血流量下降率升高( P <0.05);與抑眩寧顆粒組比較,抑眩寧顆粒+EX527組大鼠給藥后血流量下降率升高( P <0.05);與EX527組比較,抑眩寧顆粒+EX527組大鼠給藥后血流量下降率降低( P <0.05)。詳見(jiàn)表2。
2.3 各組大鼠腦組織病理變化
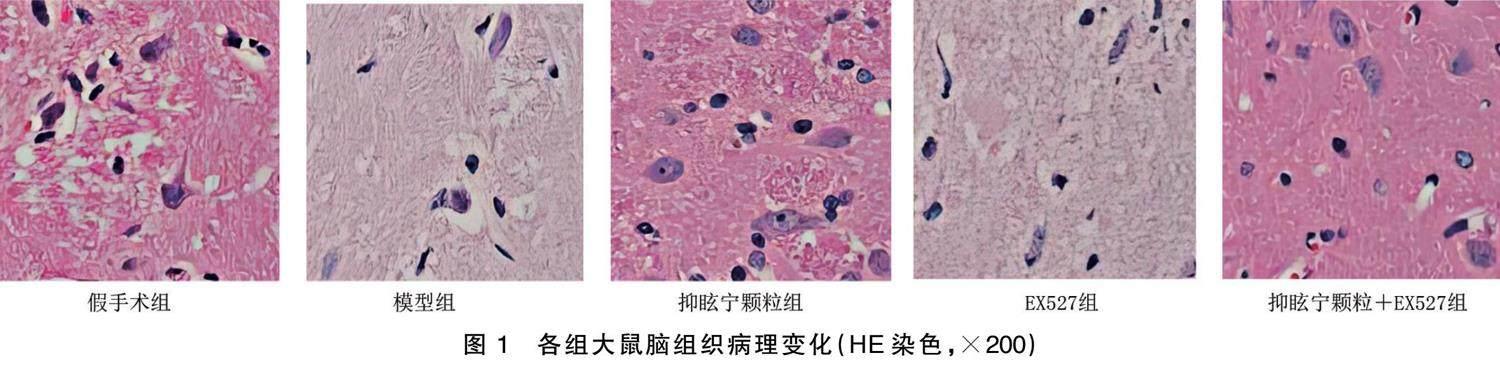
對(duì)照組大鼠腦組織可見(jiàn)明顯的多級(jí)神經(jīng)元和粗大的尼氏體,大量正常細(xì)胞;模型組大鼠腦組織神經(jīng)細(xì)胞變形、固縮和凋亡;抑眩寧顆粒組大鼠腦組織中凋亡變異的細(xì)胞數(shù)目減少,膠質(zhì)周?chē)恼<?xì)胞數(shù)量增多;EX527組大鼠腦組織神經(jīng)細(xì)胞嚴(yán)重變形,固縮和凋亡現(xiàn)象顯著;抑眩寧顆粒+EX527組大鼠腦組織神經(jīng)細(xì)胞形態(tài)較EX527組改善,細(xì)胞固縮和凋亡現(xiàn)象緩解。詳見(jiàn)圖1。
2.4 各組大鼠腦組織SOD活性及MDA、NO、IL.1β、TNF.α含量比較
與假手術(shù)組比較,模型組大鼠腦組織MDA及NO、IL.1β、TNF.α含量升高( P <0.05),SOD活性降低( P <0.05);與模型組比較,抑眩寧顆粒組大鼠腦組織MDA及NO、IL.1β、TNF.α含量降低( P <0.05),SOD活性升高( P <0.05),EX527組大鼠腦組織MDA及NO、IL.1β、TNF.α含量升高( P <0.05),SOD活性降低( P <0.05);與抑眩寧顆粒組比較,抑眩寧顆粒+EX527組大鼠腦組織MDA及NO、IL.1β、TNF.α含量升高( P <0.05),SOD活性降低( P <0.05);與EX527組比較,抑眩寧顆粒+EX527組大鼠腦組織MDA、NO、IL.1β及TNF.α含量降低( P <0.05),SOD活性升高( P <0.05)。詳見(jiàn)表3。
2.5 各組大鼠腦組織SIRT1、PGC.1α、Bax、Bcl.2蛋白表達(dá)比較
與假手術(shù)組比較,模型組大鼠腦組織SIRT1、PGC.1α和Bcl.2蛋白表達(dá)水平降低( P <0.05),Bax蛋白表達(dá)水平升高( P <0.05);與模型組比較,抑眩寧顆粒組大鼠腦組織SIRT1、PGC.1α和Bcl.2蛋白表達(dá)水平升高( P ?<0.05),Bax蛋白表達(dá)水平降低( P <0.05), EX527組大鼠腦組織SIRT1、PGC.1α和Bcl.2蛋白表達(dá)水平降低( P <0.05),Bax蛋白表達(dá)水平升高( P <0.05);與抑眩寧顆粒組比較,抑眩寧顆粒+EX527組大鼠腦組織SIRT1、PGC.1α和Bcl.2蛋白表達(dá)水平降低( P <0.05),Bax蛋白表達(dá)水平升高( P <0.05);與EX527組比較,抑眩寧顆粒+EX527組大鼠腦組織SIRT1、 PGC.1α和Bcl.2蛋白表達(dá)水平升高( P <0.05), Bax蛋白表達(dá)水平降低( P <0.05)。詳見(jiàn)圖2、表4。
3 討 論
缺血性眩暈常與平衡障礙并發(fā),是前庭、視覺(jué)及本體覺(jué)功能障礙引起的自我重力方向感覺(jué)異常現(xiàn)象,治療周期長(zhǎng)、副作用大、成本高 ?[9] 。其中,前庭功能感知位置和運(yùn)動(dòng),其功能障礙表現(xiàn)為運(yùn)動(dòng)異常、眩暈和平衡異常,導(dǎo)致心理衰弱和行為困難等癥狀 ?[10] 。炎癥反應(yīng)及氧化應(yīng)激誘導(dǎo)的神經(jīng)細(xì)胞凋亡是參與缺血性腦及神經(jīng)損傷的主要病理過(guò)程之一 ?[11] 。本研究通過(guò)結(jié)扎右側(cè)頸總動(dòng)脈和右側(cè)鎖骨下動(dòng)脈法構(gòu)建缺血性眩暈大鼠模型,結(jié)果發(fā)現(xiàn)建模大鼠腦組織神經(jīng)細(xì)胞變形、固縮和凋亡,跳臺(tái)逃避潛伏期、給藥后血流量下降率、腦組織MDA、NO、IL.1β、TNF.α含量及促凋亡蛋白Bax表達(dá)水平升高,SOD活性和抑凋亡蛋白Bcl.2表達(dá)水平降低。提示缺血性眩暈大鼠模型構(gòu)建成功,腦組織氧化應(yīng)激及炎癥反應(yīng)增強(qiáng)。
抑眩寧顆粒的主要成分為膽南星、枸杞、黃芩、白芍、蒼耳子、菊花、生鐵落、牡蠣、茯苓、竹茹,主要用于類(lèi)眩暈癥的治療。本研究結(jié)果顯示,經(jīng)抑眩寧顆粒治療后,大鼠腦組織凋亡變異的細(xì)胞數(shù)量減少,膠質(zhì)周?chē)恼<?xì)胞數(shù)量增多,且抑眩寧顆粒可降低缺血性眩暈大鼠跳臺(tái)逃避潛伏期、給藥后血流量下降率、腦組織中MDA、NO、IL.1β、TNF.α含量及Bax蛋白表達(dá)水平,并提高大鼠SOD活性和Bcl.2蛋白表達(dá)水平,改善大鼠缺血性眩暈癥狀。
沉默SIRT1表達(dá)可抑制大鼠神經(jīng)元細(xì)胞存活,降低細(xì)胞內(nèi)SOD活性,提高M(jìn)DA含量,加劇氧化損傷 ?[12] 。尹曉新等 ?[13] 研究顯示,激活SIRT1/PGC.1α信號(hào)通路表達(dá)可減輕腦缺血損傷大鼠神經(jīng)損傷,緩解氧化應(yīng)激。Jia等 ?[14] 研究發(fā)現(xiàn),激活心肌梗死大鼠SIRT1/PGC.1α信號(hào)通路,可降低心肌纖維化和氧化應(yīng)激,提高大鼠存活率。有研究表明,抑制SIRT1和PGC.1α表達(dá)可促進(jìn) 心肌缺血損傷 ?[15] ,而SIRT1/PGC.1α ?通路過(guò)表達(dá)可減輕錳誘導(dǎo)的小鼠神經(jīng)損傷和線粒體功能障礙 ?[16] 。相關(guān)研究顯示,多種中藥均通過(guò)SIRT1/PGC.1α ?信號(hào)通路減少疾病的產(chǎn)生和發(fā)展,如雷公藤甲素通過(guò)激活SIRT1/PGC.1α信號(hào)通路改善血管性癡呆大鼠認(rèn)知功能障礙 ?[17] ;丹酚酸B和黃連素通過(guò)激活SIRT1/PGC.1α通路,改善糖尿病小鼠腎損傷 ?[18] ;五味子酚 通過(guò)SIRT1/PGC.1α 通路降低乙酰膽堿酯酶活性,減輕氧化損傷,改善小鼠學(xué)習(xí)和記憶能力 ?[19] 。另有研究發(fā)現(xiàn),上調(diào)SIRT1、PGC.1α和Bcl.2/Bax的表達(dá)可減輕氧化應(yīng)激損傷和神經(jīng)元凋亡,但EX527可逆轉(zhuǎn)該過(guò)程 ?[20] 。本研究給予抑眩寧顆粒處理后,缺血性眩暈大鼠腦組織SIRT1、PGC.1α蛋白表達(dá)水平升高,表明抑眩寧顆粒可能通過(guò)上調(diào)SIRT1/PGC.1α通路、改善缺血性眩暈大鼠的不良癥狀;進(jìn)一步采用抑眩寧顆粒和EX527聯(lián)合處理后,缺血性眩暈大鼠腦組織SIRT1、PGC.1α蛋白表達(dá)水平較抑眩寧顆粒單獨(dú)處理降低,較EX527單獨(dú)處理升高,表明抑眩寧顆粒對(duì)缺血性眩暈大鼠的改善作用可被EX527逆轉(zhuǎn),提示抑眩寧顆粒可能通過(guò)激活 SIRT1/PGC.1α通路,發(fā)揮改善缺血性眩暈大鼠的作用。
綜上所述,抑眩寧 顆粒可能通過(guò)激活SIRT1/PGC.1α 通路,減輕缺血性眩暈大鼠腦組織氧化應(yīng)激及炎癥反應(yīng),改善眩暈癥狀。本研究為缺血性眩暈的治療提供了一定的參考,但抑眩寧顆粒治療缺血性眩暈的作用機(jī)制復(fù)雜,其可能通過(guò)干預(yù)其他通路影響缺血性眩暈癥狀,有待進(jìn)一步深入研究。
參考文獻(xiàn):
[1] ?李雪, 黃石嬌,岳文華,等.后循環(huán)缺血性眩暈機(jī)制研究及中西醫(yī)治療研究進(jìn)展[J].遼寧中醫(yī)藥大學(xué)學(xué)報(bào),2022,24(3):60.63.
[2] ?WANG G D. Aerobic exercise ameliorates myocardial ischemia/reperfusion injury and thrombosis of diabetic rats via activation of AMPK/Sirt1/PGC.1α pathway[J].General Physiology and Biophysics,2022,41(4):319.328.
[3] ?LI L, ZHI D Y,CHENG R B, et al .The neuroprotective role of SIRT1/PGC.1α signaling in limb postconditioning in cerebral ischemia/reperfusion injury[J].Neuroscience Letters,2021,749:135736.
[4] ?HAN B, LI S Y,LV Y Y, et al .Dietary melatonin attenuates chromium.induced lung injury via activating the Sirt1/PGC.1α/Nrf2 pathway[J].Food & Function,2019,10(9):5555.5565.
[5] ?LI Y, LUO W W,CHENG X, et al .Curcumin attenuates isoniazid.induced hepatotoxicity by upregulating the SIRT1/PGC.1α/NRF1 pathway[J].Journal of Applied Toxicology:JAT,2022,42(7):1192.1204.
[6] ?董永書(shū), 行書(shū)麗,周紅艷,等.快捻久留針刺法對(duì)后循環(huán)缺血性眩暈大鼠的治療作用分析[J].針灸臨床雜志,2018,34(8):66.69.
[7] ?王紫嫣, 王澤雨,王國(guó)強(qiáng),等.抑眩寧顆粒對(duì)小鼠和大鼠缺血性眩暈的治療作用及其機(jī)制[J].吉林大學(xué)學(xué)報(bào)(醫(yī)學(xué)版),2019,45(3):546.550.
[8] ?李闖, 馬曉莉,文志萍,等.香青蘭總黃酮對(duì)心肌缺血再灌注損傷大鼠氧化應(yīng)激和線粒體的保護(hù)作用[J].中成藥,2022,44(2):390.395.
[9] ?KOCAK M N, ATES O,ONDAS O, et al .Differential diagnosis of ischemic vertigo by optical coherence tomography[J].The Eurasian Journal of Medicine,2020,52(3):288.291.
[10] ?HALL C D, HERDMAN S J,WHITNEY S L, et al .Vestibular rehabilitation for peripheral vestibular hypofunction:an updated clinical practice guideline from the academy of neurologic physical therapy of the American Physical Therapy Association[J].Journal of Neurologic Physical Therapy,2022,46(2):118.177.
[11] ?HOU R H, HAN P,LIU Q, et al .RETRACTED:a new Zn(Ⅱ).coordination polymer based on m.terphenyl pentacarboxylic acid ligand for photocatalytic methylene blue degradation and protective effect against Alzheimer′s disease by reducing the inflammatory response and oxidative stress in the nerve cells[J].Arabian Journal of Chemistry,2020,13(4):5171.5180.
[12] ?ZHANG X S, LU Y,TAO T, et al .Fucoxanthin mitigates subarachnoid hemorrhage.induced oxidative damage via sirtuin 1.dependent pathway[J].Molecular Neurobiology,2020,57(12):5286.5298.
[13] ?尹曉新, 馮海松,楊濤,等.脂聯(lián)素介導(dǎo)SIRT1/PGC.1α信號(hào)通路對(duì)大鼠腦缺血損傷后的影響[J].疑難病雜志,2022,21(6):633.637.
[14] ?JIA D D, HOU L,LV Y Z, et al .Postinfarction exercise training alleviates cardiac dysfunction and adverse remodeling via mitochondrial biogenesis and SIRT1/PGC.1α/PI3K/Akt signaling[J].Journal of Cellular Physiology,2019,234(12):23705.23718.
[15] ?趙云麗, 袁勇,馬曉莉,等.基于AMPK/SIRT1/PGC.1α信號(hào)通路研究香青蘭總黃酮對(duì)大鼠心肌缺血再灌注損傷的保護(hù)機(jī)制[J].中國(guó)藥房,2021,32(3):278.283.
[16] ?LEI M Y, CONG L,LIU Z Q, et al .Resveratrol reduces DRP1.mediated mitochondrial dysfunction via the SIRT1.PGC1α signaling pathway in manganese.induced nerve damage in mice[J].Environmental Toxicology,2022,37(2):282.298.
[17] ?YAO P, LI Y L,YANG Y J, et al .Triptolide improves cognitive dysfunction in rats with vascular dementia by activating the SIRT1/PGC.1α signaling pathway[J].Neurochemical Research,2019,44(8):1977.1985.
[18] ?胡媛媛, 暴雪麗,武彥香,等.丹酚酸B.黃連素復(fù)合物對(duì)糖尿病小鼠腎損傷及SIRT1/PGC.1α信號(hào)通路的影響[J].中國(guó)中醫(yī)急癥,2022,31(4):580.583.
[19] ?HAN Y F, YANG H Y,LI L B, et al .Schisanhenol improves learning and memory in scopolamine.treated mice by reducing acetylcholinesterase activity and attenuating oxidative damage through SIRT1.PGC.1α.Tau signaling pathway[J].The International Journal of Neuroscience,2019,129(2):110.118.
[20] ?HUANG J ,LIU W,DOYCHEVA D M, et al .Ghrelin attenuates oxidative stress and neuronal apoptosis via GHSR.1α/AMPK/Sirt1/PGC.1α/UCP2 pathway in a rat model of neonatal HIE[J].Free Radical Biology & Medicine,2019,141:322.337.
(收稿日期:2022.11.09)
(本文編輯 薛妮)
- 中西醫(yī)結(jié)合心腦血管病雜志的其它文章
- 冠心病病人血清脂蛋白相關(guān)磷脂酶A2與冠狀動(dòng)脈硬化程度、心肌損傷的關(guān)系
- 基于CMR評(píng)估血府逐瘀方對(duì)急性心肌梗死病人PCI術(shù)后缺血再灌注損傷的影響
- 伊伐布雷定聯(lián)合達(dá)格列凈治療射血分?jǐn)?shù)保留型心力衰竭的臨床療效
- 清眩降壓湯聯(lián)合左旋氨氯地平治療肝陽(yáng)上亢型高血壓的臨床研究
- 應(yīng)用四維自動(dòng)左房定量評(píng)價(jià)技術(shù)測(cè)定非ST段抬高型心肌梗死病人左房心肌力學(xué)變化
- 超聲測(cè)量視神經(jīng)鞘直徑評(píng)估顱內(nèi)壓增高的研究進(jìn)展

