某院精神科住院患者艱難梭菌定植的分子流行病學特征
王玲 林珊 黃益花 段慈東 田夢倫 沈宇航 宋小軍 陳毓 趙龍友 金大智

摘要:目的 研究精神科住院患者艱難梭菌定植的分子流行病學特征,并探討定植的相關因素。方法 于2020年6月1日至9月30日期間,收集麗水市第二人民醫院精神科住院患者的糞便樣本。分離培養艱難梭菌,并進行毒素基因鑒定、多位點序列分型和抗生素敏感性試驗。結合患者的臨床資料,分析艱難梭菌定植的相關因素。結果 共收集糞便樣本442份,分離到24株(5.4%)艱難梭菌。其中,20株為TcdA和TcdB毒素基因陽性、二元毒素基因陰性(A+B+CDT-),3株為A-B+CDT-,1株為A+B+CDT+。共鑒定出14種序列分型(ST),包括1株高毒力ST11型。所有菌株對甲硝唑、萬古霉素、利福平和哌拉西林敏感,但對環丙沙星(95.8%)、克林霉素(87.5%)和紅霉素(62.5%)的耐藥率較高。二元Logistic回歸分析結果顯示,在不同科室中,年齡(≥60歲)、住院天數(>200 d)和服用勞拉西泮片與老年精神科患者艱難梭菌定植具有顯著相關性(OR=3.762~15.556,P<0.05),而住院天數(>20 d)與早期干預科患者艱難梭菌定植具有顯著相關性(OR=0.004,P<0.001)。結論 研究發現精神科住院患者存在5.4%的艱難梭菌定植率,年齡較大、住院天數較長且長期服用精神治療性藥物的患者與艱難梭菌定植間存在相關性,需加強院內感染防控監測進而遏制艱難梭菌在精神科的暴發和傳播。
關鍵詞:艱難梭菌定植;精神科;分子特征;相關因素
中圖分類號:R978.1文獻標志碼:A
Molecular epidemiological characteristics of Clostridioides difficile colonization in psychiatric inpatients in a hospital
Wang Ling1, Lin Shan2,3, Huang Yihua1, Duan Cidong3, Tian Menglun3, Shen Yuhang3,4, Song Xiaojun5,6, Chen Yu3,5, Zhao Longyou1, and Jin Dazhi3,5,6
(1 Lishui Second People's Hospital, Lishui 323020; 2 TEDA Institute of Biological Sciences and Biotechnology, Nankai University, Tianjin 300457; 3 School of Laboratory Medicine and Bioengineering, Hangzhou Medical College, Hangzhou 310053; 4 Institute of Ageing Research, School of Basic Medical Sciences, Hangzhou Normal University, Hangzhou 311121; 5 Key Laboratory of Biomarkers and in vitro Diagnosis Translation of Zhejiang Province, Hangzhou 310063; 6 Laboratory Medicine Center, Department of Clinical Laboratory, Zhejiang Provincial People's Hospital, Hangzhou Medical College, Hangzhou 310014)
Abstract Objective To investigate the molecular epidemiology of Clostridioides difficile colonization (CDC) in psychiatric inpatients and explore the associated factors. Methods Stool samples were collected from psychiatric inpatients in Lishui Second People's Hospital between June 1 and September 30, 2020. C. difficile was cultured and analyzed for toxin gene identification, multilocus sequence typing, and antimicrobial resistance. Associated factors for CDC were analyzed according to patients' clinical data. Results Out of 442 stool samples, 24 (5.4%) C. difficile isolates were obtained. Among them, 20 isolates were identified as TcdA and TcdB positive and binary toxin genes negative (A+B+CDT-), three as A-B+CDT-, and one as A+B+CDT+. Fourteen sequence types (ST) were identified, including one hypervirulent ST11. All isolates were susceptible to metronidazole, vancomycin, rifampin, and piperacillin, but exhibited high resistance rates to ciprofloxacin (95.8%), clindamycin (87.5%), and erythromycin (62.5%). Binary logistic regression results showed that in different departments, age (≥60 years), length of hospital stays (>200 days), and lorazepam usage were significantly associated with CDC (OR=3.762~15.556, P<0.05). In contrast, there was a significant association between length of hospital stays (>20 days) and CDC (OR=0.004, P<0.001). ConclusionThe study revealed a 5.4% colonization rate among psychiatric inpatients. There is a correlation between older age, prolonged hospitalization, and long-term usage of psychotropic medications with CDC. Monitoring and controlling nosocomial infection should be enforced to prevent the outbreak and transmission of C. difficile in this hospital.
Key words Clostridioides difficile colonization; Psychiatry department; Molecular characteristics; Associated factors
艱難梭菌(Clostridioides difficile)是一種革蘭陽性芽孢桿菌,是引起院內感染腹瀉的主要病原體之一[1]。艱難梭菌感染(C. difficile infection, CDI)的臨床表現范圍從輕度腹瀉到偽膜性結腸炎,甚至可能導致死亡[2]。2019年美國CDC發布了抗生素耐藥性威脅報告,將艱難梭菌列為最高級別的“極危”等級[3]。同時,報告指出在美國約有22.39萬例CDI病例,導致1.28萬人死亡,相關醫療費用高達10億美元[4]。近年來,國內臨床已檢出高毒力核糖體027型和078型菌株[5]。同時,攜帶TcdA毒素基因陰性、TcdB毒素基因陽性和二元毒素基因陰性(A-B+CDT-)菌株的CDI病例正呈上升趨勢,并且這些菌株對多種抗生素呈現出更高的耐藥性[6]。因此,艱難梭菌已成為國內外臨床高度關注的病原體之一。
艱難梭菌作為人體腸道菌群的一部分,常定植于人體大腸或結腸內[7]。然而,當長期接受抗生素治療時,定植的艱難梭菌(C. difficile colonization, CDC)可迅速增殖并釋放毒素TcdA/B,導致機體出現腹瀉等臨床感染癥狀[1]。當前研究表明,艱難梭菌在成年人中的定植率約為4%至15%,在住院患者中約為3%至21%,在醫護人員中約為4.2%;而在長期護理機構的患者中可高達51%[8]。值得注意的是,已有報道指出CDC菌株的型別具有多樣性[9],而且CDC攜帶者容易發展為CDI患者[10],因此深入研究CDC的分子流行病學對于控制該病原體的傳播至關重要。盡管國內臨床已對神經外科[11]、血液科[12]和老年醫學科[13]患者的CDC進行了研究,但目前仍缺乏其他疾病患者CDC的相關數據。精神科住院患者長期服用精神治療性藥物,且具有住院時間長、自理能力差、認知力缺乏的特點[14],增加了艱難梭菌在醫院內傳播的風險。因此,本研究旨在闡明精神科住院患者CDC的分子流行病學特征,以期為早期識別和及時控制CDI的院內感染和暴發流行提供必要的科學依據。
1 材料與方法
1.1 研究對象
本橫斷面研究于2020年6月1日—9月30日在麗水市第二人民醫院進行,該醫院是一所三級甲等精神病專科醫院。在研究期間,采集非腹瀉精神科住院患者入院48 h后的糞便標本進行艱難梭菌分離檢測。同時,收集患者的臨床資料,包括年齡、性別、住院天數、診斷及藥物使用史等。CDC病例定義為在沒有CDI癥狀的患者中攜帶艱難梭菌[15]。本研究通過麗水市第二人民醫院倫理委員會審批(審批號:20201012-01),以確保在研究過程中遵循倫理原則和規范。
1.2 研究方法
1.2.1 艱難梭菌培養
按照文獻所述方法[16],從糞便中分離并培養艱難梭菌。簡要流程如下,取200 mg糞便標本,加入800 μL無水乙醇中,振蕩混勻。室溫靜置1 h后,8000 r/min離心2 min,取沉淀物接種于CDCA顯色培養基(購自浙江青谷生物工程有限公司),于37 ℃厭氧培養24 h。將疑似艱難梭菌菌落再次接種CDCA,37 ℃厭氧培養24 h,獲得純的艱難梭菌菌落后,將菌株于-80 ℃保存。
1.2.2 毒素基因鑒定
采用Qiagen基因組提取試劑盒(貨號:Cat. No. 69504)提取菌株基因組DNA,具體操作見說明書。根據Griffiths等方案[17],擴增毒素基因tcdA和tcdB。反應體系總量為25 μL,包括Premix Taq緩沖液4.7 μL,上、下游引物(10 μmol/L)各1 μL,DNA模板2 μL,ddH2O 16.3 μL。通過1.5%瓊脂糖凝膠電泳檢測PCR產物。
1.2.3 多位點序列分型(MLST)
根據Griffiths等方案[17],擴增7個管家基因(adk、atpA、dxr、glyA、recA、sodA和tpi),反應體系同“1.2.2”部分。選取條帶明亮的PCR產物送至生工生物工程(上海)股份有限公司進行Sanger測序。隨后,測序結果上傳至艱難梭菌MLST在線數據庫(https://pubmlst. org/organisms/clostridioides-difficile)進行比對,以獲得相應的序列分型(sequence type,ST)。最后,根據ST型的種類,使用基于MSTree V2算法的GrapeTree軟件構建最小生成樹[18]。
1.2.4 抗生素敏感性試驗
根據美國臨床實驗室標準化協會(CLSI)發布的M100-S33標準[19],采用瓊脂稀釋法測定菌株對12種抗生素(甲硝唑、萬古霉素、紅霉素、克林霉素、夫西地酸、利福平、四環素、哌拉西林、左氧氟沙星、莫西沙星、加替沙星和環丙沙星)的最小抑菌濃度(minimal inhibitory concentration,MIC)。進一步計算MIC值的相關參數,包括MIC50、MIC90、MIC的幾何平均數(geometric mean,GM)和MIC范圍。其中,紅霉素和利福平的折點判定參照相關文獻[20],萬古霉素和夫西地酸的折點判定參照歐洲抗生素敏感性測試委員會(EUCAST)標準[21],其余抗生素的折點判定則遵循CLSI標準[19]。選用艱難梭菌標準菌株(ATCC 700057)和脆弱擬桿菌(ATCC25285)作為抗生素敏感性試驗的質控菌株[20]。菌株若對3種及以上不同種類的抗生素呈現耐藥性,將其定義為多重耐藥株[20]。
1.3 統計學分析
采用SPSS 26.0軟件進行數據分析。計量資料使用(x±s)表示,計數資料用率或百分比描述。計量資料分析使用t檢驗或Mann-Whitney U檢驗,計數資料分析采用χ2檢驗或Fisher精確檢驗法。采用二元Logistic回歸計算比值比(OR)和95%置信區間(CI),進一步采用多元Logistic回歸確定獨立相關因素。P<0.05認為差異具有統計學意義。
2 結果
2.1 艱難梭菌分離培養與毒素基因鑒定
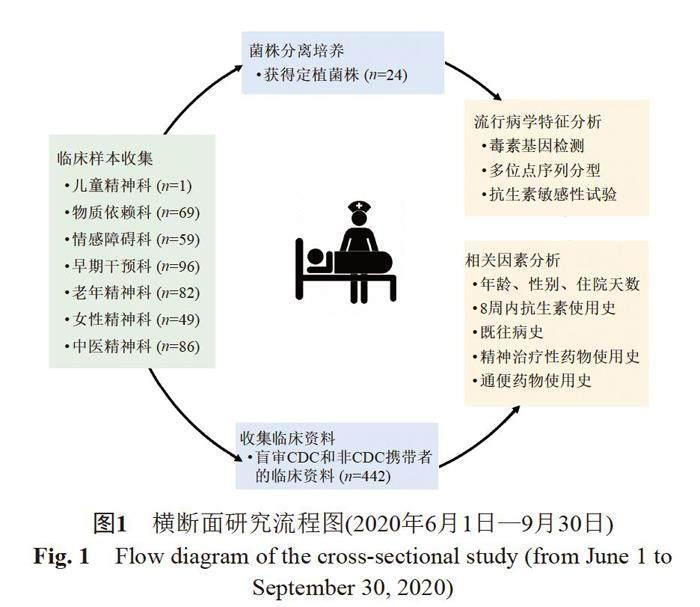
本研究共收集442名住院患者的糞便樣本,包括兒童精神科(n=1)、物質依賴科(n=69)、情感障礙科(n=59)、早期干預科(n=96)、老年精神科(n=82)、女性精神科(n=49)和中醫精神科(n=86),具體實驗研究流程詳見圖1。研究結果顯示,在442份糞便樣本中,共檢出24株艱難梭菌,定植率為5.4%。毒素基因鑒定結果顯示,24株菌株均為產毒型艱難梭菌,其中20株為A+B+CDT-(83.3%,20/24),3株為A-B+CDT+(12.5%,3/24),1株為A+B+CDT+(4.2%,1/24)。
2.2 臨床基本資料
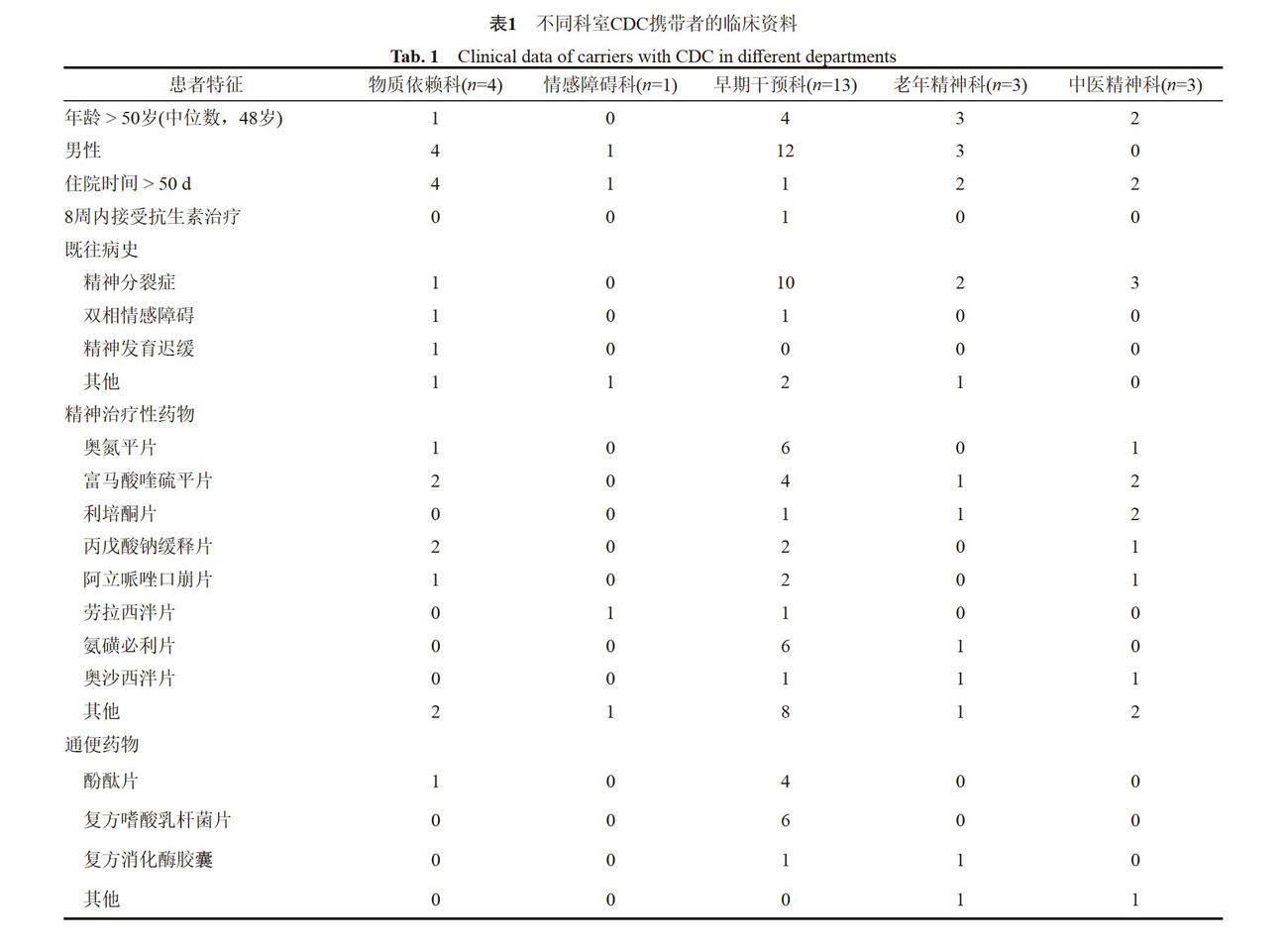
24例CDC攜帶者中,男性20例(83.3%),女性4例(16.7%),平均年齡為(45.7±12.4)歲,平均住院時間為(157.8±244.0) d。臨床資料顯示,在早期干預科中,僅有1位CDC攜帶者在8周內接受了抗生素(阿奇霉素)治療。值得注意的是,在不同科室中,早期干預科的陽性率最高(54.2%,13/24),其次為物質依賴科(16.7%,4/24)、老年精神科(12.5%,3/24)、中醫精神科(12.5%,3/24)和情感障礙科(4.2%,1/24)。此外,在早期干預科中,精神分裂癥患者的占比較大(76.9%,10/13)。這些精神分裂癥患者中,使用奧氮平片、氨磺必利片和富馬酸喹硫平片的人數最多,分別為6、6和4人。同時,這些患者還使用了通便藥物,其中4人使用酚酞片、6人使用復方嗜酸乳桿菌片和1人使用復方消化酶膠囊。詳細數據見表1。
2.3 MLST
經過MLST分析,24株艱難梭菌共檢出14種ST型。這些ST型主要分布在Clade1中,占比為75.0%(共18株)。具體而言,Clade1中包括ST2和ST129(均為16.7%,3/18), ST3、ST35和ST48(均為11.1%,2/18),以及ST8、ST14、ST29、ST42、ST102和ST139(均為5.6%,1/18)。值得注意的是,在Clade4中檢出了3株ST37(60%,3/5)和2株ST39(40%,2/5)。同時,還檢出1株Clade5中的高毒力ST11株(100%,1/1),詳見圖2。
在不同科室中,根據ST型的分布情況構建最小生成樹,詳見圖3。圓形代表ST型,圓形大小和分割份數表示相應菌株的數量,圓形之間連線上的數字表示相鄰ST型之間的位點變化數量。在早期干預科中檢測到的ST48是所有ST型的共同祖先,與物質依賴科中的ST8、老年精神科和中醫精神科中的ST3以及早期干預科中的ST102之間有2個位點差異,親緣關系較近;與情感障礙科中的ST29之間有3個位點差異;與物質依賴科中的ST35之間有6個位點差異;而與早期干預科中的ST37和老年精神科中的高毒力ST11之間則存在8個位點差異,親緣關系較遠。
2.4 抗生素敏感性分析
24株CDC菌株對12種抗生素的MIC分布和耐藥情況詳見表2。所有菌株均對甲硝唑、萬古霉素、利福平和哌拉西林敏感(0,0/24)。然而,這些菌株對環丙沙星的耐藥率最高(95.8%,23/24),其次為克林霉素(87.5%,21/24)和紅霉素(62.5%,15/24)。有18株菌株具有多重耐藥特征,占總數的75%。此外,在不同年齡段(35、40、45、50、55和60歲)之間,未觀察到耐藥率有顯著性差異(P>0.05,數據未顯示)。
2.5 CDC相關因素
在本研究中,對每位患者的病歷資料進行了盲審,并運用二元Logistic回歸分析評估了CDC的相關因素。在物質依賴科、情感障礙科和女性精神科中未觀察到CDC的相關因素(P>0.05,數據未顯示)。在早期干預科中,住院時間(>20 d)與CDC的發生存在顯著相關性(OR=0.004,P<0.001)。同時,在老年精神科中,年齡(≥60歲)、住院時間(>200 d)以及服用勞拉西泮片與CDC的發生也存在顯著相關性(OR= 3.762~15.556,P<0.05,見表3)。進一步針對這些具有顯著性差異的參數進行多元Logistic回歸分析,未發現老年精神科中CDC的獨立相關因素(P>0.05,數據未顯示)。
3 討論
CDC和CDI是艱難梭菌在體內引起的不同宿主反應,當長期使用抗生素或人體免疫功能低下時,CDC菌株會迅速增殖并釋放毒素引發CDI[22]。一項Meta分析研究表明,入院時攜帶產毒型艱難梭菌的CDC攜帶者發展為CDI患者的概率是無攜帶者的5.9倍[10]。盡管無癥狀CDC攜帶者被認為是醫療環境中艱難梭菌傳播的重要媒介,但由于其不是院內感染控制的關注重點,因而不會接受主動的定植監測[23]。精神科住院患者通常病程長,住院時間長,其臨床特征主要表現為明顯的意識和行為功能障礙[24]。因此,在病房封閉管理的情況下,患者間的相互接觸可能較為頻繁,從而增加了CDI的風險[24]。然而,目前國內尚未對精神科住院患者開展艱難梭菌的分子流行病學調查。因此,及時掌握這類無癥狀CDC攜帶者的分子特征及相關因素,對于有效預防和控制艱難梭菌在院內傳播至關重要。
在本研究中,精神科住院患者的CDC定植率為5.4%。這一比率低于上海地區ICU患者的定植率(19.02%)[25]、江蘇地區神經外科患者的定植率(16.15%)[26],以及浙江地區結直腸癌術前患者的定植率(16.10%)[7]。這種差異可能是由于這些科室的患者通常病情危重、免疫力低下,需要接受復雜的治療,包括長期抗生素治療、使用免疫抑制藥物以及有創性操作等[27],從而增加了感染艱難梭菌的風險。臨床資料顯示,在所有精神科住院患者中,僅有6人使用了抗生素,包括替硝唑、左氧氟沙星、鹽酸莫西沙星以及阿奇霉素(數據未顯示)。同時,在24名CDC攜帶者中僅有1人使用了阿奇霉素,這表明這類精神科住院患者的腸道菌群相對穩定。值得注意的是,盡管精神科住院患者長期服用精神治療性藥物可能導致機體免疫力下降[14],但由于大部分精神治療性藥物具有抗膽堿能作用,可以通過抑制乙酰膽堿的分泌來減緩胃腸道的蠕動[28-29],這可能在一定程度上抑制了腹瀉癥狀,因而有可能使得這類CDC攜帶者在精神治療過程中未發展成為CDI患者。然而,在結束階段性治療后是否會出現CDI尚不清楚。同時,除情感障礙科外,其他科室均有部分CDC攜帶者使用通便藥物,如酚酞片、復方嗜酸乳桿菌片、復方消化酶膠囊等,說明這類CDC攜帶者可能存在便秘。因此,后續需要對精神疾病治療結束后CDI發病情況及精神類藥物對腸道的影響等進行更深入的研究,以闡明精神病患者中CDC和CDI之間的關系。
本研究共檢出14種ST型別,這些型別呈現散在分布。當前國外研究指出,CDI和CDC菌株中存在相同的流行型別,并且CDC菌株的型別類型更具多樣化[9],這與我們在浙江地區開展的另一項研究結果一致[30]。因此,CDC菌株可在人群中形成多條傳播鏈,從而加速其在院內傳播。同時,本研究檢出了3株ST37型菌株,這是亞太地區主要的流行型別之一,并且在國內與引起臨床重癥CDI有關[31]。值得注意的是,這3株菌株在早期干預科中被集中檢出,且分離時間在35 d內。根據流行病學調查結果,該科室精神病患者通常隨意走動,無固定床位,因此該科室極有可能出現ST37型菌株的暴發流行。此外,本研究首次在老年精神科中檢出高毒力ST11菌株。盡管該患者未表現出與CDI相關的臨床癥狀,但考慮到患者的高齡(68 歲)和長時間住院(83 d),存在服用抗生素后發展為CDI的潛在風險。因此,有必要加強該患者病房的消毒措施,以有效控制ST11型菌株在該醫院迅速蔓延。
抗生素敏感性試驗結果顯示,除了甲硝唑和萬古霉素外,利福平和哌拉西林對所有CDC菌株敏感。相反,環丙沙星對CDC菌株的耐藥率最高(95.8%),這與該藥物對亞太地區CDI菌株的高耐藥率(95.1%)和對結直腸癌患者中CDC菌株的高耐藥率(78.8%)一致[7, 32]。盡管在本研究中,第三代喹諾酮類藥物環丙沙星(95.8%)和左氧氟沙星(16.7%)對CDC菌株的耐藥率高于第四代藥物莫西沙星和加替沙星(均為8.3%)。然而,左氧氟沙星對這些CDC菌株的耐藥率明顯低于其對亞太地區CDI菌株的耐藥率(93.4%)和對結直腸癌患者CDC菌株的耐藥率(66.7%)[7,32]。此外,克林霉素和紅霉素對CDC菌株的耐藥率也相對較高,分別為87.5%和62.5%,與亞太地區報道的克林霉素(86.3%)和紅霉素(54.4%)對CDI菌株的耐藥率,以及結直腸癌患者中克林霉素和紅霉素(均為63.6%)對CDC菌株的耐藥率相一致[7,32]。值得注意的是,在本研究中,多重耐藥株的比例較大(75.0%),尤其是3株ST37型菌株均為多重耐藥株。因此,需要持續監測這些CDC菌株的耐藥水平變化,以指導臨床合理用藥。
目前,國內仍然缺乏CDC相關因素的數據。在本研究中,二元Logistic回歸分析結果顯示,年齡(≥60 歲)、住院時間(>200 d)以及服用勞拉西泮片與CDC的發生存在顯著相關性。據報道,6個月內使用抗生素可增加CDC風險3.7倍[33]。然而,與ICU中CDC攜帶者的危險因素分析結果一致[34],本研究未發現抗生素使用是老年精神科患者CDC的相關因素,這可能與這類患者均未使用抗生素有關。此外,本研究首次發現服用勞拉西泮片與老年精神科患者CDC的發生存在相關性,并且其可使CDC的發生增加15.6倍。因此,在臨床治療中應謹慎使用該藥物。然而,盡管已有研究顯示,住院天數是ICU患者CDC的獨立危險因素[35]。在本研究中,由于病例數量限制,多元Logistic回歸分析結果顯示上述變量差異均無統計學意義(P>0.05)。另外,在本研究中,住院時間(>20 d)與早期干預科患者CDC的發生存在相關性。臨床資料顯示,早期干預科中的CDC攜帶者具有年輕化(41.92±12.05)歲的特點。當前,已有證據顯示,與CDI患者相比,CDC攜帶者往往更年輕,并且查爾森共病指數(Charlson Comorbidity Index)得分較低[9]。因此,持續監測對于防控CDC攜帶者的院內傳播及其發展為CDI患者至關重要。
本研究存在一定的局限性。首先,所有臨床樣本均來自同一家醫院,未來應開展多中心合作,覆蓋不同地理位置和醫療機構,以全面描述精神科住院患者CDC的分子流行病學特征。其次,未能獲取環境樣本,因而無法全面評估艱難梭菌在精神科住院患者中的傳播情況。未來應進一步采用全基因組測序技術,以描繪CDC攜帶者之間的傳播鏈條。最后,未能對CDC攜帶者進行追蹤隨訪,因而無法判斷這些CDC攜帶者精神疾病治療停止后是否發展為CDI患者。后續需要開展長期隨訪,為評估精神科住院患者CDC的疾病發展模式提供必要的科學依據。
綜上所述,精神科住院患者存在5.4%的艱難梭菌定植率,定植的菌株均為產毒型艱難梭菌,且對環丙沙星、克林霉素和紅霉素存在較高耐藥率。年齡較大、住院天數較長且長期服用精神治療性藥物,特別是服用勞拉西泮片的患者與艱難梭菌定植存在相關性。這些研究成果對深入了解精神科住院患者CDC的分子流行病學特征及防控艱難梭菌的院內感染傳播具有重要意義。
參 考 文 獻
林珊, 宋小軍, 屈平華, 等. 艱難擬梭菌重命名及相關致病因子研究進展[J]. 疾病監測, 2021, 36(4): 344-349.
Jin D, Tang Y, Riley T. Editorial: Clostridium difficile infection in the Asia-Pacific region[J]. Front Cell Infect Microbiol, 2022, 12: 983563.
林珊, 宋廣忠, 胡繼紅, 等. 艱難梭菌感染的檢測方法與實驗室診斷策略[J]. 中華傳染病雜志, 2021, 39(10): 642-646.
Centers for Disease Control and Prevention (CDC): Antibiotic resistance threats in the United States[J/OL]. [2023-12-28]. https://www.cdc.gov/drugresistance/biggest-threats.html.
Wu Y, Wang Y Y, Bai L L, et al. A narrative review of Clostridioides difficile infection in China[J]. Anaerobe, 2022, 74: 102540.
許星星, 羅蕓, 王賢軍, 等. 國內外艱難梭菌感染現狀分析[J]. 傳染病信息, 2018, 31(2): 175-180.
Zheng Y, Luo Y, Lv Y, et al. Clostridium difficile colonization in preoperative colorectal cancer patients[J]. Oncotarget, 2017, 8(7): 11877-11886.
Crobach M J T, Vernon J J, Loo V G, et al. Understanding Clostridium difficile colonization[J]. Clin Microbiol Rev, 2018, 31(2): e00021-17.
Kim B, Seo M R, Kim J, et al. Ribotype variability of Clostridioides difficile strains in patients with hospital-acquired C. difficile infections, community-acquired C. difficile infections, and colonization with toxigenic and non-toxigenic strains of C. difficile[J]. Anaerobe, 2019, 60: 102086.
Zacharioudakis I M, Zervou F N, Pliakos E E, et al. Colonization with toxinogenic C. difficile upon hospital admission, and risk of infection: A systematic review and meta-analysis[J]. Am J Gastroenterol, 2015, 110(3): 381-390.
祁琪, 高潔, 石荃, 等. 神經外科患者入院時產毒性艱難梭菌定植率及其危險因素研究[J]. 中華醫院感染學雜志, 2020, 30(6): 872-877.
王潔, 楊靖, 劉曉雷, 等. 血液病患者產毒艱難梭菌無癥狀定植和感染相關危險因素的前瞻性研究[J]. 中國感染與化療雜志, 2021, 21(6): 641-645.
顧吉娜, 金慧, 蔡雅衛, 等. 老年醫學科患者艱難梭菌檢測結果與定植危險因素分析[J]. 中華醫院感染學雜志, 2016, 26(10): 2183-2185.
趙勝楠, 周莉萍, 連卓. 精神科住院患者院內感染影響因素分析及應對措施[J]. 河南醫學研究, 2020, 29(25): 4651-4653.
Johnson S, Lavergne V, Skinner A M, et al. Clinical practice guideline by the infectious diseases society of America (IDSA) and society for healthcare epidemiology of America (SHEA): 2021 focused update guidelines on management of Clostridioides difficile infection in adults[J]. Clin Infect Dis, 2021, 73(5): 755-757.
邊俏, 羅蕓, 許星星, 等. 一種用于艱難梭菌分離培養的新型顯色培養基的性能評價[J]. 臨床檢驗雜志, 2019, 37(4): 301-304.
Griffiths D, Fawley W, Kachrimanidou M, et al. Multilocus sequence typing of Clostridium difficile[J]. J Clin Microbiol, 2010, 48(3): 770-778.
周秀娟, 崔妍, 何逸塵, 等. 沙門氏菌泛耐藥基因組特征分析[J]. 微生物學報, 2021, 61(8): 2358-2369.
CLSI. Performance standards for antimicrobial susceptibility testing (M100-S33)[S]. Wayne, PA: CLSI, 2023.
Jin D, Luo Y, Huang C, et al. Molecular epidemiology of Clostridium difficile infection in hospitalized patients in eastern China[J]. J Clin Microbiol, 2017, 55(3): 801-810.
EUCAST. EUCAST guidelines for susceptibility testing (Version 13.1)[S]. V?xj?, Sweden: EUCAST, 2023.
苗瑞雪, 汪志凌, 周偉, 等. 艱難梭菌在兒童腸道定植和感染的研究進展[J]. 重慶醫學, 2019, 48(1): 134-137.
Khanafer N, Vanhems P, Bennia S, et al. Factors associated with Clostridioides (Clostridium) difficile infection and colonization: Ongoing prospective cohort study in a French university hospital[J]. Int J Environ Res Public Health, 2021, 18(14): 7528.
袁景, 孫蓮芳. 住院精神分裂癥患者并發感染影響因素分析[J]. 河北醫科大學學報, 2022, 43(9): 1029-1032.
Mi H, Bao R, Xiao Y, et al. Colonization of toxigenic Clostridium difficile among intensive care unit patients: A multi-centre cross-sectional study[J]. Front Cell Infect Microbiol, 2020, 10: 12.
馬開慧, 呂治, 周妍妍, 等. 住院患者艱難梭菌定植和感染特征分析[J]. 檢驗醫學, 2023, 38(2): 153-156.
宋曉超, 丁蔚, 金美娟. 重癥監護室與普通病房碳青霉烯類耐藥鮑曼不動桿菌醫院感染分布與耐藥性分析[J]. 中國消毒學雜志, 2024, 41(1): 33-37.
Rodríguez-Ramallo H, Báez-Gutiérrez N, Prado-Mel E, et al. Association between anticholinergic burden and constipation: A systematic review[J]. Healthcare (Basel), 2021, 9(5): 581.
Joshi Y B. Cholinergic functioning, cognition, and anticholinergic medication burden in Schizophrenia[J]. Curr Top Behav Neurosci, 2023, 63: 393-406.
Shen Y, Lin S, You P, et al. Rapid discrimination between clinical Clostridioides difficile infection and colonization by quantitative detection of TcdB toxin using a realtime cell analysis system[J]. Front Microbiol, 15: 1348892.
Xu X, Luo Y, Chen H, et al. Genomic evolution and virulence association of Clostridioides difficile sequence type 37 (ribotype 017) in China[J]. Emerg Microbes Infect, 2021, 10(1): 1331-1345.
Luo Y, Cheong E, Bian Q, et al. Different molecular characteristics and antimicrobial resistance profiles of Clostridium difficile in the Asia-Pacific region[J]. Emerg Microbes Infect, 2019, 8(1): 1553-1562.
Nissle K, Kopf D, R?sler A. Asymptomatic and yet C. difficile-toxin positive? Prevalence and risk factors of carriers of toxigenic Clostridium difficile among geriatric in-patients[J]. BMC Geriatr, 2016, 16(1): 185.
Cui Y, Dong D, Zhang L, et al. Risk factors for Clostridioides difficile infection and colonization among patients admitted to an intensive care unit in Shanghai, China[J]. BMC Infect Dis, 2019, 19(1): 961.
Yu M, Zhao B, Chen Y, et al. Epidemiology and risk factors for hospital acquired Clostridium difficile infection and colonization in emergency intensive care unit of a general hospital in Shanghai[J]. Chin Crit Care Med, 2021, 33(11): 1358-1361.

