實驗用豬非洲豬瘟綜合防控


摘要:近年來,非洲豬瘟疫情在世界范圍內流行,嚴重影響生豬生產供應,不僅給我國生豬養殖業產生嚴重的負面影響,而且嚴重影響用于科學實驗的實驗用豬的質量和實驗動物生物安全。本文通過歸納非洲豬瘟病毒防控中存在的難點,結合實驗動物管理要求,分別從政策執行、硬件優化、豬源控制、人員管理、物資管理、環境控制、飼喂管理、疫病監測、應急預案等方面進行了總結,可以作為實驗用豬非洲豬瘟綜合防控體系建設的參考建議。
關鍵詞:實驗用豬;非洲豬瘟;綜合防控
非洲豬瘟(African swine fever,ASF),是由非洲豬瘟病毒(African swine fever virus, ASF)感染引起的一種急性、發熱、高度接觸性傳染性豬病,其特征是發病過程短,高熱,病死率高,病死率可高達100%[1]。世界動物衛生組織將其列為法定報告動物疫病,在我國屬于重點防范的一類動物疫病[2]。2007年以來,非洲豬瘟病毒在全球多個國家擴散和流行,特別是俄羅斯及周邊地區[3],2018年非洲豬瘟在我國遼寧省沈陽市沈北新區某養殖場第一次出現[4],并迅速在全國蔓延開來,嚴重影響我國生豬生產。非洲豬瘟病毒不僅可以感染野豬和家豬,還可以感染實驗小型豬[5],金梅林等在ABSL-3實驗室內用ASFV感染了巴馬小型豬,發現ASFV感染的巴馬小型豬的病理變化與非洲豬瘟病毒感染家豬和野豬的特征性病變一致。因此,規范ASF綜合防控措施,對降低ASF在獸用藥品和生物制品研發,生物醫學科學研究中的不利影響非常重要。
1 非洲豬瘟的防控難點
1.1 致病力強
ASFV是非洲豬瘟科非洲豬瘟病毒屬的唯一成員。病毒粒子的直徑為175~215 nm,具有復雜的多層結構,呈20面體對稱,有囊膜。基因組為雙股線狀DNA,大小170~190 kb[6]。ASFV主要通過呼吸道和消化道作為入侵門戶,病毒感染機體后,首先在扁桃體中進行增殖, 進入循環系統引起病毒血癥,也可在幾種類型的細胞中增殖,網狀內皮細胞和單核巨噬細胞是主要復制場所。豬感染ASFV后的臨床癥狀主要表現為持續發熱(40~42 ℃),伴有食欲廢絕、呼吸困難、心跳加快、分泌物增多,以及胃腸黏膜和淋巴結明顯出血、極度虛弱等癥狀,死亡率高達100%[7]。即使是慢性感染,病毒處于排毒狀態,機能指標異常,且很難康復,不可用于實驗研究和測試[8]。
1.2 抵抗力強
非洲豬瘟病毒在自然條件下和低溫環境下抵抗力很強,低溫暗室內存在血液中的病毒可存活長達數年,在室溫下的糞便中可存活11 d;在污染的土壤中存活數周至數月;在4 ℃水中存活至少60 d,在室溫水中存活50 d;在污染的飼料中存活至少30 d;在未經熟制的帶骨肉、香腸、煙熏肉制品等中可存活1~6個月甚至更長時間;在冷凍肉中可存活數年[9];在餐廚剩余物(泔水)中也可存活較長時間。雖然當溫度達到60 ℃, 30 min即可滅活病毒,在無血清介質中, 酸性(pH<3.9) 或堿性 (pH>11.5)環境也可使病毒滅活,對次氯酸鹽溶液、甲醛溶液、苯酚、碘化合物等消毒劑也比較敏感[10];但在防疫衛生和消毒措施不規范時,非洲豬瘟病毒有很大的概率隨實驗用品、生物試劑、飼養物資、豬體或人體進入實驗用豬設施,感染豬群。
1.3 傳染性極強
家豬與野豬對非洲豬瘟病毒都具有自然易感性,各品種及各不同年齡之豬群同樣具有易感性[11]。非洲豬瘟的傳染源為病豬、隱性感染豬、康復豬、軟蜱。健康豬通過以下三種方式感染本病:直接接觸、間接接觸、媒介蜱傳播。健康豬直接接觸病豬、采食被病毒污染的飼料、飲水、使用被污染的墊料、接觸被污染的車輛、設備等而感染。短距離也可通過空氣傳播,導致呼吸道感染。疫區內蜱及其他吸血昆蟲的叮咬也是傳播該病的重要途徑。非洲豬瘟病毒可在鈍緣蜱中增殖,并使其成為主要的傳播媒介[12]。本病無明顯的季節性,可常年發病。
1.4 暫無有效疫苗
雖然非洲豬瘟病毒早在20世紀初就被發現,但因為ASFV 是一種具有復雜分子結構的線性雙鏈DNA病毒,基因組大小在170~190 kb之間,能夠編碼超過200種蛋白質,其結構和功能復雜多樣的特性阻礙了病毒-宿主間作用機制的探明及疫苗研發進程,宿主保護性反應的機制和保護性抗原也未完全確定,這對非洲豬瘟疫苗的深入研究形成阻力[13]。當前,全球還沒有一個安全有效的疫苗投入臨床使用,ASF滅活疫苗因免疫原性的差異會受到影響,接種之后雖然產生抗體但不能對機體起到保護作用[14]。在研的重組減毒活疫苗證明可以抵抗親本強毒株的攻擊,但對交叉免疫保護的效果需要進一步研究。亞單位疫苗、活載體疫苗和核酸疫苗均有團隊在開展研究,但由于ASFV 基因組龐大,仍有大量蛋白功能尚不清楚,ASFV免疫逃逸機制和具體抗原的知識匱乏,需要大量的資源和長期的實踐來開展探索[15]。缺乏安全有效疫苗使得ASF的防控變得異常復雜。
1.5 實驗用豬質量標準高,防控難度大
根據《NYT 3466—2019實驗用豬微生物學等級及監測》和各省市地方實驗用豬微生物等級標準要求,實驗用豬一般分為普通級、SPF級和無菌級。按照《GB/T 18648 非洲豬瘟診斷技術》開展檢測,所有等級的非洲豬瘟病毒檢測結果均要求陰性,質量控制標準較高。傳染病防控最有效的方法就是隔離,實驗用豬生產機構可以參照規模化豬場生豬生產模式進行全封閉式管理,減少外界環境感染豬群的風險,但在實驗用豬使用機構和一些小型生產機構,飼養和實驗人員全封閉管理的難度較高,一旦人員和物資在動物設施外接觸并攜帶ASFV,將會增加ASFV隨人員或物品被帶入動物實驗設施的風險,增加防控難度。而豬群一旦感染ASFV,將給實驗用豬的健康和實驗結果造成嚴重損失。
2 非洲豬瘟綜合防控措施
目前全世界尚無安全和有效的疫苗用于預防非洲豬瘟病毒,也無有效藥物進行治療,但是巴西和西班牙分別在1984年和1995年實現了非洲豬瘟根除計劃,歷史經驗告訴我們,必須采取綜合性的防控措施,搭建綜合防控體系,才能最大程度減少非洲豬瘟病毒對實驗用豬的感染風險[16]。根據非洲豬瘟病毒流行特點,結合實驗動物質量控制要求,建議采取非洲豬瘟綜合措施來防控非洲豬瘟病毒[17]。
2.1 嚴格執行國家和地方相關規章制度和標準規范要求
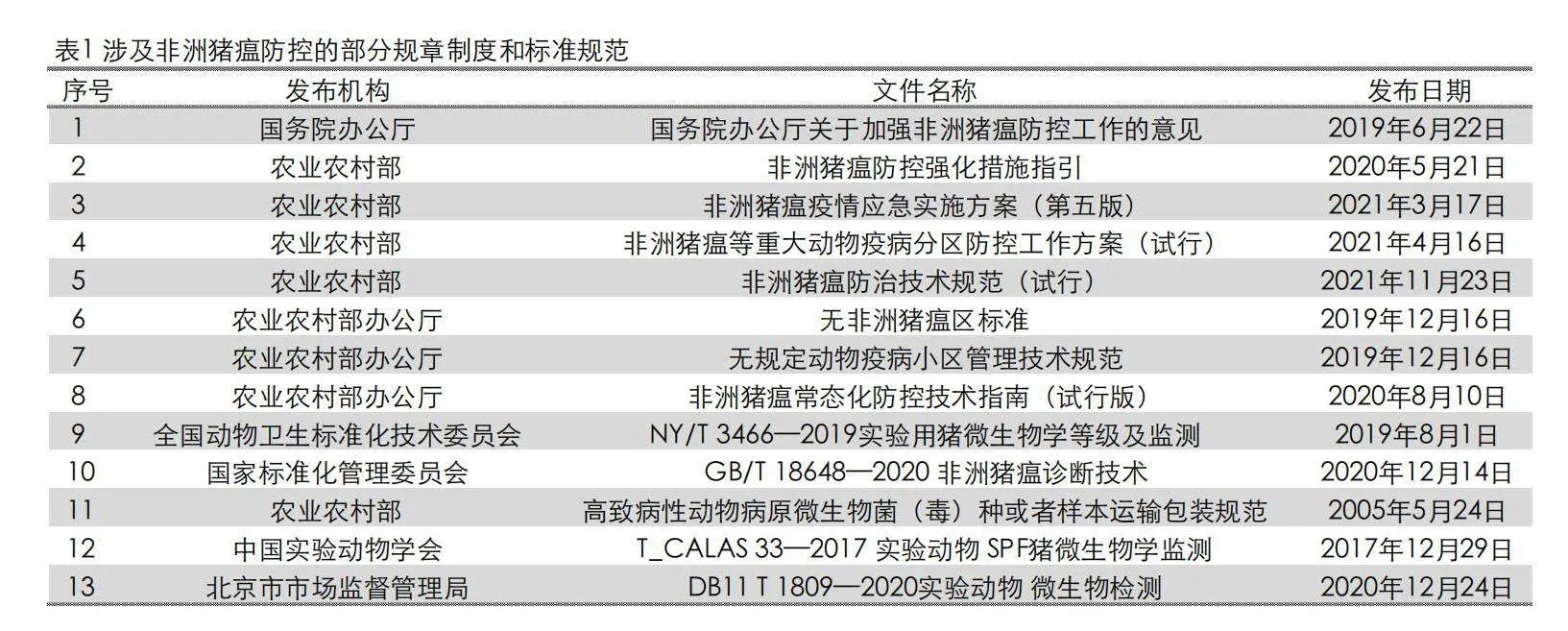
根據《中華人民共和國動物防疫法》,國家對動物疫病實行預防為主的方針。非洲豬瘟在我國被列為一類動物疫病,其危害是顯而易見的,國家獸醫主管部門針對非洲豬瘟出臺了一系列的規章制度和標準規范(表1),中國實驗動物學會和部分省市也出臺了涉及實驗豬非洲豬瘟控制的標準規范。生豬養殖和使用機構應嚴格按照這些規章制度和標準規范,采取科學、統一行動,方能實現非洲豬瘟的預防、控制和撲滅。
2.2 優化硬件設施
實驗用豬設施可參照《實驗動物設施建筑技術規范》(GB 50447 )和《規模豬場建設》(GB/T 17824.1)來進行建設,一般分為普通環境和屏障環境,可根據場區位置、場內布局等因素,考慮總體效益情況,配套自動飼喂、供水飲水設施、機械通風、水簾、中央空調等硬件設施,降低人力成本,提高生產效率,降低人流物流強度,降低病毒污染風險。按照生物風險等級和設施類型,劃分生產區、實驗區等核心區,以及辦公區、生活區等輔助區域。設施場區內應設置隔離檢疫區,采取凈道與污道分開原則,設置人流、物流和動物流路線通道。在不同生物風險等級區域之間,設置消毒池和噴霧消毒通道,降低交叉污染風險[18]。有條件的實驗用豬機構,可建立正壓屏障環境飼養實驗豬,豬舍內相通區域壓強梯度不低于10 pa,送入豬舍的空氣經過高效過濾器過濾,保證空氣潔凈度達到7級,換氣次數不低于15次/h,避免外界的病毒氣溶膠進入豬舍。
2.3 嚴控豬源質量
引進實驗用豬必須經過嚴格篩選,一般按照國家和各省市地方對實驗用豬微生物等級標準的要求從具有《實驗動物生產許可證》資質的豬場采購引進,每一頭豬應有《實驗動物合格證》(注明微生物等級)、最近的微生物檢測報告和免疫證明,特別要排除非洲豬瘟病毒感染,盡可能使用SPF級的實驗用豬。如果采購家豬作為實驗用豬,應從無非洲豬瘟病毒感染豬場引種或采購[19]。為防止運輸過程接觸感染和潛伏感染,引進的實驗豬必須進行至少7 d的隔離觀察飼養,在隔離觀察期間采樣進行非洲豬瘟病毒檢測,檢測合格后方能進入飼養或試驗區域[20]。
2.4 加強人員管理
人員活動是傳播非洲豬瘟病毒的重要因素之一[21]。對于實驗用豬生產機構的工作人員必須執行嚴格的隔離管理程序。外來人員和休假工作人員進入設施場區,存在較大風險,人員進入設施場區前應進行有效隔離,對需要回場人員進行ASFV檢測,檢測合格后,回場人員執行淋浴、更換衣服和鞋,注意清洗頭發、剪指甲,經2~3 d生活區隔離后,方可進入生產區核心區。對于實驗機構的工作人員應在自己崗位區域活動,不到其他豬舍串門,更不能到其他養殖場串門。建議進入核心區前3 d不去農貿市場、屠宰廠(場)、無害化處理廠及動物產品交易市場等高風險場所。
除了盡可能避免工作人員接觸高風險因子,還應要求所有工作人員在進入豬舍時穿戴好個人防護裝備,包括連體服或長袍、口罩、帽子、手套、靴子等,進入屏障設施的工作人員應穿戴無菌服。個人防護裝備不僅可以保護人員不被人獸共患病原體感染,也可以防止人員將設施外的病原微生物帶入豬舍。
另外,還要嚴禁非工作人員或與本實驗無關人員進出核心區,特別要注意各類運輸人員、維修人員、外場獸醫、技術顧問、獸藥飼料銷售人員、工作人員家屬等。
2.5 規范物資管理
非洲豬瘟病毒抵抗力強,會隨著未消毒滅菌的物品進入豬場設施內,因此,除了飼料、藥物、疫苗及必要生活物資,應減少或禁止其他物資進入實驗用豬場區。
外來運豬車、飼料運輸車、病死豬收集車、糞污收集車、私人車輛等外來車輛將非洲豬瘟病毒帶入場區的風險較大,應避免這些車輛靠近或進入豬場。為了方便運輸,場內應有拉豬車、拉料車、糞污和病死豬運輸的專用內部車輛,并且車輛不能混用。
飼料是豬設施內進入量最大的物品,入場前要對飼料車進行徹底消毒,飼料可通過中轉接駁或管道運輸的方式進入設施場區[22]。飼料在進入核心區域前,應放置在密閉房間中或通過傳遞窗用臭氧或過氧化氫對外包裝進行熏蒸消毒處理[23]。其他進入飼養或試驗區域的物品必須經過消毒處理后方可進入。藥物疫苗、必要生活物資等在場區外進行2次表面噴霧消毒和1次臭氧或過氧化氫熏蒸消毒,耐高溫的物品經過加熱或高壓滅菌處理后進入場區內。疫苗、試劑和實驗樣本等對溫度有要求的物品,應拆掉外層紙質包裝,經過有效消毒藥物浸泡,臭氧熏蒸消毒后置于冰箱儲存。來源于豬的精液、輸精管、血清等樣本應經過檢測排除非洲豬瘟病毒[24]。同時,設施場區內外物品,以及各區域的物品應嚴格分開,嚴禁物品交叉混淆使用。
場區內產生的廢棄物和垃圾應當天及時轉移到場區外,豬舍內不設置垃圾桶,避免滋生蟲、蠅等蟲媒。
2.6 做好環境控制
豬舍環境分為豬舍外圍環境和豬舍內部環境。只有將豬舍內外環境都做好才能最大限度地減少非洲豬瘟病毒風險因子對豬的影響。
保持豬舍外圍地面衛生,在高風險時段,地面可使用生石灰進行鋪撒,雨天過后及時重新鋪撒,每天對外圍環境進行消毒水噴霧消毒。豬場內部道路應水泥硬化,場內空地盡量不留泥土地面和積水洼地,可做硬化、鋪鵝卵石或厚黑膠膜。場內盡可能不種植樹木、綠化帶、草坪、蔬菜、水果等,以免滋生蚊蟲,還可定期噴灑殺蟲劑,防止蚊蠅、蜱滋生,放置捕鼠器等撲滅野鼠。豬場門口要設置大于常規貨輛占地面積的硬化路面,便于對到場車輛進行徹底消毒。
豬舍內部地面和墻面應硬化、耐腐蝕、耐高溫,便于糞尿排泄、日常沖洗、消毒劑噴灑消毒和火焰噴射消毒。地面不能積水,以防蚊蠅滋生[25]。應根據普通環境和屏障環境的要求保持豬舍內適宜的溫度(16~28 ℃)、濕度(30%~80%)、通風(普通環境不低于10次/h,屏障環境不低于15次/h)、光照(100~200 lx)和氨濃度(不高于14 mg/m3)。普通環境內要經常檢查豬舍內有無賊風,防止出現對流風、穿堂風,減少豬的應激反應。有機械通風的設施進行定期更換空氣過濾器。采用排風扇定時抽風,抽風時段應保證對溫度影響控制在4 ℃以內,以免溫差較大,引起應激反應[26]。屏障環境主要依靠中央空調送排風,因此,要特別注意房間的換氣次數和氨氣濃度不要超標。
工作人員要經常查看地面是否有飼料遺撒、糞便和尿水積存;豬欄、圍墻、水管、料槽等部位是否積存塵土,舍內是否有蜘蛛網。及時清掃豬舍,杜絕衛生死角。豬舍內還可以懸掛捕蠅燈和粘蠅貼等進行滅蠅[27]。豬舍門口可設置擋鼠板、粘鼠板和紗網,做好防鼠、防鳥工作,防止周邊豬場的鼠類或鳥類遷徙尋食,將風險帶入豬舍[28]。
2.7 加強疫病監測
根據《NY T 3466—2019實驗用豬微生物學等級及監測》要求,豬群應每半年至少檢測一次ASFV,為增加檢出率,豬場可以增加檢測頻率,特別是在疫情高發地區和時期,可對豬群每個季度甚至每個月進行一次隨機抽樣采樣。采樣數量根據豬群的大小確定(表2)。診斷方法包括臨床觀察、PCR核酸檢測、ELISA抗原/抗體檢測、熒光RAA檢測等方法(表3)。為提高檢測效率,建議優先使用熒光PCR檢測或熒光RAA檢測核酸方法,以及間接免疫熒光抗體方法檢測。同時要加強對場區環境采樣進行核酸檢測,發現陽性立即進行隔離、撲殺和全面消毒。平時要做好日常巡視排查,注意豬群健康狀況,發現異常豬只及時處理,及時淘汰病弱豬只,異常豬只及時采集口鼻拭子及血拭子檢測,發現疫情立即按要求報告。同時,還要加強對豬繁殖與呼吸綜合征、豬圓環病毒病、豬瘟、豬偽狂犬病、口蹄疫等其他常見疫病的監測。普通級豬需要疫苗免疫的,要及時免疫接種,做好抗體水平檢測,確保免疫效果,提高豬群整體免疫力[29]。
2.8 保證飼喂質量
確保實驗用豬攝入足夠營養,是維持豬群良好免疫力和抵抗力的基礎[30]。根據實驗用豬各個生長階段的營養需求,實驗用豬的飼料可分為開口料、生長料、哺乳料和維持料,要選擇最適合每個階段的全價配合飼料。實驗用豬的飼料應該無毒、無害、不得摻入抗生素、驅蟲劑、防腐劑、色素、促生長劑以及激素等添加劑。除了進行粗蛋白、粗脂肪、粗纖維、水、鈣、磷、微量元素要符合不同類別飼料的要求,還要滿足砷、鉛、六六六、黃曲霉素B等化學污染物和總菌落數、大腸桿菌、沙門氏菌等微生物指標,進入屏障環境和隔離環境的飼料和飲水還要經過高壓或輻照滅菌,達到無菌要求。日常飼喂中,工作人員要定期查看料槽,確保不缺料,保證豬只均能自由采食。不得飼喂霉變飼料,每天定時清理料槽,避免飼料殘留。每日檢查飲水管是否有破損,水壓水流是否正常,豬只能否正常飲水。要保證水源質量滿足動物需求,定期檢測水質,定期消毒飲水設備。
2.9 制定應急預案
設施場區發現非洲豬瘟疫情后,要第一時間對豬舍內的實驗豬進行緊急撲殺,并對尸體進行高溫高壓消毒無害化處理[31]。撲殺完成后及時對動物房使用甲醛或過氧化氫熏蒸的方式進行全面消毒。熏蒸完成后,組織人員對實驗區域所有物品進行消毒,能經受高溫高熱消毒的使用高壓蒸汽滅菌器或火焰噴射器烘烤消毒,不能經受高溫高熱消毒的物品使用消毒水浸泡方式消毒。必要時,首次清場完成后可進行多輪消毒劑熏蒸消毒。
發現疫情區域人員嚴格隔離,所有穿戴物品進行浸泡消毒,隔離完成后取樣檢測非洲豬瘟,檢測合格后方能離開隔離區。
設施重新啟用前,必須對設施環境進行采樣檢測非洲豬瘟病毒,檢測合格后購買哨兵豬飼養至少15 d,再進行非洲豬瘟病毒檢測,檢測合格后方能引進新的實驗用豬。
3 結語
非洲豬瘟一旦傳入實驗豬群,會對實驗用豬種群和實驗本身造成巨大損失。非洲豬瘟的防控,不能只依賴于某一項具體措施,而應充分評估生物風險因素,按照生物安全管理理念,科學開展風險評估,采取綜合防控措施,建立完善的生物安全防控體系和應急機制。實驗用豬的養殖規模相對于肉用生豬的規模比較小眾,受外界生豬疫情的影響非常大,在當前非洲豬瘟疫情依然存在巨大威脅的形勢下,實驗用豬生產和使用機構除了要建立好本機構的生物防控體系,還應依據當地的非洲豬瘟疫情防控政策,加入區域聯防聯控,采取綜合防控措施,強化監測排查,共享防控信息,方能將非洲豬瘟的風險降到最低程度。■
參考文獻:
[1] COSTARD S, MUR L, LUBROTH J, et al. Epidemiology of African swine fever virus[J]. Virus Res, 2013,173(1): 191-197.
[2] 羅玉子,孫元,王濤,等.非洲豬瘟-我國養豬業的重大威脅[J].中國農業科學, 2018, 51(21): 4177-4187.
[3] COSTARD S, WIELAND B, De GLANVILLE W, et al. African swine fever: how can global spread be prevented?[J]. Philos Trans R Soc Lond B Biol Sci, 2009, 364 (1530) :2683-2696.
[4] 王清華,任煒杰,包靜月,等.我國首例非洲豬瘟的確診[J].中國動物檢疫, 2018, 35(9): 1-4.
[5] CHANGJIE L, JINGYU Y, LI Z, et al. Infection characteristics and transcriptomics of African swine fever virus in Bama minipigs[J]. Microbiology spectrum, 2022, 10(6):e0383422.
[6] 歐云文,馬小元,王俊,等.非洲豬瘟分子病原學及分子流行病學研究進展[J].中國獸醫學報, 2018, 38(2): 416-420.
[7] BLOME S, GABRIEL C, BEER M. Pathogenesis of African swine fever in domestic pigs and European wild boar[J]. Virus Research, 2013, 173 (1) : 122-130.
[8] 閆文倩,楊博,郝雨,等.非洲豬瘟病毒感染致豬生理生化指標變化的研究進展[J].中國獸醫科學, 2022, 52(10): 1317-1322.
[9] JURADO C, MUR L, PEREZ A M, et al. Risk of African swine fever virus introduction into the United States through smuggling of pork in air passenger luggage[J].Scientific Reports,2019,9(1):14423.
[10] De LORENZI G, BORELLA L, ALBORALI G L, et al. African swine fever: A review of cleaning and disinfection procedures in commercial pig holdings[J]. Research in veterinary science, 2020, 132: 262-267.
[11] ENDRIS R G, HASLETT T M, HESS W R. Experimental transmission of African swine fever virus by the tick Ornithodoros(Alectorobius)puertoricensis(Acari: Argasidae)[J]. Journal of Medical Entomology, 1991, 28(6): 854-858.
[12] PIETSCHMANN J, MUR L, BIOME S, et al. African swine fever virus transmission cycles in Central Europe:Evaluation of wild boar-soft tick contacts through detection of antibodies against Ornithodoros erraticus saliva antigen[J]. BMC Veterinary Research, 2016, 12(1): 1-5.
[13] 扈榮良,于婉琪,陳騰.非洲豬瘟及防控技術研究現狀[J].中國獸醫學報, 2019, 39(2): 357-369.
[14] 陳平,梁昌鏞.非洲豬瘟病毒減毒活疫苗研究進展[J].福建農林大學學報(自然科學版), 2022, 51(6): 721-729
[15] 張洪亮,金銘,趙越,等.非洲豬瘟病毒免疫學及疫苗研究進展[J].病毒學報, 2019, 35(3): 533-541.
[16] 王靜.西班牙與巴西非洲豬瘟防控經驗[J].中國畜牧業, 2020 (16): 51-53
[17] 王琴,趙啟祖.加強生物安全措施是養豬場防控非洲豬瘟的關鍵[J].中國獸藥雜志, 2018, 52(12): 1-5.
[18] 李玉杰,王慶偉,陳志飛.現代規模化豬場生物安全體系的規劃建設[J].養豬, 2018 (6): 73-76.
[19] 朱燕,石海橋.非洲豬瘟背景下引種思考[J].豬業科學, 2022, 39(11):45-47.
[20] JURADO C, MARTINEZ-AVILES M, De La TORRE A, et al. Relevant measures to prevent the spread of African swine fever in the European Union domestic pig sector[J]. Frontiers in Veterinary Science, 2018, 5:77.
[21] 任曉明.防控“非瘟”,人的因素第一[J].今日養豬業, 2021(2):10-12.
[22] 白潔,李瀚明.新形勢下豬場車輛洗消中心建設分析[J].中國動物檢疫,2019, 36(8): 51-53.
[23] 王麗,高開國,楊雪芬,等.新冠肺炎疫情和非瘟形勢下豬飼料生物安全防控策略[J].廣東畜牧獸醫科技, 2020, 45(2): 1-4
[24] THACKER B J, LARSEN R E, JOO H S, et al. Swine diseases transmissible with artificial insemination[J]. JAVMA, 1984, 185 (5) : 511~516
[25] 郭銳,周丹娜,劉澤文,等.某規模化豬場外環境中非洲豬瘟監測及防控建議[J].養殖與飼料, 2023, 22(2): 69-72.
[26] 顧馨,高春起.非洲豬瘟的致病機理及其防控措施研究進展[J].黑龍江畜牧獸醫, 2020 (19): 31-35
[27] 張靖菊,陳孝杰,張志博,等.非洲豬瘟病毒傳播媒介研究進展及豬場高效消毒劑的選用[J].中國豬業,2020, 15(5): 63-68.
[28] 陳澤,羅建勛,殷宏.非洲豬瘟的生物媒介[J].畜牧獸醫學報, 2011, 42(5): 605-612.
[29] 劉靜,劉飛,蔣正軍,等.無非洲豬瘟小區建設要點及成效[J].中國動物檢疫, 2022, 39(1): 48-54.
[30] 江濤,汪長城.我國生豬養殖模式與疫病防控[J].畜牧與飼料科學, 2009, 30(9):158-159.
[31] 康京麗,宋建德,龐素芬,等.國際組織和有關國家非洲豬瘟撲殺措施[J].中國動物檢疫, 2019, 36(3):55-58.

