乳腺癌改良根治術術后患者復發轉移的危險因素分析
【摘要】目的 分析影響乳腺癌改良根治術患者術后復發轉移的危險因素,為臨床提供參考。方法 回顧性分析2018年1月至2022年2月于無錫市第二人民醫院行乳腺癌改良根治術的120例乳腺癌患者的臨床資料,根據是否發生復發轉移分為復發轉移組(42例)與未復發轉移組(78例)。比較兩組患者臨床資料,分析影響乳腺癌改良根治術患者術后復發轉移發生的獨立危險因素。結果 復發轉移組患者腫瘤最大直徑>5 cm占比、糖類抗原125(CA125)水平、環加氧酶-2(COX-2)水平均高于未復發轉移組,TNM分期整體差于未復發轉移組(均P<0.05)。多因素Logistic回歸分析結果顯示,腫瘤最大直徑>5 cm、TNM分期為Ⅲ期、CA125與COX-2水平升高均是影響乳腺癌改良根治術患者術后復發轉移發生的獨立危險因素(均P<0.05)。結論 腫瘤最大直徑>5 cm、TNM分期為Ⅲ期、CA125與COX-2水平升高均是影響乳腺癌改良根治術患者術后復發轉移發生的獨立危險因素,臨床應注意監測。
【關鍵詞】乳腺癌改良根治術;復發轉移;危險因素
【中圖分類號】R737.9 【文獻標識碼】A 【文章編號】2096-2665.2024.22.0129.03
DOI:10.3969/j.issn.2096-2665.2024.22.043
乳腺癌為乳腺上皮細胞在多種致癌因素影響下出現的異常增殖。該病在初期階段常出現乳房腫塊、乳頭異常分泌液體等癥狀。晚期腫瘤細胞可能發生遠端轉移,對患者的生命安全造成威脅[1]。臨床主要采用手術治療等方式治療乳腺癌[2]。其中,乳腺癌改良根治術是一種治療早期乳腺癌的手術方式,可在不切除胸大肌和胸小肌的情況下,徹底清除腋窩淋巴結,實現根治的目的[3]。然而,臨床實踐顯示,部分乳腺癌患者在手術后2年內會出現癌癥復發或轉移的情況[4]。因此,針對患者術后復發及轉移的預防與治療為臨床研究的重點。基于此,本研究分析影響患者術后復發轉移的危險因素,現報道如下。
1 資料與方法
1.1 一般資料 回顧性分析2018年1月至2022年2月于無錫市第二人民醫院行乳腺癌改良根治術的120例乳腺癌患者的臨床資料,根據是否發生復發轉移(通過胸部X線、CT掃描或MRI,監測腫瘤標志物的變化進行診斷[5])分為復發轉移組(42例)與未復發轉移組(78例)。復發轉移組患者年齡30~70歲,平均年齡(55.34±5.36)歲;BMI 20~27 kg/m2,平均BMI(23.47±1.06)kg/m2。未復發轉移組患者年齡31~70歲,平均年齡(55.47±5.38)歲;BMI 20~27 kg/m2,平均BMI(23.51±1.28)kg/m2。兩組患者一般資料比較,差異均無統計學意義(均P>0.05),組間具有可比性。本研究經無錫市第二人民醫院醫學倫理委員會批準。納入標準:⑴符合乳腺癌的診斷標準[5];⑵符合手術指征;⑶術前未出現遠處轉移。排除標準:⑴合并認知功能障礙者;⑵存在嚴重器質性病變者;⑶妊娠期或哺乳期婦女;⑷存在凝血功能障礙者;⑸合并其他惡性腫瘤者。
1.2 手術方法 兩組患者均行乳腺癌改良根治手術,術前常規消毒、鋪巾。患者取仰臥位,將術側肩背部墊高,根據腫瘤部位與患者乳房的形態、大小設計梭形切口,梭形切口與腫瘤邊緣之間的距離>3cm,皮瓣厚度為0.5~1.0 cm,術中僅將胸小肌予以切除,保留胸大肌,清掃淋巴結,再進行切口縫合。術后切口愈合后予以常規化療,取注射用異環磷酰胺(瀚暉制藥有限公司,國藥準字H20084188,規格:0.5 g)500 mg/m2(最大劑量不超過1 000 mg/m2)+5%氯化鈉注射液500 mL進行靜脈滴注、注射用鹽酸表柔比星(浙江海正藥業股份dOVBNT4+nro7SzPi5hMnbA==有限公司,國藥準字H20183145,規格:10 mg)30 mg/m2(最大劑量不超過60 mg/m2)+5%氯化鈉注射液250 mL進行靜脈滴注、注射用氟尿嘧啶[吉斯美(武漢)制藥有限公司,國藥準字H20050465,規格:0.125 g]500 mg/m2(最大劑不超過量800 mg/m2)+5%葡萄糖液500 mL進行靜脈滴注,1次/周,共治療3周。化療結束后1個月放療,固定體位后行CT掃描,掃描部位包括區域淋巴結、胸壁及內乳區。根據檢查結果,制訂放療計劃并復位,完成后安排患者放療,患者平躺至治療機房治療床上,行體膜固定,根據激光線進行擺位,擺至合適位置后行照視完成放療,共治療7周。放療結束后通過電話、電子郵件和門診隨訪的方式對患者進行每月1次為期2年的隨訪,并記錄患者的復發轉移情況。
1.3 觀察指標 ⑴比較兩組患者臨床資料。包括腫瘤最大直徑(>5 cm、≤5 cm)、TNM分期[6](Ⅰ期、Ⅱ期、Ⅲ期)、病理類型(導管癌早期浸潤、浸潤性非特殊型癌、浸潤性特殊型癌)、淋巴結轉移(<4個、≥4個)、吸煙史(連續或累計吸煙6個月或以上)、飲酒史(連續或累計飲酒5年以上,等效酒精含量大于40 g/d)、糖類抗原125(CA125)、環加氧酶-2(COX-2)。采集兩組患者術前清晨空腹靜脈血5 mL,采用離心機以3 000 r/min的轉速離心5 min(離心半徑為10 cm),取上清液,采用電化學發光法檢測CA125水平,采用酶聯免疫吸附法檢測COX-2水平。⑵分析影響乳腺癌改良根治術患者術后復發轉移發生的獨立危險因素。
1.4 統計學分析 采用SPSS 22.0統計學軟件處理數據。計數資料以[例(%)]表示,組間比較采用χ2檢驗,等級資料比較采用秩和檢驗;計量資料以(x)表示,組間比較采用獨立樣本t檢驗。影響因素采用多因素Logistic 回歸分析。以P<0.05為差異有統計學意義。
2 結果
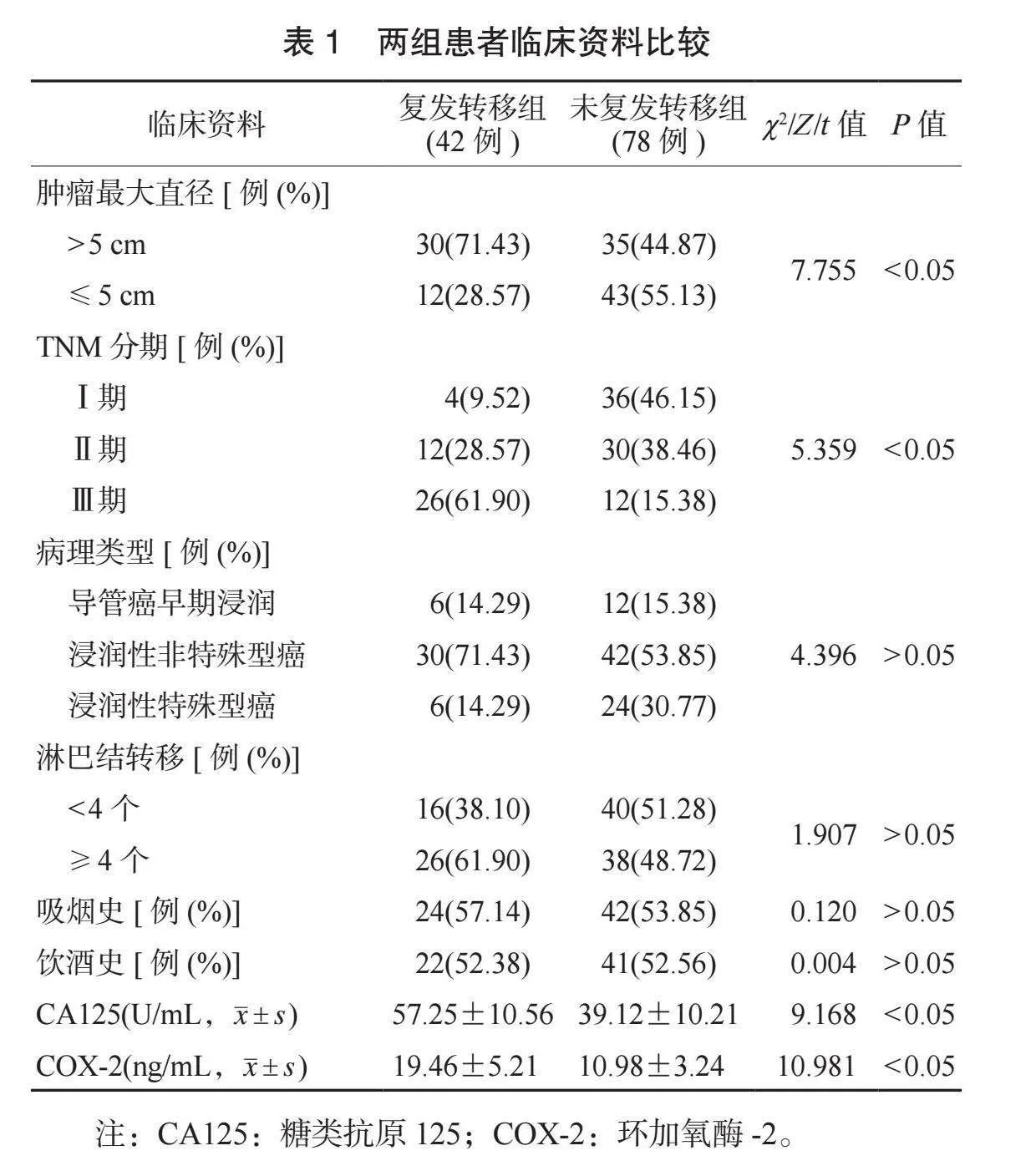
2.1 兩組患者臨床資料比較 兩組患者病理類型、淋巴結轉移、吸煙史與飲酒史占比比較,差異均無統計學意義(均P>0.05);復發轉移組患者腫瘤最大直徑>5 cm占比、CA125水平、COX-2水平均高于未復發轉移組,TNM分期整體差于未復發轉移組,差異均有統計學意義(均P<0.05),見表1。
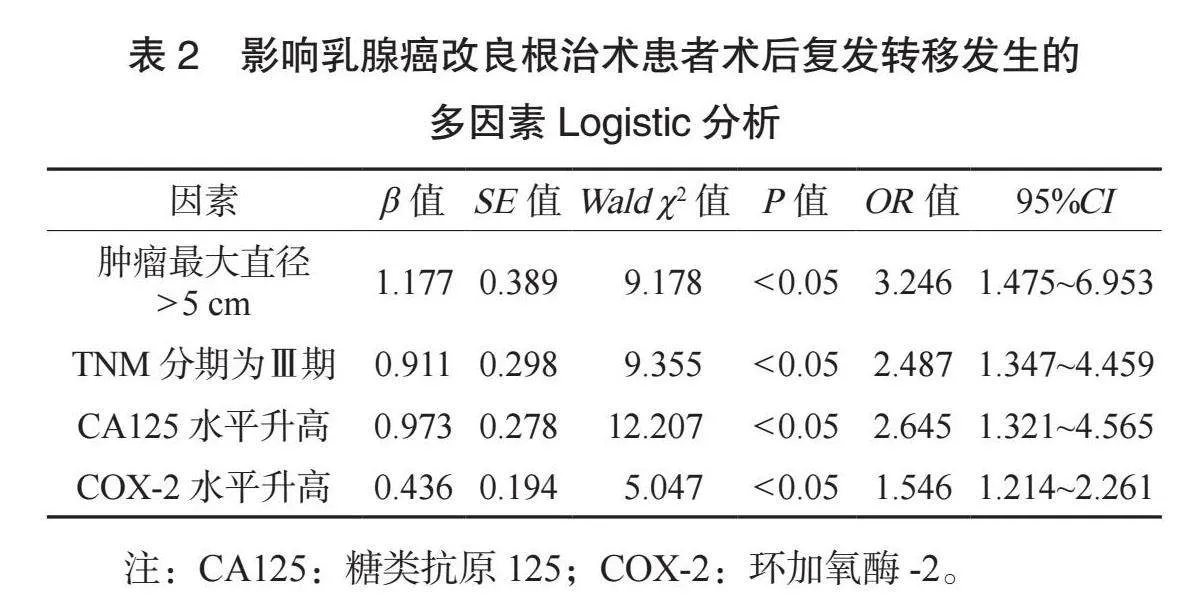
2.2 影響乳腺癌改良根治術患者術后復發轉移發生的多因素Logistic分析 將可能影響乳腺癌改良根治術患者術后復發轉移發生的因素量化賦值,以是否發生術后復發轉移為因變量(是=1,否=0),以腫瘤最大直徑(>5 cm=1,≤5 cm=0)、TNM分期(Ⅲ期=1,Ⅰ期、Ⅱ期=0)、CA125(連續變量)、COX-2(連續變量)為自變量。多因素Logistic回歸分析結果顯示,腫瘤最大直徑>5 cm、TNM分期為Ⅲ期、CA125與COX-2水平升高均是影響乳腺癌改良根治術患者術后復發轉移發生的獨立危險因素(均P<0.05),見表2。
3 討論
乳腺癌發病機制復雜,與多種因素有關,包括激素水平、生活方式、環境因素及個人病史等[7]。早期乳腺癌患者5年生存率相對較高,因此,及早發現并采取合適的治療手段,對于提高患者生存率極為關鍵[8]。乳腺癌改良根治術在治療乳腺癌的過程中展現出卓越的治療成果,但仍存在術后復發與轉移的問題,影響患者術后生存質量[9]。一旦手術后出現復發或轉移,患者的病情惡化,有可能引起一系列的并發癥,影響預后。因此,探討影響術后復發轉移的危險因素具有極其重要的意義。
本研究結果顯示,復發轉移組患者腫瘤最大直徑>5 cm占比、CA125水平、COX-2水平均高于未復發轉移組,TNM分期整體差于未復發轉移組;多因素Logistic回歸分析結果顯示,腫瘤最大直徑>5 cm、TNM分期為Ⅲ期、CA125與COX-2水平升高均是影響乳腺癌改良根治術患者術后復發轉移發生的獨立危險因素。這提示上述因素均與乳腺癌患者術后復發轉移有關。分析原因為,腫瘤最大直徑>5 cm提示腫瘤細胞更易穿透基底膜,進入血管或淋巴管,增加腫瘤細胞全身擴散的風險。這一擴散過程被稱為轉移,是導致乳腺癌患者術后復發的主要因素之一。此外,腫瘤最大直徑較大通常表示腫瘤的生長速度較快,這可能與腫瘤細胞的侵襲性和異質性增強有關,腫瘤細胞所呈現的基因表達模式存在發生轉換的可能性,導致其對治療的抵抗性增強。有研究顯示,腫瘤體積越大,術中徹底清除的難度越高,較大的病灶易導致殘留,使術后復發的風險相應增加[10]。TNM分期是根據腫瘤的大小(T)、淋巴結轉移情況(N)和遠處轉移(M)來評估癌癥的嚴重程度和預后的重要指標。乳腺癌患者的TNM分期越高,提示腫瘤體積較大、淋巴結轉移廣泛或存在遠處轉移。高TNM分期的乳腺癌患者具有更高的腫瘤異質性,腫瘤細胞在基因和表型上表現出更多的多樣性,使腫瘤更易適應環境壓力,在手術后迅速增殖和擴散。免疫逃逸也是導致高TNM分期乳腺癌患者術后復發轉移的重要機制之一,腫瘤細胞能夠通過下調腫瘤抗原的表達、分泌免疫抑制因子或招募調節性免疫細胞等,使腫瘤細胞能在體內存活并擴散至其他部位。有研究顯示,CA125能夠通過激活磷脂酰肌醇3-激酶(PI3K)/蛋白激酶B(Akt)和絲裂原激活蛋白激酶(MAPK)/細胞外信號調節激酶(ERK)信號傳導通路,促使腫瘤細胞增長并提升其抗凋亡功能,從而加速腫瘤的生長速度[11]。COX-2是一種在體內廣泛分布的酶,能夠促進前列腺素E2(PGE2)的生成,PGE2是一種具有多種生物活性的脂質介質,能夠通過與其受體結合激活下游信號通路,從而加速腫瘤細胞的增長、擴散和血管新生;COX-2還能夠通過抑制細胞凋亡、促進腫瘤微環境的免疫逃逸等機制,進一步增強腫瘤細胞的生存能力[11]。
綜上所述,腫瘤最大直徑>5 cm、TNM分期為Ⅲ期、CA125與COX-2水平升高均是影響乳腺癌改良根治術患者術后復發轉移發生的獨立危險因素,臨床應注意監測,為早期診斷和干預提供參考依據。
參考文獻
成香,杜若飛,周會月,等.乳腺癌患者癥狀群管理的研究進展[J].中國實用護理雜志, 2020, 36(28): 2224-2229.
梁欣,劉維,荊海紅.早期乳腺癌患者改良根治術與保乳手術治療的效果及對患者術后生活質量的影響[J].實用癌癥雜志, 2021, 36(5): 793-795.
董馬鋒,李永剛.乳腺癌改良根治術后切口感染患者的降鈣素原、C反應蛋白、凝血功能指標變化及臨床意義[J].血栓與止血學, 2022, 28(3): 1002-1004.
何梅,趙振慧,李迅.乳腺癌規范化根治術后復發轉移的多因素調查[J].河北醫藥, 2021, 43(11): 1735-1738, 1742.
中國抗癌協會乳腺癌專業委員會.中國抗癌協會乳腺癌診治指南與規范(2015版)[J].中國癌癥雜志, 2015, 25(9): 692-754.
楊文濤,步宏.乳腺癌新輔助化療后的病理診斷專家共識[J].中華病理學雜志, 2015, 44(4): 232-236.
李佳圓.中國乳腺癌危險因素研究現況及其風險預測模型研究展望[J].中國循證醫學雜志, 2020, 20(7): 745-748.
湯濤.早期乳腺癌不同手術治療方案的安全性、臨床療效及對患者生活質量的影響[J].實用癌癥雜志, 2018, 33(5): 821-823, 826.
吳云,金漢生.區段切除術和改良根治術治療乳腺癌療效比較[J].中國現代普通外科進展, 2022, 25(1): 62-64.
張澤玉,賈婷婷,邱體紅,等.影響乳腺癌改良根治術患者術后復發轉移的有序logistic分析[J].實用癌癥雜志, 2020, 35(2): 263-266.
許思哲,賀功建,曾黎,等.乳腺癌根治術患者化療前后血清CA153、CA125、TPS水平變化及對預后的影響[J].實用癌癥雜志, 2020, 35(4): 639-642.

