棉花抗黃萎病相關(guān)基因GhERF020 功能的初步分析
摘要:黃萎病(Verticillium wilt)是影響我國(guó)棉花產(chǎn)量和品質(zhì)的重要病害,其病原菌是大麗輪枝菌(Verticillium dahliae)。AP2/ERF類(lèi)轉(zhuǎn)錄因子在植物生長(zhǎng)發(fā)育和脅迫適應(yīng)性響應(yīng)中的作用日益突顯。為挖掘棉花抗黃萎病相關(guān)基因并探究其生物學(xué)功能,利用擬南芥抗大麗輪枝菌相關(guān)基因AT1G22810.1,同源比對(duì)獲得棉花抗黃萎病候選基因GhERF020(XM_016842745.1)。生物信息學(xué)分析結(jié)果表明,GhERF020 開(kāi)放閱讀框的長(zhǎng)度為441 bp,編碼147個(gè)氨基酸;其蛋白含有1個(gè)保守的AP2結(jié)構(gòu)域,相對(duì)分子質(zhì)量為16.16 kD,無(wú)跨膜結(jié)構(gòu),屬于親水蛋白;預(yù)測(cè)其啟動(dòng)子區(qū)域含有水楊酸、茉莉酸甲酯和脫落酸等響應(yīng)元件。基因表達(dá)模式分析發(fā)現(xiàn),GhERF020 受大麗輪枝菌侵染誘導(dǎo)表達(dá)。亞細(xì)胞定位分析表明,GhERF020蛋白定位于細(xì)胞核中。利用病毒誘導(dǎo)的基因沉默(virus-induced gene silencing, VIGS)技術(shù)下調(diào)GhERF020 表達(dá)后,棉花植株對(duì)大麗輪枝菌的敏感性顯著增強(qiáng),病情指數(shù)和病原菌生物量明顯升高。由此表明,GhERF020是棉花抗黃萎病的正向調(diào)控因子。
關(guān)鍵詞:棉花黃萎病;大麗輪枝菌;轉(zhuǎn)錄因子;GhERF020;VIGS
doi:10.13304/j.nykjdb.2023.0407
中圖分類(lèi)號(hào):S562;Q78 文獻(xiàn)標(biāo)志碼:A 文章編號(hào):1008‐0864(2024)09‐0112‐10
棉花是重要的經(jīng)濟(jì)作物之一,也是我國(guó)農(nóng)業(yè)安全的重要組成部分[1]。棉花黃萎病(Verticilliumwilt,VW)主要是由大麗輪枝菌(Verticilliumdahliae)引發(fā)的土傳性真菌維管束病害。大麗輪枝菌通過(guò)土壤傳播,入侵植物維管組織進(jìn)而引發(fā)病害,嚴(yán)重影響棉花的品質(zhì)和產(chǎn)量[2];其具有寄主范圍廣、傳播速度快、破壞面積大和環(huán)境適應(yīng)性強(qiáng)等特點(diǎn),防治極為困難。目前還沒(méi)有針對(duì)大麗輪枝菌的有效殺菌劑[3]。因此,深入挖掘棉花抗黃萎病相關(guān)基因資源,探究棉花抗黃萎病分子機(jī)制,進(jìn)而利用生物育種的方式培育抗病品種是防治黃萎病的穩(wěn)定而有效的方法。
轉(zhuǎn)錄因子(transcription factors,TF)在植物響應(yīng)逆境脅迫中發(fā)揮著不可或缺的作用,可調(diào)控與抗逆性狀相關(guān)基因的表達(dá),使植物抗逆性得到顯著改善。因此,轉(zhuǎn)錄因子的發(fā)掘鑒定已逐漸成為植物抗逆育種的關(guān)鍵。AP2/ERF是植物特有的一類(lèi)轉(zhuǎn)錄因子,具有60~70個(gè)氨基酸的AP2/ERF型DNA結(jié)合域[4]。根據(jù)其序列相似性和AP2/ERF結(jié)構(gòu)域的數(shù)量,將其分成4 類(lèi),分別為AP2(APETALA2)、ERF(ethylene-responsive elementbinding factors)、RAV(related to ABI3/VP1)和DREB (dehydration-responsive element bindingprotein)亞家族[5]。其中,ERF 亞家族只含有1 個(gè)AP2 保守結(jié)構(gòu)域,可特異性結(jié)合基因上游AGCCGCC 元件(CCC-box),參與植物水楊酸(salicylicacid,SA)、茉莉酸(jasmonicacid,JA)和乙烯(ethylene,ET)等多個(gè)信號(hào)傳導(dǎo)途徑,在植物生長(zhǎng)發(fā)育和脅迫應(yīng)答中發(fā)揮著重要的調(diào)控作用[6]。
近年來(lái),ERF類(lèi)轉(zhuǎn)錄因子得到廣泛關(guān)注,已在擬南芥[5]、水稻[5]、大豆[7]、番茄[8]、楊樹(shù)[9]等植物中鑒定出來(lái)并對(duì)其功能進(jìn)行闡述。ERF類(lèi)轉(zhuǎn)錄因子的調(diào)控方式復(fù)雜,不僅可正向調(diào)控植物抗性,也可負(fù)調(diào)控植物抗性。在擬南芥中過(guò)表達(dá)AtERF1可提高植株對(duì)灰霉菌和黃瓜織球殼菌等壞死性真菌的抗性[10]。過(guò)表達(dá)馬鈴薯StERF94 基因可增強(qiáng)與編碼病程相關(guān)防御基因的表達(dá),抑制病菌繁殖,從而增強(qiáng)馬鈴薯對(duì)枯萎病的抵抗力[11]。水稻OsERF922的RNAi沉默轉(zhuǎn)化子增強(qiáng)了水稻對(duì)稻瘟病菌抗性,過(guò)表達(dá)該基因使植株對(duì)稻瘟病菌的入侵更加敏感[12],并且利用CRISPR/Cas9(clusted regularlyinterspaced short palindromic repeats and CRISPassociatedprotein 9)技術(shù)編輯水稻OsERF922 可提高水稻抗稻瘟病菌的能力[13]。研究表明,擬南芥ERF019通過(guò)抑制病原體相關(guān)分子模式(pathogenassociatedmolecular patterns,PAMP)激發(fā)的免疫反應(yīng)負(fù)向調(diào)控對(duì)寄生疫霉菌的抗性[14]。植物感受并識(shí)別來(lái)自病菌的信號(hào)后,通過(guò)激活SA、ET和JA等植物激素的信號(hào)轉(zhuǎn)導(dǎo)途徑,從而準(zhǔn)確調(diào)控植物的防衛(wèi)反應(yīng),有些ERF轉(zhuǎn)錄因子在抗病信號(hào)交叉途徑中發(fā)揮重要作用,是關(guān)鍵的連接因子[15-17]。
在野生型擬南芥中,ERF1 受ET 和茉莉酸甲酯(methyl jasmonate,MEJA)誘導(dǎo)表達(dá),作用于ET和JA交叉途徑的下游,是探究2種信號(hào)聯(lián)合調(diào)控抗病機(jī)制的關(guān)鍵元素,可調(diào)節(jié)下游防御反應(yīng)基因[18]。ERF96可結(jié)合ET和JA響應(yīng)的防衛(wèi)基因PDF1.2a、PR-3 和PR-4 的GCC 基序,進(jìn)而正向調(diào)控植物對(duì)死體營(yíng)養(yǎng)型病原菌的抗性[19]。在陸地棉(Gossypium hirsutum L.)中共鑒定了220個(gè)包含AP2單結(jié)構(gòu)域的基因[20],然而和抗性相關(guān)的相對(duì)較少,尤其是與黃萎病抗性相關(guān)的ERF亞族轉(zhuǎn)錄因子亟待深入研究。本實(shí)驗(yàn)室前期通過(guò)對(duì)接種大麗輪枝菌的擬南芥進(jìn)行轉(zhuǎn)錄組和代謝組學(xué)分析,發(fā)現(xiàn)了大量差異表達(dá)基因(differentialexpression genes, DEGs)。通過(guò)生物信息學(xué)分析錨定擬南芥抗大麗輪枝菌基因AT1G22810.1,并從NCBI網(wǎng)站獲得棉花基因組中與其高度同源的基因GhERF020(XM_016842745.1),利用亞細(xì)胞定位和病毒誘導(dǎo)的基因沉默(virus-induced genesilencing,VIGS)技術(shù)對(duì)該基因在棉花抗黃萎病中的功能進(jìn)行初步探究,為進(jìn)一步闡述該基因的抗病分子機(jī)制奠定基礎(chǔ)。
1 材料與方法
1.1 試驗(yàn)材料
以陸地棉品種R15為試驗(yàn)材料。棉花VIGS載體為pTRV1、pTRV2、pTRV2-CLA1,大麗輪枝菌為強(qiáng)致病力菌系V991,大腸桿菌Trans1-T1 感受態(tài)細(xì)胞、大腸桿菌DH5α 菌株、根瘤農(nóng)桿菌GV3101感受態(tài)細(xì)胞均由中國(guó)農(nóng)業(yè)科學(xué)院生物技術(shù)研究所提供。
1.2 試驗(yàn)試劑
植物總RNA小量提取試劑盒購(gòu)自廣州美基(Magen)生物有限公司;質(zhì)粒小提試劑盒購(gòu)自天根生化科技(北京)有限公司;DNA Marker、反轉(zhuǎn)錄試劑盒MonScriptTM RT Ⅲ all-in-one Mix(withdsDNase)購(gòu)自莫納(Monad)生物科技有限公司;2×Taq PCR Mix購(gòu)自北京艾德萊生物科技有限公司;限制性?xún)?nèi)切酶EcoR Ⅰ、BamH Ⅰ購(gòu)自NEB(北京)有限公司;2×Assembly Mix、熒光定量試劑盒2×ChamQ Universal SYBR qPCR Master Mix 購(gòu)自南京諾唯贊生物科技股份有限公司。
1.3 試驗(yàn)方法
1.3.1 GhERF020 生物信息學(xué)分析
在NCBI 網(wǎng)站中比對(duì)擬南芥抗黃萎病基因AT1G22810.1,發(fā)現(xiàn)棉花高度同源基因GhERF020 (XM_016842745.1)。利用MEGA 11對(duì)來(lái)自不同物種的同源基因的氨基酸序列構(gòu)建系統(tǒng)進(jìn)化樹(shù);利用Cotton FGD 網(wǎng)站(https://cottonfgd.org/)獲得GhERF020 的編碼區(qū)(coding sequence, CDS)及基因組DNA 序列;使用NCBI 在線(xiàn)工具Batch CDsearch(https://www.ncbi.nlm.nih.gov/Structure/cdd/wrpsb.cgi)預(yù)測(cè)基因的保守結(jié)構(gòu)域;使用ProtParam在線(xiàn)網(wǎng)站(http://web.expasy.org/protparam)預(yù)測(cè)GhERF020蛋白的分子量、氨基酸組成、不穩(wěn)定指數(shù)、理論等電點(diǎn)、總平均親水性等理化性質(zhì);使用TMHMM(http://www.cbs.dtu.dk/services/TMHMM/)預(yù)測(cè)跨膜結(jié)構(gòu)域;使用SignalP5.0(http://www.cbs.dtu. dk/services/SignalP/index. php)預(yù)測(cè)信號(hào)肽;使用SOPMA (http://npsa-pbil. ibcp. fr/cgi-bin/npsa_automat.pl?page=npsa_sopma.html)預(yù)測(cè)蛋白質(zhì)二級(jí)結(jié)構(gòu);使用SWISS-MODEL(https://www.swissmodel.expasy.org/)預(yù)測(cè)蛋白質(zhì)三級(jí)結(jié)構(gòu);使用Plant-mPLoc 網(wǎng)站(http://www. csbio. sjtu. edu. cn/bioinf/plant-multi/)預(yù)測(cè)GhERF020 蛋白的功能結(jié)構(gòu)域。
1.3.2 基因表達(dá)分析
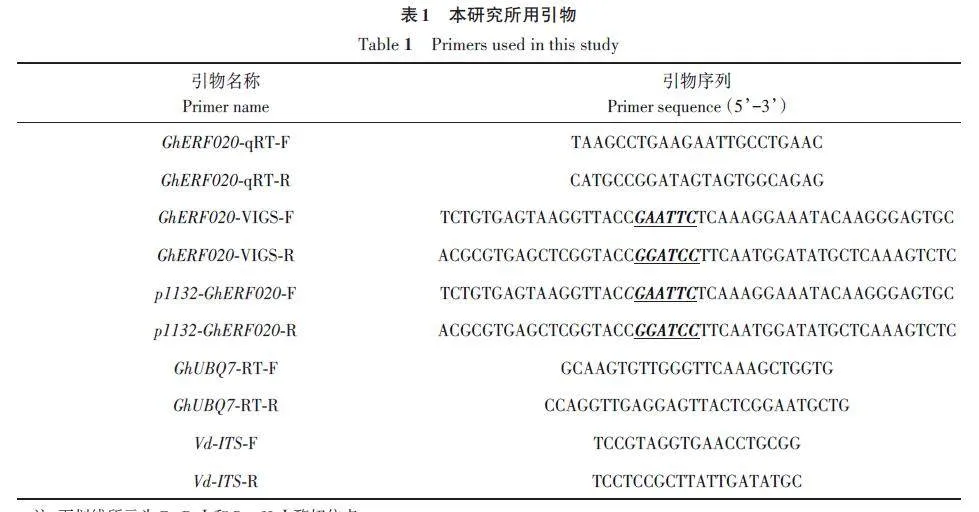
取V991菌液(107 CFU·mL-1)1 mL加入含有卡那青霉素和羧芐青霉素抗生素的CM(complete medium)培養(yǎng)基(6 g·L-1酵母提取物、6 g·L-1 酸水解酪蛋白和10 g·L-1 蔗糖)中,28 ℃、220 r·min-1 震蕩培養(yǎng)4~5 d,鏡檢觀(guān)察孢子并利用血球計(jì)數(shù)板統(tǒng)計(jì)孢子含量。當(dāng)孢子量達(dá)到107 CFU·mL-1時(shí)用4層紗布過(guò)濾掉菌絲體,收集孢子液。當(dāng)棉花長(zhǎng)至2葉1心時(shí),將其根部浸泡在V991 孢子懸浮液中0.0、0.5、1.0、2.0、4.0、8.0 和12.0 h后,分別提取根、莖、葉組織的RNA,并反轉(zhuǎn)錄合成cDNA。以棉花管家基因GhUBQ7(LOC107925174)作為內(nèi)參基因,使用GhUBQ7-RT-F/R 與GhERF020-qRT-F/R( 表1)進(jìn)行RTqPCR擴(kuò)增,每個(gè)樣本3次重復(fù)。反應(yīng)結(jié)束后,根據(jù)目的基因和內(nèi)參基因的Ct值,使用2-ΔΔCt法[21]計(jì)算目的基因的表達(dá)量。
1.3.3 GhERF020 亞細(xì)胞定位
結(jié)合在線(xiàn)平臺(tái)WoLFPROST(https://wolfpsort.hgc.jp/)預(yù)測(cè)的亞細(xì)胞定位結(jié)果,用p1132-GhERF020-F/R(表1,下劃線(xiàn)處為EcoR Ⅰ和BamH Ⅰ酶切位點(diǎn))克隆GhERF020基因的開(kāi)放閱讀框(open reading frame, ORF)序列,并插入含有綠色熒光蛋白(green fluorescentprotein,GFP)基因表達(dá)載體pYBA1132(BamH Ⅰ和EcoR Ⅰ酶切位點(diǎn))中。將構(gòu)建成功的質(zhì)粒轉(zhuǎn)入農(nóng)桿菌EHA105中并在煙草中瞬時(shí)表達(dá)。注射煙草下表皮48 h后在LSM980共聚焦激光掃描顯微鏡(Zeiss,Jena,Germany)下觀(guān)察熒光亞細(xì)胞定位情況。細(xì)胞核標(biāo)記載體pH2B-mCherry[22]由中國(guó)農(nóng)業(yè)科學(xué)院生物技術(shù)研究所王磊研究員提供。
1.3.4 棉花VIGS
設(shè)計(jì)特異性引物GhERF020-VIGS-F/R(表1),PCR 擴(kuò)增GhERF020 基因VIGS片段,插入pTRV2 多克隆位點(diǎn)EcoR Ⅰ和BamH Ⅰ間。利用電擊轉(zhuǎn)化法將pTRV2-GhERF020 質(zhì)粒轉(zhuǎn)入農(nóng)桿菌GV3101。農(nóng)桿菌介導(dǎo)的棉花VIGS操作按照Gao等[23]的方法進(jìn)行。注射VIGS菌液之后,觀(guān)察注射pTRV2-CLA1 菌液植株葉片的白化情況,當(dāng)?shù)?片真葉出現(xiàn)葉脈網(wǎng)格狀白化即可進(jìn)行沉默效率檢測(cè),取沉默植株與對(duì)照植株葉片大小一致的第1 片真葉,提取RNA 并反轉(zhuǎn)錄合成cDNA,使用引物GhERF020-qRT-F/R(表1),采用RT-qPCR檢測(cè)沉默效率。
1.3.5 GhERF020 棉花沉默植株黃萎病抗病性鑒定
使用1.3.2的棉花接菌方法,將棉花的根浸泡在孢子液(107 CFU·mL-1)5 min,然后重新移栽至營(yíng)養(yǎng)土中。10 d后觀(guān)察棉花表型并統(tǒng)計(jì)病情指數(shù)。病情分為5級(jí):0級(jí),無(wú)病葉,正常生長(zhǎng);1級(jí),子葉變黃,真葉無(wú)病;2級(jí),所有子葉均發(fā)病,1~3片真葉發(fā)病;3級(jí),包括子葉在內(nèi)的5片以上棉花葉片發(fā)病;4級(jí),所有葉片發(fā)病,并有葉片脫落,或植物死亡[24]。病情指數(shù)的計(jì)算公式如下[25]。
病情指數(shù)=Σ(每一級(jí)病株數(shù)× 相應(yīng)病害等級(jí)/(10 × 4) )×100(1)
提取棉花基因組DNA,在大麗輪枝菌基因組DNA中核糖體RNA基因ITS1和ITS2區(qū)域(Z29511)檢測(cè)真菌生物量,使用的引物為Vd-ITS-F/R,內(nèi)參基因?yàn)镚hUBQ7(表1)。RT-qPCR反應(yīng)在ABI7500 Fast儀器上進(jìn)行,數(shù)據(jù)通過(guò)2-ΔΔCt法[21]分析。
2 結(jié)果與分析
2.1 GhERF020 基因生物信息學(xué)分析
2.1.1 棉花GhERF020 基因的同源性及結(jié)構(gòu)分析
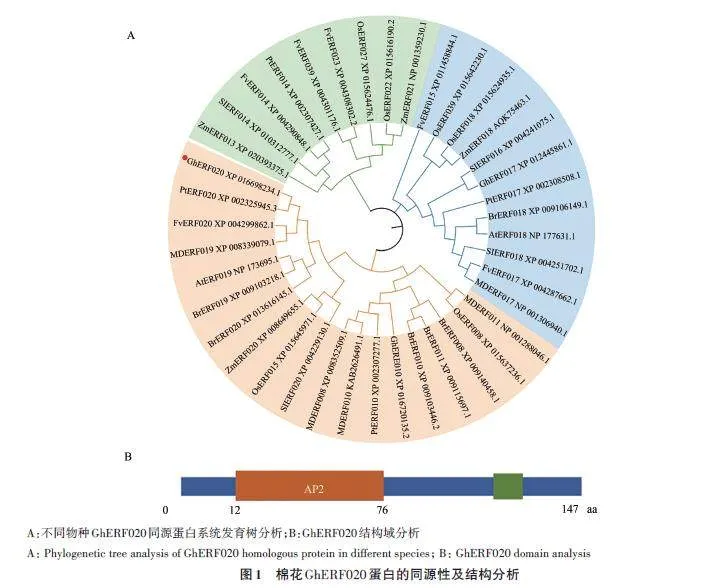
通過(guò)在NCBI 網(wǎng)站中比對(duì)擬南芥基因AT1G22810.1,獲得棉花基因組中與其高度同源的基因XM_016842745.1,將其命名為GhERF020。利用MEGA 11對(duì)來(lái)自不同物種同源基因的氨基酸序列構(gòu)建系統(tǒng)進(jìn)化樹(shù),結(jié)果(圖1A)發(fā)現(xiàn),GhERF020 基因與毛楊、蘋(píng)果的親緣關(guān)系較近,與草莓、土豆等的親緣關(guān)系較遠(yuǎn)。該基因全長(zhǎng)444bp,無(wú)內(nèi)含子,編碼147個(gè)氨基酸;僅含有1個(gè)AP2保守結(jié)構(gòu)域,位于12~76位氨基酸之間,推測(cè)屬于AP2/ERF轉(zhuǎn)錄因子超家族ERF亞家族類(lèi)轉(zhuǎn)錄因子(圖1B)。
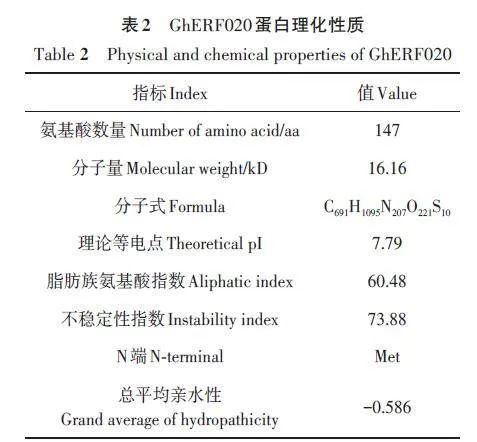
2.1.2 GhERF020 蛋白理化性質(zhì)分析
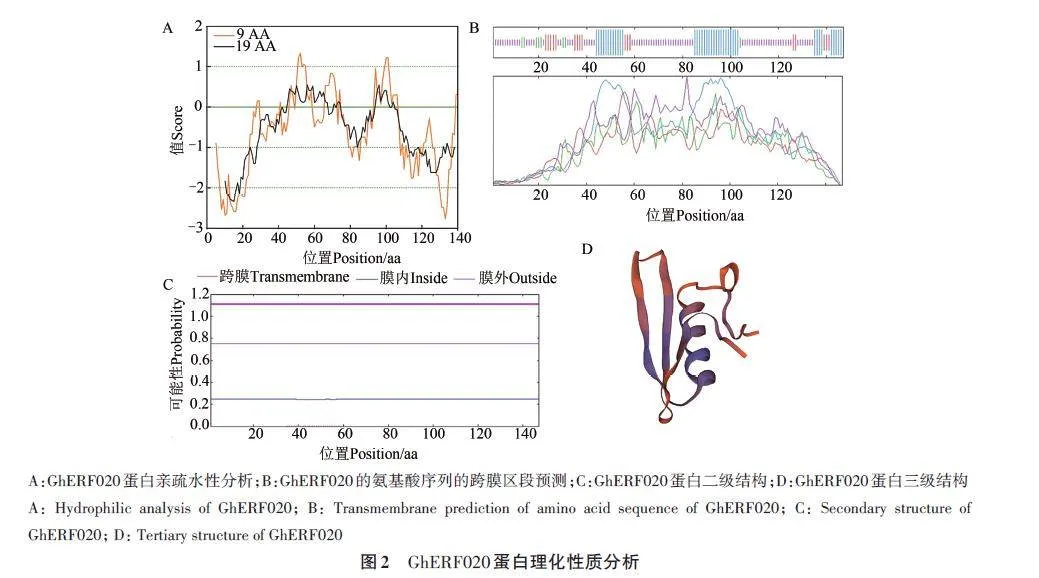
對(duì)GhERF020蛋白的組成成分及其理化性質(zhì)進(jìn)行分析,結(jié)果(表2)表明,GhERF020 蛋白分子式為C691H1095N207O221S10,分子量為16.16 kD,含有丙氨酸(Ala)、精氨酸(Arg)、天冬酰胺(Asn)等20種氨基酸,其中絲氨酸(Ser)、丙氨酸(Ala)、甘氨酸(Gly)含量較高,分別為12.2%、9.5%、8.2%;親疏水性分析顯示,該蛋白為親水性蛋白(圖2A);二級(jí)結(jié)構(gòu)主要由α-螺旋、延伸鏈、β-折疊和無(wú)規(guī)則卷曲構(gòu)成(圖2B),4種結(jié)構(gòu)包含的氨基酸數(shù)量分別為40、18、8、81,占比分別為27.21%、12.24%、5.44%和55.10%。跨膜結(jié)構(gòu)域預(yù)測(cè)GhERF020蛋白為非膜蛋白,位于膜外側(cè),因此推測(cè)該蛋白游離在細(xì)胞質(zhì)中發(fā)揮作用(圖2C);三級(jí)結(jié)構(gòu)具α-螺旋、β-折疊和無(wú)規(guī)則卷曲等空間結(jié)構(gòu)(圖2D)。
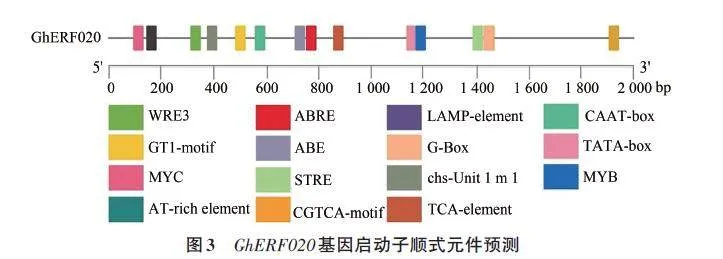
2.1.3 GhERF020 基因上游啟動(dòng)子順式元件分析
利用Plant CARE在線(xiàn)分析軟件對(duì)GhERF020基因起始密碼子上游約2 000 bp啟動(dòng)子序列反義鏈進(jìn)行分析,該啟動(dòng)子上有15個(gè)真核生物所必需的核心元件CAAT-box和24個(gè)TATA-box;除此之外,在啟動(dòng)子區(qū)域還有許多功能性元件,如ABRE脫落酸響應(yīng)元件、ARE 厭氧誘導(dǎo)作用元件、CGTCA-motif MEJA反應(yīng)元件、水楊酸響應(yīng)有關(guān)的順式結(jié)構(gòu)元件TCA-element及光響應(yīng)元件GT1-box、LAMP-element、G-box等(圖3)。因此,GhERF020 可能受到激素誘導(dǎo)進(jìn)而調(diào)控抗病相關(guān)基因參與抗黃萎病脅迫反應(yīng)。
2.2 GhERF020 基因表達(dá)模式分析
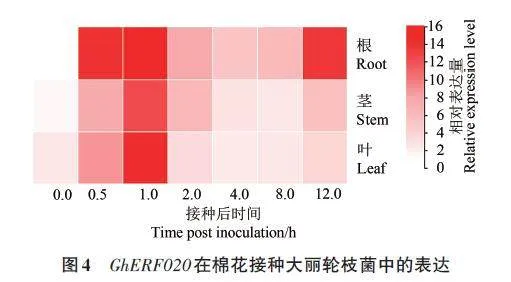
RT-qPCR結(jié)果(圖4)顯示,GhERF020 在大麗輪枝菌侵染0.5 h時(shí)輕度誘導(dǎo)表達(dá),1.0 h時(shí)達(dá)到峰值;組織特異性分析結(jié)果表明,GhERF020 在棉花根、莖和葉中均有表達(dá)。綜上所述,GhERF020 在棉花感染大麗輪枝菌后被誘導(dǎo)表達(dá),并參與棉花對(duì)大麗輪枝菌的抗性反應(yīng)。
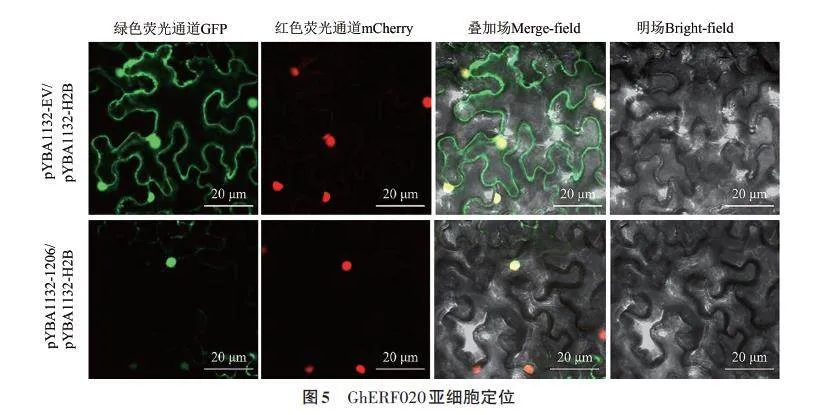
2.3 GhERF020 亞細(xì)胞定位分析
為了確定GhERF020的亞細(xì)胞定位,構(gòu)建了pYBA1132-GhERF020-GFP 融合質(zhì)粒,并將對(duì)照pYBA1132-GFP 載體和核定位基因H2B-mCherry轉(zhuǎn)化到煙草葉片中瞬時(shí)表達(dá),結(jié)果(圖5)顯示,作為對(duì)照的pYBA1132-GFP蛋白定位在細(xì)胞膜、細(xì)胞質(zhì)和細(xì)胞核,表明煙草瞬時(shí)表達(dá)體系建立;GhERF020-GFP融合蛋白與H2B-mCherry的共定位信號(hào)僅在細(xì)胞核中可見(jiàn)。因此,GhERF020可能是核定位蛋白,在激活下游抗病基因表達(dá)方面發(fā)揮作用。
2.4 GhERF020 基因沉默導(dǎo)致棉花對(duì)黃萎病的敏感性增加
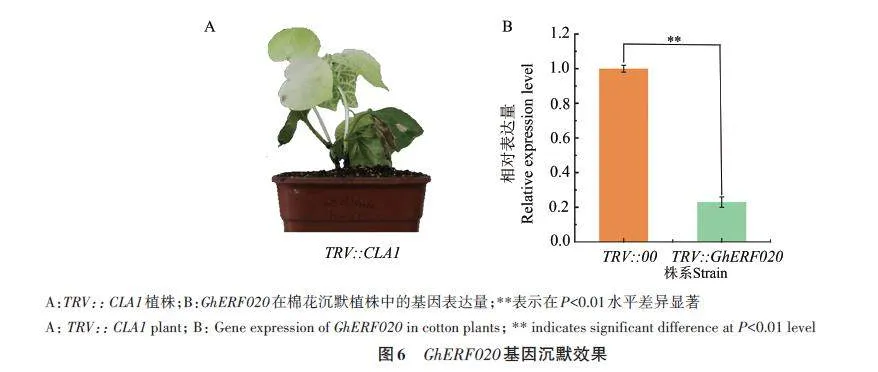
為探究GhERF020 在棉花抗黃萎病中的作用,對(duì)棉花幼苗進(jìn)行VIGS處理10 d后,沉默CLA1基因的棉苗(TRV2::CLA1)新生真葉出現(xiàn)白化表型(圖6A)。利用RT-qPCR檢測(cè)基因表達(dá),結(jié)果(圖6B)顯示,沉默組(TRV2::GhERF020)的GhERF020基因表達(dá)量較對(duì)照組(TRV2::00)降低76.7%,沉默效果顯著。由此表明,VIGS體系建立成功,并且成功獲得GhERF020 沉默植株,可繼續(xù)用于抗黃萎病功能分析。
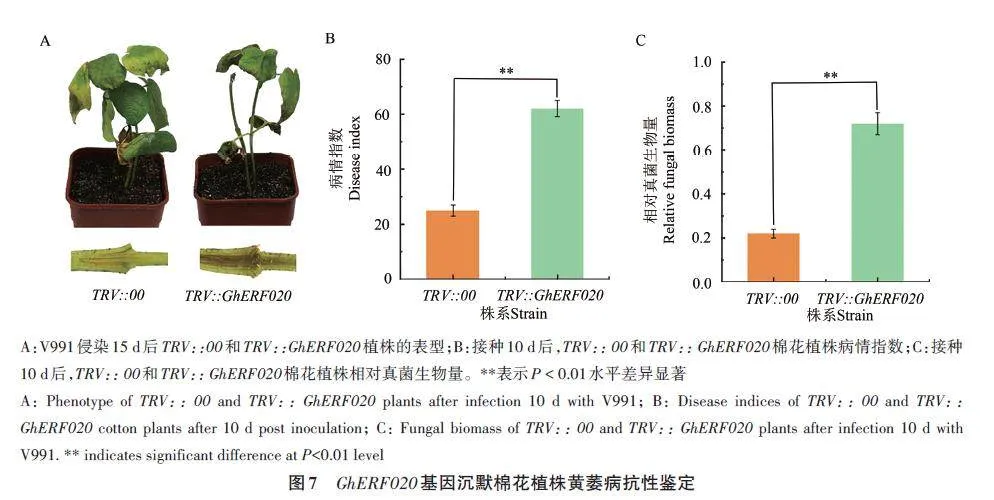
將對(duì)照組和沉默組植株接種V991 10 d后,對(duì)照組表現(xiàn)為個(gè)別葉片葉緣黃化、向下卷曲;GhERF020 沉默組表現(xiàn)出嚴(yán)重的植株萎蔫、葉片脫落等黃萎病癥狀。取GhERF020沉默組和對(duì)照組植株的子葉連接處分別進(jìn)行剖桿觀(guān)察,結(jié)果(圖7A)顯示,沉默組植株的維管束褐化,出現(xiàn)更加明顯的褐色條紋。同時(shí),GhERF020 沉默組植株的病情指數(shù)、相對(duì)真菌生物量較對(duì)照組顯著升高(圖7B和C)。因此,推測(cè)GhERF020 基因在棉花抵御黃萎病過(guò)程中起重要調(diào)控作用。
3 討論
黃萎病是嚴(yán)重威脅棉花生產(chǎn)的重要病害,該病的防治非常困難。通過(guò)傳統(tǒng)的雜交育種方法選育抗病品種難度大、周期長(zhǎng),不能有效滿(mǎn)足現(xiàn)實(shí)生產(chǎn)發(fā)展的需求。因此,挖掘棉花抗病相關(guān)基因,探究棉花抗黃萎病基因調(diào)控網(wǎng)絡(luò)及其抗病分子機(jī)制,將為棉花抗病分子育種提供理論依據(jù)及基因資源。
轉(zhuǎn)錄因子可以調(diào)控多個(gè)與抗病相關(guān)基因的表達(dá),使植物抗病性得到明顯改善。近年來(lái),ERF轉(zhuǎn)錄因子在植物生長(zhǎng)發(fā)育和脅迫適應(yīng)性中的作用日益突顯,在脅迫下通常正調(diào)控植物的抗性,但也會(huì)因低溫、缺鐵、干旱等一些原因負(fù)調(diào)控植物的抗性[26]。本研究室前期通過(guò)對(duì)接種大麗輪枝菌擬南芥進(jìn)行轉(zhuǎn)錄組和代謝組學(xué)分析,發(fā)現(xiàn)了大量差異表達(dá)基因,通過(guò)生物信息學(xué)分析錨定擬南芥抗黃萎病基因AtERF019(AT1G22810.1),通過(guò)同源比對(duì)獲得棉花同源基因GhERF020,該基因含有1個(gè)AP2 結(jié)構(gòu)域;AP2 結(jié)構(gòu)域是ERF 的DNA 結(jié)合域,是其行使轉(zhuǎn)錄調(diào)控的關(guān)鍵。
研究表明,SA、JA 和ET 是主要的抗病信號(hào)[27‐28]。黃榆普[29]研究發(fā)現(xiàn),ERF012 能夠與JA合成基因的啟動(dòng)子結(jié)合,并上調(diào)JA 合成基因的表達(dá),促進(jìn)JA合成。作為ET應(yīng)答因子,ERF轉(zhuǎn)錄因子可以特異性結(jié)合基因組上游的GCC-box,從而參與調(diào)控ET 應(yīng)答、抗病及非生物脅迫[30]。對(duì)GhERF020 啟動(dòng)子順式元件進(jìn)行預(yù)測(cè)發(fā)現(xiàn),GhERF020 基因啟動(dòng)子區(qū)域具有參與SA、MEJA、ABA響應(yīng)等功能性元件,推測(cè)GhERF020 基因可能受激素誘導(dǎo),進(jìn)而調(diào)控抗病相關(guān)基因參與抗黃萎病脅迫反應(yīng)。煙草的瞬時(shí)過(guò)表達(dá)結(jié)果表明,ERF019的核定位對(duì)其抗病功能至關(guān)重要[14]。本研究通過(guò)亞細(xì)胞定位同樣發(fā)現(xiàn),GhERF020蛋白定位于細(xì)胞核中,可能是激活下游抗病基因表達(dá)的潛在因子。
Zafar等[20]對(duì)4類(lèi)棉花和野生型擬南芥中ERF基因家族成員進(jìn)行系統(tǒng)發(fā)育樹(shù)分析發(fā)現(xiàn),GhERF020 與GhERF012 在同一分支上,并且與AtERF014 親緣關(guān)系較近。在AtERF014-RNAi 沉默植株中,病原菌和flg22誘導(dǎo)的活性氧(reactiveoxygen species,ROS)爆發(fā)、PTI 基因表達(dá)和SA 誘導(dǎo)的防御被部分抑制,而在超表達(dá)AtER014 植株中,病原菌誘導(dǎo)的ROS 和flg22 誘導(dǎo)的免疫反應(yīng)被激活增強(qiáng)[31‐32]。本研究通過(guò)RT-qPCR 分析表明,GhERF020 能夠響應(yīng)黃萎病菌誘導(dǎo)處理,推測(cè)其在棉花抗黃萎病反應(yīng)中發(fā)揮重要作用。利用VIGS 技術(shù)沉默該基因,沉默植株對(duì)黃萎病菌的抗性顯著降低,病情指數(shù)和真菌生物量均高于對(duì)照植株;剖桿檢測(cè)發(fā)現(xiàn),GhERF020 沉默植株維管束的褐變程度更加嚴(yán)重,真菌的生物量顯著高于對(duì)照植株。由此表明,GhERF020 正向調(diào)控棉花抗黃萎病反應(yīng),但該基因的抗病分子機(jī)制及可能參與的抗病信號(hào)通路仍需進(jìn)一步解析。
綜上,本研究鑒定了1個(gè)ERF亞家族的轉(zhuǎn)錄因子編碼基因GhERF020,其ORF為441 bp,編碼147個(gè)氨基酸;GhERF020蛋白的相對(duì)分子質(zhì)量為16.16 kD,無(wú)跨膜結(jié)構(gòu)域,為親水性蛋白。該基因受大麗輪枝菌侵染誘導(dǎo),并定位于細(xì)胞核,GhERF020 下調(diào)表達(dá)可顯著降低棉花對(duì)大麗輪枝菌的抗性。以上研究結(jié)果為棉花抗黃萎病基因資源的挖掘利用奠定了基礎(chǔ),并為生物育種提供重要的基因資源。
參考文獻(xiàn)
[1] 范鑫,趙雷霖,翟紅紅,等.AtNEK6 在棉花旱鹽脅迫響應(yīng)中的功能分析[J].中國(guó)農(nóng)業(yè)科學(xué),2018,51(22):4230-4240.
FAN X, ZHAO L L, ZHAI H H, et al.. Functional characterizationof AtNEK6 overexpression in cotton under drought and saltstress [J]. Sci. Agric. Sin., 2018, 51(22):4230-4240.
[2] WANG P, ZHOU L, JAMIESON P, et al .. The cotton wallassociatedkinase GhWAK7A mediates responses to fungal wiltpathogens by complexing with the chitin sensory receptors [J].Plant Cell, 2020, 32(12):3978-4001.
[3] 李秀青,李月,劉超,等.棉花黃萎病相關(guān)基因GhAAT 的克隆與功能鑒定[J].分子植物育種,2020,18(4):1048-1053.
LI X Q, LI Y, LIU C, et al .. Cloning and functionalidentification of cotton Verticillium wilt related gene GhAAT[J]. Mol. Plant. Breed., 2020, 18(4):1048-1053.
[4] 張計(jì)育,王慶菊,郭忠仁.植物AP2/ERF類(lèi)轉(zhuǎn)錄因子研究進(jìn)展[J].遺傳,2012,34(7):835-847.
ZHANG J Y, WANG Q J, GUO Z R. Progresses on plant AP2/ERF transcription factors [J]. Hereditas, 2012, 34(7):835-847.
[5] NAKANO T, SUZUKI K, FUJIMURA T, et al .. Genome-wideanalysis of the ERF gene family in Arabidopsis and rice [J].Plant Physiol., 2006, 140(2):411-432.
[6] 莫紀(jì)波,李大勇,張慧娟,等.ERF轉(zhuǎn)錄因子在植物對(duì)生物和非生物脅迫反應(yīng)中的作用[J]. 植物生理學(xué)報(bào),2011,47(12):1145-1154.
MO J B, LI D Y, ZHANG H J, et al .. Roles of ERFtranscription factors in biotic and abiotic stress response inplants [J]. Acta Phytophysiol. Sin., 2011, 47(12):1145-1154.
[7] ZHANG G Y, CHEN M, CHEN X P, et al .. Phylogeny, genestructures, and expression patterns of the ERF gene family insoybean (Glycine max L.) [J]. J. Exp. Bot., 2008, 59(15):4095-4107.
[8] SHARMA M K, KUMAR R, SOLANKE A U, et al ..Identification, phylogeny, and transcript profiling of ERFfamily genes during development and abiotic stress treatmentsin tomato [J]. Mol. Genet. Genom., 2010, 284(6):455-475.
[9] ZHUANG J, CAI B, PENG R H, et al .. Genome-wide analysisof the AP2/ERF gene family in Populus trichocarpa [J].Biochem. Biophys. Res. Commun., 2008, 371(3):468-474.
[10] BERROCAL-LOBO M, MOLINA A, SOLANO R. Constitutiveexpression of ethylene‐response‐factor1 in Arabidopsis confersresistance to several necrotrophic fungi [J]. Plant J., 2002, 29(1):23-32.
[11] CHARFEDDINE M, SAMET M, CHARFEDDINE S, et al ..Ectopic expression of StERF94 transcription factor in potatoplants improved resistance to Fusarium solani infection [J].Plant Mol. Biol. Rep., 2019, 37(5):450-463.
[12] LIU D F, CHEN X J, LIU J Q, et al.. The rice ERF transcriptionfactor OsERF922 negatively regulates resistance to Magnaportheoryzae and salt tolerance [J]. J. Exp. Bot., 2012, 63(10):3899-3911.
[13] WANG F J, WANG C L, LIU P Q, et al .. Enhanced rice blastresistance by CRISPR/Cas9-targeted mutagenesis of the ERFtranscription factor gene OsERF922 [J/OL]. PLoS One, 2016,11(4):e0154027 [2023-04-30]. https://doi.org/1371/journal.pone.0154027.
[14] LU W Q, DENG F Y, JIA J B, et al .. The Arabidopsis thalianagene AtERF019 negatively regulates plant resistance to Phytophthoraparasitica by suppressing PAMP-triggered immunity [J]. Mol. PlantPathol., 2020, 21(9):1179-1193.
[15] FEYS B J, PARKER J E. Interplay of signaling pathways in plantdisease resistance [J]. Trends Genet., 2000, 16(10):449-455.
[16] GLAZEBROOK J. Genes controlling expression of defenseresponses in Arabidopsis [J]. Curr. Opin. Plant Biol., 2001, 4(4):301-308.
[17] 吳朝峰. 棉花腺體形成相關(guān)基因GhERF105 的功能分析[D].武漢:華中農(nóng)業(yè)大學(xué), 2020.
WU C F. Functional analysis of GhERF105 gene related togland formation in cotton [D]. Wuhan: Huazhong AgriculturalUniversity, 2020.
[18] LORENZO O, PIQUERAS R, SANCHEZ-SERRANO J J, et al..Ethylene response factor1 integrates signals from ethylene andjasmonate pathways in plant defense [J]. Plant Cell, 2003, 15(1):165-178.
[19] CATINOT J, HUANG J B, HUANG P Y, et al .. Ethylenerespense factor 96 positively regulates Arabidopsis resistance tonecrotrophic pathogens by direct binding to GCC elements ofjasmonate-and ethylen-responsive defence genes [J]. Plant CellEnviron., 2015, 38(12):2721-2734.
[20] ZAFAR M M, REHMAN A, RAZZAQ A, et al .. Genome-widecharacterization and expression analysis of Erf gene family incotton [J]. BMC Plant Biol., 2022, 22(1):1-18.
[21] KENNETH J, LIVAK, THOMAS D, et al .. Analysis of relativegene expression data using real-time quantitative PCR andthe 2? ΔΔCt method [J]. Methods, 2001, 25 (4):402-408.
[22] LIU L, WANG D, ZHANG C, et al.. The heat shock factorGhHSFA4a positively regulates cotton resistance to Verticilliumdahliae [J]. Front. Plant Sci., 2022, 13:1050216-1050230.
[23] GAO X, BRITT JR R C, SHAN L, et al .. Agrobacteriummediatedvirus-induced gene silencing assay in cotton [J]. J.Vis. Exp., 2011, 20(54):2938-2943.
[24] SPARKES I A, RUNIONS J, KEARNS A, et al .. Rapid,transient expression of fluorescent fusion proteins in tobaccoplants and generation of stably transformed plants [J]. Nat.Prot., 2006, 1(4):2019-2025.
[25] LI X K, SU X F, LU G Q, et al .. VdOGDH is involved in energymetabolism and required for virulence of Verticillium dahliae [J].Curr. Genet., 2020, 66(2):345-359.
[26] 許世達(dá),耿興敏,王露露.植物乙烯響應(yīng)因子(ERF)的結(jié)構(gòu)、功能及表達(dá)調(diào)控研究進(jìn)展[J]. 浙江農(nóng)林大學(xué)學(xué)報(bào),2021,38(3):624-633.
XU S D, GENG X M, WANG L L. A review of the structure,function and expression regulation of ethylene response factors(ERF) in plant [J]. J. Zhejiang Aamp;F Univ., 2021, 38(3):624-633.
[27] 劉茜,王愛(ài)云,榮瑋.ERF轉(zhuǎn)錄因子在作物抗病基因工程中的研究進(jìn)展[J].種子,2014,33(1):48-53.
LIU Q, WANG A Y, RONG W. Progress of ERF transcriptionfactors in genetic engineering for disease resistance in crops [J].Seed, 2014, 33(1):48-53.
[28] PIETERSEC M, LEON-REYES A, VAN DER ENT S, et al ..Networking by small-molecule hormones in plant immunity [J].Nat. Chem. Biol., 2009, 5(5):308-316.
[29] 黃榆普.茉莉酸參與缺硼抑制擬南芥生長(zhǎng)的分子機(jī)制[D].武漢:華中農(nóng)業(yè)大學(xué),2020.
HUANG Y P. Molecular mechnism of jasmonate mediated low-boron-induced growth inhibition in Arabidopsis [D]. Wuhan:Huazhong Agricultural University, 2020.
[30] OHOME-TAKAGI M, SHINSHI H. Ethylene-inducible DNAbinding proteins that interact with an ethylene-responsiveelement [J]. Plant Cell, 1995, 7(2):173-182.
[31] ZHANG H J, HONG Y B, HUANG L, et al .. ArabidopsisAtERF014 acts as a dual regulator that differentially modulatesimmunity against Pseudomonas syringae pv. tomato andBotrytis cinerea [J/OL]. Sci. Rep., 2016, 6(1):30251 [2023-04-30]. https://doi.org/10.1038/srep30251.
[32] ONATE-SANCHEZ L, ANDERSON J P, YOUNG J, et al ..AtERF14, a member of the ERF family of transcription factors,plays a nonredundant role in plant defense [J]. Plant Physiol.,2007, 143(1):400-409.
基金項(xiàng)目:河北省重點(diǎn)研發(fā)計(jì)劃項(xiàng)目(22322912D);國(guó)家自然科學(xué)基金項(xiàng)目(32160624)。

