紫外分光光度法測定氧氟沙星的解離常數
黃群蓮,鄧以平,徐紹友(1.瀘州醫學院附屬醫院藥劑科,瀘州市646000;.四川寶光藥業股份有限公司,瀘州市646100)
氧氟沙星(Ofloxacin,OFLX)又名氟嗪酸,是第3代喹諾酮抗菌藥,由于分子結構中具有疏水性的N-甲基哌嗪環以及親水性的嗪環,同時6位C原子上氟原子的引入,使得該藥物具有良好的組織滲透性。其對革蘭陽性和陰性菌、大腸桿菌、葡萄球菌和肺炎球菌均有強的抗菌活性[1],與早期的喹諾酮類藥物相比,具有抗菌譜廣、抗菌活性強,低毒、高效、副作用小等特點[2],因此臨床上主要用于淋病、尿路感染、呼吸道感染以及胃腸道感染的治療。
酸堿性是藥物重要的理化性質,同時該性質與藥物在體內的吸收、分布和溶解度密切相關,而解離常數(pKa)是與藥物溶解度和pH值有關的理化常數,藥物解離常數的測定可為在分子水平上研究藥物的吸收與受體結合提供重要的信息[3],同時也在藥物新劑型和新配方的研制中具有重要的指導意義[4]。
測定解離常數的方法目前主要有電位滴定法[5]、電導率法[6]、熒光法[7]、電泳法[8]以及紫外分光光度法[9]等。由于紫外分光光度法具有操作簡單、快速、精密度高、重現性好、數據處理方便等特點,特別適合于一元弱酸(堿)性藥物解離常數的測定。通過對氧氟沙星在不同pH值緩沖溶液中進行紫外吸收掃描,發現在293 nm波長處存在最大紫外吸收,故本文采用紫外分光光度法測定氧氟沙星的2個解離常數。氧氟沙星的化學結構見圖1。
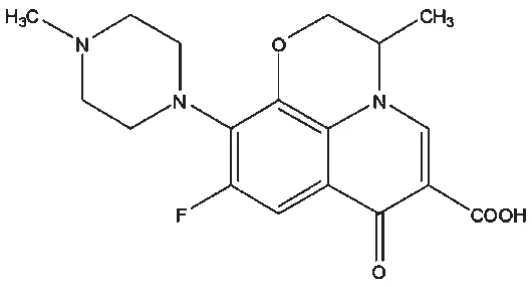
圖1 氧氟沙星的化學結構Fig 1The molecular structure of ofloxacin
1 材料
1.1 儀器
UV-2550型紫外分光光度計(日本島津公司);PHS-P1型酸度計(上海雷磁儀器廠);FA2104電子天平(上海民橋精密科學儀器有限公司)。
1.2 試藥
氧氟沙星(臺州市新星醫藥化工有限公司,批號:20100230,純度:99.12%);氧氟沙星標準品(中國藥品生物制品檢定所,批號:20891006,供含量測定用);醋酸、醋酸鈉、鹽酸、三羥甲基氨基甲烷、氫氧化鈉、硼砂均為分析純。
2 方法與結果
2.1 氧氟沙星解離常數測定的基本原理
氧氟沙星中由于羧基與氨基的存在,因此在不同pH值的范圍內應存在不同的電離形式。通過對其在不同pH值緩沖溶液中進行紫外吸收掃描,發現pH值在3.16以下,6.96~7.22及9.12以上時,其分別以酸性(AA+)、中性(AA0)和堿性(AA-)的形式存在,而在3.16~6.96和7.22~9.12則分別以酸性(AA+)和中性(AA0)、中性(AA0)和堿性(AA-)的形式共存。氧氟沙星在不同pH值溶液中的解離形式如圖2所示。

圖2 氧氟沙星在不同pH值溶液中的解離形式Fig 2The dissociation forms of ofloxacin in solutions with different pH values
設在25℃的環境中測定解離常數pKa,用1.0 cm的吸收池,在特定波長處測得吸光度為A,對任意pH值的緩沖溶液樣品,則根據吸光度的加和原理,可得氧氟沙星在酸性(式(1))和堿性(式(2))時解離常數的計算公式:
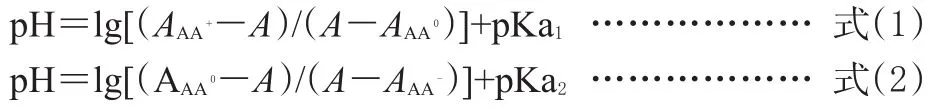
根據公式(1)和(2),只要測出AAA+、AAA0及不同pH值下的吸光度A,分別以lg([AAA+-A)(/A-AAA)0]或lg([AAA0-A)/(A-AAA-)]為橫坐標,pH值為縱坐標作圖得一直線,縱坐標上的截距就是氧氟沙星的2個解離常數pKa。
2.2 試液的制備
氧氟沙星溶液:稱取0.1345 g的氧氟沙星,醋酸溶解并定容于250 mL的容量瓶中,得到濃度為1.50×10-3mol·L-1的氧氟沙星醋酸溶液。
緩沖溶液:將0.1 mol·L-1的醋酸鈉與0.1 mol·L-1的鹽酸或0.1 mol·L-1的醋酸按不同的比例混合,以及0.1 mol·L-1的三羥甲基氨基甲烷與0.1 mol·L-1的鹽酸按不同的比例混合,制備成pH值為2.87~8.12的一系列緩沖溶液;將0.025 mol·L-1硼砂與0.1 mol·L-1的鹽酸或者氫氧化鈉溶液按不同比例混合,制備成pH值為8.48~10.20的一系列緩沖溶液。
2.3 測定條件的選擇
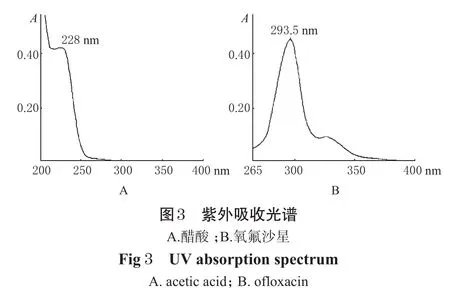
分別制備2%的醋酸溶液和1.50×10-7mol·L-1(1.50×10-3mol·L-1的氧氟沙星醋酸溶液0.5 mL稀釋至50 mL)的氧氟沙星醋酸溶液50 mL,分別以蒸餾水和醋酸作參比,用紫外分光光度計在200~400 nm波長范圍掃描,得到醋酸和氧氟沙星的紫外吸收光譜,見圖3。
從圖3A可以看出,醋酸在288 nm波長處為醋酸酯羰基的最大紫外吸收,而約在285 nm波長以上則無紫外吸收,在205 nm波長處的強吸收為溶劑水的羥基吸收。對比圖3B可以看出,在293.5 nm波長處氧氟沙星有1個明顯的最大紫外吸收,這是氧氟沙星的分子結構中α,β-不飽和羰基的紫外吸收;同時氧氟沙星溶液在330 nm波長左右有1個弱吸收,這是氧氟沙星分子結構中的苯環與α,β-不飽和羰基中的雙鍵共軛所引起的弱紫外吸收;而265 nm波長以下為醋酸酯羰基所引起的紫外吸收,對氧氟沙星在293.5 nm波長處的最大紫外吸收沒有影響。因此選擇醋酸作為氧氟沙星的溶劑,不影響其測定結果。
2.4 含量測定方法學考察
2.4.1 標準曲線的制備。根據《中國藥典》2005年版二部附錄中“藥品質量標準分析方法驗證指導原則”,取氧氟沙星標準品,精密稱定,用醋酸溶解制備成2.5013、3.7855、5.0152、6.3245、7.5866、8.8542、10.1106 μg·mL-1的氧氟沙星醋酸溶液,在293.5 nm波長處測得吸光度分別為0.232、0.341、0.446、0.552、0.672、0.774、0.882。以各梯度溶液濃度(C,μg·mL-1)為橫坐標,吸光度(A)為縱坐標,進行線性回歸,回歸方程:A=0.0856C+0.0168(R2=0.9998),表明氧氟沙星檢測濃度線性范圍為2.5013~10.1106 μg·mL-1。
2.4.2 精密度試驗。取氧氟沙星醋酸溶液(3.7855 μg·mL-1),重復測定其吸光度6次,其RSD=0.22%(n=6)。
2.4.3 穩定性試驗。取氧氟沙星醋酸溶液(3.7855 μg·mL-1),分別在0、2、4、8、16、24 h測定其吸光度,結果其RSD=1.21%(n=6),表明溶液在24 h內基本穩定。
2.4.4 加樣回收率試驗。取已知氧氟沙星含量的樣品的醋酸溶液50 mL,共6份,分別在其中精密加入一定量的氧氟沙星標準品,依法測定,結果見表1。

表1 加樣回收率試驗結果Tab 1Results of recovery test
2.5 氧氟沙星pKa的粗測
在25℃的條件下,將氧氟沙星與鹽酸按照1∶1的摩爾比例混合,在水中反應完全后制備成1.50×10-5mol·L-1的氧氟沙星溶液,由于反應完全后[AA+]=[AA0],此時pKa1≈pH;同理,將氧氟沙星與氫氧化鈉按照1∶1的摩爾比例混合,在水中反應制備成1.50×10-5mol·L-1的氧氟沙星溶液,由于反應完全后[AA0]=[AA-],此時pKa2≈pH。分別用酸度計測得以上2個反應液的pH值,即得氧氟沙星粗測的pKa值,粗測得pKa1=5.68,pKa2=8.32。
2.6 氧氟沙星pKa1、pKa2的作圖計算
取16只50 mL的容量瓶,各加入1.50×10-3mol·L-1的氧氟沙星醋酸溶液0.5 mL,分別用不同pH值(2.87、3.16、4.48、4.98、5.62、6.15、6.86、6.96、7.22、7.72、8.12、8.68、8.90、9.20、9.32、10.20)的緩沖溶液定容及作參比,在25℃的室溫下于293.5 nm波長處測定不同pH值下氧氟沙星溶液的吸光度,每個樣品平行測定3次,取其平均值,結果見表2。
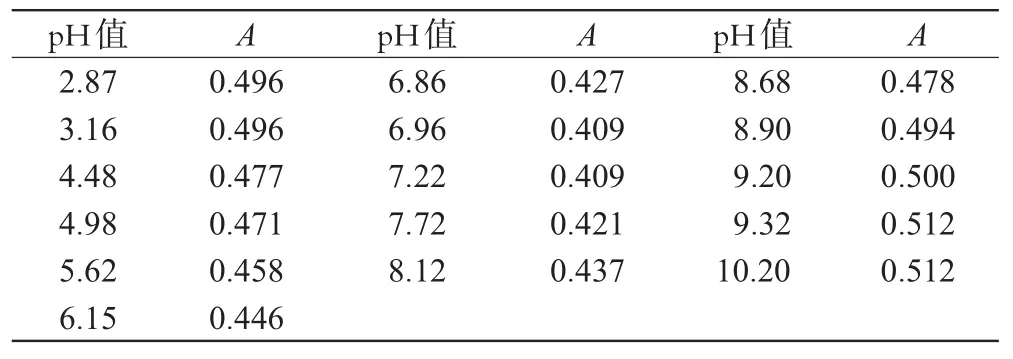
表2 氧氟沙星在不同pH值緩沖溶液中的吸光度(25℃)Tab 2The absorbance values of ofloxacin in buffer solutions with different pH values(25℃)
從表2可以看出,氧氟沙星的吸光度與緩沖溶液的pH值有關。相同濃度的氧氟沙星在pH 6.86以下的溶液中,隨著pH值的增大,吸光度逐漸減小,這是因為紫外光譜與n電子和π電子的躍遷有關。當pH值增大時,即氧氟沙星的羧基電離后,使得羧基中氧上的n電子與π電子的共軛程度增加,降低了n電子和π電子躍遷的幾率,使得吸收強度減小,因此吸光度降低。相同濃度的氧氟沙星在pH 7.22以上的溶液中,吸光度隨著pH值增大而增大,由于在高pH值下分子中的叔胺基電離出的H+離子被堿中和后,羧基與堿中的陽離子成鹽后,相反降低了羧基中氧上的n電子與π電子的共軛程度,因此增加了n電子和π電子躍遷的幾率,使得吸收強度增加,導致吸光度增大。
從表2中還可以看出,在pH值小于3.16的緩沖溶液中,吸光度恒定,即氧氟沙星全部以質子化(即AA+)的形式存在,此時AAA+=0.496;pH值在6.96~7.22之間時主要以氧氟沙星分子(即AA0)形式存在,此時AAA0=0.409;pH值大于9.32時全部以完全去質子化(即AA-)的形式存在,此時AAA-=0.512。根據式(1)和(2),在不同pH值下分別以lg[(AAA+-A)/(A-AAA0)]和lg[(AAA0-A)/(A-AAA-)]為橫坐標(用x表示),pH值為縱坐標(用y表示)作圖,見圖4。
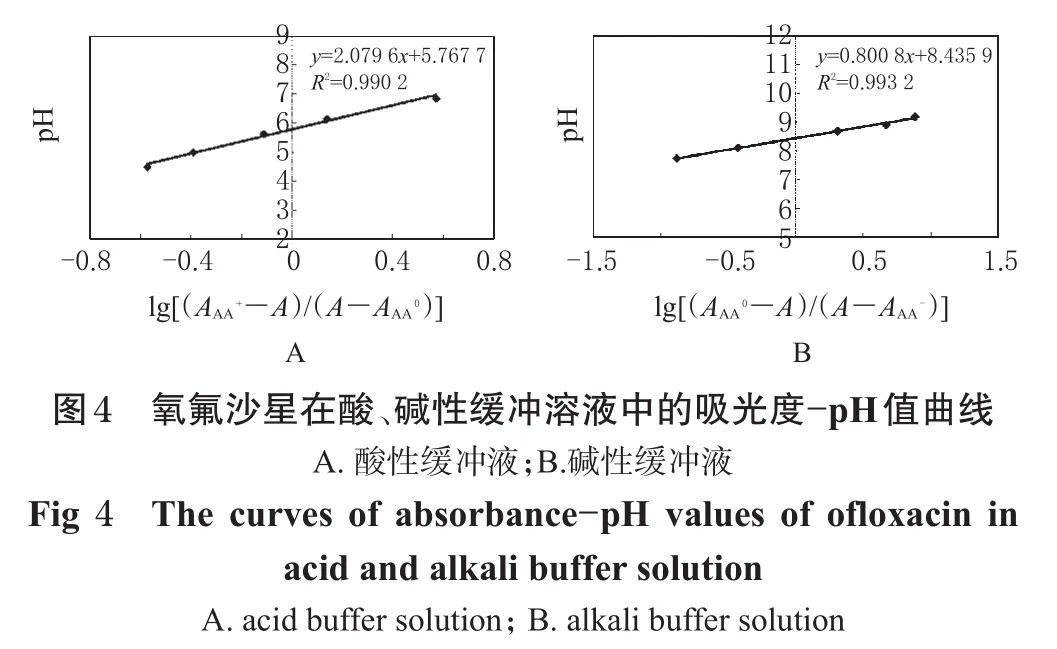
通過作圖得氧氟沙星在酸、堿性緩沖溶液中的線性方程分別為y=2.0796x+5.7677(R2=0.9902)、y=0.8008x+8.4359(R2=0.9932)。相關系數R2分別為0.9902和0.9932,表明線性擬合后近似于直線;由截距可知,氧氟沙星的解離常數pKa1約為5.77、pKa2約為8.44,與粗測值相比,相對誤差分別為1.56%和1.44%。
3 討論
氧氟沙星在水中溶解度較差,需成鹽后才溶解。本文以醋酸作溶劑,用紫外分光光度計測得氧氟沙星在293.5 nm波長處有最大紫外吸收,而在265 nm波長以下,醋酸對氧氟沙星的最大吸收沒有影響,因此選擇293.5 nm的波長作為氧氟沙星定性定量分析的測定波長。
通過作圖法求得氧氟沙星的2個解離常數:pKa1為5.77,pKa2為8.44。對解離常數的測定,關鍵是選擇適宜pH值范圍的緩沖溶液,以保證測定結果的準確性和可靠性。
綜上所述,該方法簡便、快速,結果準確、可靠。氧氟沙星2個解離常數的測定對進一步研究其在生物體內的吸收、分布、代謝、排泄的規律以及對該藥物的制備工藝的篩選、制劑分析等方面提供了基礎性的理論研究數據。
[1]王劍,劉忠芳,劉紹璞.銅(Ⅱ)-氟喹諾酮類抗生素螯合物與赤蘚紅體系的吸收、熒光和共振Rayleigh散射光譜及其分析應用研究[J].中國科學B輯:化學,2007,37(5):453.
[2]莫慧貞,李靜.HPLC法測定氧氟沙星膠囊中氧氟沙星的含量[J].廣東藥學,2005,15(6):10.
[3]陳金蓉,劉家琴,羅英,等.大豆黃素解離常數的分光光度法測定[J].綿陽師范學院學報,2008,27(2):64.
[4]李廣領,張育平.水楊酸pKa的紫外-可見分光光度法測定[J].河南科技學院學報(自然科學版),2005,33(1):75.
[5]朱志良,梁曉明,張榮華.聚天冬氨酸酸解離常數的測定[J].分析化學研究簡報,2005,33(12):1722.
[6]凌小紅.電導(率)法測定醋酸解離常數的數據處理方法研究——Excel的應用[J].首都師范大學學報(自然科學版),2006,27(4):39.
[7]李俊,張冬梅,陶力.熒光法測定核黃蛋白-核黃素的解離常數[J].大學化學,2000,15(3):39.
[8]馮海清,傅崇崗.毛細管電泳電化學檢測法同時測定3種氨基酸的電離常數[J].分析試驗室,2006,25(8):21.
[9]劉西京,楊大堅,羅杰英,等.紫外分光光度法測定葛根素的解離常數[J].時珍國醫國藥,2006,17(11):2206.

