轉氨酶水平檢驗在脂肪肝診斷中的應用價值
譚錦平,肖雪云,蘇小杰
廣東省東莞市洪梅醫院檢驗科,廣東東莞 523160
轉氨酶是人體內的一種主要酶類,當前研究純化出來的有20余種,主要作用是催化氨基酸與酮酸之間的氨基轉移[1],是維持生命反應的必要酶類。20世紀50年代研究結果表明脂肪肝患者血清丙氨酸氨基轉移酶(ALT)和天冬氨酸氨基轉移酶(AST)成高表達,并提出把上述兩者作為脂肪肝的常規檢測指標[2]。ALT與AST的變化能直接反映肝細胞的病理生理情況,如急性肝炎或慢性肝炎活動期患者血清ALT與AST水平呈不同程度升高[3]。筆者為此通過觀察脂肪肝患者手術治療前、后血清轉氨酶的變化,探討轉氨酶水平檢驗在脂肪肝診斷中的應用價值。
1 資料與方法
1.1 一般資料
選擇2008年10月~2010年10月間我科連續施行手術治療的危重脂肪肝患者60例,其中男40例,女20例;年齡28~65歲,平均51.9歲。所有患者均符合相關診斷標準[4]。
1.2 轉氨酶檢測
于術后第l、3、7天測定空腹血清ALT、AST的含量。受檢者均要求檢查前1 d素食,禁飲酒,采集隔夜空腹靜脈血5 ml,并以3 000 r/min離心分離血清,在當天內完成全部指標測定。采用美國GE 2000型全自動生化分析儀測定,并采用嚴格的質量控制保證。
1.3 影響因素記錄
入肝血流阻斷;術中出血量(ml)=吸引瓶血量+紗布墊含血量;手術時間=手術切皮開始至手術縫合結束所用的時間(min);手術方式=以切肝范圍進行評分,肝段肝切除:0分,肝葉切除:1分;半肝切除:2分;超過半肝切除:3分。
1.4 統計學方法
所有數據采用SPSS 17.0統計軟件進行分析,血清轉氨酶計量資料數據以均數±標準差(±s)表示,單因素分析采用線性分析,P<0.05為差異有統計學意義。
2 結果
2.1 血清轉氨酶的變化
脂肪肝患者術后第1、3、7天血清轉氨酶水平較術前均有顯著升高(P<0.05或P<0.01),術后第1天到達峰值(P<0.01),然后逐漸降低,術后第7天比較接近術前水平(P>0.05)。見表1。
2.2 影響血清轉氨酶水平的因素
單因素回歸試驗表明,術中入肝血流阻斷、手術方式2個因素具有統計學意義(P<0.05)。其中入肝血流阻斷是術后第1、3、7天血清轉氨酶增高的最主要影響因素,均P<0.01;術中出血量、手術時間與術后血清轉氨酶無明顯相關性,均P>0.05。 見表2。
表1 手術治療前后血清轉氨酶變化( ±s,U/L)
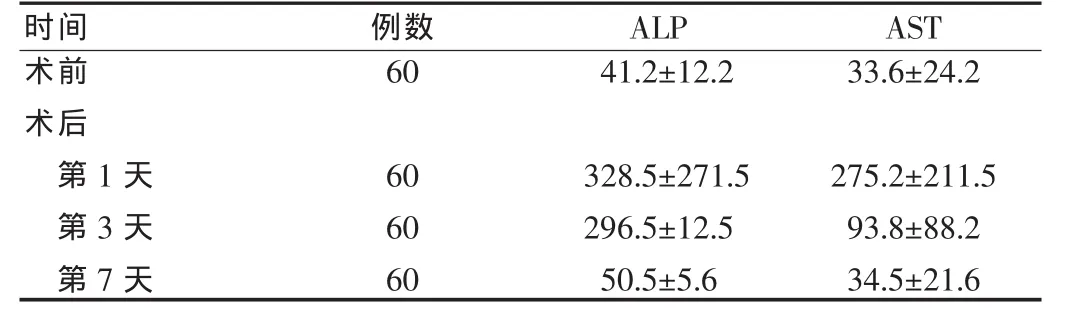
表1 手術治療前后血清轉氨酶變化( ±s,U/L)
時間 例數 ALP AST術前術后第1天第3天第7天6041.2±12.233.6±24.2 60 60 60 328.5±271.5 296.5±12.5 50.5±5.6 275.2±211.5 93.8±88.2 34.5±21.6

表2 影響血清轉氨酶變化的術中因素的單因素分析(n=60)
3 討論
脂肪肝者一般體重超標或嚴重超標。這與飲食結構不當、飲食過量、嗜酒無度、缺乏運動等有關,是典型的“富貴病”。轉氨酶是催化氨基酸與酮酸之間氨基轉移的一類酶,是維持生命活動的必要酶類。普遍存在于動物、植物組織和微生物中,在組織器官中,其可在心肌、肝、腎、腦等組織中存在。
轉氨酶中的血清丙氨酸氨基轉移酶主要存在于細胞漿中,天冬氨酸氨基轉移酶主要存在于細胞漿的線粒體中。但是當肝細胞損傷或者發生炎癥時,血清丙氨酸氨基轉移酶能隨時進入血中。當肝細胞嚴重損傷或者嚴重炎癥直至危及線粒體時,天冬氨酸氨基轉移酶也會進入血中[5]。為此血清丙氨酸氨基轉移酶和天冬氨酸氨基轉移酶都會升高,那么判斷ALT與AST的含量水平可以顯示肝細胞損傷與炎癥的嚴重程度[6]。
本組資料表明,60例脂肪肝患者手術治療后,血清ALT、AST于術后第1天達到峰值,然后逐漸下降,至術后第7天基本與術前接近,表明血清ALT、AST在脂肪肝的檢測中占有重要影響。在影響ALT、AST發生變化的因素方面,術中入肝血流阻斷、手術方式是導致術后血清轉氨酶升高的主要因素,與術后血清轉氨酶增高呈線性關系。不過當前也有研究認為,轉氨酶水平的高低不能完全代表肝細胞損傷或者發生炎癥的程度,其之間并不呈現直接相關性,可能只是間接相關[7]。有研究顯示,慢性乙型肝炎病毒攜帶者,乙型肝炎病毒指標一直陽性,但丙氨酸氨基轉移酶和天冬氨酸氨基轉移酶卻沒有明顯變化[8],一些肝硬化和肝癌患者在做肝臟活組織檢查能發現肝臟的炎癥反應很嚴重,但是ALT、AST也不升高[9],還有不少急性和慢性丙型肝炎患者也有類似情況[10]。表明轉氨酶水平檢驗還需要繼續觀察研究。
總之,對手術后血清轉氨酶的檢測,可以有效檢測脂肪肝患者手術后的生理變化,指導患者的身體康復,也可為規范手術操作提供科學的依據。
[1]董繼俊,李建功,馬興久,等.血清丙氨酸轉氨酶變化與肝細胞癌手術患者預后的關系[J].山東醫藥,2002,42(17):33-34.
[2]Lindblom P,Rafter I,Copley C,et al.Isoforms of alanine aninotransferases in human tissues and serum-differential tissue expression using novel antibodies[J].Arch Biochem Biophys,2007,466(1):66-77.
[3]Field K,Dow C,Michael M,et al.Part I:Liver function in oncology:biochemistry and beyond[J].Lancet Oncol,2008,9(11):1092-1101.
[4]Garcea G,Gescher A,Steward W,et al.Oxidative stress in humans following the Pringle manoeuvre[J].HPD Int,2006,5(2):210-214.
[5]黃耿文,楊連粵,魯偉群,等.肝癌切除術后并發癥的多元回歸分析[J].中國實用外科雜志,2006,26(6):428-429.
[6]鄭樹森.肝切除技術現況和進展[J].中國實用外科雜志,2005,25(2):65-67.
[7]Vetelainen R,Vaniet A,Gouma DJ,et al.Steatosi s as a ri sk factor in l iver surgery Ann Surg,2007,245(1):20-30.
[8]何強,彭寶崗,梁力建,等.肝癌合并肝硬化大塊肝切除的手術風險性[J].中國現代醫學雜志,2006,16(1):14.
[9]張愛民,常艷敏.脂肪肝患者血清膽堿酯酶、肝功能、血脂水平的觀察[J].醫學檢驗與臨床,2006,17(1):64.
[10]侯秀芝.脂肪肝的超聲診斷與實驗室相關檢查的關系分析[J].安徽衛生職業技術學院學報,2004,3(6):23-26.

