IgM腎病十例臨床特點(diǎn)分析
楊 旭,吳 巖,李晗笑,王艷秋
IgM腎病是一免疫病理診斷,其發(fā)病機(jī)制不清,對(duì)其臨床特點(diǎn)的描述也不盡相同。現(xiàn)對(duì)2008年3月—2009年3月中國(guó)醫(yī)科大學(xué)附屬盛京醫(yī)院收治的10例IgM腎病患者的臨床資料進(jìn)行回顧性分析,總結(jié)其臨床表現(xiàn)、病理特點(diǎn)、尿足細(xì)胞排泄特點(diǎn)及治療反應(yīng),進(jìn)一步探討IgM腎病的發(fā)病機(jī)制。
1 資料與方法
1.1 一般資料 本組10例患者均于我院腎內(nèi)科經(jīng)腎穿刺活檢證實(shí)為IgM腎病,男6例,女4例;年齡20~68歲,平均45歲;腎穿刺前病程7 d~18個(gè)月。其中復(fù)發(fā)性腎病1例,激素依賴性腎病1例,其余患者為初次發(fā)病。
1.2 方法 回顧性收集10例IgM腎病患者的臨床資料,總結(jié)其臨床特征。
2 結(jié)果
2.1 臨床表現(xiàn) 10例患者中表現(xiàn)為腎病綜合征9例,腎小球腎炎1例。均有不同程度的水腫,血尿3例,均為鏡下血尿(血尿定義為尿常規(guī)紅細(xì)胞 >4.5個(gè)/HP)。伴高血壓者4例,其中3例為原發(fā)性高血壓,1例為腎性高血壓。伴腎功能損害者1例。前驅(qū)感染3例,均為上呼吸道感染。乙肝病毒攜帶者1例,腎組織無(wú)乙型肝炎表面抗原 (HBsAg)沉積。10例患者的基本情況見表1。
2.2 腎臟病理學(xué)特點(diǎn) 所有患者在B超引導(dǎo)下行經(jīng)皮腎穿刺活組織檢查證實(shí)為IgM腎病,除外IgA腎病、微小病變、局灶節(jié)段性腎小球硬化等。所有患者獲得的腎組織標(biāo)本均含10個(gè)以上腎小球。5例患者有全球硬化 (1~9個(gè),占全部腎小球的0.03% ~39.00%),年齡均在40歲及以上,但與年齡不完全成比例,與病程和高血壓程度相關(guān)。所有患者光鏡下可見彌漫性中度系膜細(xì)胞增生和系膜基質(zhì)增多(1例為輕~中度),部分毛細(xì)血管管腔狹窄或毛細(xì)血管襻皺縮,臟層上皮細(xì)胞腫脹,間質(zhì)損害輕微。灶性小管萎縮,4例患者管腔內(nèi)見透明蛋白管型。6例見灶性間質(zhì)水腫,7例有灶性炎性細(xì)胞浸潤(rùn),為單核細(xì)胞及淋巴細(xì)胞,其中3例有嗜酸粒細(xì)胞浸潤(rùn) (其中1例有較多的嗜酸粒細(xì)胞浸潤(rùn),其外周血嗜酸粒細(xì)胞計(jì)數(shù)也明顯增加),1例有灶性纖維化,臨床表現(xiàn)為腎小球腎炎。10例患者均可見小動(dòng)脈的透明變性,以入球小動(dòng)脈為主,其中3例小葉間動(dòng)脈有透明變性,2例弓形動(dòng)脈分支內(nèi)見小動(dòng)脈壁增厚。3例均為原發(fā)性高血壓患者。
2.3 免疫病理特點(diǎn) 所有患者IgM(++)顆粒狀沉積在系膜區(qū),C3顆粒狀沉積于系膜區(qū),(++)者1例,(+)者8例,(±)者1例。1例C1q(+),此例為乙肝病毒攜帶者,且血中提示病毒有復(fù)制,HBVDNA>5E7(正常 <10E3),但腎組織中HBsAg(-),HBcAg(-)。1例IgA(±)沉積在系膜區(qū)。
2.4 尿足細(xì)胞排泄特點(diǎn) 采用免疫酶細(xì)胞化學(xué)方法podocalyxin(PCX)單克隆抗體進(jìn)行標(biāo)記,計(jì)數(shù)足細(xì)胞。10例患者中9例尿中無(wú)足細(xì)胞排出,1例有少量排出,為2個(gè)/20HP。病理上有灶性纖維化,臨床表現(xiàn)為腎小球腎炎。
2.5 治療方法及對(duì)治療的反應(yīng) 采用激素治療為主的治療方案,單純激素 (潑尼松1 mg/kg)治療7例,來(lái)氟米特 (愛若華)治療2例,潑尼松聯(lián)合來(lái)氟米特治療1例,激素依賴性患者加用環(huán)磷酰胺治療。隨診患者觀察治療效果。絕大多數(shù)患者對(duì)治療的反應(yīng)良好,9例完全緩解(臨床表現(xiàn)完全消失,血漿清蛋白>35 g/L,尿蛋白定量<0.3 g/24 h,腎功能正常),其中2例自發(fā)緩解,但仍應(yīng)用激素系統(tǒng)治療;1例部分緩解 (臨床表現(xiàn)完全消失,尿蛋白定量較基礎(chǔ)值下降50%以上,但>0.3 g/24 h,腎功能正常)。3例復(fù)發(fā) (在減藥過程中或停藥后又出現(xiàn)相應(yīng)的臨床表現(xiàn)和實(shí)驗(yàn)室結(jié)果異常),其中1例為停藥 (來(lái)氟米特)6個(gè)月后復(fù)發(fā),再次應(yīng)用來(lái)氟米特效果仍很好,用藥1.5個(gè)月尿蛋白轉(zhuǎn)陰;1例在激素減量過程中復(fù)發(fā),加用環(huán)磷酰胺治療1.5個(gè)月,尿蛋白轉(zhuǎn)陰;1例用藥4個(gè)月停藥后復(fù)發(fā),目前在用藥觀察中。
3 討論
IgM腎病占原發(fā)性腎小球疾病腎活檢病例的4.4% ~10.3%[1],在本文中占同期腎活檢總例數(shù)的5.3% (10/187)。既往報(bào)道該病發(fā)病年齡較輕[2],而本組患者平均年齡偏大 (45歲),考慮與各單位不同年齡段患者腎穿刺的指征不完全相同有關(guān)。在我科,青少年初發(fā)腎病綜合征一般先治療,而中老年腎病患者因病理類型復(fù)雜,多接受腎活檢病理檢查。IgM腎病臨床表現(xiàn)以腎病綜合征為主,無(wú)肉眼血尿,可有少量的鏡下血尿。有前驅(qū)感染4例,血IgM升高4例,只有1例明顯升高,且與感染無(wú)相關(guān)性。IgG降低或正常。補(bǔ)體C3無(wú)降低。病理特點(diǎn)是彌漫性系膜細(xì)胞和系膜基質(zhì)增生,間質(zhì)改變輕微,但可見到血管病變,以入球小動(dòng)脈為代表的小動(dòng)脈透明變性最為典型。免疫病理特點(diǎn)是IgM及C3在系膜區(qū)呈顆粒樣沉積,而很少合并其他免疫球蛋白沉積。對(duì)激素及來(lái)氟米特的治療反應(yīng)良好,但減量過快可造成復(fù)發(fā)。
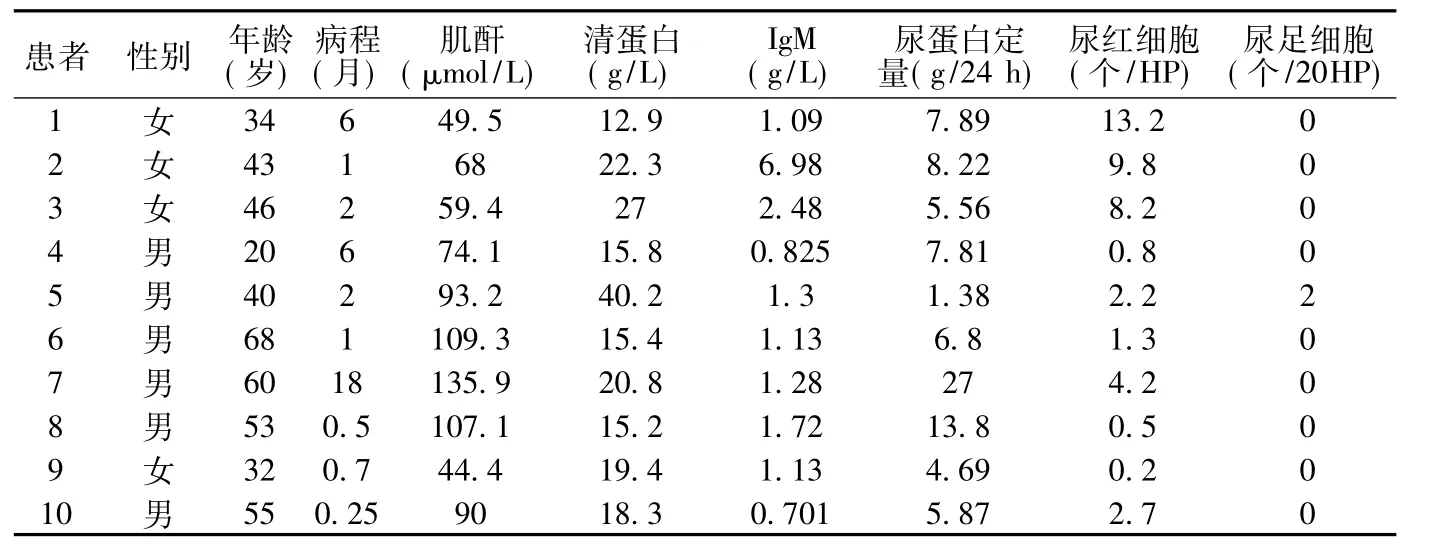
表1 IgM腎病患者的基本情況Table 1 The basic situation of patients with IgM Nephropathy
足細(xì)胞是腎小球?yàn)V過屏障的重要組成部分,在各種損傷因素作用下,足細(xì)胞發(fā)生形態(tài)改變,早期為足突融合,損傷嚴(yán)重時(shí)可以從基底膜上脫離,從尿中排出,臨床上出現(xiàn)蛋白尿和腎功能不全。足細(xì)胞是終末分化的細(xì)胞,不具有再生和轉(zhuǎn)分化的特點(diǎn),一旦脫落不能再生,并可造成球囊粘連,進(jìn)而造成腎小球硬化,腎功能減退。一些研究已發(fā)現(xiàn),尿液中脫落足細(xì)胞的數(shù)量對(duì)于判斷多種蛋白尿性疾病的活動(dòng)性和進(jìn)展有臨床意義[3-5]。小鼠抗人足細(xì)胞podocalyxin單克隆抗體尿沉渣染色,是一種特異性檢測(cè)尿足細(xì)胞的方法,被廣泛應(yīng)用[6]。本研究觀察了 IgM腎病患者足細(xì)胞排泄情況,有9例患者尿足細(xì)胞排泄量為0/20HP,僅有1例為2個(gè)/20HP。無(wú)足細(xì)胞排泄,說明足細(xì)胞未從基底膜脫離,腎臟無(wú)嚴(yán)重?fù)p傷,結(jié)合腎臟病理顯示的臟層上皮細(xì)胞腫脹,很少有球囊粘連,間質(zhì)損傷輕微,可以解釋為什么10例患者表現(xiàn)出對(duì)激素和免疫抑制劑的良好反應(yīng)性。但因本組病例數(shù)較少,隨診時(shí)間短,其遠(yuǎn)期預(yù)后還需進(jìn)一步隨診觀察。
IgM腎病的發(fā)病機(jī)制不清,一些學(xué)者觀察到IgM的沉積部位與病變嚴(yán)重程度相關(guān),因此認(rèn)為IgM參與IgM腎病的致病[1,7],但一些研究并未發(fā)現(xiàn) IgM 沉積有致病作用[8]。在這10例患者的腎組織中IgM均沉積于系膜區(qū),在血管壁沒有沉積,因此臨床預(yù)后較好。另外患者外周血中有4例IgM升高,3例輕度升高,1例明顯升高,完善相關(guān)檢查除外骨髓瘤,激素治療效果很好,尿蛋白2周轉(zhuǎn)陰,隨診半年,但I(xiàn)gM仍明顯升高,目前正處于密切監(jiān)測(cè)中。因此IgM在疾病中所起的作用不清,本研究的樣本量較小,需進(jìn)一步擴(kuò)大樣本量來(lái)總結(jié)該病臨床表現(xiàn),實(shí)驗(yàn)室檢查特點(diǎn)與病理之間的關(guān)系。
1 莊永澤,謝福安,余英豪,等.成人IgM腎病臨床病理與預(yù)后的探討[J].中華腎臟病學(xué),1998,14(3):185.
2 蔣煒,黎磊石,俞雨生,等.163例IgM腎病的臨床病理聯(lián)系及臨床資料分析 [J].金陵醫(yī)院學(xué)報(bào),1993,6(3):231-233.
3 尚瑜,尹愛萍.特發(fā)性膜性腎病患者尿中足細(xì)胞與蛋白尿的相關(guān)性分析 [J].西安交通大學(xué)學(xué)報(bào) (醫(yī)學(xué)版),2011,32(3):328-331.
4 張敏,朱彤瑩,彭艾,等.氯沙坦對(duì)糖尿病腎病患者尿足細(xì)胞排泄的影響 [J].中華腎臟病雜志,2006,22(2):72-75.
5 李驚子,黃海長(zhǎng),劉穎等.檢測(cè)尿足細(xì)胞在活動(dòng)性腎小球疾病中的意義 [J].北京大學(xué)學(xué)報(bào) (醫(yī)學(xué)版),2005,37(5):463-466.
6 劉穎,李驚子,黃海長(zhǎng),等.免疫細(xì)胞化學(xué)法檢測(cè)尿足細(xì)胞的臨床應(yīng)用 [J].中國(guó)中西醫(yī)結(jié)合雜志,2007,8(9):511-514.
7 陳海平,王質(zhì)剛,劉艷勛,等.IgM腎病與單純系膜增生性腎炎腎病綜合征臨床病理分析 [J].腎臟病與透析腎移植雜志1996,5(2):24-28.
8 馬恒顥,莊昭勤,謝祥鰲,等.小兒特發(fā)性IgM腎病與微小病變腎病綜合征的臨床病理關(guān)系 [J].中華腎臟病雜志,1994,10(1):8-11.

