卡培他濱聯合奧沙利鉑治療Ⅲ期結直腸癌的療效觀察
黃東海,談凱(1.湖北省腫瘤醫院藥劑科,武漢市 430079;.湖北省腫瘤醫院腹泌外科,武漢市 430079)
卡培他濱聯合奧沙利鉑治療Ⅲ期結直腸癌的療效觀察
黃東海1*,談凱2(1.湖北省腫瘤醫院藥劑科,武漢市 430079;2.湖北省腫瘤醫院腹泌外科,武漢市 430079)
目的:觀察卡培他濱聯合奧沙利鉑治療Ⅲ期結直腸癌的療效和安全性。方法:選擇我院2004年1月-2010年6月收治的214例Ⅲ期結直腸癌患者,隨機分為初治組102例(首次接受化療)和復治組112例(既往接受化療但未接受卡培他濱聯合奧沙利鉑化療)。采用卡培他濱1 500 mg·m-2口服,聯合奧沙利鉑100 mg·m-2靜脈滴注的方案進行化療,所有患者在化療期間每周進行1次血常規檢查,在每個療程前后進行心電圖、電解質、肝腎功能等檢查。化療2個療程后,在第42天進行CT掃描評價化療療效。同時,記錄患者的各種不良反應。結果:初治組(46.08%)與復治組(24.11%)總有效率比較差異有統計學意義(P<0.01)。卡培他濱聯合奧沙利鉑的化療方案的近期總有效率達34.58%。治療中的主要不良反應有惡心、嘔吐、腹瀉、脫發、白細胞減少、血小板減少、貧血、感覺神經病變、肝功能損害等,所有病例未出現Ⅳ級毒性反應。結論:卡培他濱聯合奧沙利鉑治療Ⅲ期結直腸癌療效較好,安全性較高,但初治組比復治組效果更好。
卡培他濱;奧沙利鉑;Ⅲ期結直腸癌;療效;安全性
結直腸癌是我國臨床常見的惡性腫瘤,近年來發病率逐步升高,并有年輕化的趨勢,且一般發現較晚,臨床中結直腸癌患者就診時Ⅲ期約占30%~40%,因此Ⅲ期結直腸癌患者是主要治療人群[1,2]。結直腸癌可采用外科手術方法治療,但容易發生術后局部復發和遠處轉移[3]。化療是Ⅲ期結直腸癌主要的治療措施,5-氟尿嘧啶(Fluorouracil,5-FU)、亞葉酸鈣(Leucovorin,LV)聯合奧沙利鉑(Oxaliplatin)的化療方案是結直腸癌化療的經典方案,有文獻報道化療可延長患者的生存期,并有效降低死亡風險[4]。近年來由于聯合用藥的化療新方案不斷出現,Ⅲ期結直腸癌化療的療效得到一定改善,安全性有一定提高。我院將卡培他濱(Capecitabin)與奧沙利鉑聯合用于Ⅲ期結直腸癌的化療,取得較好的療效,現報道如下。
1 資料與方法
1.1 一般資料
我院于2004年1月-2010年6月采用卡培他濱聯合奧沙利鉑治療了214例Ⅲ期結直腸癌患者。其中,男性126例,女性88例,年齡41~83歲,平均年齡(66.4±8.5)歲。所有病例均經病理切片或細胞學確診為Ⅲ期結直腸癌[5],其中結腸腺癌142例、直腸腺癌72例;初治患者98例,復發轉移者116例;腫瘤轉移部位為單純淋巴結轉移44例,單純肺轉移12例,單純肝轉移38例,其余復發轉移者為腫瘤多處轉移;低分化管狀腺癌112例,中分化管狀腺癌74例,黏液腺癌28例。所有病例卡氏評分(KPS)均>120分,無化療禁忌證,化療前血常規、肝、腎、心、肺等器官功能均正常,均有實質性腫瘤病灶,近1個月內未接受放射治療及其他化療藥物治療。將214例患者隨機分為2組,初治組102例為首次接受化療的患者;復治組112例為既往接受過化療的患者,但未接受卡培他濱聯合奧沙利鉑化療。2組性別、年齡等一般資料比較差異無統計學意義(P>0.05),具有可比性。
1.2 治療方法
卡培他濱(希羅達)1 500 mg·m-2,每日2次,飯后30 min口服,連服14 d為1個療程,接著停藥7 d,在第21天時開始第2個療程。奧沙利鉑注射液100 mg·m-2,加入5%葡萄糖注射液250 mL中緩慢靜脈滴注,在每個療程的第1天進行,即第1天、第21天靜脈滴注。化療前采用阿扎司瓊注射液預防化療可能引起的惡心、嘔吐等不良反應,并采用還原型谷胱甘肽注射液保護肝功能。化療前囑咐患者在每個療程期間禁止食用冷飲與冷食,并禁止冷浴,以減少化療引起的末梢神經不良反應,并防止喉痙攣等癥狀。所有患者化療前均簽署化療知情同意書。
1.3 療效評定標準[6]
所有患者在化療期間每周進行1次血常規檢查,在每個療程前后進行心電圖、電解質、肝腎功能等檢查。化療2個療程后,在第42天進行CT掃描評價化療的療效。同時,在化療期間詳細記錄患者的各種不良反應。化療的療效為近期客觀療效,按照世界衛生組織(WHO)制定的標準,共分為4類。(1)完全緩解(CR):腫瘤完全消失至少維持4周以上,且未出現新病灶;(2)部分緩解(PR):腫瘤消退≥50%至少維持4周,且未出現新病灶;(3)無變化(NC):腫瘤消退<50%或腫瘤增大<25%;(4)進展(PD):腫瘤增大≥25%或出現新病灶。總有效率(RR)=(CR例數+PR例數)/總例數×100%。化療的安全評價考察其不良反應,按照WHO制定的標準分為0~Ⅳ級。
1.4 統計學方法
2 結果
2.1 化療的療效
卡培他濱聯合奧沙利鉑治療214例Ⅲ期結直腸癌的療效見表1。
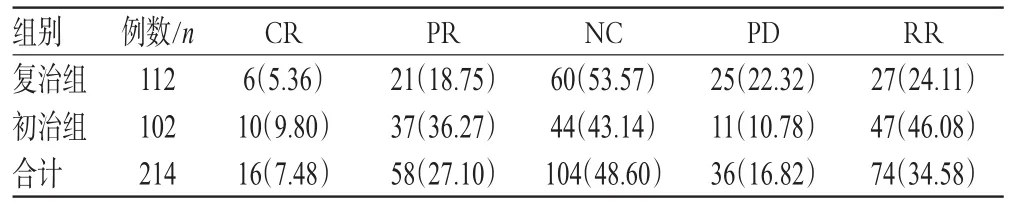
表1 卡培他濱聯合奧沙利鉑的療效(n,%%)Tab 1 Efficacy evaluation of chemotherapy of capecitabine combined with oxaliplatin(n,%%)
由表1可見,初治組與復治組RR比較,差異有統計學意義(P<0.01)。結果表明,卡培他濱聯合奧沙利鉑治療Ⅲ期結直腸癌具有較好的療效,初治組比復治組療效更佳。
2.2 化療的不良反應
卡培他濱聯合奧沙利鉑治療214例Ⅲ期結直腸癌的不良反應見表2。
由表2可見,所有病例未見Ⅳ級毒性反應,表明卡培他濱聯合奧沙利鉑治療Ⅲ期結直腸癌具有較低的不良反應發生率。
3 討論
卡培他濱是5-FU的前體藥物,具有靶向性,口服給藥后在機體中能被腫瘤組織中的胸苷磷酸化酶選擇性轉化為5-FU,從而發揮抗腫瘤活性[7]。卡培他濱在胃腸道內的吸收幾乎完全,由肝臟中的羧酸酯酶轉化成中間物5’-脫氧-5-氟胞苷。而實體瘤中存在比正常細胞表達更多的胞苷脫氨酶,上述中間物會在胞苷脫氨酶作用下轉化為5’-脫氧-5-氟尿苷,后者又會被腫瘤組織中的胸腺嘧啶磷酸化酶轉化為抗腫瘤活性物5-FU[8]。有文獻[9]報道卡培他濱具有高效性,且安全性高,國外大規模臨床試驗結果表明,卡培他濱單獨治療結直腸癌時,有效率可達20%以上,因此卡培他濱有成為一線化療藥物的潛力。
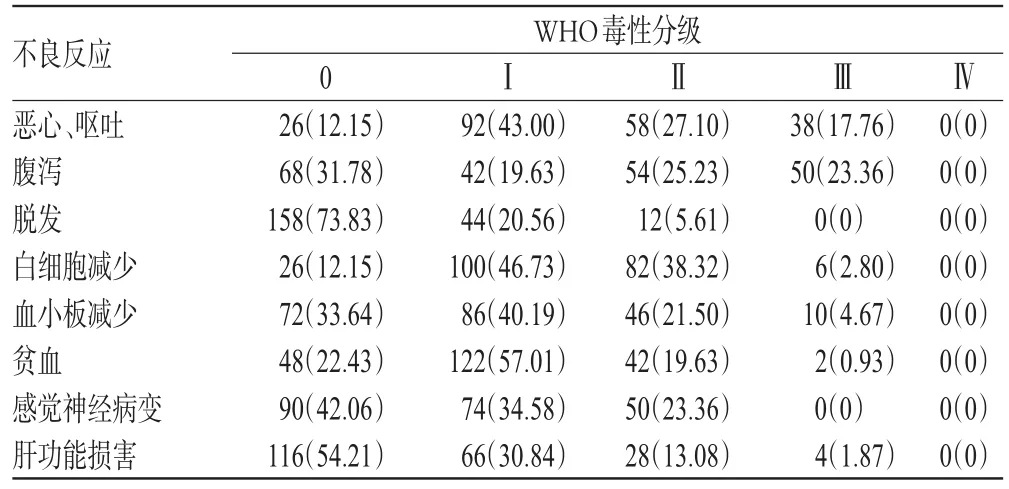
表2 化療的不良反應(n,%%)Tab 2 Adverse drug reaction induced by chemotherapy(n,%%)
奧沙利鉑是新一代鉑類抗腫瘤藥物,其作用機制為阻斷腫瘤組織DNA的復制和轉移,對多種腫瘤具有顯著的抑制作用。有文獻[10]表明,奧沙利鉑與5-FU有協同作用,在機體內與DNA結合速度更快、更牢固,可發揮更強的細胞毒作用。
目前,全身化療是Ⅲ期結直腸癌有效的治療手段之一,奧沙利鉑、卡培他濱等新藥的問世給Ⅲ期結直腸癌患者帶來福音。本文分析卡培他濱與奧沙利鉑聯合治療214例Ⅲ期結直腸癌化療的臨床病例,其總有效率為34.58%。治療中的主要不良反應為消化道反應、免疫抑制、骨髓抑制、外周神經毒性、肝毒性等,但所有病例未見Ⅳ級毒性反應,絕大多數患者可耐受。綜上所述,卡培他濱聯合奧沙利鉑治療Ⅲ期結直腸癌療效較好,安全性較高,但初治組比復治組效果更好。
[1]畢經旺,王寶成,劉 欣,等.奧沙利鉑聯合卡培他濱治療老年晚期大腸癌療效觀察(附48例報告)[J].山東醫藥,2009,49(14):81.
[2]Sumpter K,Harper-Wynne C,Cunningham D,et al.Oxaliplatin and capecitabine chemotherapy for advanced colorectal cancer:a single institution's experience[J].Clin Oncol(R Coil Radiol),2003,15(5):221.
[3]張紅梅.伊立替康聯合5-氟尿嘧啶/亞葉酸鈣雙周方案治療晚期結直腸癌的臨床觀察[J].中國藥房,2010,21(32):3 021.
[4]郭建新,陶慶松,陳 俊,等.奧沙利鉑或依立替康聯合卡培他濱治療晚期大腸癌[J].中國癌癥雜志,2007,17(6):503.
[5]王洪義,顧 晉,彭亦凡,等.Ⅲ期結直腸癌分期分層及其臨床意義探討[J].中華普通外科雜志,2007,22(1):8.
[6]王吉林,唐潔婷,房靜遠.Ⅰ~Ⅲ期結直腸癌患者圍手術期肝臟局部化療對術后肝轉移及生存率影響的Meta分析[J].中國癌癥雜志,2010,20(8):615.
[7]張 華,鄭登云,羅榮城.羥基喜樹堿聯合卡培他濱二線治療晚期結直腸癌[J].實用醫學雜志,2009,(15):2 546.
[8]Zeuli M,Nardoni C,Pino MS,et al.PhaseⅡstudy of eapecitabine and oxaliplatin as first-line treatment in advanced colorectal cancer[J].Ann Oncol,2003,14(9):1 378.
[9]黃明敏,王 春,楊 立,等.奧沙利鉑聯合卡培他濱治療老年胃腸惡性腫瘤臨床觀察[J].南京醫科大學學報(自然科學版),2006,26(1):44.
[10]Hoff PM,Ansari R,Batist G,et al.Comparison of oral capecitabine versus intravenous fluorouracil plus leucovorin as first line treatment in 605 patients with metastatic colorectal cancer:resuhs of a randomized phase Ⅲ study[J].J Clin Oncol,2001,19(8):2 282.
Efficacy and Safety Evaluation of Capecitabine Combined with Oxaliplatin in Stage ⅢColorectal Cancer
HUANG Dong-hai(Dept.of Pharmacy,Hubei Provincial Cancer Hospital,Wuhan 430079,China)
TAN Kai(Dept.of Abdominal and Urinarg Surgery,Hubei Provincial Cancer Hospital,Wuhan 430079,China)
OBJECTIVE:To evaluate the therapeutic efficacy and safety of capecitabin combined oxaliplatin in the treatment of stageⅢ colorectal cancer.METHODS:214 patients suffering from stageⅢ colorectal cancer were admitted in our hospital during Jan.2004~Jun.2010.Those patients were randomly divided into initial treatment group with 102 cases(receiving chemotherapy for the first time)and retreatment group with 112 cases(had
chemotherapy without combined therapy of capecitabine and exaliplatin).Those patients received oral dose of capecitabin 1 500 mg·m-2,intravenous injection of oxaliplatin 100 mg·m-2and chemotherapy regimen.Blood routine examination was conducted every week during chemotherapy.The electrocardiogram,electrolyte and liver and kidney function were determined before and after each treatment course.After 2 treatment courses,the therapeutic efficacy of chemotherapy was evaluated by CT scanning at 42th day.The adverse drug reactions of all patients were recorded.RESULTS:There was significant difference in effective rate between initial treatment group and retreatment group(46.08%vs.24.11%).The chemotherapy regimen showed total effective rate was 34.58%.The adverse drug reactions included nausea,vomiting,diarrhea,lipsotrichia,leukopenia,thrombocytopenia,anemia,sensory neuropathy,liver function impairment,etc.No Ⅳ degree toxicity reaction was found.CONCLUSION:Capecitabin combined with oxaliplatin is effective and safe in the treatment of stageⅢcolorectal cancer.The therapeutic efficacy of initial treatment group is better than that of retreatment group.
Capecitabin;Oxaliplatin;StageⅢ colorectal cancer;Therapeutic efficacy;Safety
R735.2
A
1001-0408(2011)20-1897-03
*主管藥師,本科。研究方向:抗腫瘤藥物。電話:027-87670346。E-mail:huangdonghaikp@sohu.com
2011-01-13
2011-03-22)

