門靜脈灌注化療聯合5-氟尿嘧啶緩釋劑區域性植入治療進展期胃癌療效觀察
邵 華,何治軍,苗永昌,夏春咸,王 剛
門靜脈灌注化療聯合5-氟尿嘧啶緩釋劑區域性植入治療進展期胃癌療效觀察
邵 華,何治軍,苗永昌,夏春咸,王 剛
目的 觀察門靜脈灌注化療聯合5-氟尿嘧啶 (5-FU)緩釋劑區域性植入治療進展期胃癌的療效。方法 選取2007年10月—2009年3月我科診治的進展期胃癌患者136例,根據是否進行術中門靜脈灌注化療或5-FU緩釋劑區域性植入,分為門靜脈灌注化療聯合5-FU緩釋劑區域性植入組37例 (A組),單純5-FU緩釋劑區域性植入組34例 (B組),單純門靜脈灌注化療組33例 (C組),單純手術對照組32例 (D組)。各組患者均根據腫瘤部位和侵犯程度行標準D2根治性手術,術后4周統一行5-FU、奧沙利鉑 (OXA)、亞葉酸鈣 (CF)方案 (FOLFOX6方案)化療6個周期。觀察各組出現的并發癥及不良反應情況,血常規及肝腎功能變化。各組患者定期復查并隨訪3年,了解其肝轉移或局部復發情況,記錄患者3年生存率。結果 術后各組患者均完成了隨訪,無失訪病例。A組肝轉移或局部復發率為10.8%(4/37)、B組為29.4%(10/34)、C組為30.3%(10/33)、D組為56.3%(18/32),差異有統計學意義 (χ2=16.670,P<0.05);其中A組肝轉移或局部復發率低于B組、C組和D組,差異均有統計學意義 (χ2值分別為3.873,4.142和16.313,P<0.05);B組和C組肝轉移或局部復發率低于D組,差異均有統計學意義 (χ2值分別為4.861和4.461,P<0.05)。A組3年生存率為91.9% (34/37)、B組為73.5% (25/34)、C組為72.7%(24/33)、D組為46.9%(15/32),差異有統計學意義 (χ2=17.352,P<0.05);其中A組3年生存率高于B組、C組和D組,差異均有統計學意義 (χ2值分別為4.254,4.510和16.894,P<0.05);B組和C組3年生存率高于D組,差異均有統計學意義 (χ2值分別為4.905和4.524,P<0.05)。各組均有并發癥及不良反應發生,但A、B、C組未影響術后化療,且血常規及肝腎功能無明顯異常。結論 門靜脈灌注化療聯合5-FU緩釋劑區域性植入治療可顯著降低進展期胃癌患者肝轉移或局部復發率,提高其3年生存率,效果優于單純門靜脈灌注化療或5-FU緩釋劑區域性植入,且操作簡單、定位準確、安全可行,值得臨床推廣應用。
胃腫瘤;化學療法,腫瘤,局部灌注;氟尿嘧啶;門靜脈
胃癌是世界范圍內最常見的消化道惡性腫瘤之一,在南美洲、東歐、亞洲及前蘇聯地區發病率較高[1]。進展期胃癌根治性術后體內微小轉移灶 (亞臨床病灶)是術后治療的重點,也是影響患者預后的關鍵因素[2]。體積微小的轉移灶以及尚未在肝臟內正式著床的腫瘤轉移細胞對化療敏感性較高,根治術中結合化療等措施可有效地殺滅殘留在肝臟內的微小轉移灶或癌細胞,以達到防止肝轉移、提高臨床療效的目的[3]。本研究回顧性分析我科診治的136例進展期胃癌患者的臨床資料,探討術中門靜脈灌注化療聯合5-氟尿嘧啶 (5-FU)緩釋劑區域性植入治療對進展期胃癌術后局部復發、肝轉移、生存時間、并發癥及不良反應的影響。
1 資料與方法
1.1 一般資料 選取2007年10月—2009年3月我科診治的進展期胃癌患者136例,根據是否進行術中門靜脈灌注化療或5-FU緩釋劑區域性植入,分為門靜脈灌注化療聯合5-FU緩釋劑區域性植入組37例 (A組),單純5-FU緩釋劑區域性植入組34例 (B組),單純門靜脈灌注化療組33例 (C組),單純手術對照組32例 (D組)。各組患者術前均無遠處轉移,卡氏評分>80分,術后無化療禁忌證。各組患者的性別、年齡、病理類型、胃癌TNM分期、手術方式比較,差異均無統計學意義 (P>0.05,見表1),具有可比性。
1.2 治療方法 各組患者均根據腫瘤部位和侵犯程度行標準D2根治性手術,手術由同一醫療小組實施。各組患者于術后4周統一行5-FU、奧沙利鉑 (OXA)、亞葉酸鈣 (CF)方案 (FOLFOX6方案)化療6個周期。
1.2.1 5-FU緩釋劑區域性植入 根據術中腫瘤部位,將5-FU緩釋劑 (先聲蕪湖中人藥業)800 mg植入腫瘤切緣及淋巴結清掃區域,每一植藥點植藥不超過150 mg,為避免影響手術吻合口愈合,要求植藥點與吻合口距離≥2 cm。給藥方法:術中直視下使用專用穿刺針刺入目標部位,有潛在殘留的組織中各穿刺植入點間隔1~2 cm形成立體網狀結構,擴大藥物的作用面積。
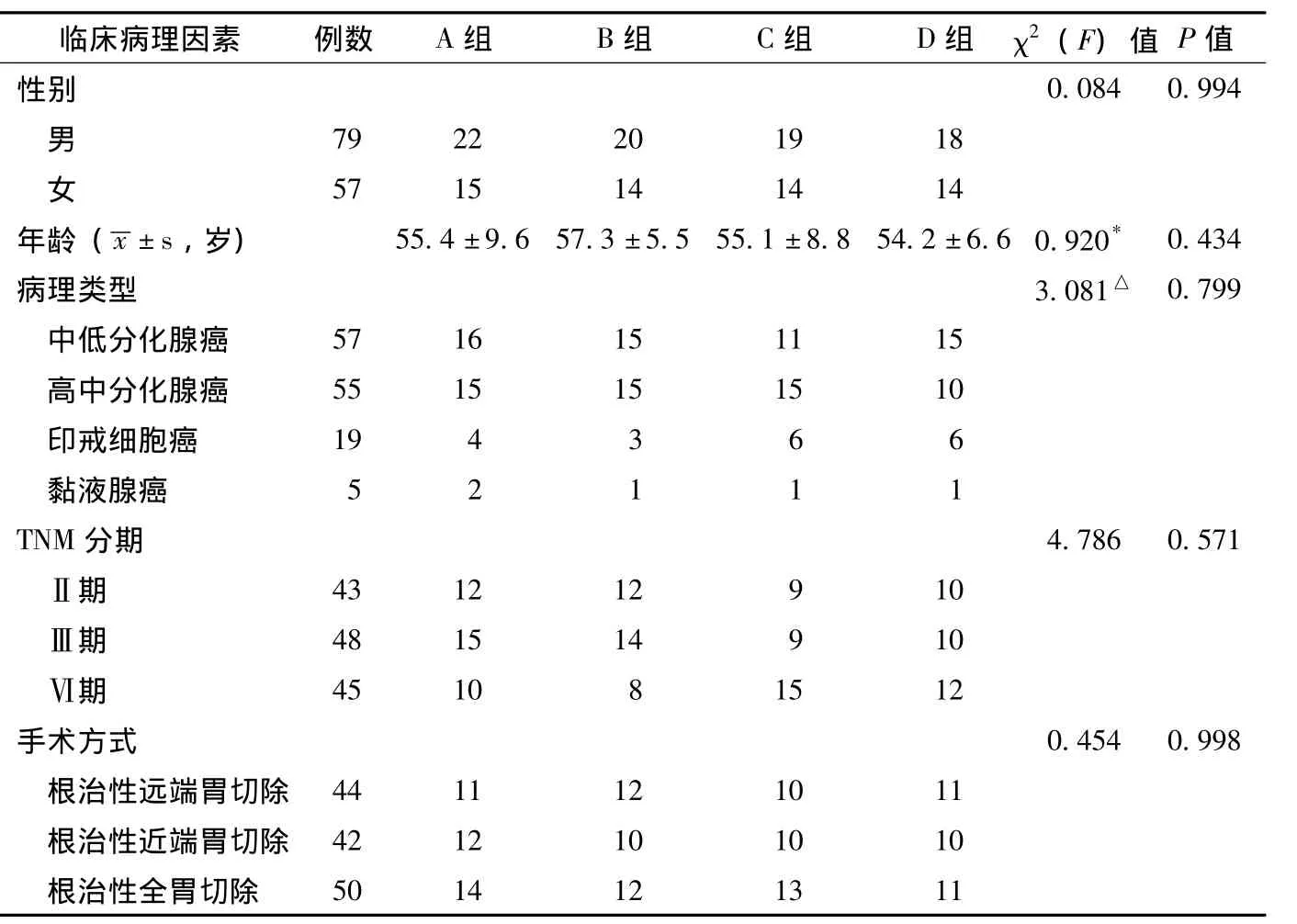
表1 各組一般資料比較Table 1 Comparison of general information in each group
1.2.2 門靜脈灌注化療 術中選擇相應的胃右靜脈、胃左靜脈進行門靜脈灌注化療,靜脈插管困難者解剖胃網膜右靜脈,分離血管后置入內徑為1.00 mm的硅膠管,灌注化療藥物為阿霉素40 mg、絲裂霉素8 mg、5-FU 500 mg,灌注結束后拔除導管,結扎靜脈后再行胃癌根治術。
1.3 觀察指標 記錄患者術后有無出血、吻合口漏、腸穿孔、腸梗阻、腹腔化膿性感染等并發癥及不良反應;觀察并記錄患者血常規變化,術后第3天、第7天、第14天復查肝腎功能。
1.4 隨訪 以門診或電話方式進行隨訪,隨訪3年,截止日期為2012-03-31。患者術后3年內每3個月復查1次,復查內容包括查體、癌胚抗原 (CEA)測定、肝臟B超及上腹CT檢查,以了解肝轉移或局部復發情況;記錄患者3年生存率。
1.5 統計學方法 應用SPSS 17.0軟件包進行統計學分析,計量資料以 (±s)表示,采用單因素方差分析;計數資料采用χ2檢驗,以P<0.05為差異有統計學意義。
2 結果
2.1 肝轉移或局部復發情況 術后各組患者均完成了隨訪,無失訪病例。A組肝轉移或局部復發率為10.8%(4/37),B組為 29.4% (10/34)、C組為 30.3%(10/33)、D組為56.3%(18/32)。各組肝轉移或局部復發率比較,差異有統計學意義 (χ2=16.670,P<0.05);其中 A組肝轉移或局部復發率低于B組、C組和D組,差異均有統計學意義 (χ2值分別為3.873,4.142和 16.313,P<0.05);B組和C組肝轉移或局部復發率低于D組,差異均有統計學意義 (χ2值分別為4.861和4.461,P<0.05)。
2.2 3年生存率 隨訪到截止日期,A組生存率為 91.9% (34/37)、B組為73.5%(25/34)、C組為 72.7% (24/33)、D組為46.9%(15/32)。各組3年生存率比較,差異有統計學意義 (χ2=17.352,P<0.05);其中 A組3年生存率高于B組、C組和D組,差異均有統計學意義 (χ2值分別為4.254,4.510和16.894,P<0.05);B組和C組3年生存率高于D組,差異均有統計學意義 (χ2值分別為4.905和4.524,P<0.05)。
2.3 觀察指標 各組患者手術切口均為Ⅰ期/甲級愈合。并發癥方面,A組出現吻合口漏1例,B組腸梗阻1例、腸穿孔1例,C組內出血1例,D組吻合口漏1例、腸穿孔1例、腹腔內感染2例;不良反應方面,A組出現血常規或肝腎功能異常2例,惡心嘔吐2例,腹痛2例;B組出現血常規或肝腎功能異常2例,惡心嘔吐1例,腹痛反應1例;C組出現惡心嘔吐2例,腹痛2例,均未影響術后化療;D組出現惡心嘔吐3例,腹痛2例。各組患者血常規及肝腎功能無明顯異常。
3 討論
目前東西方在D2根治性手術作為胃癌的標準手術方式上已初步達成共識[4-5]。進展期胃癌多伴有區域性淋巴結轉移,其中20%~80%的患者伴有腹腔內脫落或游離的腫瘤細胞,是影響腫瘤復發及術后生存率的主要因素,而全身化療對降低局部復發率效果欠佳[6-7]。腹腔灌注化療可以在腹腔局部形成較高的藥物濃度并直接作用于癌細胞,對于術后殘留的微小轉移灶,尤其是腹膜轉移者,早期給予腹腔灌注化療療效較好。但傳統的腹腔內灌注化療因藥物可被腹膜迅速吸收,控制效果常不滿意[8-9]。5-FU 緩釋劑區域性植入可在局部形成持續的較高的藥物濃度,動物實驗證實,5-FU緩釋劑區域性植入的有效藥物濃度可維持360 h以上,滲透擴散半徑為 3 ~5 cm[10]。
陳積賢等[11]研究發現,胃癌患者探查前門靜脈血癌細胞陽性率為53%,而探查后升高為81%,考慮與手術操作和擠壓等有關,其使癌細胞脫落增加,進而導致肝內微小轉移。趙增順等[12]對胃癌患者門靜脈血單細胞轉移進行研究,結果發現其門靜脈血癌細胞總陽性率達60%。早期解決進展期胃癌患者肝內轉移對延長患者生存率十分重要。門靜脈灌注化療可預防腫瘤細胞在門靜脈系統內著床并抑制初期腫瘤細胞的增殖,可減少化療藥物在外周血和其他部位的擴散,進而降低了不良反應發生率[13-14],其應用在大腸癌的治療中較為廣泛且技術相對成熟,而關于胃癌門靜脈灌注化療的研究報道較少。門靜脈灌注化療有置泵和術中一次性灌注等途徑,但各有優缺點,5-FU緩釋劑區域性植入可彌補術中門靜脈一次性灌注化療的不足。
本研究采用門靜脈灌注化療聯合5-FU緩釋劑區域性植入治療進展期胃癌患者,結果發現A組患者肝轉移或局部復發率顯著低于B組、C組和D組,且B組和C組顯著低于D組,表明門靜脈灌注化療聯合5-FU緩釋劑區域性植入治療可顯著降低進展期胃癌患者肝轉移或局部復發率,效果優于單純門靜脈灌注化療或5-FU緩釋劑區域性植入。對患者進行隨訪發現,A組患者3年生存率顯著高于B組、C組和D組,且B組和C組高于D組,表明門靜脈灌注化療聯合5-FU緩釋劑區域性植入治療可顯著提高進展期胃癌患者3年生存率。各組患者術后切口愈合良好,雖有不同程度的并發癥及不良反應出現,但均未影響治療,且血常規及肝腎功能無明顯異常,表明門靜脈灌注化療聯合5-FU緩釋劑區域性植入治療安全可行,且操作簡單、定位準確,值得臨床推廣應用。
但本研究樣本例數較少,隨訪時間較短,對門靜脈灌注化療聯合5-FU緩釋劑區域性植入治療進展期胃癌的遠期療效和確切機制有待進一步研究驗證。
1 Ajani JA.Chemotherapy for gastric carcinoma[J].New and Old Options,1998,12(10 Suppl 7):44-47.
2 Cervantes A,Rosell S,Roda D,et al.The treatment of advanced gastric cancer:current strategies and future perspectives[J].Ann Oncol,2008,19(5):103 -107.
3 Narita M,Oussoultzoglou E,Chenard MP,et al.Impact of biomarkers expression before and after portal vein embolization on recurrence after two-stage hepatectomy for colorectal liver metastases [J].J Gastrointest Surg,2012,16(3):5554-561.
4 Sasako M,Sano T,Yamamoto S,et al.D2lymphadenectomy alone or with para-aortic nodal dissection for gastric cancer[J].N Engl J Med,2008,359(5):453 -462.
5 Songun I,Putter H,Kranenbarg EM,et al.Surgical treatment of gastric cancer:15-year follow-up results of the randomized national Dutch D1 D2 trial [J]. LancetOncol,2010,11(5):439-449.
6 Sethna KS,Sugarbaker PH.New prospects for the control of peritoneal surface dissemination of gastric cancer using perioperative intraperitoneal chemotherapy [J].Cancer Ther,2004,2:79-84.
7 Sugarbaker PH.Strategies for the prevention and treatment of peritoneal carcinomatosis from gastrointestinal cancer [J].Cancer Invest,2005,23(2):155-172.
8 Sugarbaker PH,Yu W,Yonemura Y.Gastrectomy,peritoneal,and perioperative intraperitonealchemotherapy:the evolution of treatment strategies for advanced gastric cancer[J].Semin Surg Oncol,2003,21(4):233-248.
9 Sautner T,Hofbauer F,Depisch D,et al.Adjuvant intraperitoneal cisplatin chemotherapy does not improve long-term survival after surgery for advanced gastric cancer[J].J Clin Oncol,1994,12(5):970 -974.
10 Sato A,Nakamachi M.Clinical development of chemotherapy for advanced gastric cancer[J].Gan To Kagaku Ryoho,2008,35(9):1461-1466.
11 陳積賢,黃建武,張潔,等.胃癌患者門靜脈血中p53和k-ras基因突變的檢測及其臨床意義 [J].中華普通外科雜志,2006,21(10):739-741.
12 趙增順,王少文,焦喜林,等.門靜脈單細胞轉移檢測在胃癌根治術中的應用[J].中華外科雜志,1999,37(5):317.
13 Ishida H,Iwama T,Mishima.The significance of portal vein chemotherapy for liver micrometastasis:an experimental study of a rat model[J].Surg Today,1994,24:900-905.
14 Cagol PP,Pasqual E,Bacchetti S.Potential advantages of locoregional intra-arterial chemotherapy [J].IvVivo,2006,20(6A):777-779.
Regional Sustained-release Chemotherapy Combined with Interventional Therapy in Treatment of Gastric Cancer
SHAO Hua,HE Zhi-jun,MIAO Yong -chang,et al.Department of Gastrointestinal Surgery,the Second Hospital of Lianyungang,Lianyungang 222006,China
s】 Objectives To explore the effect of 5-fluorouracil(5-FU)sustained release chemotherapy coupled with interventional therapy in treating gastric cancer(GC).Methods A total of 136 GC patients were divided into groups A(n=37,given chemotherapies of combined portal vein infusion and sustained-release 5-FU),B(n=34,given 5-FU chemotherapy),C(n=33,given portal vein infusion),D(n=32,given operation).All patients were given standard D2 radical surgery based on tumor sites and invading degrees,and 6-cycle FOLFOX6 chemotherapy regime 4 weeks after operation.Complications,adverse reactions and changes of blood and functions of liver and kidney were observed.Three- year survival rates recorded.ResultsAll groups completed follow - ups,without loss to follow cases.The rate of hepatic metastasis and local failure was 4/37 in group A,10/34 in group B,10/33 in group C,18/32 in group D,the difference was significant(χ2=16.670,P <0.05);thereinto lower in group A than in groups B,C,D(χ2=3.873,4.142,16.313,respectively,P <0.05);lower in groups B,C than in group D(χ2=4.861,4.461,respectively,P <0.05).Three-year survival rate was 34/37 in group A,25/34 in group B,24/33 in group C,15/32 in group D,the difference was significant(χ2=17.352,P <0.05);thereinto higher in group A than in groups B,C,D(χ2=4.254,4.510,16.894,respectively,P <0.05),higher in groups B,C than in group D(χ2=4.905,4.524,respectively,P <0.05).Each group had complications and adverse reactions,not influencing curative effects.ConclusionChemotherapy of combined portal vein infusion and 5 -FU,easy to operate,safe and feasible with accurate positioning,can reduce the rate of hepatic metastasis and local failure of advanced GC patients and is worth generalizing and applying clinically.
Stomach neoplasms;Chemotherapy,cancer,regional perfusion;Fluorouracil;Portal vein
R 735.2
B
1007-9572(2012)10-3405-03
10.3969/j.issn.1007-9572.2012.10.067
222006江蘇省連云港市第二人民醫院胃腸外科
2012-05-15;
2012-09-09)
(本文編輯:鹿飛飛)

