云南省140例HIV/AIDS患者抗病毒治療效果和耐藥檢測分析
張云桂,周曾全,刑 輝,廖玲潔,段 松,勞云飛,李惠琴
(1.云南省傳染病專科醫院,云南 昆明 650301;2.中國疾病預防控制中心性病艾滋病中心,北京 102206;3.德宏州疾病預防控制中心,云南 德宏 678400)
我國自2004年全面開展了免費高效抗逆轉錄病毒治療(HAART),顯著降低了艾滋病病毒(HIV)感染者和艾滋病(AIDS)病人(簡稱HIV/AIDS患者)的病死率,提高了他們的生活質量。但是隨著治療時間的延長,HIV在高速復制、高度遺傳變異和在藥物選擇壓力的作用下,產生了耐藥突變,導致藥物耐藥。為了解中國現行一線抗病毒藥物治療的HIV/AIDS患者,在治療1年內免疫應答、病毒載量抑制效果,以及產生耐藥性情況,云南省傳染病專科醫院作為HIV耐藥哨點,于2007年2月~8月共招募并入組HIV/AIDS患者140例,進行前瞻性隊列研究。本次調查為首次在云南HIV/AIDS患者中建立前瞻性隊列研究,對治療效果和耐藥情況進行動態觀察,這有助于系統地評價本地區抗病毒治療的效果和耐藥發生情況。
1 研究對象
采用隨機整群抽樣的方法,選取2007年2月~8月昆明市、德宏州隴川縣、瑞麗市、潞西市符合抗病毒治療的 HIV/AIDS患者作為入組對象,共招募并入組HIV/AIDS患者140例,所有患者既往均未接受過抗病毒治療。入組時選用統一國家一線治療方案:司他夫定(D4T)/拉米夫定(3TC)/奈韋拉平(NVP)。
140例患者基線情況如下:性別:男77例,女63例。年齡:20歲以下2例,20~29歲44例,30~39歲66例,40~49歲20例,50歲以上8例。民族:漢族73例,傣族33例,景頗族24例,其他少數民族10例。婚姻狀況:已婚28例,未婚112例。文化程度:文盲21例,小學39例,初中56例,高中11例,大專及以上13例。可能感染途徑:性途徑89例,靜脈吸毒35例,不詳16例。
免疫學(CD4,單位:個/μl):CD4≤50 個/μl 26 例;51~100個/μl 22例;101~200個/μl 32例;201~300個/μl 55例;301~350個/μl 5例。病毒學(VL,單位:拷貝/ml):VL>500000拷貝/ml 5例;100000~500000拷貝/ml 40例;100000~10000拷貝/ml 75例;1000~10000拷貝/ml 17例;<1000拷貝/ml 3例。
2 方法
在治療0月、6月、12月對入組患者進行流行病學調查、臨床觀察,檢測CD4、VL, 對治療6月,12月時VL>1000拷貝/ml的血標本進行HIV耐藥檢測。采用實驗室自建(In-house)的HIV耐藥基因型檢測方法:采用套式反轉錄-聚合酶鏈反應(RT-PCR)擴增pol基因區部分片段,對擴增產物測序,隨后進行序列拼接、編輯和清理。清理后的序列與 standford HIV Drug Resistance Database 中的共享序列進行比對,以判斷是否發生耐藥突變,并對耐藥程度進行分析。所有收集到的流行病學、臨床及實驗室數據通過Epidata軟件進行雙錄入,并作一致性檢驗后生成最終數據庫。數據分析通過SPSS軟件完成。
3 結果
共有140例HIV/AIDS患者進入研究隊列。132例完成6月隨訪,占94%,其中5例失訪,2例自行停藥,1例因合并嚴重機會性感染死亡。126例完成12月隨訪,占90%,其中在治療6月隨訪后新增5例失訪,1例因乳酸酸中毒停止抗病毒治療。
3.1 免疫學治療效果
抗病毒治療前患者CD4平均值為164個/μl,大多數病人免疫力極低下。治療6個月CD4平均數上升至327 個/μl,上升了163 個/μl。治療12個月CD4平均數上升至377 個/μl,上升了213 個/μl。
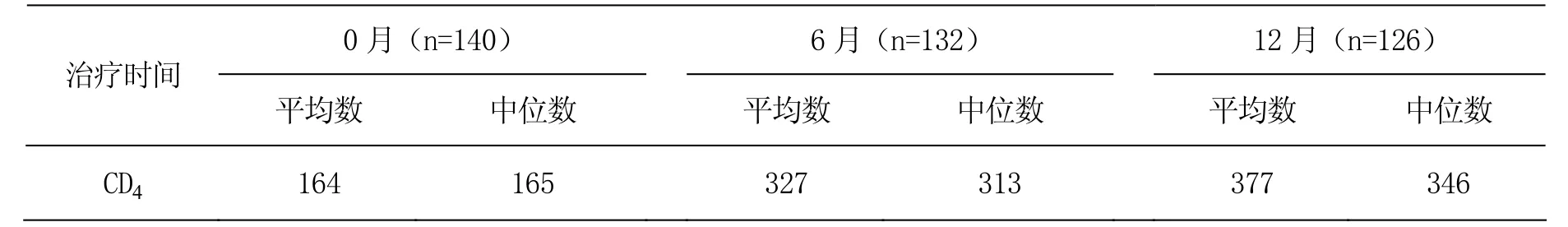
表1 入組的HIV/AIDS患者CD4變化
3.2 病毒學治療效果
抗病毒治療前大多數患者病毒載量處于較高水平,基線VL>10000 拷貝/ml的120例,占入組病人的85.7%(120/140)。基線VL<1000 拷貝/ml的3例,占2.1%(3/140)。治療6月VL<1000 拷貝/ml的125例,占94.7%(125/132),其中病毒完全抑制(VL<50拷貝/ml)81例,占 61.4%(81/132)。治療 12月 VL<1000 拷貝/ml的119例,占94.4%(119/126),其中病毒完全抑制(VL<50拷貝/ml)77例,占61.1%(77/126)。
3.3 HIV耐藥情況
基線樣本的耐藥性檢測未發現主要耐藥突變。治療6月時病毒載量檢測發現7例患者VL>1000 拷貝/ml,7例檢測均未發現耐藥位點。此7例患者治療12月隨訪時4例患者VL<50拷貝/ml,1例VL<400拷貝/ml,2例失訪。治療12月時病毒載量檢測發現亦有7例患者VL>1000 拷貝/ml:其中PCR擴增成功5例,3例對核苷類藥物和非核苷類藥物均有不同程度的耐藥,耐藥發生率為2.4%(3/126),2例未發現耐藥位點。
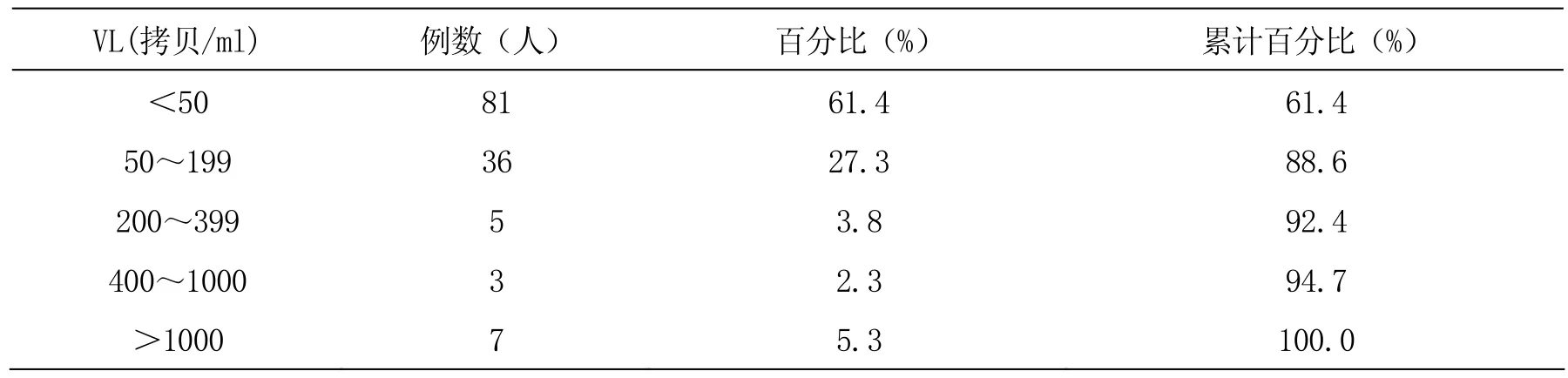
表2 治療6月病毒載量結果(n=132人)
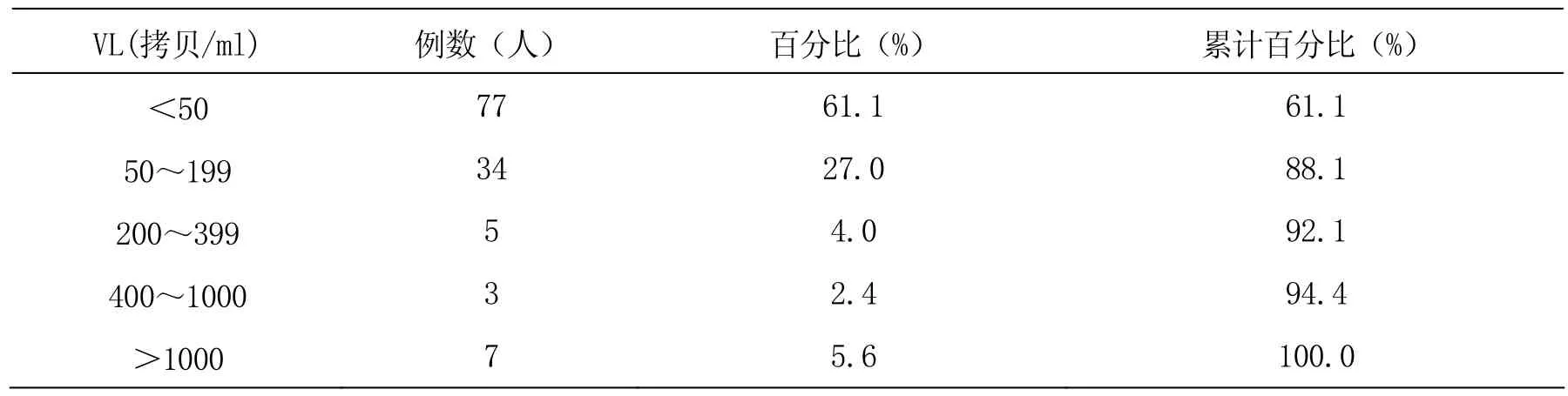
表3 治療12月病毒載量結果(n=126人)
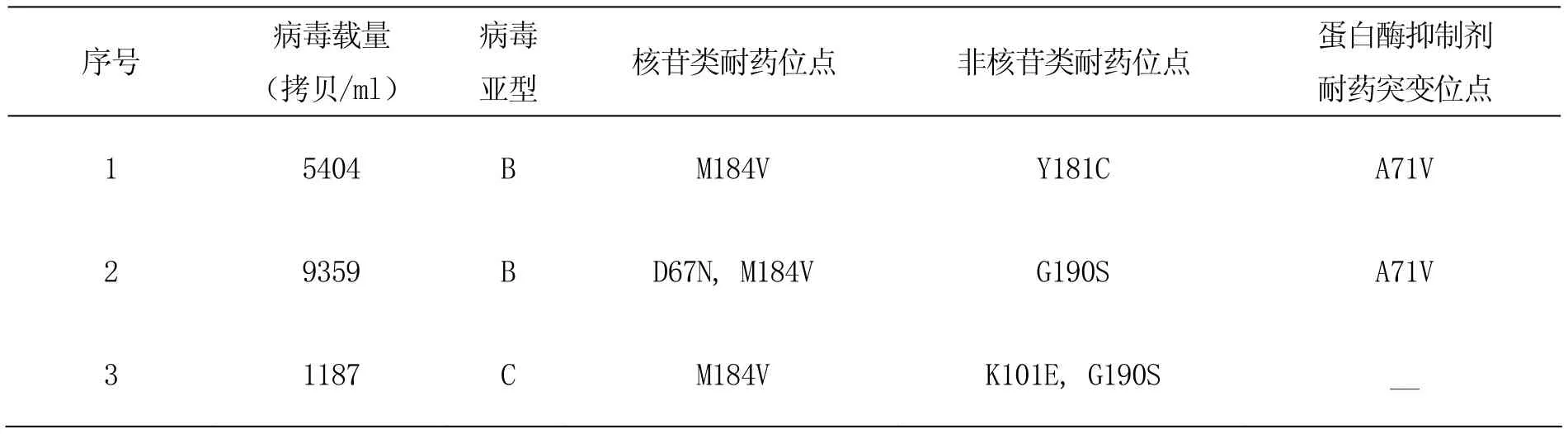
表4 3例產生HIV耐藥的患者情況及耐藥突變位點
3例患者均出現M184V突變,對拉米夫定(3TC)、恩曲他濱(FTC)高度耐藥。1例患者出現D67N突變,對阿巴卡韋(ABC)低度耐藥。2例患者分別出現G190S和K101E、 G190S突變,對奈韋拉平(NVP)、依非韋侖(EFV)高度耐藥。1例患者出現Y181C突變,對EFV低度耐藥,對NVP高度耐藥。2例患者分別出現1個蛋白酶抑制劑次要耐藥位點A71V,對所有蛋白酶抑制劑均無耐藥。
4 討論
4.1 免疫學、病毒學治療效果明顯
自從我國艾滋病抗病毒治療工作全面開展以來,顯著降低了HIV/AIDS患者的病死率,抗病毒治療工作已經取得了顯著療效[1]。國產抗病毒藥物在免疫學應答與病毒抑制效果方面與國外相關研究相近[2]。本研究結果顯示,云南省研究隊列使用一線抗病毒治療方案取得了良好的治療效果,獲得了良好的免疫學應答和病毒抑制效果。126例患者治療1年CD4中位數為346 個/μl,較全國水平高。為消除實驗室誤差和單一的病毒載量“脈沖”(blips)的影響,2011年1月美國指南中ACTG (AIDS Clinical Trials Group)更新了定義病毒學失敗為VL>200拷貝/ml[3],按照這個標準,治療6月和12月的病毒學抑制率(VL<200拷貝/ml)分別為 88.6%和 88.1%。良好的治療效果與病人的早期發現和治療、省-州-縣抗病毒定點醫院模式的有效運行密切相關。
4.2 耐藥突變位點檢測
本研究對初次抗病毒治療的患者進行治療前耐藥突變位點檢測,未發現耐藥突變位點。在河南省某地區進行的一次 HIV 感染者治療和耐藥調查中發現,未行抗病毒治療的76 例患者中低中度耐藥相關突變例數為1 例(1.3%) ,高度耐藥突變例數為2例(2.6%)[4]。美國40 個城市進行的一項多中心研究對371名未治療的HIV-1感染者的耐藥性突變進行調查,發現其中14%的感染者至少存在一個耐藥性突變[5]。我國治療前基線耐藥突變檢測率遠遠低于發達國家水平,主要原因是絕大多數病人既往未使用單一或者兩聯抗病毒治療藥物以及規范開展HAART。本研究中治療半年時7例VL>1000拷貝/ml的患者進行耐藥突變位點檢測,未發現耐藥位點。7例患者均存在服藥依從性差的問題,通過加強依從性教育后病毒載量均能得到明顯抑制。治療半年后通過檢測病毒載量能及時發現治療效果不佳的病人,加強依從性管理,能避免這部分患者進一步出現耐藥,因此治療后每半年檢測病毒載量非常重要。加強患者依從性管理是抗病毒治療工作中的重點。
本研究中治療1年時3例患者同時出現對核苷類藥物和非核苷類藥物耐藥,耐藥率為2.4%(3/126),低于新疆同期的隊列研究結果(耐藥率為10.6%)[6]。其中2例患者出現了蛋白酶抑制劑的次要突變位點A71V突變,但未導致蛋白酶抑制劑耐藥。核苷類藥物耐藥機制主要是藥物與宿主細胞DNA鏈末端結合的能力下降。3例患者均出現了M184V突變。M184V是最常見的核苷類耐藥位點,單一位點突變就可引起對3TC/ FTC的高度耐藥,但此位點突變使病毒對齊多夫定(AZT)、去羥肌苷(DDI)、替諾福韋(TDF)敏感性增強[7],因此一般繼續使用3TC,并合用其他敏感的藥物進行治療。1例患者出現了D67N突變,屬于胸苷類似物突變( Thymidine analogmutation ,TAM) 。TAMs主要包括6 個位點的突變:M41L、D67N、K70R、L210W、T215 Y、K219Q。這類突變可以使包括AZT、D4T、ABC 和 ddI 在內的核苷類似物耐藥。3 個(或 3 個以上)TAM 外加M184V 和(或) L74V 可以產生對ABC 的耐藥性,但產生高水平的AZT 耐藥性僅僅需要兩個TAM,通常單獨存在的TAM 并不妨礙D4T、ABC 或者ddI 的使用[8]。隨著治療時間的延長,單獨存在的TAM會累積,形成TAMs導致核苷類多種藥物的耐藥。因此出現耐藥時需要及時更換抗病毒治療方案,避免耐藥位點的累積導致交叉耐藥,保障抗病毒治療療效。非核苷類耐藥機制主要是降低藥物與逆轉錄酶的親和力,導致藥物的抗病毒活性降低,最終使治療失敗。單一突變就可以對一種或多種非核苷類藥物產生高水平耐藥性[9]。治療1年時3例患者出現了非核苷類耐藥位點:Y181C、G190S、K101E,導致了NVP和EFV均耐藥。因此一旦出現NVP和EFV耐藥,需要及時更換為耐藥基因屏障高的非核苷類藥物依曲韋林或蛋白酶抑制劑。
云南省使用現行一線抗病毒治療方案取得了良好的治療效果,提高了HIV/AIDS患者的生存質量。下一步工作重點為進一步擴大治療覆蓋面,進一步降低艾滋病相關病死率,同時以治療作為預防手段,對單陽家庭中的HIV陽性一方開展治療,降低HIV新感染率。云南省治療前基線耐藥突變檢測率很低,但需要加強每半年病毒載量檢測,及時發現耐藥并更換二線抗病毒藥物,保障抗病毒治療療效。
[1]Zhang FJ,Dou ZH, Ma Y,et al. Five-year Outcomes of the China National Free Antiretroviral Treatment Program[J].Ann Intern Med,2009,151(4):242-251.
[2]李太生.國內外艾滋病抗病毒治療研究進展[J].傳染病信息,2008,2(6):324-326.
[3]A Working Group of the office of AIDS Research Advisory Council(OARAC),Guideline for the use of antiretroviral agents in HIV-1- Infected Adolescents,January 10,2011.website:http:/aidsinfo.nih.gov
[4]郭萬申,胡清海,張 旻,等.河南省某地區 HIV 感染者治療和耐藥現況調查[J].中國艾滋病性病,2006,12(4):304-306.
[5]Ross L , Lim M , Liao Q , et al. Prevalence of antiretroviral drug resistance and resistance mutations in antiretroviral therapy(ART) naive HIV infected individuals from 40 United States cities[J].HIV Clin Trial,2007,8(1):1-8.
[6]佐合拉·吐爾地,廖玲潔,董永慧,等.新疆部分艾滋病病人抗病毒治療效果和耐藥變異分析,中國艾滋病性病,2011,17(2):107-110.
[7]Miller MD, Margot N,Lu B et al. genotypic and phenotypic predictors of the magnitude of response to tenofovir disoproxil fumarate treatment in antiretroviral-experienced patients[J].J Infec Dis,2004,189(5):837-846.
[8]毛 霖.抗 HIV藥物臨床耐藥研究進展[J].中國艾滋病性病,2011,17(1):92-95.
[9]Antinori A , Zaccarelli M,Cingolani A,et al.Crossresistance among nonnucleoside reverse transcriptase inhibitors limits recycling efavirenz after nevirapine failure[J].AIDS Res Hum Retroviruses,2002,18:835.

