新課程下高考理綜化學實驗試題考查動向評析
劉 鴻
(曲靖市富源縣勝境中學,云南 曲靖 655500)
探究學習的方法是新課程改革的核心。高中化學新課程標準要求學生“具有較強的問題意識,能夠發現和提出有探究價值的化學問題”,并通過“經歷對化學物質及其變化進行探究的過程,進一步理解科學探究的意義,學習科學探究的基本方法,提高科學探究能力”。由于化學是以實驗為基礎的學科,實驗是化學問題解決的重要手段,同時實驗又是以實驗探究為其主要形式,所以實驗探究自然成為學科的著眼點。通過分析近幾年高考新課標寧夏卷和全國卷的理綜化學試題,我們不難發現,作為高考主打題型的非選擇題部分實驗題既能夠在注重對化學學科中的基礎知識、基本能力和重要方法考查的同時,又能夠突出對信息整合能力、問題解決能力尤其是實驗探究能力的考查,從而很好地體現了新課程特點。本文主要就近四年的高考新課標寧夏卷和全國卷理綜化學非選擇題部分實驗試題從探究角度的考查動向方面作評析,希望能給高三理綜化學備考復習工作帶來一些啟示。
一、以實驗方案為切入點
[例1](2008年新課標高考理綜化學試題·寧夏卷)為測定一鐵片中鐵元素的含量,某課外活動小組提出下面兩種方案并進行了實驗(以下數據為多次平行實驗測定結果的平均值):
方案一:將a g鐵片完全溶解于過量稀硫酸中,測得生成氫氣的體積為580mL(標準狀況);
方案二:將(a/10)g鐵片完全溶解于過量稀硫酸中,將反應后得到的溶液用0.02mol·L-1的KMnO4溶液滴定,達到終點時消耗了25.00mL KMnO4溶液。
請回答下列問題:
(1)配平下面的化學方程式(將有關的化學計量數填入答題卡的橫線上):
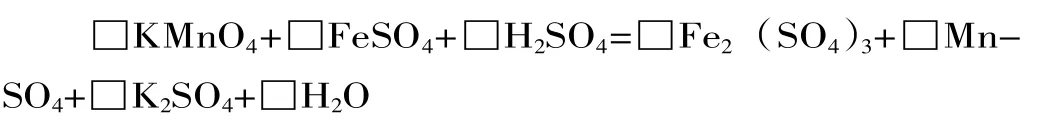
(2)在滴定實驗中不能選擇_____式滴定管,理由是__________;
(3)根據方案一和方案二測定的結果計算,鐵片中鐵的質量分數依次為_____和_____;(鐵的相對原子質量以55.9計)
(4)若排除實驗儀器和操作的影響因素,試對上述兩種方案測定結果的準確性做出判斷和分析。
①方案一 __________(填“準確”“不準確”“不一定準確”),理由是 __________;
②方案二 __________(填“準確”“不準確”“不一定準確”),理由是 __________。
【評析】本題綜合性很強,既是一道立足基礎實驗操作的試題,又是一道實驗評價的試題,還是一道開放型試題。通過設置全新情境考查了學生對實驗原理的理解、實驗操作的掌握、有關實驗的計算、實驗方案的評價等方面的探究能力。
題目給出的四個問題,每個問題各有側重。第(1)問是配平方案二中的一個化學方程式,利用化合價升降法容易配平。第(2)問是考查酸式滴定管、堿式滴定管的特點及使用條件。第(3)問是根據化學方程式的計算。第(4)問是對實驗方案的評價,具有開放性,很好地體現了新課標的理念,也準確考查了學生的思維能力和表達能力,對學生思維能力的考查上升到一個較高的層次,只有思維深刻的學生才能全面分析,得出正確的結論,反之回答起來就會失之偏頗。對于方案一:如果鐵片中只含單質鐵及鐵的氧化物,用生成氫氣的量只能測出單質鐵的量,不能測出鐵的氧化物中鐵的量。如果鐵片中還含有其他金屬也能與稀硫酸反應生成氫氣,則由氫氣的量推不出單質鐵的量。如果鐵片中不含雜質,用上述方法可以。對于方案二:如果鐵片中只含單質鐵及氧化鐵,該方案只能測出單質鐵的含量。如果鐵片中含有其他金屬,該金屬與稀硫酸反應生成的金屬離子也能被高錳酸鉀氧化,則鐵片中單質鐵的量就測不出。如果鐵片中不含雜質或只含有單質鐵及氧化亞鐵,該方案可以。以上兩個方案均有缺陷,因而測得的結果不一定準確。
本題學科特色明顯,對分析問題的能力要求較高。考查的知識在書中或在題內,但學生的學習、思維可以延伸到題外。可以說,題目彰顯了新的課程理念,有利于培養學生自學和深入思考探究的習慣。
二、以測定組成為切入點
[例2](2009年新課標高考理綜化學試題·寧夏卷)堿式碳酸銅可表示為:xCuCO3·yCu(OH)2·zH2O,測定堿式碳酸銅組成的方法有多種。
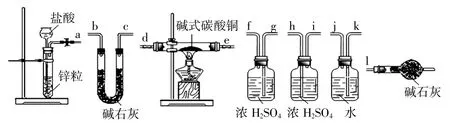
(1)現采用氫氣還原法,請回答如下問題:
①寫出 xCuCO3·yCu(OH)2·zH2O 與氫氣反應的化學方程式_______;
②試驗裝置用下列所有儀器連接而成,按氫氣流方向的連接順序是(填入儀器接口字母編號):(a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l)
③稱取23.9g某堿式碳酸銅樣品,充分反應后得到12.7g殘留物,生成4.4g二氧化碳和7.2g水。該樣品的結晶水質量為_______g,化學式為_______;
(2)某同學以氮氣代替氫氣,并用上述全部或部分儀器來測定堿式碳酸銅的組成,你認為是否可行?請說明理由:_______。
【評析】本題難度中等,要求學生根據提供的儀器和藥品,來完成實驗目的、設計實驗方案并處理相關的實驗問題,考查了學生綜合實驗知識與技能的應用能力、設計和完成實驗的能力。
第(1)問①的堿式碳酸銅與氫氣反應看似一個很難的信息,其實細心一點只要把它理解為CuCO3和Cu(OH)2受熱分解后產物CuO再與氫氣反應即可解決;對于②要能分析出測定反應后CO2和H2O質量,因此對于氫氣發生器后儀器的選擇是除氯化氫和水蒸氣,防止對后續測定影響,因為測定H2O和CO2分別用濃硫酸和堿石灰是固定的。(2)其實在分析(1)①方程式書寫時便得到了堿式碳酸銅熱分解方程式:xCuCO3·yCu(OH)2·zH2O=(x+y)CuO+xCO2↑+(y+z)H2O↑,稍加分析可知,依據堿式碳酸銅、CuO、CO2和H2O質量(或其中任意三個量),即可計算出其組成。
解此題的關鍵是明確實驗目的、了解實驗原理,其基本解題思路為:實驗目的→實驗原理→實驗方案的選擇→實驗藥品的選擇,實驗儀器的組裝→運用實驗知識和實驗技能處理相關細節問題。這類題將常見物質的性質實驗改編成實驗題,對我們平時的學習指出了新的要求,要改原來注重化學方程式的學習為實用性學習,要在平時的學習中養成對物質性質進行實驗探究的習慣。
三、以實驗結論為切入點
[例3](2010年新課標高考理綜化學試題·寧夏、吉林等五省卷)某同學在用稀硫酸與鋅制取氫氣的實驗中,發現加入少量硫酸銅溶液可加快氫氣的生成速率。請回答下列問題:
(1)上述實驗中發生反應的化學方程式有______;
(2)硫酸銅溶液可以加快氫氣生成速率的原因是_______;
(3)實驗室中現有 Na2SO4、MgSO4、Ag2SO4、K2SO4等4種溶液,可與上述實驗中CuSO4溶液起相似作用的是_______;
(4)要加快上述實驗中氣體產生的速率,還可采取的措施有_______(答兩種);
(5)為了進一步研究硫酸銅的量對氫氣生成速率的影響,該同學設計了如下一系列實驗。將表中所給的混合溶液分別加入到6個盛有過量Zn粒的反應瓶中,收集產生的氣體,記錄獲得相同體積的氣體所需時間。
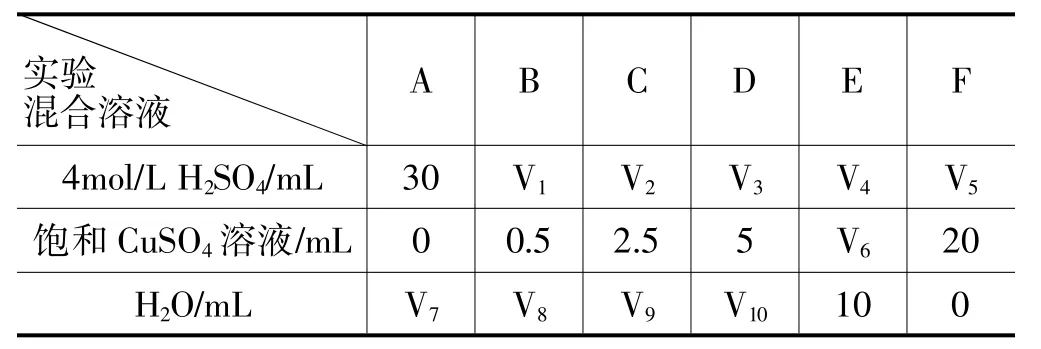
實驗混合溶液 A B C D E F 4mol/L H2SO4/mL 30 V1 V2 V3 V4 V5飽和CuSO4溶液/mL 0 0.5 2.5 5 V6 20 H2O/mL V7 V8 V9 V10 10 0
①請完成此實驗設計,其中:V1=_____,V6=_____,V9=_____。
②反應一段時間后,實驗A中的金屬呈色,實驗E中的金屬呈色。
③該同學最后得出的結論為:當加入少量CuSO4溶液時,生成氫氣的速率會大大提高。但當加入的CuSO4溶液超過一定量時,生成氫氣的速率反而會下降。請分析氫氣生成速率下降的主要原因__________。
【評析】本題為一道實驗基礎題,以原電池反應原理為載體,重點考查了原電池反應對化學反應速率的影響,具有一定的綜合性,主要考查的是學生的分析能力、數據處理能力和綜合理解能力。
第(1)~(4)問難度較小,第(5)問難度較大。而本題的亮點則是第(5)問實驗探究的設計,其中①中的V1、V6、V9數值的判斷,是對學生觀察能力、思維能力及實驗設計能力的綜合考查,學生只有通過觀察判斷,確定出只有保持H+濃度不變,才可以成功研究出CuSO4溶液的多少對反應速率的影響程度。②則是對學生是否在高中化學學習中經常進行實驗操作的真實再現,只有常做實驗的學生才有可能知道Zn與酸反應后期由于含雜質而顯灰黑色,E中置換出的Cu在后期也因雜質影響而顯暗紅色。③中則是考查表面積大小對速率的影響。
通過此題可看出,只有那些平常勤于動手實驗、善于動腦思考的學生,才有可能在新課程理念下的化學探究性實驗考核中取得優異的成績。同時新課程高考化學對我們今后的實驗教學及復習備考也提出了新的挑戰,只有真正地讓學生走進實驗室,手腦動起來,才有可能為國家培養出真正的化學人才。
四、以物質制備為切入點
[例4](2011年新課標高考理綜化學試題·全國卷)氫化鈣固體是登山運動員常用的能源提供劑。某興趣小組擬選用如下裝置制備氫化鈣。
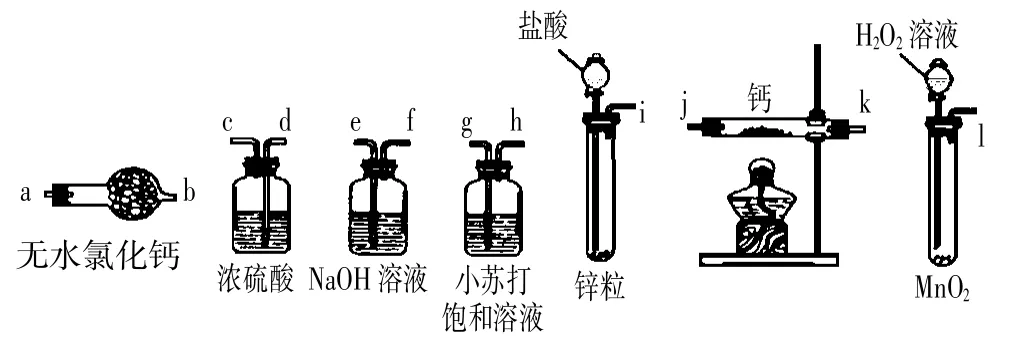
請回答下列問題:
(1)請選擇必要的裝置,按氣流方向連接順序為________(填儀器接口的字母編號)。
(2)根據完整的實驗裝置進行實驗,實驗步驟如下:檢查裝置氣密性后,裝入藥品;打開分液漏斗活塞;_________(請按正確的順序填入下列步驟的標號)。
A.加熱反應一段時間 B.收集氣體并檢驗其純度
C.關閉分液漏斗活塞 D.停止加熱,充分冷卻
(3)實驗結束后,某同學取少量產物,小心加入水中,觀察到有氣泡冒出,溶液中加入酚酞后顯紅色,該同學據此判斷,上述實驗確有CaH2生成。
①寫出CaH2與水反應的化學方程式_________。
②該同學的判斷不正確,原因是_____________。
(4)請你設計一個實驗,用化學方法區分鈣與氫化鈣,寫出實驗簡要步驟及觀察到的現象___________。
(5)登山運動員常用氫化鈣作為能源提供劑,與氫氣相比,其優點是________________。
【評析】本題開始以學生熟悉的裝置連接入手,而后命題一改以往考查模式,要求學生自選裝置及藥品、實驗儀器,設計實驗,用語言表述對實驗問題的理解,體現了實驗考查向實驗設計的轉型,這些改變正是新課程所倡導的。第(1)(2)問是設計裝置的選擇、設計實驗操作流程,反映學生對基本知識的理解過程。首先是從元素觀和變化觀出發,理解CaH2制取的反應原理,然后選擇氫氣的制取裝置,與主反應裝置,完成設計的主框架。接下來,按照“制氣→除雜→主反應→產品保護→尾氣處理”的常規方法選擇其他裝置及其次序,結合實驗設計的原則解決第(1)小問。第(2)問要求學生理解實驗操作的關鍵,從而選擇最佳的實驗操作程序,以便保證實驗成功安全的進行。第(3)(4)問巧妙地設問,意在引導學生不但能從原理上作出判斷,而且能從證據強弱的角度進行對比實驗的設計,從而既考查了實驗知識,還考查了實驗方法。最后的第(5)問是有關化學知識的應用,在規定了“與氫氣相比”的前提下,做出有理由的分析和判斷。
此題是一道常規題型,所不同的是課本之外的實驗,但是該題更加貼近生活,學生用課內所學過的知識就能夠解決這一問題,而且題目引入了猜想模式,這也是今后高考的一個方向,更加開放,更加貼近生活。

