活性炭基Li2SO4水系電解液超級電容器
孫現眾 張 熊 張大成 馬衍偉
(中國科學院電工研究所,北京100190)
活性炭基Li2SO4水系電解液超級電容器
孫現眾 張 熊 張大成 馬衍偉*
(中國科學院電工研究所,北京100190)
采用中性Li2SO4水溶液代替H2SO4和KOH作為電解液制備了活性炭(AC)基對稱型超級電容器,使水系超級電容器的工作電壓由1.0 V提高到了1.6 V.采用循環伏安和充放電測試研究了電容器的穩定電化學窗口.電化學充放電測試表明電容器在0.25 A·g-1電流密度下單電極比容量可達129 F·g-1,在功率密度為160 W· kg-1時能量密度達到10 Wh·kg-1(以正負極活性物質的總質量計).1.6 V恒壓充電1 h后電容器漏電流為0.22 mA.超級電容器的庫侖效率接近100%,充放電循環5000次后容量仍可保持在92%以上.研究了電解液的濃度對電容器電化學性能的影響,發現隨著Li2SO4濃度的增大電容器的電荷轉移電阻顯著減小,大電流充放電性能提高.活性炭基Li2SO4水系電解液超級電容器具有工作電壓高、能量密度高和對環境友好等優點,因此有很好的產業化前景.
超級電容器;活性炭;中性水系電解液;Li2SO4
1 引言
超級電容器也稱電化學電容器,是一種新型的儲能元件,兼有常規電容器的功率密度大和化學電源能量密度高的優點,可快速充放電,使用壽命長,既可以單獨使用作為主要的儲能器件,也可以與充電電池組成復合電源系統,在新能源發電、電動汽車、信息技術、航空航天和國防等領域都有廣闊的應用前景.1-4
超級電容器根據電解液的不同可分為有機體系和水溶液體系超級電容器,3,5前者電化學窗口較大(工作電壓2-4 V),但電解液價格比較昂貴,制作電容器時需要干燥的生產環境,工藝成本比較高;而水系電解液成本較低,電容器的生產工藝簡單,但電解液電化學窗口較小,工作電壓一般為1.0 V.根據公式E=1/2CU2可知,超級電容器的能量密度E與電容C成正比,與電壓U的平方成正比,因此要提高超級電容器的能量密度,可以從提高電極材料的比容量和超級電容器的工作電壓兩個方面入手.前者可以通過高比容量電極材料的制備和改性來提高材料的比容量和能量密度,6-13后者則可通過采用水系非對稱結構(如活性炭(AC)/MnO2,14,15AC/MoO3,16,17AC/Ni(OH)2,18AC/LiMn2O4,19WO3/VOx,20MnFe2O4/ LiMn2O421等)或者有機體系來提高電容器的電壓窗口.
活性炭基超級電容器的水系電解液通常采用H2SO4和KOH水溶液,而中性電解液如堿金屬硫酸鹽的水溶液則是用于非對稱超級電容器中.22,23Qu等24采用三電極體系研究了活性炭電極在中性的Li2SO4、Na2SO4、K2SO4水溶液中的電化學性能,發現在三種電解液中電極的容量和循環性能差別不大,而K2SO4水溶液中電極的大電流放電性能較好. Demarconnay等25從AC/MnO2非對稱型超級電容器的工作中得到啟發,首次將Na2SO4電解液應用于制備活性炭對稱型超級電容器,由于電極在中性電解液中的析氧/析氫過電位與在H2SO4和KOH水溶液中不同,從而可將水系超級電容器的工作電壓由1.0 V提高至1.6 V.由于Na2SO4在水中的溶解度較低,且隨溫度變化比較大(1.4 mol·L-1,20°C;0.35 mol·L-1,0°C),限制了其在低溫環境中的應用.為此,本文選擇了溶解度更高且低溫溶解度穩定的Li2SO4(3.2 mol·L-1,20°C;3.3 mol·L-1,0°C)作為超級電容器的電解質鹽,制備了電容器的器件,并研究了其電化學性能.
2 實驗
電容器的正負極活性物質均采用上海合達炭素材料有限公司生產的比表面積為2500 m2·g-1的活性炭,導電劑為上海榮仲實業有限公司提供的50%壓縮乙炔黑,粘結劑選用Aldrich公司提供的濃度為60%的聚四氟乙烯乳液,隔膜為深圳市比源電子有限公司提供的超級電容器用聚丙烯隔膜,電解液為采用廣東光華化學廠生產的分析純一水合硫酸鋰配制成的0.5-2.0 mol·L-1的Li2SO4水溶液(若無特別說明,濃度均為1.0 mol·L-1).超級電容器的制備方法為:先將活性炭、乙炔黑和聚四氟乙烯按70:20:10的質量比混合均勻,加入異丙醇攪拌成糊狀,加熱至60°C破乳,用手動軋機搟成薄膜壓覆在不銹鋼網上,放入真空干燥箱中在120°C下干燥8 h,沖制成直徑為14 mm的極片.將極片和隔膜放入扣式電池殼中,滴加電解液后封口組裝成扣式電容器.
在上海辰華公司CHI660c電化學工作站上對電容器進行了電化學阻抗、循環伏安等測試.電化學阻抗測試采用的交流信號振幅為5 mV,頻率范圍為0.01-100 kHz;循環伏安測試采用的掃描速率為5 mV·s-1,掃描的起始電壓為0 V,截止電壓為1.0-2.0 V.電容器的恒流充放電、循環性能和漏電流測試均采用了美國Arbin公司MSTAT 4電化學測試系統.漏電流的測試方法為先用恒流方法將電容器充電至1.6 V,然后用恒壓充電的方法充電1 h,恒壓充電過程中的電流即為漏電流.采用兩電極系統和三電極系統測試了在充電過程中電位變化的過程以及活性炭電極的循環伏安曲線,參比電極為飽和甘汞電極(SCE)并轉化為相對于標準氫電極的電位(vs NHE),三電極系統的對電極為鉑片.
3 結果與討論
圖1所示為不同截止電壓下電容器的循環伏安曲線,可以看到截止電壓在1.0-1.6 V范圍內循環伏安曲線都為近似對稱的矩形曲線,表明該電容器具備良好的電容特性.掃描過程中未出現明顯的氧化-還原峰,這說明電容器電荷的存儲是雙電層機制.隨著電容器的充電截止電壓增大2.0 V,正向電流顯著增加,在反向掃描過程中也出現了相應的電流增大部分,這表明電容器的正極和/或負極發生了氧化還原反應.
圖2所示為相應的不同截止電壓下的恒流充放電曲線,電流密度為0.25 A·g-1(以正負極活性物質的總質量計).可以看到,在較小的電壓窗口下充放電曲線表現為良好的線性特性和對稱性等雙電層電容的特征;隨著充電電壓大于1.8 V,充電曲線斜率逐漸增加而偏離了線性特性,這表明電極表面在發生雙電層電荷存儲的同時還發生了部分的電化學氧化還原反應.
為了研究超級電容器的充放電過程,我們利用兩電極系統在對電容器充電的同時還監測了正負極電位的變化,如圖3所示.在充電過程中電容器電壓從0 V增大到2.0 V,相應的,相對于NHE參比電極,正極電位從+0.29 V升高到+1.14 V,同時負極電位從+0.29 V降低到-0.86 V,據此,我們利用三電極系統測試了活性炭電極在-0.86-+1.14 V(vs NHE)范圍內的循環伏安曲線(圖4).從圖3中發現,在0-1.7 V的電壓范圍內電極的電位與電容器的電壓成線性關系,但是電壓超過1.7 V后正極電位開始出現電位平臺;由循環伏安曲線可以看到,正向掃描過程中當電極電位高于+1.1 V(對應于圖3所示1.7 V充電電壓下的正極電位)時響應電流顯著增大,這表明在正極發生了活性炭電極的氧化反應.在反向掃描過程中,當電極電位低于-0.65 V(對應于1.7 V充電電壓下的負極電位)時,響應電流迅速增大,表明發生了水的分解和在活性炭中氫的化學吸附,25,26這一過程可以表示為:H2O+e-→H+OH-和C+H?CHad,其中Had為活性炭的吸附氫.為此,為了提高電容器的庫侖效率,避免電極發生的不可逆氧化反應降低電容器的循環性能,我們選定Li2SO4體系電容器的穩定電化學窗口為0-1.6 V.

圖1 1.0-2.0 V截止電壓下電容器的循環伏安曲線Fig.1 Cyclic voltammograms of capacitor with cut-off voltages from 1.0 to 2.0 V
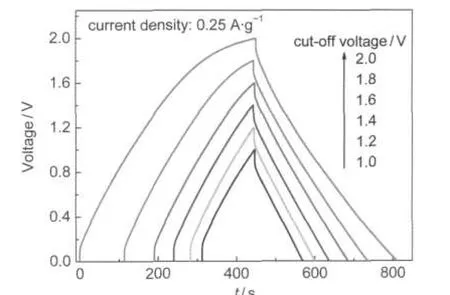
圖2 1.0-2.0 V截止電壓下電容器的恒流充放電曲線Fig.2 Galvanostatic charge/discharge curves of capacitor varied with cut-off voltages from 1.0 to 2.0 V
圖5所示為電容器的特征的最初三個循環的充放電曲線(0.25A·g-1).在第一個充放電循環,電荷效率較低,這可以歸結為活性炭材料表面含氧基團發生了不可逆的氧化反應.27經首次電化學活化后,電容器充放電過程的電荷效率大大提高,充放電曲線具有良好的三角形對稱性分布,電容器電壓隨充放電時間的變化呈線性關系.

圖3 充電過程中正、負極電位相對于電容器電壓的變化Fig.3 Potential plots of the positive and negative electrodes vs voltage during charging process

圖4 三電極體系活性炭電極在Li2SO4電解液中的循環伏安曲線Fig.4 Three-electrode cyclic voltammogramms of activated carbon electrode in Li2SO4electrolyte

圖5 電容器的恒流充放電曲線Fig.5 Galvanostatic charge/discharge curves of capacitor
圖6所示為不同濃度Li2SO4電解液的電容器電化學阻抗譜圖.電容器的阻抗譜由高頻區的半圓弧、中低頻區中傾角約為45°的斜線和低頻區與虛軸接近平行的直線等三部分組成.通常認為半圓弧主要對應于電解液和電極的本征阻抗和電荷轉移阻抗,半圓弧在實軸的截距為電容器的內阻Rs,其值包括溶液電阻、活性炭材料的電阻和電極片與集流體之間以及活性炭顆粒與導電劑之間的接觸電阻等;半圓弧的直徑為電荷轉移電阻Rct,代表在電極/電解液界面電荷轉移的動力學電阻或電解液和多孔電極的本征電荷轉移電阻.中低頻區的斜線對應于離子在固體顆粒內有限長度擴散的Warburg阻抗Zw.低頻區的直線部分代表了器件的電容特性,斜率越大表示越接近于理想電容.28從圖中可以看出,超級電容器的譜圖在低頻段趨近于與實軸垂直,對應于0.5-2.0 mol·L-1的Li2SO4電解液譜圖低頻段與實軸的夾角分別為84.5°、85.8°、86.0°和86.6°,表明活性炭電極趨于完全極化狀態,顯示了良好的電容特性,并且隨電解液濃度的增加電容特征更為顯著,同時Warburg阻抗減小.圖6插圖顯示,隨著電解液濃度的增加,阻抗譜半圓弧的直徑顯著減小,表明隨著電解質離子濃度的增加,電極的電荷轉移電阻Rct減小.

圖6 電容器的電化學阻抗譜圖和高頻區的放大圖(插圖)Fig.6 Nyquist plots of capacitors and enlarged high-frequency parts(inset)

圖7 采用不同濃度Li2SO4電解液的活性炭電極的比容量與放電電流密度關系曲線Fig.7 Relationship between the specific capacitance of AC electrode in Li2SO4electrolyte with different concentrations and discharging current density
根據公式C=4It/(MΔU)可以計算出電容器電極的比容量,其中,I為放電電流,t為放電時間,ΔU為充放電的電壓窗口,M為正、負極活性物質的總質量.25在0.25 A·g-1電流下電極比容量可達129 F·g-1,在低電流下電極比容量比較接近,但由于阻抗的差異,隨著放電電流的增加,低濃度電解液的電容器比容量下降較快,而采用高濃度電解液的電容器的比電容仍能保持較高的值(見圖7).根據公式P=ΔUI/2M和E=Pt可以計算出電容器的功率密度P和能量密度E,28由圖8所示的電容器的Ragone圖可以看出,電容器的能量密度可達10 Wh·kg-1,隨著放電倍率的增大,電容器放電比容量均有不同程度的降低,但總體而言,采用高濃度電解液的電容器由于阻抗較低其大電流性能更佳.

圖8 不同濃度Li2SO4電解液電容器的Ragone曲線Fig.8 Ragone plots of capacitors with different Li2SO4 electrolyte concentrations
電容器的漏電主要有以下三方面的原因:(1)由于極片或電解液中存在雜質而在電極表面形成微電化學電池;(2)由電勢差和電解質離子濃度梯度引起的雙電層電荷向溶液本體擴散;29(3)集流體和殼體由于毛刺等刺穿隔膜引起微短路.采用Li2SO4電解液制備的電容器漏電流很小,如圖9所示,電容器的漏電流在1.6 V恒壓充電條件下2 min內由2.2 mA迅速降低至0.5 mA以下,隨著恒壓時間的增加漏電流逐漸減小,10 min后基本趨于穩定,1 h之后漏電流降低至0.22 mA.

圖9 電容器的漏電流曲線Fig.9 Leakage current curve of capacitor
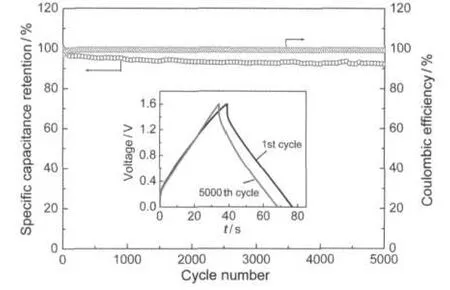
電容器比電容保持率和庫侖效率與循環次數的關系Evolution of the specific capacitance retention and coulombic efficiency versus the number of cyclesis the charge/discharge curves at current density of 1A·g-1.
圖10為電容器的充放電循環性能曲線,電流密度為1 A·g-1.電容100次循環后容量保持率降低96.6%,5000次循環后容量保持率緩慢降低至92.2%,比100次循環時僅衰減了4.4%;庫侖效率100次循環后由97.0%上升到99.3%,此后基本保持不變,這說明電容器具有良好的循環穩定性.由圖10插圖中還可以看到,5000次循環后充放電曲線的線性特征更加明顯,對稱性更好,而這一變化可歸因于活性炭表面的含氧基團發生的不可逆法拉第反應,27在經過多次充放電循環后,這部分含氧基團被消耗,從而表現出了完全的雙層電容性質.
4 結論
采用中性的Li2SO4水溶液電解液制備活性炭基對稱型超級電容器.采用不同截止電壓的循環伏安曲線和充放電曲線表明,電容器雖然可以在0-2.0 V范圍內充放電,但電壓超過1.7 V后正極的活性炭會發生顯著的氧化反應;電容器在1.6 V的電壓下循環充放電5000次都保持了較高的容量,這表明選擇1.6 V的工作電壓是合適的.電容器在0.25 A·g-1電流密度下單電極比容量可達129 F·g-1,在160 W· kg-1時電容器能量密度達到10 Wh·kg-1(以正負極活性物質的總質量計).電化學阻抗譜和充放電測試表明,電容器表現了良好的電容特性,且電容器的阻抗隨Li2SO4濃度的增大而減小,相應地大電流充放電性能提高.
(1) Miller,J.R.;Simon,P.Science 2008,321,651.
(2) Ji,Q.Q.;Guo,P.Z.;Zhao,X.S.Acta Phys.-Chim.Sin.2010, 26,1254.[季倩倩,郭培志,趙修松.物理化學學報,2010,26, 1254.]
(3) Zhu,Y.;Murali,S.;Stoller,M.D.;Ganesh,K.J.;Cai,W.; Ferreira,P.J.;Pirkle,A.;Wallace,R.M.;Cychosz,K.A.; Thommes,M.;Su,D.;Stach,E.A.;Ruoff,R.S.Science 2011, 332,1537.
(4) Simon,P.;Gogotsi,Y.Nat.Mater.2008,7,845.
(5) Chen,Y.;Zhang,X.;Yu,P.;Ma,Y.W.J.Power Sources 2010, 195,3031.
(6)Chen,Y.;Zhang,X.;Zhang,D.C.;Yu,P.;Ma,Y.W.Carbon 2011,49,573.
(7)Zhang,D.C.;Zhang,X.;Chen,Y.;Yu,P.;Wang,C.H.;Ma,Y. W.J.Power Sources 2011,196,5990.
(8)Yu,L.Q.;Chen,S.L.;Chang,S.;Li,Y.H.;Gao,Y.Y.;Wang, G.L.;Cao,D.X.Acta Phys.-Chim.Sin.2011,27,615.[于麗秋,陳書禮,常 莎,李云虎,高胤義,王貴領,曹殿學.物理化學學報,2011,27,615.]
(9) Wang,H.;Gao,Q.;Jiang,L.Small 2011,7,2454.
(10) Lu,X.H.;Zheng,D.Z.;Zhai,T.;Liu,Z.Q.;Huang,Y.Y.;Xie, S.L.;Tong,Y.X.Energ.Environ.Sci.2011,4,2915.
(11) Xu,B.;Zhang,H.;Cao,G.P.;Zhang,W.F.;Yang,Y.S.Prog. Chem.2011,23,605.[徐 斌,張 浩,曹高萍,張文峰,楊裕生.化學進展,2011,23,605.]
(12) Xu,B.;Yue,S.F.;Sui,Z.Y.;Zhang,X.T.;Hou,S.S.;Cao,G. P.;Yang,Y.S.Energ.Environ.Sci.2011,4,2826.
(13) Lin,P.;She,Q.J.;Hong,B.L.;Liu,X.J.;Shi,Y.N.;Shi,Z.; Zheng,M.S.;Dong,Q.F.J.Electrochem.Soc.2010,157,A818.
(14) Deng,L.;Zhu,G.;Wang,J.;Kang,L.;Liu,Z.H.;Yang,Z.; Wang,Z.J.Power Sources doi:10.1016/j.jpowsour.2011.09.005.
(15) Li,W.C.;Gao,P.C.;Lu,A.H.J.Power Sources 2011,196, 4095.
(16) Brezesinski,T.;Wang,J.;Tolbert,S.H.;Dunn,B.Nat.Mater. 2010,9,146.
(17)Tang,W.;Liu,L.;Tian,S.;Li,L.;Yue,Y.;Wu,Y.;Zhu,K. Chem.Commun.2011,47,10058.
(18) Hu,G.X.;Li,C.X.;Gong,H.J.Power Sources 2010,195, 6977.
(19)Wen,Z.B.;Tian,S.;Qu,Q.T.;Wu,Y.P.Prog.Chem.2011,23, 589.[溫祖標,田 舒,曲群婷,吳宇平.化學進展,2011,23, 589.]
(20)Li,J.M.;Chang,K.H.;Hu,C.C.Electrochem.Commun.2010, 12,1800.
(21) Lin,Y.P.;Wu,N.L.J.Power Sources 2011,196,851.
(22) Mosqueda,H.A.;Crosnier,O.;Athou?l,L.;Dandeville,Y.; Scudeller,Y.;Guillemet,P.;Schleich,D.M.;Brousse,T. Electrochim.Acta 2010,55,7479.
(23) Zhang,X.;Yang,W.S.;Ma,Y.W.Electrochem.Solid.St.2009, 12,A95.
(24) Qu,Q.T.;Wang,B.;Yang,L.C.;Shi,Y.;Tian,S.;Wu,Y.P. Electrochem.Commun.2008,10,1652.
(25) Demarconnay,L.;Raymundo-Pin~ero,E.;Béguin,F. Electrochem.Commun.2010,12,1275.
(26) Béguin,F.;Jurewicz,K.;Frackowiak,E.Appl.Phys.A 2004,78, 981.
(27)Khomenko,V.;Raymundo-Pin~ero,E.;Béguin,F.J.Power Sources 2010,195,4234.
(28) Xu,C.;Du,H.;Li,B.;Kang,F.;Zeng,Y.J.Electrochem.Soc. 2009,156,A435.
(29) Li,J.;Lai,Y.Q.;Jin,X.D.;Peng,R.F.;Liu,Y.X.Chinese Battery Industry 2010,15,131. [李 晶,賴延清,金旭東,彭汝芳,劉業翔.電池工業,2010,15,131.]
October 11,2011;Revised:December 7,2011;Published on Web:December 13,2011.
Activated Carbon-Based Supercapacitors Using Li2SO4Aqueous Electrolyte
SUN Xian-Zhong ZHANG Xiong ZHANG Da-Cheng MA Yan-Wei*
(Institute of Electrical Engineering,Chinese Academy of Sciences,Beijing 100190,P.R.China)
In this work,we prepared activated carbon-based symmetric supercapacitors using Li2SO4aqueous electrolyte instead of H2SO4and KOH,and obtained devices with an improved working voltage of 1.6 V from 1.0 V.Cyclic voltammetry and galvanostatic charging/discharging measurements were used to study the electrochemical properties.The results showed that the electrode specific capacitance can reach 129 F·g-1,and the energy density can be as high as 10 Wh·kg-1at a power density of 160 Wh·kg-1. Electrochemical impedance analysis measurements showed that the charge-transfer resistance of the capacitors decreased markedly with the increase of the concentration of Li2SO4,and the rate capability improved accordingly.The leakage current of the supercapacitor was 0.22 mA after constant-voltage charging at 1.6 V for 1 h,and the columbic efficiency was nearly 100%.The capacitance of the supercapacitor remained above 90%after 5000 charge-discharge cycles.Activated carbon-based supercapacitors using Li2SO4aqueous electrolyte have many advantages,such as high working voltage,high energy density,and environmental compatibility,and therefore have good industrialization prospects.
Supercapacitor;Activated carbon;Neutral aqueous electrolyte;Li2SO4
10.3866/PKU.WHXB201112131
*Corresponding author.Email:ywma@mail.iee.ac.cn;Tel:+86-10-82547129;Fax:+86-10-82547137.
The project was supported by the Knowledge Innovation Program of the ChineseAcademy of Sciences(KJCX2-YW-W26),Science and
Technology Project of Beijing,China(Z111100056011007),and National Natural Science Foundation of China(21001103,51025726).
中國科學院知識創新工程重要方向項目(KJCX2-YW-W26),北京市科技計劃項目(Z111100056011007)和國家自然科學基金(21001103, 51025726)資助
O646

