酸堿平衡體系基于Excel的直觀計算
王業根
鹽城衛生職業技術學院,江蘇鹽城 224005
酸堿平衡體系的計算一般有代數法、圖解法、計算機法。代數法是基礎,其他兩種方法是工具[1]。代數法的關鍵是推導前與推導中表達式的簡化,不恰當的簡化容易引起較大的誤差。圖解法需要準備多種圖形模板,準確度不高,對于復雜體系無能為力。計算機法可以達到較高的準確度,但必須選擇簡便、直觀的軟件[2]。
基于Excel工作表與宏,建立包含公式的酸堿平衡體系模板,計算滴定過程中的酸度變化,繪制滴定曲線,判斷滴定突躍,整個過程簡便直觀。該方法可修改參數,求解未知量(如酸度、物料濃度與體積、酸常數、緩沖容量等),同時由于沒有計算公式的簡化,計算結果更為準確。
1 原理
1.1 共軛酸生成常數
酸堿常數是酸堿平衡體系計算的理論基礎。為了與滴定常數表達一致,建議統一改用共軛酸生成常數(質子化常數)。以三元弱酸為例。
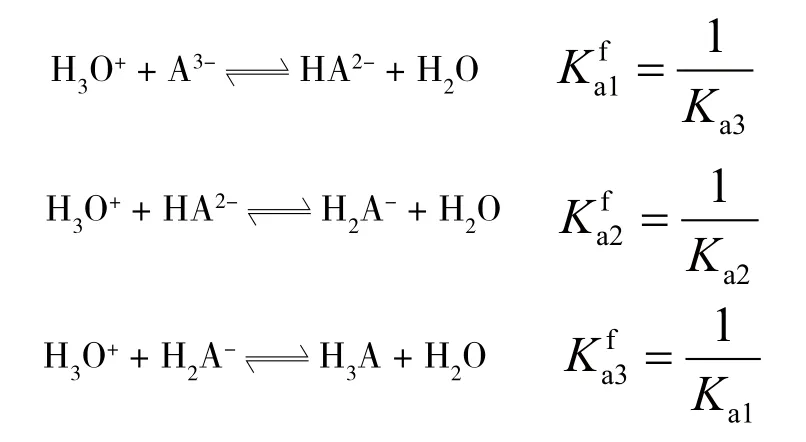
1.2 型體平衡濃度
多種溶液混合時,溶液總體積增大,物料分析濃度應通過稀釋公式計算。型體平衡濃度與物料分析濃度和型體濃度分數(分布系數)有關,型體濃度分數則取決于共軛酸生成常數與酸度。以三元弱酸為例。
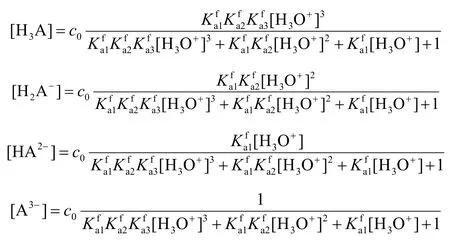
1.3 質子平衡方程
酸堿反應的本質是質子傳遞,酸堿平衡體系中得到質子的物質的量應該等于失去質子的物質的量。選擇所投物料為零水準,建立質子平衡方程。以NaOH滴定H3PO4、HAc混合酸為例,選擇H2O、H3PO4、HAc、NaOH為參考水準,質子平衡方程為:
[H3O+]+c0(NaOH)=[OH?]+[H2PO4?]+2[HPO42?]+3[PO43?]+[Ac?]
NaOH中的OH-是水溶液中的最強堿,全部得到質子生成H2O,在質子平衡方程中用c0(NaOH)表示。
1.4 滴定過程分析
隨著滴定劑的不斷滴入,溶液總體積不斷增加,物料分析濃度不斷變化,用迭代法計算滴定過程中的酸度變化,繪制滴定曲線,判斷滴定突躍。
1.5 求解未知變量
可變更多個已知條件,如共軛酸生成常數、物料投放濃度與體積、酸度等,以得失質子的物質的量相等為目標,求解未知變量。
1.6 計算緩沖容量
在溶液中加入微量強酸或強堿,計算酸度變化,相應得到溶液的緩沖容量。
2 方法
2.1 Excel工作表的構造
在Excel工作表B2∶M9區域預留條件設置單元格(如圖1,不包括圖中數據,下同)。在Excel工作表B10∶M18區域預留平衡體系計算單元格(如圖2)。在Excel工作表B35∶M1137區域預留滴定過程計算單元格(如圖3)。在Excel工作表I22∶M32區域預留滴定突躍范圍計算單元格,根據滴定劑目標體積百分數與pH繪制滴定曲線(無數據點平滑線XY散點圖),如圖4。建立用于存放常見物料參數的“參數表”工作表。
2.2 Excel宏的構建
在Excel界面,執行菜單“工具-宏-Visual Basic編輯器”。在VBA編輯器,執行菜單“插入-模塊”,輸入宏代碼。關閉VBA編輯器,回到Excel界面,創建三個超鏈接(平衡體系計算、酸度計算、緩沖容量計算)并指向相應的宏,保存Excel工作簿。
3 應用
以0.1mol/L的NaOH滴定10mL 0.1mol/L的H3PO4與10mL 0.1mol/L的HAc混合酸為例。打開已建立的Excel文件,單擊“平衡體系計算”,依次輸入(1)被測溶液中各種物料的化學式、投放濃度與體積(H3PO4、0.1、10、HAc、0.1、10);(2)滴定劑中各種物料的化學式與投放濃度(NaOH、0.1);(3)H2O的投放體積(0);(4)滴定劑目標體積(40);(5)滴定過程中型體平衡濃度取值公式(H3PO4、F14、H2PO4-、F15、HPO42-、F16、PO43-、F17、HAc、G14、Ac-、G15、H3O+、E13、OH-、E15);(6)滴定突躍控制誤差(0.5,百分號不輸入);(7)化學計量點時滴定劑體積(10、20、30,系統建議的體積可能稍有偏差)。
3.1 滴定過程數據解讀
3.1.1 滴定開始前[H3O+]≈[H2PO4-]≈1.6×10-2mol/L,體系的酸度主要由H3PO4的一級解離所決定,H3PO4一級解離出的H3O+抑制了HAc的解離,[Ac-]≈5.5×10-5mol/L,見圖3。
3.1.2 滴定過程中 pH↑,[H3PO4]↓,[H2PO4-]先↑后↓,[HPO42-]先↑后↓,[PO43-]↑,[HAc]↓,[Ac-]先↑后↓,[OH-]↑,型體平衡濃度的變化既與酸度有關,又受到溶液總體積的影響,見圖3。
3.1.3 pH變化 分別有三個突躍,第一個突躍為NaOH與H3PO4生成NaH2PO4,第二個突躍為NaOH與HAc生成NaAc,第三個突躍為NaOH與NaH2PO4生成Na2HPO4。只有第三個突躍pH=9.26~10.09,|△pH|=0.83,可選用酚酞指示劑進行滴定,見圖4。
3.2 求解未知變量
3.2.1 改變條件,重新計算酸度 例如,將NaOH溶液體積改為30.00mL,單擊“酸度計算”,溶液的pH為9.67。
3.2.2 設定酸度,計算滴定誤差 例如,將pH改為10.00,執行“工具-單變量求解”,使比值為1,NaOH溶液體積為30.06mL,滴定終點誤差為+0.2%。
3.2.3 改變條件,計算緩沖容量 例如,將NaOH溶液體積改為25.00mL,單擊“緩沖容量計算”,溶液的緩沖容量為0.013。
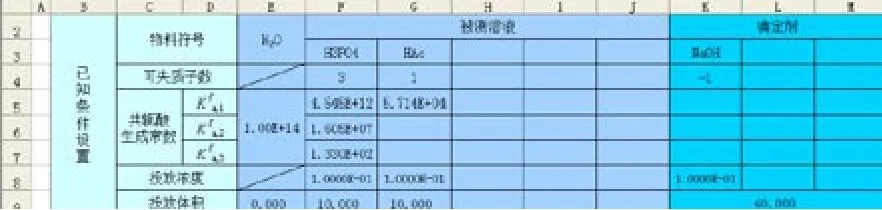
圖1 已知條件設置

圖2 平衡體系計算
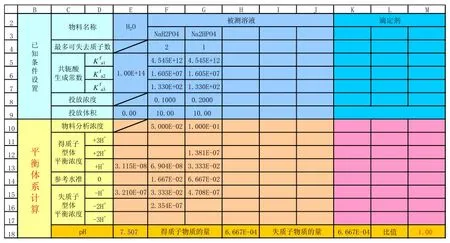
圖5 nNaH2PO4-Na2HPO4混合溶液中型體平衡濃度的取值
4 討論
4.1 關于共軛酸生成常數
共軛酸堿常數數值上與電離常數一致。將電離常數統一改成共軛酸生成常數,有時顯得不太習慣。本系統已設置好常見共軛酸生成常數,對于新的物料只需要輸入共軛酸的電離常數,系統將自動轉換成共軛酸生成常數,并增補進參數表,便于日后再次使用。
4.2 關于最多可失去質子數p
對于一、二、三元強酸(或弱酸),p分別為1、2、3。對于一、二、三元強堿,p分別為-1、-2、-3。對于弱堿,p為0。對于兩性離子,如HCO3-、HPO42-、H2PO4-,p分別為1、1、2。
4.3 關于存在多個共軛體系的物料
以20mL 0.10mol/L的(NH4)2CO3溶液為例,該溶液中除H2O外,還存在著NH4+/NH3、H2CO3/HCO3-/CO32-兩個共軛體系,可作為10mL 0.40mol/L NH4+與10mL 0.20mol/L CO32-兩種物料輸入,計算結果pH=9.18。
4.4 關于滴定劑
如滴定劑由多種物料組成,滴定過程中,各物料將共用體積項。如滴定劑目標體積設置過小,可能觀察不到某些滴定突躍,此時應適當增加滴定劑目標體積。
4.5 關于共軛體系
如果有多種物料屬于同一個共軛體系,則需要注意型體平衡濃度的加和。以NaH2PO4與Na2HPO4混合溶液為例(見圖5),各型體平衡濃度取值公式如下:
H3PO4H2PO4-HPO42-PO43-
F13+G12 F14+G13 F15+G14 F16+G15。
[1]孟凡昌,蔣勉.分析化學中的離子平衡[M].北京:科學出版社,1997:8-10.
[2]趙鑫,王殿書,叢培盛,等.pH精算及酸堿滴定曲線繪制通用軟件的開發[J].計算機與應用化學,2010,27(2):257-261.

