6-羥基山萘酚-3-O-β-葡萄糖苷抑制脫氧核糖氧化損傷的機理
王媛凱,支 鵬,張立偉,*
(1.山西大學分子科學研究所,山西 太原 030006;2.天津大學藥物科學與技術學院,天津 300072)
6-羥基山萘酚-3-O-β-葡萄糖苷抑制脫氧核糖氧化損傷的機理
王媛凱1,支 鵬2,張立偉1,*
(1.山西大學分子科學研究所,山西 太原 030006;2.天津大學藥物科學與技術學院,天津 300072)
目的:研究6-羥基山萘酚-3-O-β-葡萄糖苷(6-HK-3-O-G)抑制Fenton反應和對羥自由基清除的能力,并對其抑制Fenton反應的機理進行初步探討。方法:利用脫氧核糖氧化損傷的實驗檢測模型和DPPH自由基的清除實驗。結果:6-HK-3-O-G對羥自由基具有較強的清除能力;對Fenton反應引起的2-脫氧核糖氧化損傷具有保護作用,其保護作用機理與6-HK-3-O-G直接對Fenton反應所產生的羥自由基的清除作用有關,但更主要的可能是由于6-HK-3-O-G與Fe2+的絡合作用,阻斷了Fenton反應的進行。結論:6-HK-3-O-G具有強的抗氧化活性,在生理條件下,6-HK-3-O-G與Fe2+的絡合作用可能是其抑制Fenton反應的關鍵因素。
6-羥基山萘酚-3-O-β-葡萄糖苷(6-HK-3-O-G);Fenton反應;2-脫氧核糖;DPPH自由基
羥自由基是氧自由基中最活潑、毒性最強的一種,可使細胞發生氧化損傷而引發多種疾病。Fenton 反應是體內產生羥自由基的主要機理之一,也是引起細胞損傷而導致心腦血管、老年性癡呆等疾病的重要因素之一[1-4]。生物體內普遍存在的VC 、Fe2+、Cu2+,可使細胞在有氧代謝過程中發生Fenton反應而產生羥自由基[5]。而紅花為傳統用于治療心腦血管疾病的常用中藥,其所含的紅花黃色素是紅花的主要藥效部位,具有抗氧化[6-7]、保護心肌[8]等作用。6-羥基山萘酚-3-O-β-葡萄糖苷(6-HK-3-O-G)是紅花黃色素的主要活性成分之一[9],目前有關6-HK-3-O-G抗氧化和抗氧化機理的研究尚未見報道。本實驗利用Fenton反應所造成的脫氧核糖氧化損傷模型和DPPH自由 基的清除實驗,研究6-HK-3-O-G抑制Fenton反應的能力和對羥自由基的清除能力,并對其抑制Fenton反應的機理進行初步探討,旨在為紅花的藥理作用機制提供科學依據。
1 材料與方法
1.1 材料與試劑
2-硫代巴比妥酸(TBA) 上海國藥集團化學試劑有限公司;2-脫氧核糖 上海生物科技有限公司;6-HK-3-O-G(純度≥95%) 本研究室自制[10];抗壞血酸、H2O2(30%) 天津基準化學試劑有限公司;三氯乙酸(TCA) 天津市天力試劑有限公司;乙二胺四乙酸二鈉(EDTA)北京化工廠;1,1-二苯基-2-三硝基苯肼(DPPH)上海索萊寶生物技術有限公司;硫酸亞鐵銨 天津市恒興化學試劑制造有限公司。
1.2 儀器與設備
Agilent 1200型高效液相色譜儀 美國安捷倫公司;色譜柱Venusil XBP-C18(4.6mm×250mm,5μm) 天津博納艾杰爾科技有限公司;Cary-50Bio型紫外-可見分光光度計 美國Varian公司。
1.3 方法
1.3.1 2-脫氧核糖氧化損傷能力測定
6-HK-3-O-G對2-脫氧核糖氧化損傷保護作用實驗按文獻[11]方法、步驟進行。在10mL試管中依次加入10mmol/L磷酸鹽緩沖液7.5mL(pH7.2,二次蒸餾水配制),0.3mL Fe2+(用0.1mol/L鹽酸配制),0.3mL 6-HK-3-O-G(用甲醇配制)或EDTA(二次蒸餾水配制),濃度為0.2mmol/L的2-脫氧核糖和抗壞血酸(二次蒸餾水配制)各0.3mL,再加入2mmol/L的H2O20.3mL啟動反應,各實驗組均在37℃條件下孵育10min,然后再加入0.5mL 質量濃度為10g/100mL 的TCA終止反應,最后加入0.5mL 1g/100mL的TBA(用40mmol/L NaOH配制),并置80℃加熱15min,用冰水迅速冷卻后測波長532nm處吸光度。蒸餾水代替藥物作為對照組,蒸餾水代替2-脫氧核糖作為空白。6-HK-3-O-G對2-脫氧核糖氧化損傷的抑制率用式(1)計算。
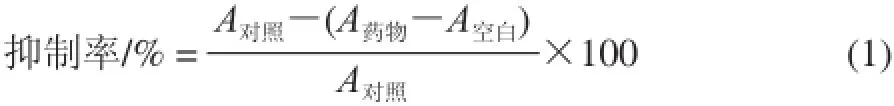
1.3.2 DPPH自 由 基 清除能力測定
在5mL試管中依次加入0.3mL 1.0mmol/L的DPPH無水乙醇溶液、2.4mL無水乙醇和0.3mL 2mmol/L 6-HK-3-O-G(或0.3mL 2mmol/L 6-HK-3-O-G與Fe2+的混合溶液),迅速混合后放置30min,然后在波長524nm處測定吸光度。
1.3.3 紫外-可見光譜測定
在10mL試管中加入9.7mL KBP緩沖液(20mmol/L,pH7.2,二次蒸餾水配制)和0.3mL濃度為0.5mmol/L的6-HK-3-O-G,混合均勻,取2.5mL至石英杯中,然后每隔2min滴加5μL Fe2+溶液(濃度為10mmol/L,用0.1mol/L鹽酸配制)一次,迅速混合均勻,測定吸光度(直至吸收光譜沒明顯變化為止)。
1.3.4 HPLC測定
在10mL試管中加入9.7mL KBP緩沖液(20mmol/L,pH7.2,二次蒸餾水配制)和0.3mL濃度為0.5mmol/L的6-HK-3-O-G(用甲醇配制),混合均勻。取2.5mL溶液作為待測液1;另取2.5mL溶液加入10μL Fe2+溶液(濃度為10mmol/L,用0.1mol/L鹽酸配制),混合均勻,作為待測液2。待測液靜置5min后,測定HPLC譜。色譜測定條件為:Venusil XBP-C18(4.6mm×250mm,5μm)色譜柱,以CH3OH(A)和H2O(0.2mol/L NaClO4-0.2‰HClO4)(B)為流動相,梯度洗脫,t=0時,V(A):V(B)=26:74;t=120min時,V(A):V(B)=35:65,流速1mL/min,柱溫25℃,檢測波長350nm,進樣量20μL。
2 結果與分析
2.1 6-HK-3-O-G對2-脫氧核糖氧化損傷的保護作用
6-HK-3-O-G對2-脫氧核糖氧化損傷的保護作用可用Fenton反應所致的2-脫氧核糖氧化損傷實驗進行評估。
O-G對2-脫氧核糖氧化損傷的抑制率Fig.1 Inhibitory rate of 6-HK-3-圖1 6-HK-3-O-G on oxidative damage to 2-deoxyribose
羥自由基可氧化損傷2-脫氧核糖生成產物丙二醛,TBA與丙二醛反應可生成在波長532nm處有吸收的發色基團。因此,當體系產生的羥自由基越多,2-脫氧核糖的損傷就會越嚴重,532nm波長處的吸光度就會越大[12]。若6-HK-3-O-G對體系的羥自由基具有清除作用或可阻斷Fenton 反應產生羥自由基,那么就會抑制Fenton反應對2-脫氧核糖的氧化損傷,體系在532nm波長處的吸光度就會減小。由圖1可見,當6-HK-3-O-G濃度在0~40μmol/L范圍內時,隨著濃度的增加6-HK-3-O-G對2-脫氧核糖氧化損傷的抑制率增強,當濃度達到40μmol/L時,抑制率可達93%。6-HK-3-O-G在低濃度時(0~40μmol/L)對2-脫氧核糖氧化損傷的抑制率的線性回歸方程為(圖1):y=0.0993x+0.1117。由方程可知,6-HK-3-O-G的IC50為3.91μmol/L(抑制2-脫氧核糖氧化損傷達到50%時所需濃度),說明6-HK-3-O-G對由Fenton反應引起的2-脫氧核糖氧化損傷具有較強的保護作用。6-HK-3-O-G的保護作用的機理可能有兩個方面,其一可能是6-HK-3-O-G對體系產生的羥自由基具有直接清除作用[13],第二可能是由于6-HK-3-O-G阻斷了Fenton 反應,使產生的羥自由基濃度降低[14]。
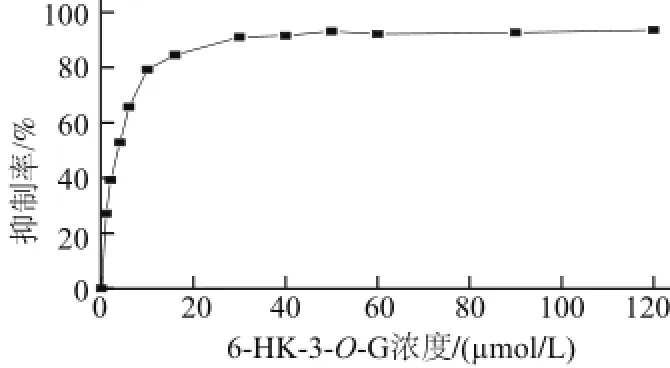
2.2 6-HK-3-O-G與Fe2+絡合前后對羥自由基的清除能力DPPH是用于羥自由基清除劑篩選的理想模型[15-16],清除劑對DPPH自由基清除能力的大小,體現了對羥自由基清除能力的大小[17-18]。一般認為有效的酚類DPPH清除劑的清除能力主要來源于游離酚羥基,清除劑所含游離酚羥基數量多則對DPPH自由基清除的能力強。由圖2可知,游離的6-HK-3-O-G對DPPH自由基具有清除作用,而6-HK-3-O-G與Fe2+混合物的清除能力降低。6-HK-3-O-G與Fe2+混合物對DPPH自由基的清除能力降低的原因可能是由于6-HK-3-O-G與Fe2+形成了絡合物,導致6-HK-3-O-G結構中游離酚羥基數量減少,因而清除能力降低。
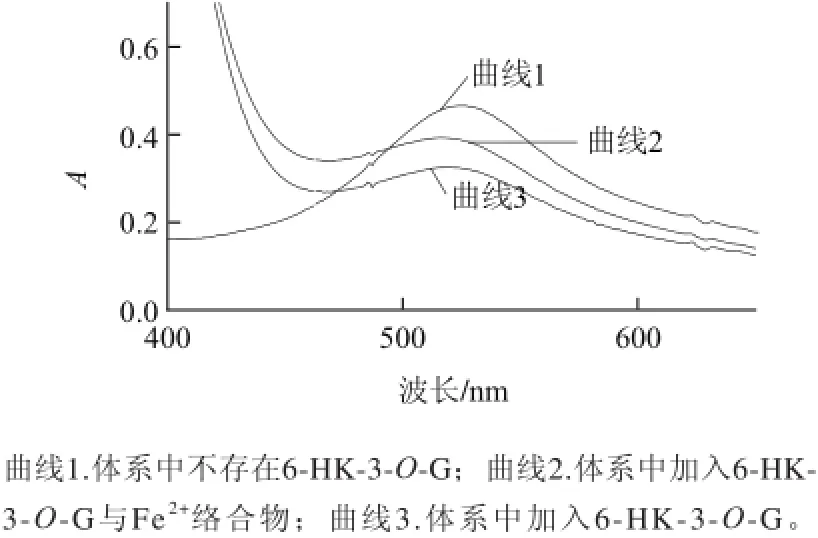
圖2 6-HK-3-O-G與Fe2+絡合前后對DPPH自由基清除能力的比較Fig.2 DPPH radical scavenging capacity of 6-HK-3-O-G and 6-HK-3-O-G-Fe2+complex
2.3 6-HK-3-O-G與Fe2+絡合的紫外光譜測定
圖3 6-HK-3-O-G與Fe2+絡合的紫外光譜滴定曲線Fig.3 UV titration curve of 6-HK-3-O-G and Fe2+(Inset shows the chelation curve of 6-HK-3-O-G with Fe2+)
紫外吸收光譜常用于判斷有機化合物與金屬離子形成配合物與否,一般具有紫外吸收的有機分子與金屬離子形成配合物后,可引起有機分子紫外吸收光譜的變化,如吸收峰的位移、吸收峰強度變化、代表新物種產生的等吸收點的出現等[19]。Fe2+的滴定6-HK-3-O-G的紫外吸收光譜變化情況如圖3所示,6-HK-3-O-G在波長220、270、363nm觀察到3個吸收帶,一般歸因于共軛3環系統π-π電子躍遷,隨著Fe2+的加入,6-HK-3-O-G在波長220nm和270nm為中心的的吸收峰強度增加,在波長357nm和415nm間區域的吸光強度減少,在波長415nm以后的吸收峰增加,吸收峰在波長360nm處的吸收峰藍移,波長357nm和415nm處出現兩個等吸收點,表明有6-HK-3-O G-Fe2+絡合物的形成。6-HK-3-O-G與Fe2+結合的光譜變化可能歸結為與Fe2+絡合后,共軛環系統π電子的進一步離域所至。滴定曲線(圖3內部圖)表明6-HK-3-O-GFe2+絡合物物質的量比為2:1。通過分析在波長357nm與415nm之間的峰值的光譜變化獲得了同樣的化學計量數。
2.4 HPLC測定6-HK-3-O-G與6-HK-3-O-G-Fe2+絡合物
在HPLC色譜分析中,可以根據色譜峰的保留時間的差異區分不同的物種,色譜保留時間不同可以認為是不同的化合物。6-HK-3-O-G與Fe2+混合前后的色譜(圖4)顯示,6-HK-3-O-G的保留時間為31.812min,6-HK-3-O-G與Fe2+混合后色譜保留時間提前為30.469min。結果說明6-HK-3-O-G與Fe2+形成新的化合物,即6-HK-3-O-G與Fe2+形成了絡合物,該結果與紫外吸收光譜分析結果一致。
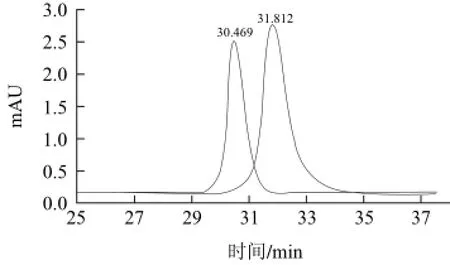
圖4 6-HK-3-O-G與6-HK-3-O-G-Fe2+的色譜圖Fig.4 Chromatogram of 6-HK-3-O-G and 6-HK-3-O-G-Fe2+complex
2.5 6-HK-3-O-G阻斷Fenton反應機制
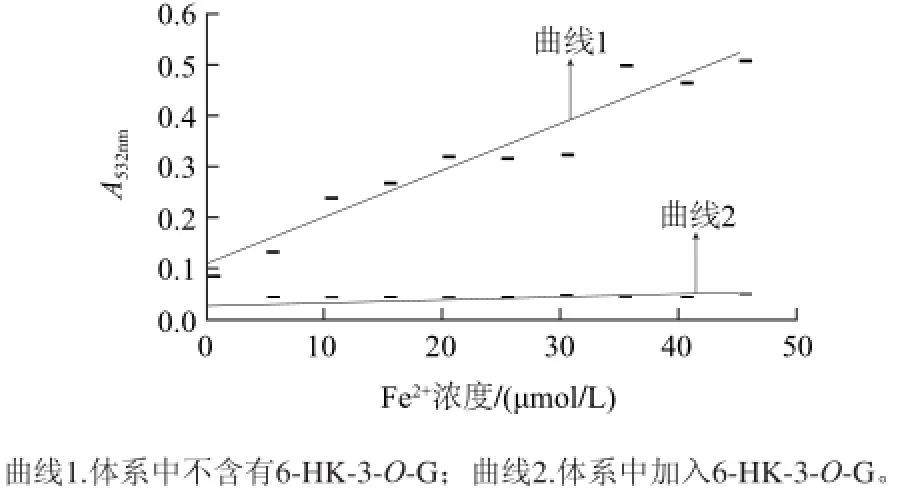
圖5 脫氧核糖的氧化損傷與Fe2+濃度的關系Fig.5 Relationship of oxidative damage to deoxyribose with various concentrations of Fe2+
由Fenton反應過程可知,2-脫氧核糖的氧化損傷主要來源于Fenton 反應產生的羥自由基。實驗1.3.1節和1.3.2節結果表明,6-HK-3-O-G可以抑制Fenton反應對2-脫氧核糖的氧化損傷,并對羥自由基具有清除作用。依據Fenton反應機理推測6-HK-3-O-G對2-脫氧核糖氧化損傷的保護作用的機理可能有兩個方面,其一可能是6-HK-3-O-G對體系產生的羥自由基具有直接清除作用,第二可能是由于6-HK-3-O-G阻斷了Fenton反應,使產生的羥自由基濃度降低。
為了進一步闡明6-HK-3-O-G的作用機理,比較了6-HK-3-O-G存在(6-HK-3-O-G與Fe2+先混合孵育,然后再加入測定體系)或不存在情況下,2-脫氧核糖的氧化損傷與Fe2+濃度變化的關系。圖5顯示,6-HK3-O-G不存在時,隨著Fe2+濃度增加氧化損傷程度增加,相反,當6-HK-3-O-G與Fe2+預先混合孵育,然后再加入測定體系時, Fe2+的濃度達到很高時2-脫氧核糖損傷都能被有效抑制。該結果說明,6-HK-3-O-G可通過與Fe2+形成絡合物進而阻斷Fenton反應。
由于6-HK-3-O-G本身具有直接清除羥自由基的能力,為了進一步確定6-HK-3-O-G抑制Fenton反應的氧化損傷機理,又進行圖6所示實驗[20]。圖6實驗結果表明,當體系中僅有Fe2+的強絡合劑EDTA存在時,2-脫氧核糖的氧化損傷不能被有效抑制(圖6,曲線1),說明體系中仍然有羥自由基的生成;當體系中既有Fe2+的強絡合劑EDTA,又有6-HK-3-O-G存在時,2-脫氧核糖氧化氧化損傷降低了75%(圖6,曲線2),該結果主要是由于6-HK-3-O-G對羥自由基的清除,因為EDTA對Fe2+的絡合能力較6-HK-3-O-G強,所以,體系中不能有效形成6-HK-3-O-G-Fe2+絡合物;當體系中存在6-HK-3-O-G,而不存在EDTA時,2-脫氧核糖的氧化損傷抑制率在90%以上(圖6,曲線3),該結果證明6-HK-3-O-G在抑制Fenton反應對2-脫氧核糖氧化損傷過程中,6對Fe2+絡合起著關鍵作用。
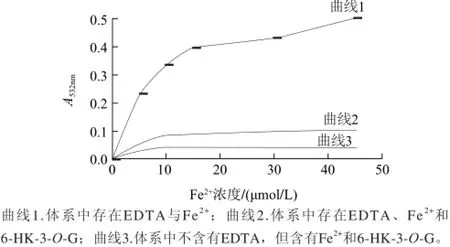
圖6 EDTA對6-HK-3-O-G阻止2-脫氧核糖氧化損傷能力的影響Fig.6 Influence of EDTA on the protective effect of 6-HK-3-O-G against oxidative damage to deoxyribose
3 結 論
紅花主要活性成分6-HK-3-O-G具有較強的清除羥自由基能力,可以抑制由Fenton反應引起的2-脫氧核糖氧化損傷作用,并且,在其抑制Fenton反應過程中,6-HK-3-O-G對Fe2+絡合起著關鍵作用;紅花所體現的抗氧化、保護心肌等藥理活性作用,可能與其主要活性成分6-HK-3-O-G的抗氧化作用有關。
[1] PARAVICINI T M, TOUYZ R M. NADPH oxidase, reactive oxygen species, and hypertension clinical implications and therapeutic possibilities[J]. Diabetes Care, 2008, 31(2): 170-180.
[2] 方允中, 楊勝, 伍國耀. 自由基、抗氧化劑、營養素與健康的關系[J]. 營養學報, 2003, 25(4): 337-343.
[3] 李勇, 孔令青, 高洪, 等. 自由基與疾病研究進展[J]. 動物醫學進展, 2008, 29(4): 85-88.
[4] 張玉錦, 洪小茜. 活性氧與心血管疾病關系的研究[J]. 醫學綜述, 2002, 8(4): 212-213.
[5] SUTTON H C, WINTERBOURN C C. On the participation of higher oxidation states of iron and copper in Fenton reactions[J]. Free Rad Biol Med, 1989, 6(1): 53-60.
[6] 金鳴, 李金榮, 吳偉. 紅花黃色素抗氧化作用的研究[J]. 中國中藥雜志, 2004, 29(5): 447-449.
[7] 李中原, 涂秀華. 紅花黃色素的藥理研究進展[J]. 中藥新藥與臨床藥理, 2005, 16(2): 153-156.
[8] 王天, 傅風華, 韓冰, 等. 羥基紅花黃色素A對實驗性心肌梗死大鼠的保護作用及機制[J]. 中草藥, 2007, 38(12): 1853-1856.
[9] 蘭藝鳳, 周璐, 張立偉. HPLC法同時測定紅花中的5種黃酮成分[J].食品科學, 2011, 32(12): 283-286.
[10] KAZUMA K, TAKAHASHI T, SATO K, et al. Quinochalones and flavonoids from fresh florets in different cultivars of Carthamus tinctorius L. [J]. Biosci Biotechnol Biochem, 2000, 64(8): 1588-1599.
[11] GUO Maolin, PEREZ C A, WEI Yibin, et al. Iron-binding properties of plant phenolics and cranberry’s bio-effects[J]. Dalton Transactions, 2007, 36(43): 4951-4961.
[12] 王愛國, 羅廣華. 羥自由基啟動下的脫氧核糖脫氧核糖降解及其產物的TBA反應[J]. 生物化學與生物物理進展, 1993, 20(2): 150-152.
[13] OGATA M, HOSHI M, SHIMOTOHNO K, et al. Antioxidant activity of magnolol honokiol, and related phenolic compounds[J]. J Am Oil Chem Soc, 1997, 74(5): 557-562.
[14] KHOKHAR S, RICHARD K O A. Iron-binding characteristics of phenolic compounds: some tentative structure-activity relations[J]. J Am Oil Chem Soc, 1997, 74(5): 557-562.
[15] 許申鴻, 杭瑚. 一種篩選自由基清除劑的簡便方法[J]. 中草藥, 2000, 31(2): 96-97.
[16] KONO Y, KASHINE S, YONEYAMA T, et al. Iron chelation by chlorogenic acid as a natural antioxidant[J]. Biosci Biotechnol Biochem, 1998, 62(1): 22-27.
[17] 彭長連, 陳少薇, 林植芳, 等. 用清除有機自由基DPPH 法評價植物抗氧化能力[J]. 生物化學與生物物理進展, 2000, 27(6): 658-661.
[18] YOKOZAW A T, DONG E, NATAGAW A T, et al. in vitro and in vivo studies on the radical scavenging activity of tea[J]. J Agric Food Chem, 1998, 46(6): 2143-2150.
[19] 劉鶯, 白燕, 朱添祥, 等. 紫外分光光度法測定Cu (Ⅱ)與含硒氨基酸絡合物的組成[J]. 光譜實驗室, 2005, 22(2): 426-427.
[20] PEREZ C A, WEI Yibin, GUO Maolin. Iron-binding and anti-Fenton properties of baicalein and baicalin[J]. Journal of Inorganic Biochemistry, 2008, 103(3): 326-332.
Mechanism Underlying Protective Effect of 6-Hydroxykaempferol-3-O-β-glucoside Deoxyribose against Oxidative Damage to Deoxyribose
WANG Yuan-kai1,ZHI Peng2,ZHANG Li-wei1,*
(1. Institute of Molecular Science, Shanxi University, Taiyuan 030006, China;2. School of Pharmaceutical Science and Technology, Tianjin University, Tianjin 300072, China)
Objective∶ To evaluate the capability of 6-hydroxykaempferol-3-O-β-glucoside (6-HK-3-O-G) for inhibiting Fenton reaction and scavenging hydroxyl free radicals, and to explore the inhibitory mechanism on Fenton reaction. Methods∶ A model to test oxidative damage to deoxyribose and a reaction system to test DPPH free radical scavenging activity were created. Results∶ 6-HK-3-O-G not only had strong scavenging activity against hydroxyl free radical, but also could protect 2-deoxyribose against oxidative damage caused by Fenton reaction. The underlying mechanisms were related to the direct scavenging of hydroxyl free radical generated from Fenton reaction but seemed to be mainly due to the chelation of 6-HK-3-O-G with Fe2+, thereby blocking Fenton reaction. Conclusion∶ 6-HK-3-O-G has strong anti-oxidation activity, and the chelation of 6-HK-3-O-G with Fe2+may play a vital role for its inhibiting Fenton chemistry under physiological conditions.
6-hydroxykaempferol-3-O-β-glucoside (6-HK-3-O-G);fenton reaction;2-deoxyribose;DPPH free radical
R286.75
A
1002-6630(2013)03-0029-04
2011-12-08
科技部“十二五”重大新藥創制科技重大專項(2011ZX09201-201-06);山西省回國留學人員科研資助項目(2009003)
王媛凱(1985—),女,碩士研究生,研究方向為天然產物。E-mail:2005290045@email. sxu.cn
*通信作者:張立偉(1963—),男,教授,博士,研究方向為天然產物。E-mail:lwzhang@sxu.edu.cn

