愈喘至圣膏微生物限度檢查法驗證
南京中醫藥大學泰州附屬醫院(225300)王威
愈喘至圣膏為醫院制劑,是肺腎雙補劑,其處方由28味中藥組成[黨參150g、熟地150g、陳皮100g、蘇子100g、沙參100g、黃芪300g、麻黃100g、法半夏100g、白芥子100g、大貝母100g、白術100g、茯苓150g、胡桃肉150g、紫河車150g、五味子50g、干姜40g、百部100g、款冬花100g、紫苑100g、黃精150g、蛤蚧一對、當歸100g、桃仁100g、杏仁100g、白果150g、紅棗150g、生姜100g、淮山藥150g],適用于肺腎兩虛,腎不納氣,痰濁蘊肺,肺氣上逆癥。癥見:長期慢性咳喘,痰涎清稀,氣短乏力,動輒尤甚,體虛自汗,易于感冒,形寒畏冷,腰膝酸軟,甚則心悸胸悶,難以平臥,雙下肢水腫,面色晄白,舌淡脈細等。通常認為愈喘至圣膏為中藥補劑,應無抗菌作用,無須進行微生物限度檢查方法驗證,直接采用常規法檢查即可。本文通過愈喘至圣膏微生物限度檢查方法系統的方法驗證實驗,說明補藥制劑其微生物限度檢查方法同樣需要驗證。
1 材料和方法
1.1 材料
1.1.1 樣品 愈喘至圣膏:膏劑,規格為2.8kg/付(泰州市中醫院批號:121014,121121,121209)。
1.1.2 試驗菌株 金黃色葡萄球菌(Staphylococcus aureus)[CMCC(B)26 003]、枯草芽孢桿菌(Bacillus subtilis)[CMCC(B)63 501]、大腸埃希菌(Escherichia coli)[CMCC(F)44 102]、白色念珠菌(Candida albicans)[CMCC(F)98 001] 、黑曲霉(Aspergillus ni-ger)[CMCC(F)98003]。
1.1.3 培養基 膽鹽乳糖增菌液(批號:120407)、玫瑰紅鈉瓊脂(批號:120105)、營養瓊脂(批號:110704)、營養肉湯(批號:070410)、改良馬丁(批號:070201)、改良馬丁瓊脂(批號:061225)。
1.1.4 儀器 試管,吸管,培養皿,0.45μm微孔濾膜,可重復使用的微孔過濾器,真空抽泵,濾瓶。
1.2 方法
1.2.1 菌液制備[1]①取經37℃培養18~24h的金黃色葡萄球菌、大腸埃希菌、枯草芽孢桿菌的營養肉湯培養物1ml,用0.9%無菌氯化鈉溶液10倍稀釋至10-5~10-7,使成50~100CFU/ml,經活菌計數后備用。②取經25℃~28℃培養18~24h的白色念珠菌的改良馬丁培養物1ml,用0.9%無菌氯化溶液10倍稀釋至10-5~10-6,使成50~100CFU/ml,經活菌計數后備用。③取經25℃~28℃培養1周的黑曲霉的改良馬丁瓊脂斜面培養物,用0.9%無菌氯化鈉溶液5ml洗下黑曲霉孢子,吸出孢子懸液1ml,加0.9%無菌氯化鈉溶液適量稀釋至與標準比濁管濁度相當的孢子懸液,取此孢子懸液1ml,用0.9%無菌氯化鈉溶液10倍稀釋到10-4,使成50~100CFU/ml,經活菌計數后備用。
1.2.2 供試液制備 稱取樣品10g,加45℃pH7.0無菌氯化鈉-蛋白胨緩沖液100ml,混勻,得1∶10供試液 。
1.2.3 培養基稀釋法 取供試液1ml/皿(1∶200稀釋),0.5ml/皿(1∶400稀釋),0.2ml/皿(1∶1000稀釋),分別與50~100CFU/ml的試驗菌注皿,然后每皿加營養瓊脂培養基15~20ml,搖勻,待凝固后,置規定溫度培養24~72h,逐日觀察結果。
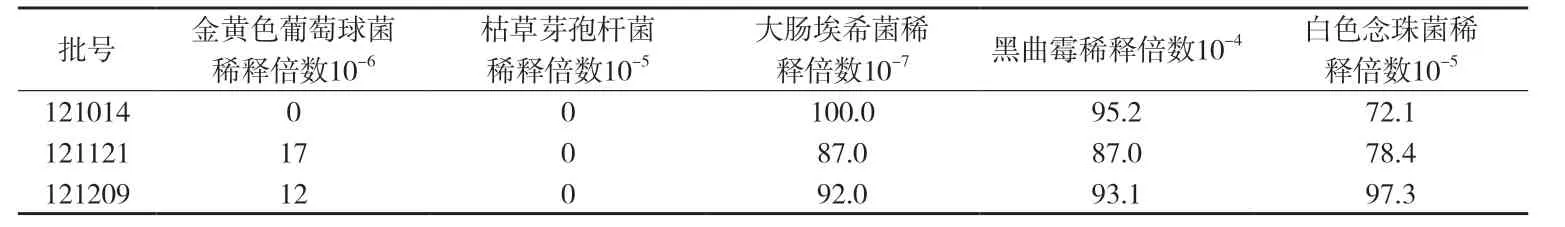
附表1 培養基稀釋法(1∶200)的回收率試驗結果(%)
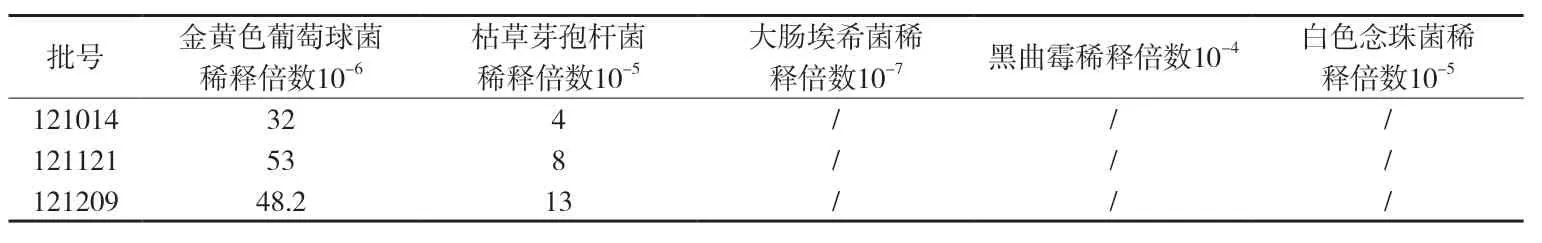
附表2 培養基稀釋法(1∶400)的回收率試驗結果(%)
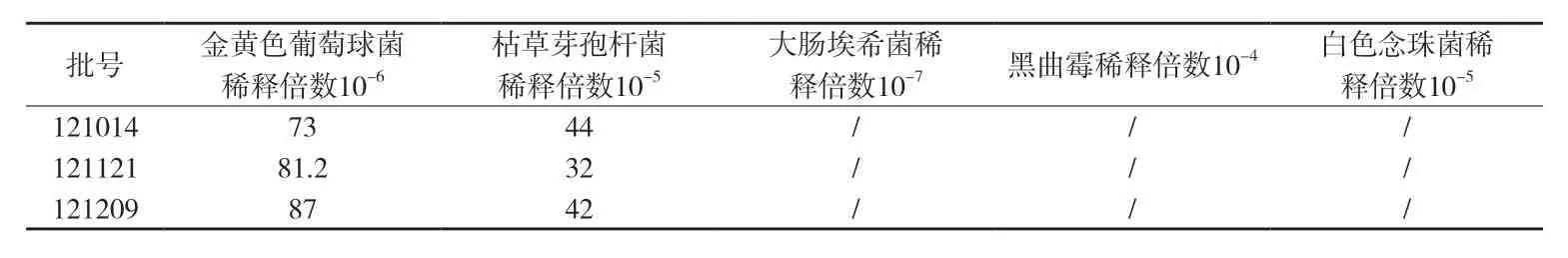
附表3 培養基稀釋法(1∶1000)的回收率試驗結果(%)

附表4 薄膜過濾法的回收率試驗結果(%)
1.2.4 薄膜過濾法[1]取靜置片刻的供試液1ml,注入薄膜過濾器,加沖洗液每次50~100ml,沖洗3次,在最后一次沖洗液中加入50~100CFU/皿的枯草芽孢桿菌、金黃色葡萄球菌。濾干,取濾膜貼于相應瓊脂平板上,置規定溫度培養24~72h,逐日觀察結果。
2 結果
細菌培養48h,逐日點計菌落數,以48h的菌落數報告;霉菌培養72h,逐日點計菌落數,以72h的菌落數報告[2][3]。菌回收率的計算[4]

常規法測定醫院制劑愈喘至圣膏的回收率:用稀釋法測定愈喘至圣膏的3個批次回收率見附表1~3。
附表1結果顯示,供試品對金黃色葡萄球菌、枯草芽孢桿菌的生長有一定抑制作用,回收率為0~45%,均低于70%,故應加大培養基稀釋級進行測定。
附表2結果顯示,采用培養基稀釋法(0.5ml/皿,1∶400),供試品對金黃色葡萄球菌、枯草芽孢桿菌的生長仍有一定抑制作用,回收率為0~62.5%,均低于70%,故應加大培養基稀釋級進行測定。
附表3結果顯示,采用培養基稀釋法1∶1000,供試品對枯草芽孢桿菌回收率仍低于70%,故應進一步采用薄膜過濾法測定,結果見附表4。
附表4結果顯示,采用薄膜過濾法供試品對金黃色葡萄球菌、枯草芽孢桿菌的生長回收率均高于70%,試驗細菌正常生長。
3 討論
中成藥的微生物檢查是保證藥品質量及安全性重要的質控指標。《中國藥典》2005年版增加了對藥品進行微生物限度檢查時,應通過微生物限度檢查方法學驗證的實驗規定,以確保該品種檢驗方法的準確性,對提高藥品質量有著重要意義 。
現有許多關于有抑菌作用的中成藥、制劑微生物限度檢查方法驗證的試驗報道,但對滋補中藥制劑的微生物限度檢查方法驗證實驗的情況尚無報道。有人認為,滋補中藥制劑沒有抑菌活性,無須進行方法學驗證。筆者通過對3個批次愈喘至圣膏的方法驗證研究發現,該制劑品種對金黃色葡萄球菌和枯草芽孢桿菌有一定的抑菌作用,對白色念珠菌、黑曲霉則無抑菌作用。
愈喘至圣膏處方中某些藥材炮制后可產生抑菌作用,如黃芪等。根據方法驗證實驗情況,在沒有確切檢查方法的時候愈喘至圣膏微生物限度細菌數檢查建議采用薄膜過濾法進行測定較為穩妥。
總之,通過對3批愈喘至圣膏的驗證試驗,可得出以下結論:①愈喘至圣膏的細菌、霉菌和酵母菌計數方法學驗證結果,不僅表明藥典規定方法學驗證的必要性,而且方法學驗證的數據對評價藥品質量提供了科學的依據;②本品進行細菌、霉菌和酵母菌計數方法驗證時,預實驗選用金黃色葡萄球菌和枯草芽孢桿菌即可快速確定本品的微生物限度檢查方法;③中藥滋補劑不可簡單作為不做驗證試驗的依據。

