心力衰竭家兔心室動作電位時程整復性變化對室性心律失常的影響
陳世健, 魏妮娜, 李 艷
(湖北民族學院附屬民大醫院心內科,湖北 恩施 445000)
心力衰竭家兔心室動作電位時程整復性變化對室性心律失常的影響
陳世健△, 魏妮娜, 李 艷
(湖北民族學院附屬民大醫院心內科,湖北 恩施 445000)
目的探討壓力負荷誘導的兔慢性心力衰竭(CHF)模型離體心室動作電位時程整復性(APDR)變化對室性心律失常(VA)的影響。方法雄性新西蘭大耳兔20只,隨機分為對照(CTL)組和CHF組,每組10只。CHF模型制備采用經腹主動脈縮窄術,造模結束4周后行心臟超聲檢查評價造模結果。在整體心臟Langendorff灌流條件下行離體電生理研究,分別記錄和測量心室不同位點的單相動作電位(MAP)及有效不應期(ERP),并繪制APDR曲線;對2組心臟進行快速電刺激,觀察室性心律失常(VA)的誘發。結果與CTL組相比,CHF組心室相同部位90%單相動作電位時程(MAPD90)、ERP及APDR曲線最大斜率(Smax)均明顯增大(均P<0.01),且VA更容易誘發(均P<0.05);此外,CHF組動物APDR曲線Smax的變異系數(COV-Smax)均較CTL組增大(均P<0.05)。結論CHF時心室APDR曲線Smax及COV-Smax均增大,促進室性心律失常的發生。
慢性心力衰竭; 動作電位時程; 整復性; 室性心律失常
慢性心力衰竭(chronic heart failure, CHF)是多種心臟器質性疾病發生發展的終末階段,包括了心臟結構重構及電重構,后者又可導致惡性室性心律失常的發生,進而增加患者心源性猝死的發生率。因此,探討CHF時室性心律失常(ventricular arrhythmia,VA)發生機制對于改善CHF患者預后具有重大意義。近年來動作電位時程整復性(action potential duration restitution, APDR)這一動態變化因素被提出,并認為其與VA發生及維持密切相關[1-2]。本實驗應用壓力負荷誘導的CHF模型,在整體心臟Langendorff灌流條件下,運用相關電生理技術探討CHF時APDR變化對VA的影響。
材 料 和 方 法
1動物模型制備與分組
實驗用新西蘭大耳兔20只,均為雄性,體重2.0~3.0 kg,由武漢大學醫學部實驗動物中心提供。將動物隨機分為2組:對照組(control, CTL組,n=10)和慢性心力衰竭組(CHF組,n=10)。CHF組動物經耳緣靜脈注射異丙腎上腺素(Sigma)(300 μg·kg-1·d-1),CTL組動物經3%戊巴比妥鈉溶液麻醉后,采用腹主動脈縮窄術制作心臟壓力負荷模型,對照組開腹不接扎。術后14 d,自由進食給水[3-4]。
2心臟超聲檢查
完成制備CHF模型4周后,對所有動物行超聲心動圖檢查。通過M型超聲獲得舒張期室間隔厚度(interventricular septal thickness in diastole,IVSd)及左室后壁厚度(left ventricular posterior wall thickness in diastole, LVPWd);在心尖四腔心切面測量左室舒張末期內徑(left ventricular end-diastolic diameter, LVEDD)及左室收縮末期內徑(left ventricular end-systolic diameter,LVESD);根據改良的Simpon公式計算出左室射血分數(left ventricular ejection fraction,LVEF)及左室短軸縮短率(left ventricular fractional shortening, LVFS)。
3離體電生理研究
以3%戊巴比妥鈉溶液(北京化學試劑公司;30 mg/kg)行耳緣靜脈注射全身麻醉,隨后繼續經耳緣靜脈注射肝素鈉2 000 U抗凝,10 min后迅速開胸取出心臟,置于100%氧飽和的4 ℃生理鹽水中剪去心包以及周圍結締組織,洗凈殘血,連接于Langendorff心臟灌流裝置經主動脈逆行灌流Tyrode’s液,灌流速度20~25 mL/min。
3.1記錄各部位單相動作電位(monophasic action potential, MAP)和有效不應期(effective refractory period, ERP) 將刺激電極置于右室基底部心外膜行基礎周長為300 ms的S1S1刺激(脈寬2 ms、刺激強度為舒張期起搏閾值的2倍),分別記錄左室前壁基底部(left anterior basal, LAB)、左室前壁心尖部(left anterior apex, LAA)、左室后壁基底部(left posterior basal, LPB)和左室后壁心尖部(left posterior apex, LPA)4個部位的MAP。并在連續發放8個起搏刺激波S1后發放早搏刺激波S2(S1S1=300 ms,S1S2=280 ms,刺激強度為舒張期起搏閾值的2倍),以10 ms反掃,記錄ERP。
3.2構建APDR曲線 測量不同S1S2間期程序化刺激過程中S2誘發動作電位的MAPD90及每個S2刺激前的舒張間期(diastolic interval, DI; S2前一個S1誘發的動作電位終點到S2誘發的動作電位起點的時間間隔)。應用Origin 6.0軟件以DI為橫坐標、S2的MAPD90為縱坐標,代入sigmoid函數公式:MAPD90=y0+A1(1-e-DI/T1)進行APDR曲線構建;計算APDR曲線最大曲線斜率(Smax):將sigmoid函數求得的A1、T1及最小DI值代入曲線斜率公式:slope=(A1/T1)*[Exp(-DI/T1)]得出APDR曲線Smax。APDR曲線Smax的變異系數(coefficient of variation of Smax,COV-Smax)定義為6個標測部位Smax標準差與均數的比值,用以評價APDR在整個心室分布的不均一性。
3.3VA的誘發 Burst刺激誘發:將刺激電極分別置于右室基底部(right basal, RB)、右室心尖部(right apex,RA)、左室基底部(left basal, LB)和左室心尖部(left apex, LA),給予50 Hz持續時間2 s的Train刺激進行VA的誘發,各個部位總刺激時間小于3 min。VA持續時間超過2 s即記為VA可誘發,超過30 s即記為持續性VA[6]。
4統計學處理
計量資料用均數±標準差(mean±SD)表示,組間比較采用兩樣本均數比較的t檢驗,以P<0.05為差異有統計學意義。應用SPSS 18.0軟件處理。
結 果
1造模結束4周后2組動物心臟超聲結果
與CTL組相比,CHF組動物LVEF和LVFS明顯降低(均P<0.01),IVSd和LVPWd減小(均P<0.05),LVEDD和LVESD明顯增大(均P<0.01),表明CHF模型制備成功,見表1。

表1 2組家兔心臟超聲檢查結果
**P<0.01vscontrol (CTL).
22組動物各部位ERR和MAPD90結果
與CTL組相比,CHF組動物心室相同部位EPR和MAPD90均增大(均P<0.05),見表2。
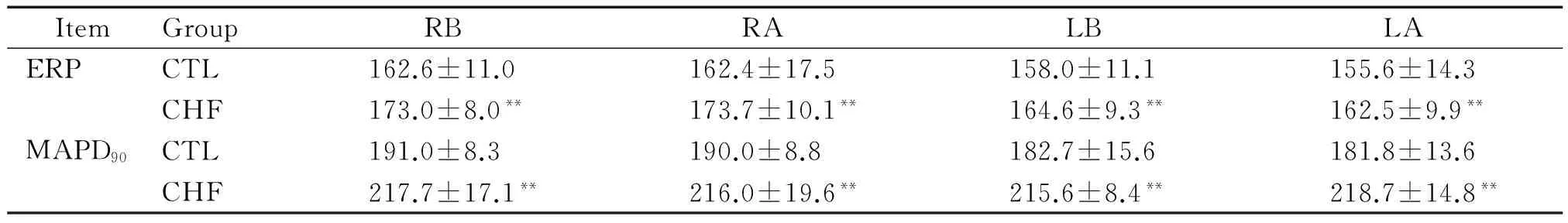
表2 2組家兔心室有效不應期和90%單相動作電位時程的變化
RB:right basal; RA: right apex; LB: left basal; LA: left apex.**P<0.01vscontrol (CTL).
32組動物各部位APDR結果
與CTL組相比,CHF組動物心室相同部位APDR曲線Smax及整個左室COV-Smax(0.38±0.05vs0.26±0.03)均增大(均P<0.01),見表3。
表32組APDR曲線最大斜率的變化
Table 3. The maximal slope of APDR curves between CTL and CHF groups (Mean±SD.n=10)
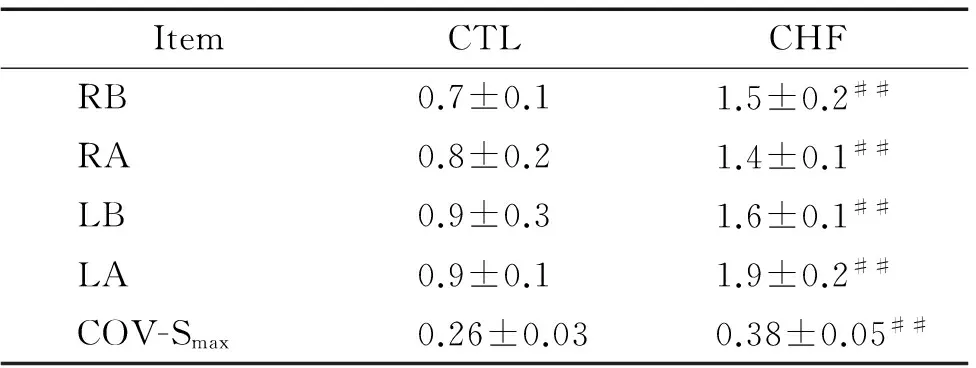
ItemCTLCHFRB0.7±0.11.5±0.2##RA0.8±0.21.4±0.1##LB0.9±0.31.6±0.1##LA0.9±0.11.9±0.2##COV-Smax0.26±0.030.38±0.05##
RB: right basal; RA: right apex; LB: left basal; LA: left apex.##P<0.01vsCTL.
4室性快速心律失常誘發率
在Burst刺激誘發下,CHF組動物心室各部位心律失常誘發率明顯高于對照組,且還出現了持續性心律失常,其中又以左室心尖部最為多見,見表4。
表42組家兔室性心律失常誘發率的變化
Table 4. The induction rate of ventricular arrhythmia between CTL and CHF groups (n=10)
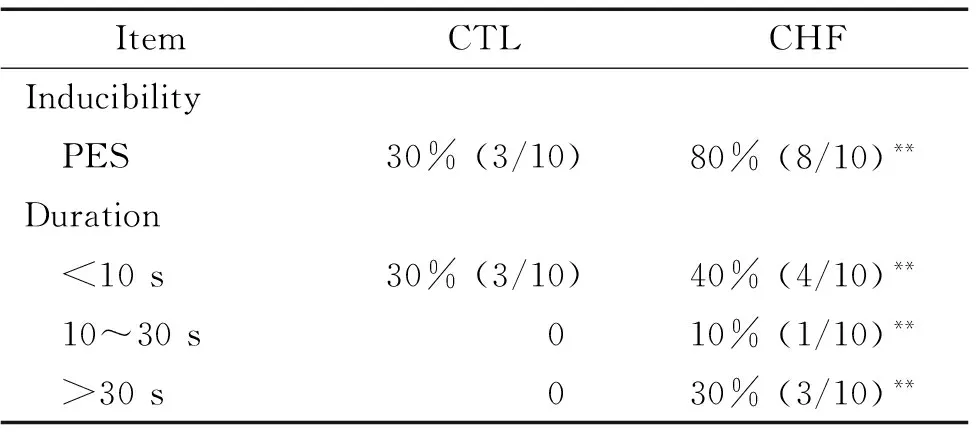
ItemCTLCHFInducibility PES30%(3/10)80%(8/10)**Duration <10s30%(3/10)40%(4/10)** 10~30s010%(1/10)** >30s030%(3/10)**
PES: programmed electrical stimulation.**P<0.01vsCTL.
討 論
在心衰發展中,伴隨著心肌組織學上肥厚性重構變化,心肌細胞的電生理特性亦發生重構性改變,主要表現為復極化過程延遲而致動作電位時程(action potential duration,APD)延長,體表心電圖上相應改變為 QT 間期延長[3-4]。至今,對心衰時 APD 延長如何誘發心律失常產生的機制仍了解不多,故揭示疾病過程中電生理重構與心律失常發生的關系是當今心血管領域研究的熱點課題。本研究也發現CHF組動物心室各部位MAPD90及ERP均較對照組相同部位明顯延長,并且多位點均呈現相同的變化趨勢。同時觀察到CHF組各標測部位APD整復性曲線斜率均較對照組相同部位明顯增大。既往研究表明APDR曲線Smax與心肌細胞電穩定性有關:即當Smax>1時,DI輕微變化即可引起APD和ERP的較大波動,這種波動可以增加相鄰部位APD復極的功能性差異有利于折返的形成,心臟就容易發生VA;而當Smax<1時,APD和ERP的波動消失,心臟則不易發生VA。Smax僅能局限地反映心臟單個標測部位的APDR,而心室不同部位心肌細胞的APDR卻存在區域性差異[5-6],且APDR的這種區域性差異增大對VA發生具有重要作用,由此可見僅僅依靠Smax是否大于1來解釋VA的發生和維持是不夠的。因此,我們也對心室不同部位的COV-Smax進行了比較,并發現CHF組COV-Smax顯著大于對照組。這也進一步解釋了CHF組心律失常發生率增加的原因。
[1] Qin M, Liu T, Hu H, et al. Effect of isoprenaline chronic stimulation on APD restitution and ventricular arrhythmogenesis[J]. J Cardiol,2013,61(2):162-168.
[2] Qin M, Huang H, Wang T, et al. Absence of Rgs5 prolongs cardiac repolarization and predisposes to ventricular tachyarrhythmia in mice[J]. J Mol Cell Cardiol,2012,53(6):880-890.
[3] 李 兵,陳香健,朱舒舒,等.培哚普利對慢性心力衰竭大鼠心肌能量代謝及超微結構的影響[J].中華急診醫學雜志,2011,20(9):955-959.
[4] 劉 韜,秦 牧,黃從新,等. 激活蛋白激酶C對離體兔心室電整復性及室性心律失常的影響[J].中華心血管病雜志2012,40(9):780-785.
[5] Weiss JN, Qu Z, Chen PS, et a1.The dynamics of cardiac fibrillation[J].Circulation, 2005, 112(8): 1232-1240.
[6] 秦 牧,劉 韜, 于勝波, 等. 蛋白激酶C的空間不均一性分布與室性心律失常發生的關系[J]. 中華心律失常學雜志,2013,17(3):219-223.
Effectsofactionpotentialdurationrestitutiononventriculararrhythmiainchronicheartfailurerabbithearts
CHEN Shi-jian, WEI Ni-na, LI Yan
(DepartmentofCardiovascularMedicine,MinDaHospitalAffiliatedtoHubeiUniversityforNationalities,Enshi445000,China.E-mail:chenshijianyun@163.com)
AIM: To determine the effects of action potential duration restitution (APDR) on ventricular arrhythmia (VA) in Langendorff-perfused chronic heart failure (CHF) rabbit hearts.METHODSTwenty male New Zea-land rabbits were equally divided into 2 groups randomly: control (CTL) group and CHF group. CHF was induced by abdominal aortic banding for 14 d. The echocardiography was applied to assess the cardiac function and structural change in both groups 4 weeks after the end of modeling. In the whole Langendorff-perfused hearts, the monophasic action potential (MAP) and the effective refractory period (ERP) were recorded and measured in ventricular chamber, and the action potential duration (APD) curves were also constructed in both groups. The burst pacing was used to induce APD alternans and VA.RESULTSCompared with the same sites of CTL group, the 90% of MAP duration (MAPD90), the ERP, the maximal slope (Smax) of APDR curves were increased in CHF group (allP<0.05). The VAs in CHF group were easier to be induced than those in CTL group (allP<0.05). The coefficients of variation of Smax(COV-Smax) of APDR curves in CHF group were greater than those in CTL group (allP<0.05).CONCLUSIONBoth Smaxand COV-Smaxof APDR curves increase during CHF to facilitate the ventricular arrhythmia.
Chronic heart failure; Action potential duration; Restitution; Ventricular arrhythmia
R363
A
10.3969/j.issn.1000- 4718.2013.11.033
1000- 4718(2013)11- 2097- 03
2013- 06- 15
2013- 09- 04
△通訊作者 Tel: 0718-8301386; E-mail: chenshijianyun@163.com

