3種處理方式對(duì)葛仙米藻膽蛋白清除超氧陰離子自由基能力的影響
程 超,薛 峰,李 偉,汪興平,
(1.湖北民族學(xué)院林學(xué)園藝學(xué)院,湖北 恩施 445000;2.湖北民族學(xué)院生物科學(xué)與技術(shù)學(xué)院,湖北 恩施 445000;3.西北農(nóng)林科技大學(xué)食品科學(xué)與工程學(xué)院,陜西 楊凌 712100)
葛仙米(Nostoc sphaeroidesKüting)是一種藍(lán)藻門(mén)藍(lán)藻綱念珠藻科念珠藻屬的低等淡水藻類,僅在湖北省鶴峰縣走馬坪鎮(zhèn)有大面積生長(zhǎng)。葛仙米中富含7%~8%的藻膽蛋白(phycobiliprotein,PBP),主要為藻藍(lán)蛋白和藻紅蛋白,其中藻藍(lán)蛋白含量是藻紅蛋白的3.5 倍左右[1]。近幾年人們對(duì)PBP抗氧化特性進(jìn)行了研究[2-6],如汪興平等[7]研究發(fā)現(xiàn)葛仙米藻膽蛋白對(duì)超氧陰離子自由基(O2-?)的清除效果較好;藻藍(lán)蛋白能減少血液和肝臟中過(guò)氧化物及丙二醛含量[8]。
葛仙米藻膽蛋白為胞內(nèi)蛋白,其提取中會(huì)涉及很多處理,如破壁、浸提、干燥等工序,這些處理方式是否會(huì)影響PBP的抗氧化特性還有待研究。本實(shí)驗(yàn)利用鄰苯三酚-魯米諾化學(xué)發(fā)光法測(cè)定樣品對(duì)的清除作用,初步評(píng)價(jià)處理方式是否會(huì)影響葛仙米藻膽蛋白對(duì)?的清除作用。
1 材料與方法
1.1 材料
葛仙米購(gòu)于湖北省恩施市鶴峰縣。
1.2 試劑
磷酸二氫鉀、氫氧化鈉、硫酸銨、乙酸、乙酸鈉、三羥甲基氨基甲烷、鹽酸、鄰苯三酚、碳酸鈉等(均為分析純);魯米諾 美國(guó)Sigma公司;胃蛋白酶(酶活力為1∶3 000)、胰蛋白酶(酶活力為1∶250) 美國(guó)Amresco公司。
1.3 儀器與設(shè)備
高速冷凍離心機(jī)、Ф660pH/Temp/Mv meter 美國(guó)Beckman Coulter公司;ALPHA1-4真空冷凍干燥機(jī) 德國(guó)Marin Chris公司;BPCL型超微弱化學(xué)發(fā)光測(cè)量?jī)x中國(guó)科學(xué)院生物物理研究所;Waters高效液相色譜儀(Waters 2998 Photodiode Array Detector,Waters e2695 Separations module) 美國(guó)沃特斯公司。
1.4 方法
1.4.1 樣品的制備
反復(fù)凍融葛仙米藻膽蛋白:稱取脫脂葛仙米粉30 g,復(fù)水后于-20 ℃反復(fù)凍融3 次,后高速勻漿,4 ℃條件下在pH 7.3 的50 mmol/L KH2PO4-NaOH緩沖液浸提,10 000 r/min離心15 min,20%飽和硫酸銨去除雜蛋白后,上清液接著用60%飽和硫酸銨沉淀,透析過(guò)羥基磷灰石柱層析后冷凍干燥得產(chǎn)品。用重蒸水、50 mmol/L pH 7.3的KH2PO4-NaOH緩沖液溶解分別得樣品水溶反復(fù)凍融葛仙米藻膽蛋白(water-soluble phycobiliprotein from repeatedly frozen-thawedNostoc sphaeroidesKüting,RFTWP)和磷溶反復(fù)凍融葛仙米藻膽蛋白(phosphate buffer-soluble phycobiliprotein from repeatedly frozenthawedNostoc sphaeroidesKüting,RFTPP)。
未反復(fù)凍融葛仙米藻膽蛋白(phycobiliprotein from non-repeatedly frozen-thawedNostoc sphaeroidesKüting,NRFTP):稱取脫脂干葛仙米粉30 g,復(fù)水后高速勻漿處理,而后按照反復(fù)凍融的方法得樣品。用重蒸水和pH 7.3的50 mmol/L KH2PO4-NaOH緩沖液溶解分別得水溶未凍融葛仙米藻膽蛋白(water-soluble phycobiliprotein from non-repeatedly frozen-thawedNostocsphaeroidesKüting,NRFTWP)和磷溶未凍融葛仙米藻膽蛋白(phosphate buffer-soluble phycobiliprotein from non-repeatedly frozen-thawedNostoc sphaeroidesKüting,NRFTPP)。
不同pH值緩沖液樣品:稱取脫脂干葛仙米粉30 g,復(fù)水后-20 ℃反復(fù)凍融3 次,分別用pH 7.3的20 mmol/L KH2PO4-NaOH、pH 5.6的20 mmol/L的乙酸-乙酸鈉、pH 8.1的20 mmol/L的Tris-HCl緩沖液在4 ℃浸提,10 000 r/min離心15 min,20%飽和硫酸銨除雜蛋白,用60%硫酸銨沉淀,透析HA處理后冷凍干燥得pH 5.6、pH 7.3和pH 8.1的葛仙米藻膽蛋白。
1.4.2 模擬胃腸液的配制方法
按照參考文獻(xiàn)[11]方法配制2×人工胃液和2×人工腸液。
1.4.3 葛仙米藻膽蛋白的模擬胃腸液降解
取50 mL三角瓶11 個(gè),每瓶加10 mL 2×人工胃液,37 ℃保溫10 min。然后分別加入10 mL 37 ℃預(yù)熱的葛仙米藻膽蛋白溶液,37 ℃保溫消化,在0、1、5、10、15、30、60、90、120、150、180 min取樣,0.168 mol/L Na2CO3溶液調(diào)pH值為7~8終止反應(yīng)。冷凍干燥得到不同時(shí)間胃液降解的樣品。
1.4.4 蛋白質(zhì)在人工腸液中降解程度
取50 mL三角瓶11 個(gè),每管加入10 mL的2×人工腸液,37 ℃保溫10 min。分別加入37 ℃預(yù)熱的10 mL葛仙米藻膽蛋白溶液,37 ℃保溫消化,在0、1、5、10、15、30、60、90、120、150、180 min取樣,90 ℃加熱5 min終止反應(yīng),冷凍干燥得不同時(shí)間腸液降解的樣品。
采用鄰苯三酚-魯米諾化學(xué)發(fā)光體系[12]:按照表1加入各種試劑。最后加入魯米諾和碳酸緩沖液以啟動(dòng)反應(yīng),間隔2 s,測(cè)定300 s。用Origin8.0軟件對(duì)曲線面積積分以此表示相對(duì)發(fā)光強(qiáng)度,按下式計(jì)算抑制率,各組數(shù)據(jù)采用±s表示。

式中:CL對(duì)照、CL本底和CL樣品分別表示對(duì)照組、本底和樣品的相對(duì)發(fā)光強(qiáng)度。

表1 鄰苯三酚-魯米諾化學(xué)發(fā)光體系Table 1 Pyragollic acid-luminol luminescence system
1.4.6 HPLC條件
將樣品用不同pH值溶液溶解后過(guò)0.44 μm濾膜后上樣,HPLC柱型號(hào):SEC-300(4.8 mm×300 mm)Sepax Technologies;洗脫液:0.1 mol/L pH 7.0磷酸鹽緩沖液,上樣量:20 μL,柱溫:27 ℃;流速:0.3 mL/min;柱壓:2.76 MPa;檢測(cè)波長(zhǎng):280 nm[13]。
1.5 數(shù)據(jù)分析
采用Origin8.0軟件作圖,SPSS16.0軟件對(duì)數(shù)據(jù)結(jié)果進(jìn)行分析。
2 結(jié)果與分析
2.1 反復(fù)凍融和不同溶劑處理葛仙米藻膽蛋白對(duì)的清除作用
周站平等[14]曾報(bào)道:藻藍(lán)蛋白經(jīng)過(guò)凍融后表現(xiàn)為清除自由基,未經(jīng)凍融的可產(chǎn)生自由基。因此本部分按照實(shí)驗(yàn)方法分別制備反復(fù)凍融和未反復(fù)凍融的藻膽蛋白,而后將其分別用重蒸水和pH 7.3的KH2PO4-NaOH緩沖液溶解,按化學(xué)發(fā)光法測(cè)定其對(duì)O2-?的清除作用,具體結(jié)果見(jiàn)圖1~4。

圖1 RFTPP對(duì)的抑制作用Fig.1 Superoxide anion radical scavenging activity of RFTPP
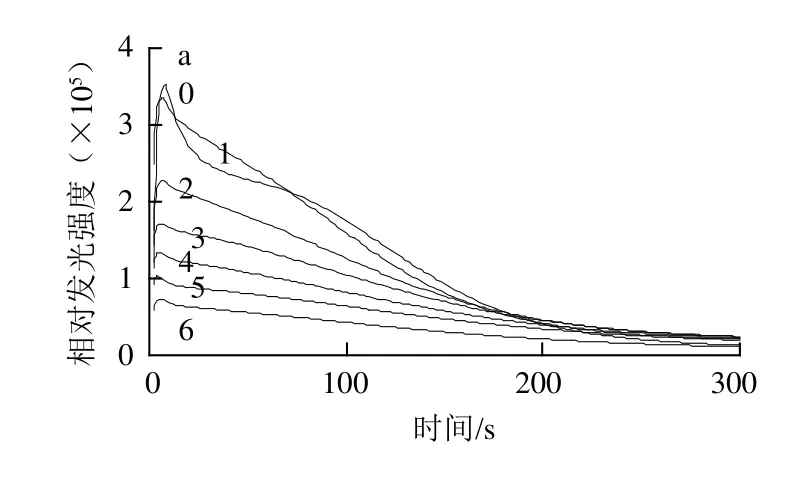

圖2 RFTWP對(duì)的抑制作用Fig.2 Superoxide anion radical scavenging activity of RFTWP

圖3 NRFTWP對(duì)的清除作用Fig.3 Superoxide anion radical scavenging activityof NRFTWP

圖4 NRFTPP對(duì)的清除作用Fig.4 Superoxide anion radical scavenging activity of NRFTPP
根據(jù)圖1~4可以計(jì)算出RFTPP、RFTWP、NFRTPP和NRFTWP對(duì)的IC50值分別為1.060、1.110、1.097、1.161 mg/mL,統(tǒng)計(jì)分析發(fā)現(xiàn)4 種處理對(duì)的清除作用差異均不顯著(P=0.187)。即反復(fù)凍融處理不會(huì)影響葛仙米藻膽蛋白對(duì)的清除作用,而且前期研究發(fā)現(xiàn):反復(fù)凍融處理還可提高葛仙米藻膽蛋白得率[15],因此提取藻膽蛋白可將葛仙米進(jìn)行反復(fù)凍融處理。本結(jié)果與周站平等的結(jié)果有差異,可能是因?yàn)閮煞N實(shí)驗(yàn)材料不同,材料差異導(dǎo)致內(nèi)含的藻膽蛋白種類不同,凍融處理對(duì)不同的藻膽蛋白種類產(chǎn)生的效果有可能不同。溶劑對(duì)藻膽蛋白的抗氧化特性有一定影響,緩沖鹽溶液可提高其對(duì)的清除能力,這可能是因?yàn)榫彌_鹽改變了溶液的離子強(qiáng)度,而離子強(qiáng)度會(huì)影響藻膽蛋白的聚集狀態(tài)(藻膽蛋白的六聚體與單體間的平衡)[16],因此以下處理均采用緩沖液。
2.2 浸提液pH值對(duì)葛仙米藻膽蛋白抗氧化特性的影響
藻膽蛋白在pH 5~8之間存在聚合度的轉(zhuǎn)變,按照參考文獻(xiàn)[17-20],本實(shí)驗(yàn)分別制備pH 5.6、pH 7.3和pH 8.1的葛仙米藻膽蛋白,其對(duì)的清除作用見(jiàn)圖5~7。

圖5 pH 5.6 PBP對(duì)的清除作用Fig.5 Superoxide anion radical scavenging activity of phycobiliprotein extracted with pH 5.6 PBP
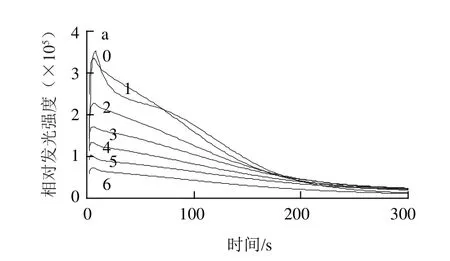

圖6 pH 7.3 PBP對(duì)的清除作用Fig.6 Superoxide anion radical scavenging activity of phycobiliprotein extracted with pH 7.3 PBP
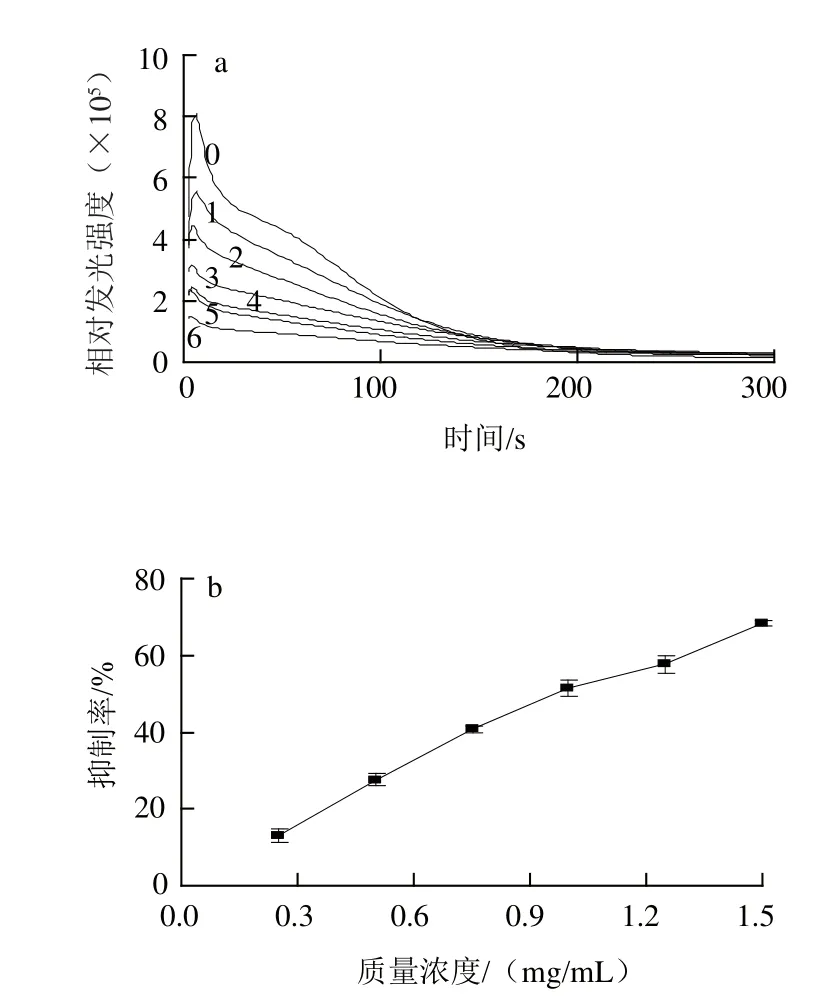
圖7 pH 8.1 PBP對(duì)的清除作用Fig.7 Superoxide anion radical scavenging activity of phycobiliprotein extracted with pH 8.1 PBP
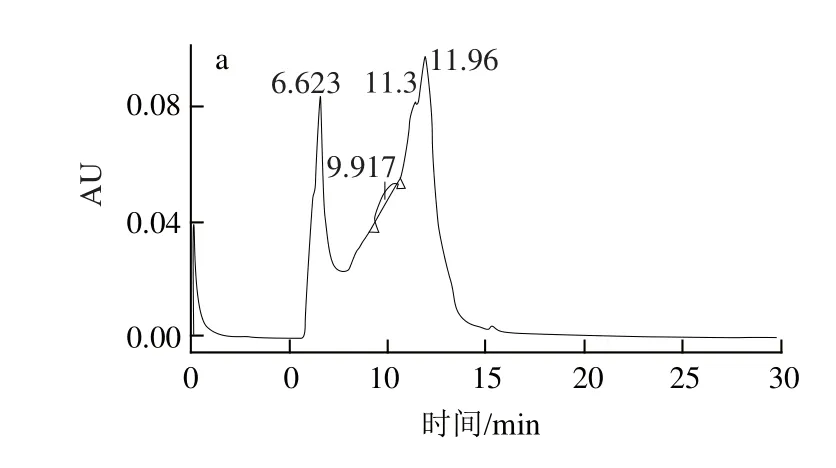
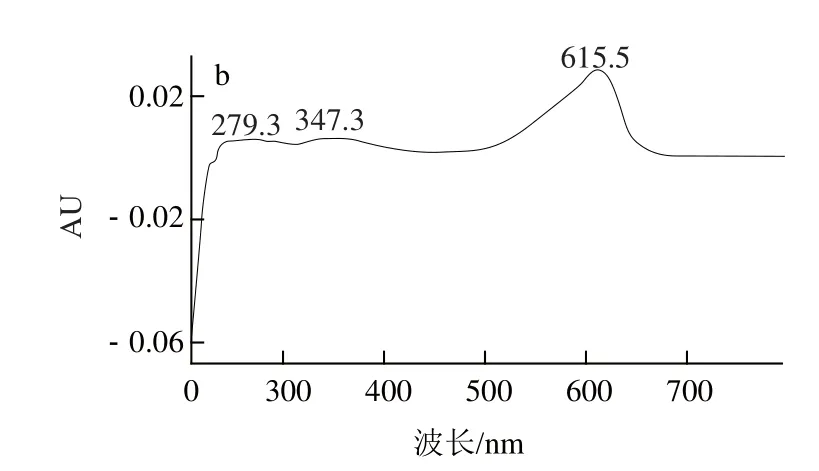
圖8 pH 5.6的葛仙米藻膽蛋白的HPLC及紫外掃描圖Fig.8 HPLC pro file and UV absorption spectrum of phycobiliprotein extracted with pH 5.6 buffer
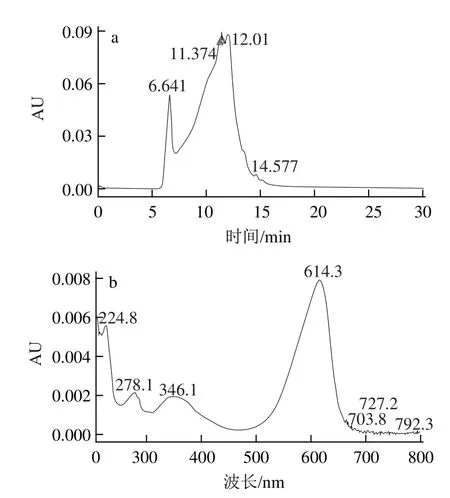
圖9 pH 7.3的葛仙米藻膽蛋白HPLC及紫外掃描圖Fig.9 HPLC pro file and UV absorption spectrum of phycobiliprotein extracted with pH 7.3 buffer

圖10 pH 8.1的葛仙米藻膽蛋白的HPLC及紫外掃描圖Fig.10 HPLC pro file and UV absorption spectrum of phycobiliprotein extracted with pH 8.1 buffer
由圖8~10可知,pH 5.6和pH 7.3浸提液中藻膽蛋白保留時(shí)間為11.300 min和11.374 min,非常接近,因此兩種浸提液中藻膽蛋白對(duì)的清除效果相當(dāng);但pH 8.1浸提液藻膽蛋白保留時(shí)間后移至16.991 min,說(shuō)明其藻膽蛋白的分子質(zhì)量減小,聚合程度下降,同時(shí)pH 8.1浸提液中增加了一個(gè)保留時(shí)間為23.056 min的吸收峰,這并不是藻膽蛋白類物質(zhì),因此綜合考慮選擇pH 7.3為浸提液。
2.3 葛仙米藻膽蛋白模擬胃腸液降解產(chǎn)物對(duì)O2-?的清除作用

圖11 模擬腸液消化產(chǎn)物對(duì)的清除作用Fig.11 Effect of simulated intestinal liquid on the superoxide anion radical scavenging activity of phycobiliprotein

圖12 模擬胃液消化產(chǎn)物對(duì)的清除作用Fig.12 Effect of simulated gastric liquid on the superoxide anion radical scavenging activity of phycobiliprotein
由圖11、12可知,隨處理時(shí)間延長(zhǎng),模擬腸液消化產(chǎn)物對(duì)自由基清除能力增強(qiáng),而模擬胃液消化產(chǎn)物對(duì)自由基清除能力下降。這可能是由于胃液或腸液的降解產(chǎn)物分子質(zhì)量不同而導(dǎo)致的[22]。
3 結(jié) 論
綜上所述,作為破壁方法之一的反復(fù)凍融處理不會(huì)影響葛仙米藻膽蛋白對(duì)的清除效果,緩沖液作為浸提液可使葛仙米藻膽蛋白對(duì)的清除作用增強(qiáng),同時(shí)不同pH值緩沖液浸提液中,由于藻膽蛋白的聚合度不同導(dǎo)致其對(duì)清除作用有差異。此外隨處理時(shí)間延長(zhǎng),模擬腸液消化產(chǎn)物對(duì)清除能力增強(qiáng),而模擬胃液消化產(chǎn)物對(duì)清除能力下降。主要是由于模擬胃液中藻膽蛋白的降解程度強(qiáng)于模擬腸液的,即模擬胃液中小分子物質(zhì)的含量遠(yuǎn)高于模擬腸液的,尤其是隨著處理時(shí)間延長(zhǎng),這種小分子物質(zhì)含量差異越明顯,而藻膽蛋白的抗氧化功能與其分子質(zhì)量具有很大關(guān)系[23],因此藻膽蛋白只有適度降解后才能增加其抗氧化功能。
[1]陳德文.葛仙米藻紅蛋白分離純化與結(jié)構(gòu)及生物活性研究[D].武漢: 華中農(nóng)業(yè)大學(xué), 2005.
[2]BERMEJO P, PI?ERO E, VILLAR á M.Iron-chelating ability and antioxidant properties of phycocyanin isolated from a protean extract ofSpirulina platensis[J].Food Chemistry, 2008, 110(2): 436-445.
[3]BHAT V B, MADYASTHA K M.C-phycocyanin: a potent peroxyl radical scavengerin vivoandin vitro[J].Biochemical and Biophysical Research Communications, 2000, 275(1): 20-25.
[4]BERMEJO-BESCóS P, PI?ERO-ESTRADA E, VILLAR del FRESNO á M.Neuroprotection bySpirulina platensisprotean extract and phycocyanin against iron-induced toxicity in SH-SY5Y neuroblastoma cells[J].Toxicology in Vitro, 2008, 22(6): 1496-1502.
[5]BENEDETTI S, BENVENUTI F, PAGLIARANI S, et al.Antioxidant properties of a novel phycocyanin extract from the blue-green algaAphanizomenon fl os-aquae[J].Life Sciences, 2004,75(19): 2353-2362.
[6]MADHYASTHA H K, SIVASHANKARI S, VATSALA T M.C-phycocyanin fromSpirulina fussiformisexposed to blue light demonstrates higher efficiency ofin vitroantioxidant activity[J].Biochemical Engineering Journal, 2009, 43(1): 221-224.
[7]汪興平, 謝筆均, 潘思軼, 等.葛仙米藻紅蛋白體外抗活性氧自由基作用的研究[J].食品科學(xué), 2005, 26(8): 404-407.
[8]汪興平, 謝筆鈞, 潘思軼, 等.葛仙米藻藍(lán)蛋白抗氧化作用研究[J].食品科學(xué), 2007, 28(12): 458-461.
[9]吳飛鵬, 蔡繼業(yè), 馬淑媛, 等.殼聚糖對(duì)超氧自由基的清除作用[J].高分子材料科學(xué)與工程, 2008, 24(8): 124-127.
[10]萬(wàn)影, 陳玉石.黃芪對(duì)超氧陰離子自由基的清除作用[J].數(shù)理醫(yī)藥學(xué)雜志, 1998, 11(1): 61-62.
[11]李英華, 董杰, 李劍虹, 等.外源蛋白在模擬胃腸環(huán)境中穩(wěn)定性測(cè)定模型初探[J].衛(wèi)生研究, 2004, 33(4): 433-437.
[12]FU Hongfei, XIE Bijun, PAN Siyi, et al.Effect of esterification with fatty acid ofβ-cryptoxanthin on its thermal stability and antioxidant activity by chemiluminescence method[J].Food Chemistry, 2010,122(3): 602-609.
[13]SONI B, TRIVEDI U, MADAMWAR D.A novel method of single step hydrophobic interaction chromatography for the purification of phycocyanin fromPhormidium fragileand its characterization for antioxidant property[J].Bioresource Technology, 2008, 99(1): 188-194.
[14]周站平, 陳秀蘭, 陳超, 等.藻膽蛋白脫輔基蛋白對(duì)其抗氧化活性的影響[J].海洋科學(xué), 2003, 27(5): 77-81.
[15]程超, 薛峰, 汪興平, 等.反復(fù)凍融增強(qiáng)葛仙米藻膽蛋白抗氧化特性[J].食品科學(xué), 2011, 32(23): 121-124.
[16]王廣策, 鄧田, 曾呈奎.藻膽蛋白的研究概況(Ⅰ): 藻膽蛋白的種類與組成[J].海洋科學(xué), 2000, 24(2): 22-24.
[17]SANTIAGO-SANTOS M C, PONCE-NOYOLA T, OLVERARAMIREZ R, et al.Extraction and purification of phycocyanin fromCalothrixsp.[J].Process Biochemistry, 2004, 39(12): 2047-2052.
[18]NIU J, WANG G, LIN X, et al.Large-scale recovery of C-phycocyanin fromSpirulina platensisusing expanded bed adsorption chromatography[J].Journal of Chromatography B, 2007, 850(1): 267-276.[19]ISAILOVIC D, LI H, YEUNG E.Isolation and characterization of R-phycoerythrin subunits and enzymatic digests[J].Journal of Chromatography A, 2004, 1051(1/2): 119-130.
[20]SONI B, KALAVADIA B, TRIVEDI U, et al.Extraction,purification and characterization of phycocyanin fromOscillatoria quadripunctulata.Isolated from the rocky shores of Bet-Dwarka,Gujarat, India[J].Process Biochemistry, 2006, 41(9): 2017-2023.
[21]LIU Luning, CHEN Xiulan, ZHANG Xiying, et al.One-step chromatography method for efficient separation purification of R-phycoerythrin fromPolysiphonia urceolata[J].Journal of Biotechnology, 2005, 116(1): 91-100.
[22]程超, 李偉, 汪興平.葛仙米藻膽蛋白體外消化特性研究[J].食品科學(xué), 2012, 33(15): 6-10.
[23]黃蓓, 王廣策, 李振剛.藻藍(lán)蛋白色素肽光動(dòng)力學(xué)抗腫瘤作用的實(shí)驗(yàn)研究[J].激光生物學(xué)報(bào), 2002, 11(3): 194-198.

